Похожие презентации:
Изопроцессы в газах. (11 класс)
1. Изопроцессы в газах
11 классГУО СОШ № 61
Изопроцессы в газах
Достал учеников
своими
презентациями ЯнСтМ
2. Цель:
установить зависимость междудвумя макроскопическими
параметрами газа при
неизменном третьем.
3.
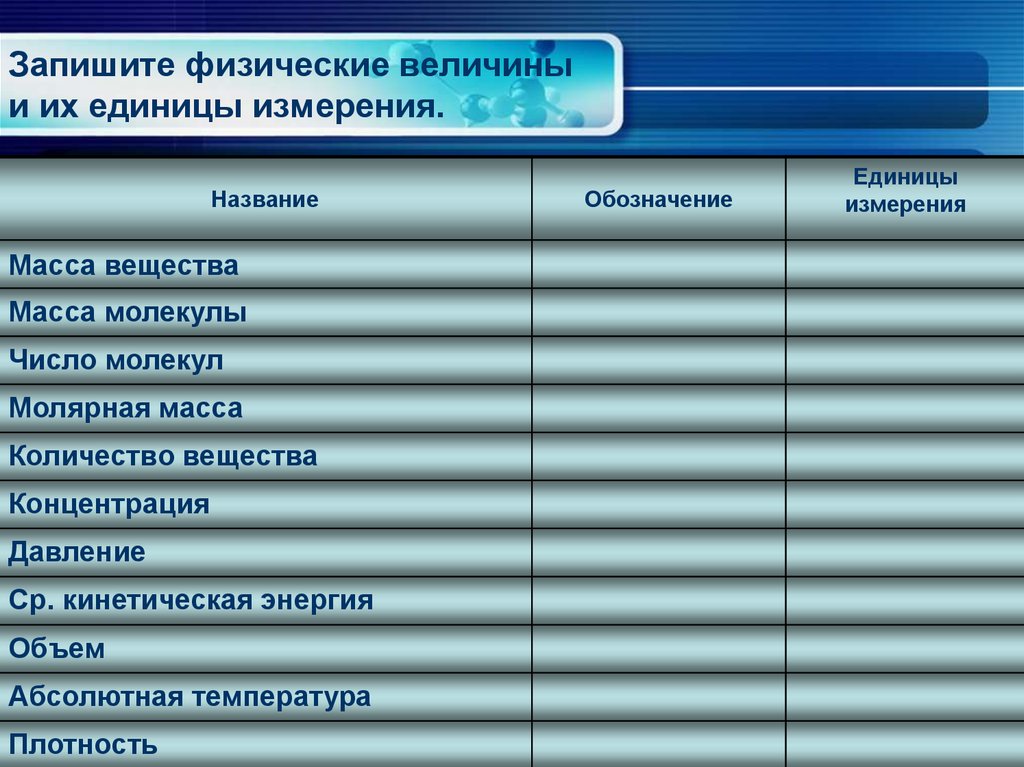
4. Запишите физические величины и их единицы измерения.
НазваниеМасса вещества
Масса молекулы
Число молекул
Молярная масса
Количество вещества
Концентрация
Давление
Ср. кинетическая энергия
Объем
Абсолютная температура
Плотность
Обозначение
Единицы
измерения
5. Изопроцесс -
Изопроцесс процесс, при котором один измакроскопических параметров
состояния данной массы газа
остается постоянным.
V, p, Т
6. Изо – (постоянный)
Изобарныйизопроцессы
Изохорный
Изотермический
7. Изотермический процесс -
Изотермическийпроцесс ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ
МАССЫ ГАЗА ПРИ ПОСТОЯННОЙ ТЕМПЕРАТУРЕ.
Т = const
m = const
8.
• Physics\DEMO.exe9.
• Поршеньлегко
подвижен
V↓ → р↑
p↓ → V↑
10. Изотермический процесс
Из уравненияКлапейрона – Менделеева следует:
m
pV
=
const
=
M
RT
11. Закон Бойля – Мариотта.
Закон экспериментально получен в:• 1662 г. Р. Бойлем;
• 1676 г. Э. Мариоттом.
T - const
Для газа данной массы при
постоянной температуре
произведение давления газа на его
объем постоянно:
p1V1 = p2V2
Р. Бойль
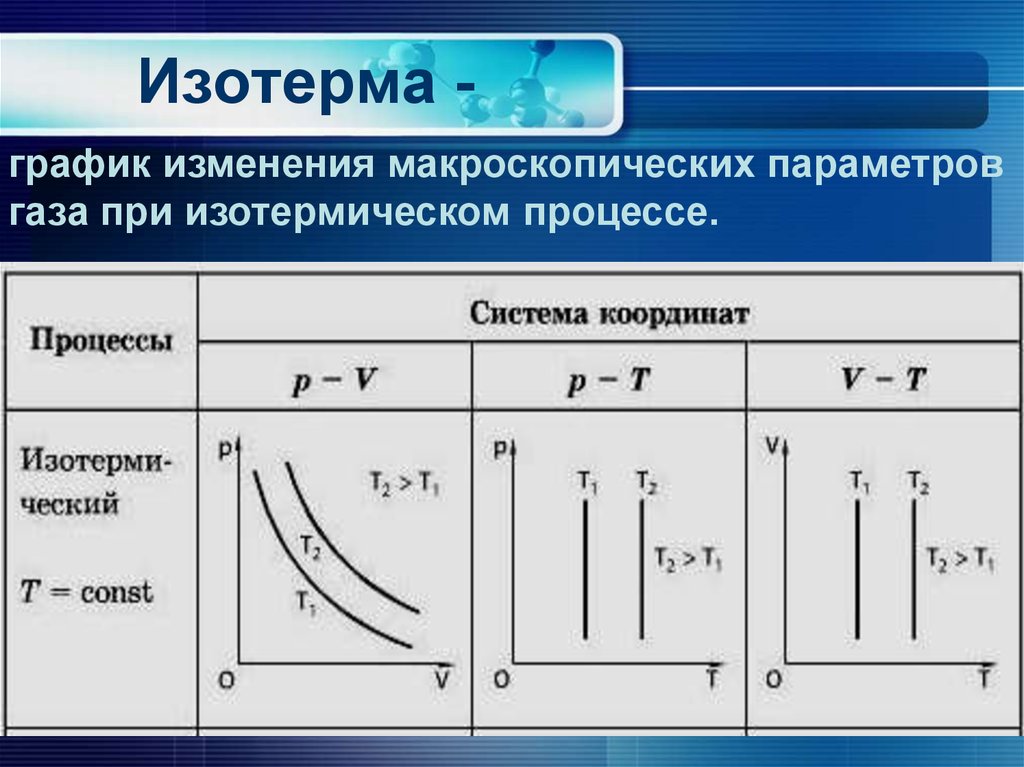
12. Изотерма -
Изотерма график изменения макроскопических параметровгаза при изотермическом процессе.
13. Изобарный процесс -
Изобарный процесс ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙМАССЫ ГАЗА ПРИ ПОСТОЯННОМ ДАВЛЕНИИ.
P = const
m = const
14.
• Physics\DEMO.exe15.
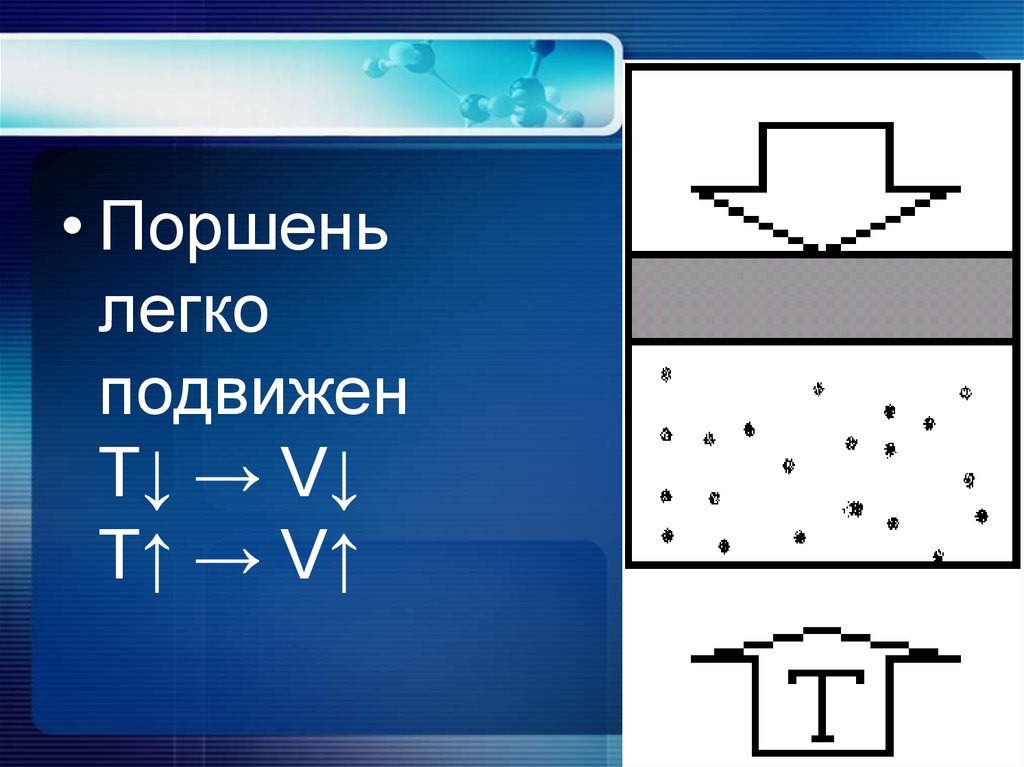
• Поршеньлегко
подвижен
T↓ → V↓
T↑ → V↑
16. Изобарный процесс
Из уравненияКлапейрона – Менделеева следует:
V
T
mR
=
const
=
Mp
17. Закон Гей-Люссака.
Закон экспериментальнополучен в 1802 г.
p - const
Для газа данной массы при
постоянном давлении отношение
объема газа к его
термодинамической температуре
постоянно:
V1 / T1 = V2 / T2
ГЕЙ-ЛЮССАК
Жозеф Луи
18. Изобара –
график изменения макроскопическихпараметров газа при изобарном процессе.
19. Изохорный процесс -
Изохорный процесс ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙМАССЫ ГАЗА ПРИ ПОСТОЯННОМ ОБЪЕМЕ.
V = const
m = const
20.
• Physics\DEMO.exe21.
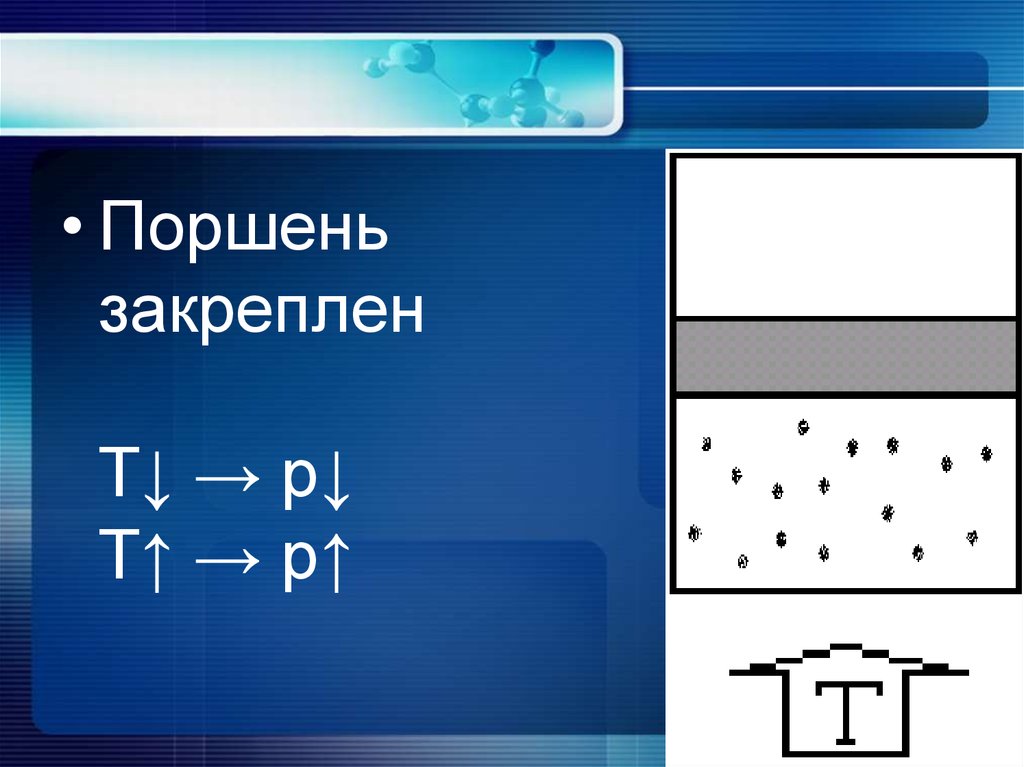
• Поршеньзакреплен
T↓ → р↓
T↑ → p↑
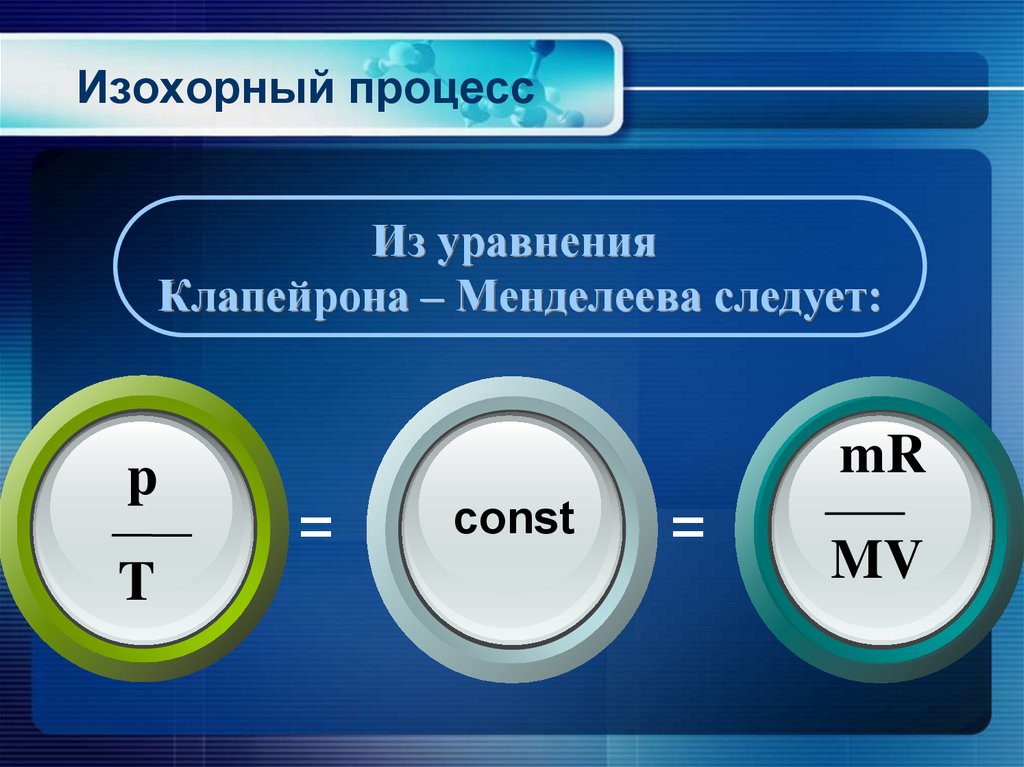
22. Изохорный процесс
Из уравненияКлапейрона – Менделеева следует:
p
T
mR
=
const
=
MV
23. Закон Шарля.
Закон экспериментальнополучен в 1787 г.
V - const
Для газа данной массы при
постоянном объеме отношение
давления газа к его
термодинамической температуре
постоянно:
p1 / T1 = p2 / T2
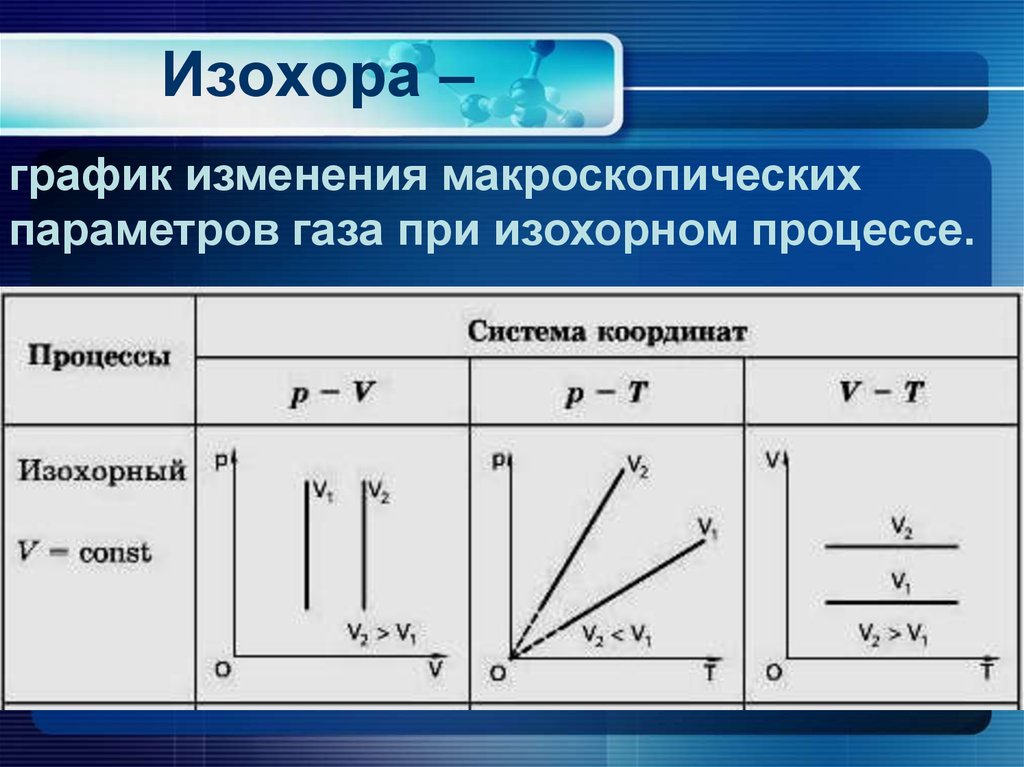
24. Изохора –
график изменения макроскопическихпараметров газа при изохорном процессе.
25.
26. Закон Дальтона
• Если идеальный газ являетсясмесью нескольких газов, то
давление смеси идеальных газов
равно сумме парциальных давлений
входящих в нее газов.
• Парциальное давление - это такое
давление, которое производил бы
газ, если бы он один занимал весь
объем, равный объему смеси.
27.
28. Цикл 1
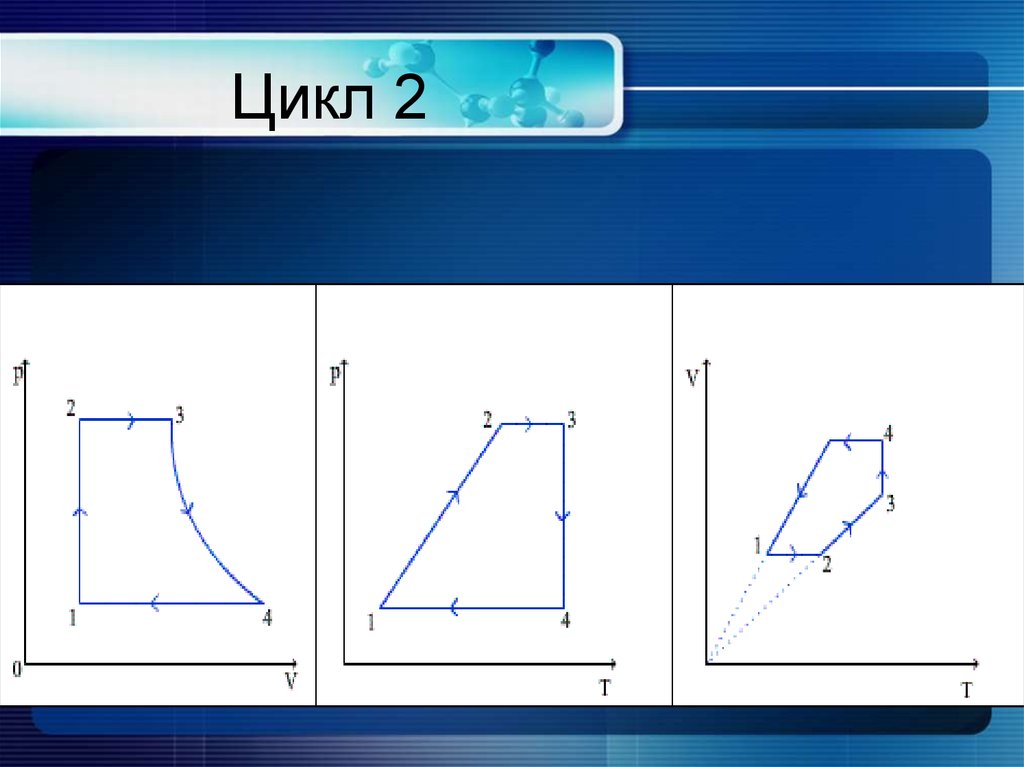
29. Цикл 2
30. Домашнее задание
1. Какой изопроцесс изображенна каждом участке графика?
2. Как изменяются ТДпараметры?
31. Домашнее задание
Решите задачу .При температуре 27oС
давление газа в закрытом
сосуде было 75 кПа. Каким
будет давление этого газа
o
при температуре -13 С ?
























 Физика
Физика