Похожие презентации:
Периодический закон и ПС
1.
2.
3.
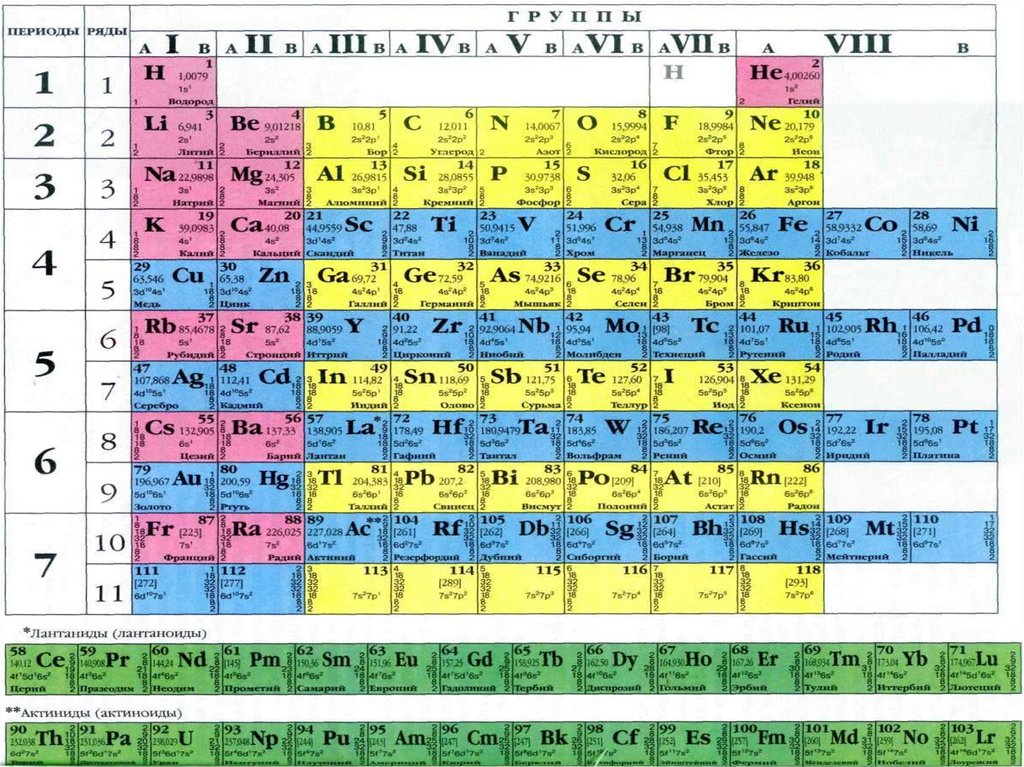
Периодическая системахимических элементов
В 1869 г. русским химиком Д.И.
Менделеев представил Русскому
химическому обществу,
периодический закон химических
элементов, а также первый вариант
периодической таблицы, в которой
63 элемента были расположены в
порядке возрастания атомных весов, и
отражалась периодичность изменения
свойств элементов.
4.
ФормулировкаПериодического закона (1869 г)
«Свойства простых тел, а также
форма и свойства соединений
элементов, находятся в
периодической зависимости от
величины атомных весов
элементов».
5.
Как Д.И. Менделееев пришел к открытию ПЗ6.
7.
Систематизируя химические элементыД.И. Менделеев уделял большое
внимание также свойствам элементов и
их соединений, распределяя элементы
со сходными свойствами в
вертикальные столбцы – группы.
Иногда нарушая выявленную им
закономерности он более тяжелые
металлы ставил перед элементами с
меньшей Мr.
8.
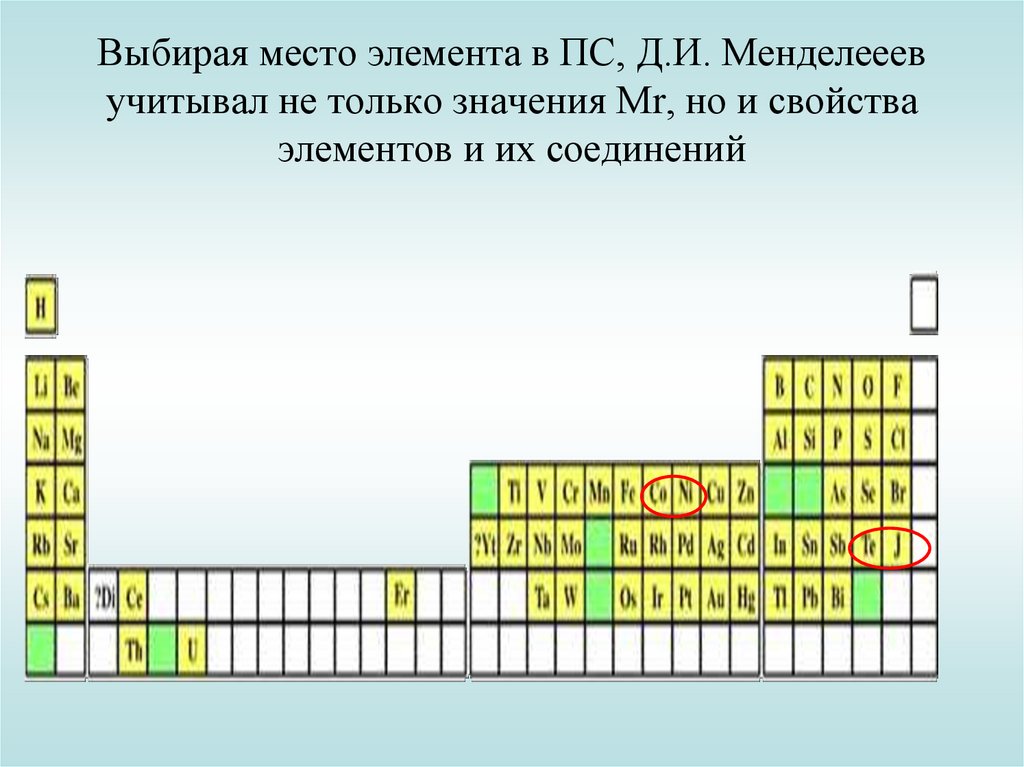
Выбирая место элемента в ПС, Д.И. Менделееевучитывал не только значения Мr, но и свойства
элементов и их соединений
9.
10.
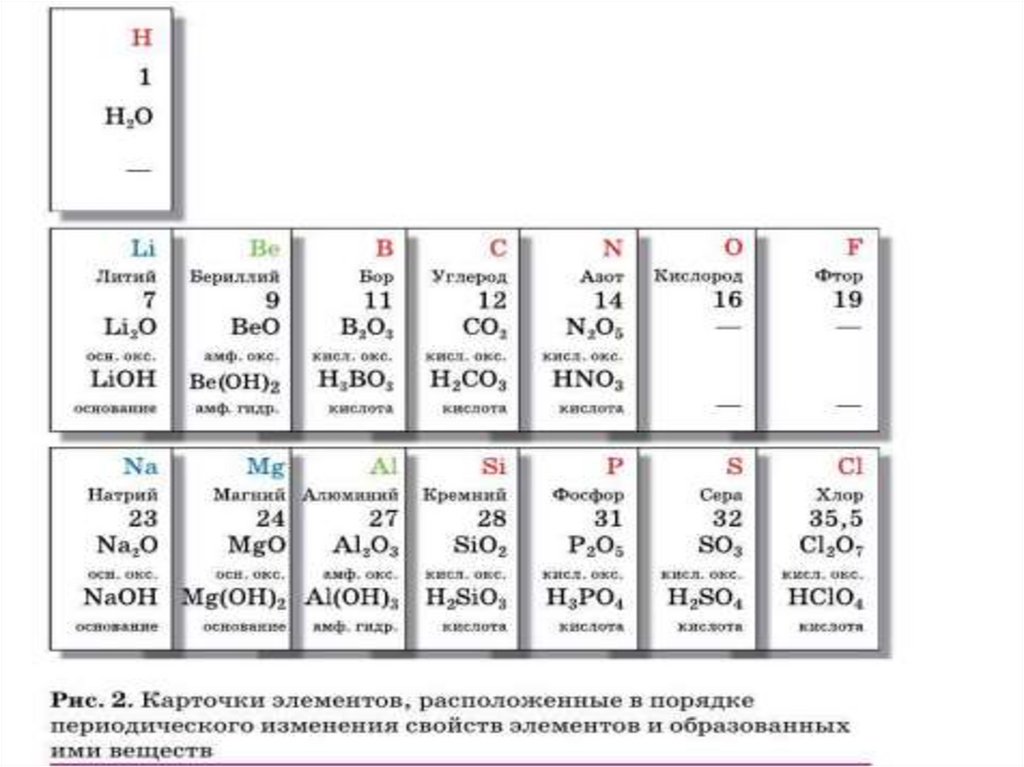
Закономерные изменения свойств элементовв пределах периода
металлические свойства ослабевают,
неметаллические свойства усиливаются,
степень окисления элементов в высших оксидах
увеличивается + 1 до + 8,
• степень окисления элементов в летучих водородных
соедиениях увеличивается от
-4 до -1,
• оксиды от основных через амфотерные сменяются
кислотными,
• гидроксиды от щелочей через амфотерные гидроксиды
сменяются кислородсодержащими кислотами.
11.
Периодический законсформулированный
Д.И. Менделеевым 1869 г.
12.
Изотопы• Атомы, имеющие одинаковый заряд ядра, а
значит и тождественные свойства, но
разное число нейтронов, а следовательно,
разные массовые числа называются
изотопами.
17 О
18 О
• 168О
8
8
13.
Современная формулировкапериодического закона
14.
Периодичность в изменении свойствэлементов и их соединений
объясняется периодической
повторяемость в строении внешних
энергетических уровней их атомов.
15.
Значение ПС и ПЗ Д.И. Менделеева• Обобщают сведения о химических
элементах и образованных ими веществах.
• Объясняют периодичность в изменении их
свойств и причину сходства свойств
элементов одной и той же группы.
• Возможность прогнозировать, т. е.
предсказывать, описывать свойства и
указывать пути открытия новых
химических элементов.
16.
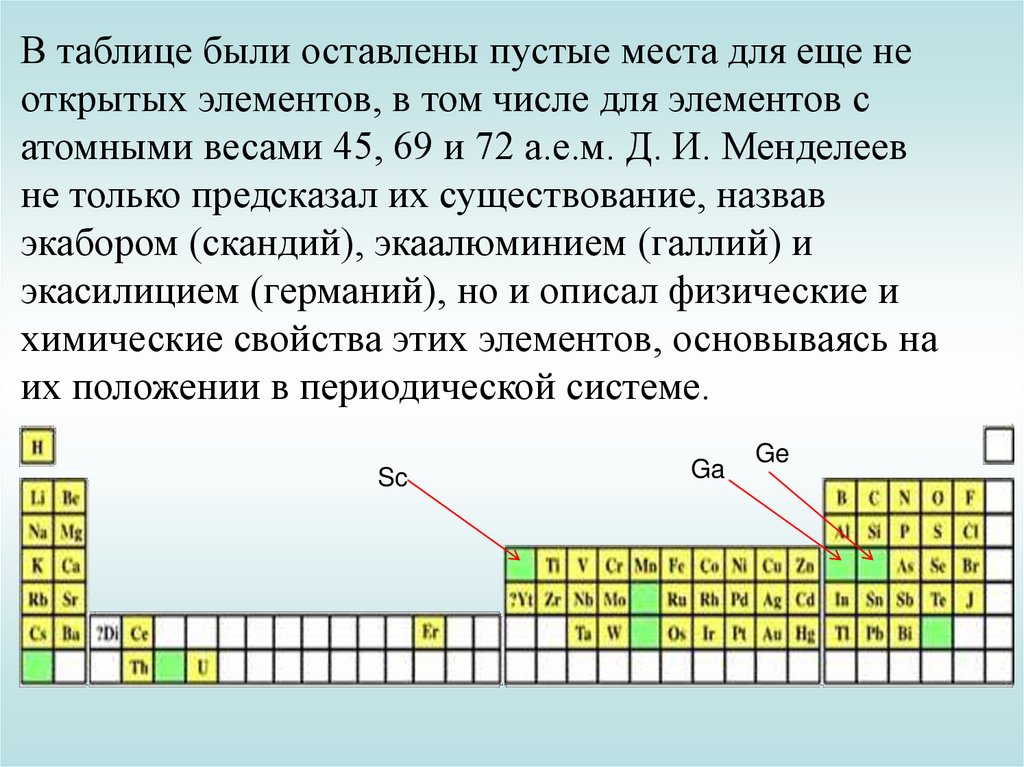
В таблице были оставлены пустые места для еще неоткрытых элементов, в том числе для элементов с
атомными весами 45, 69 и 72 а.е.м. Д. И. Менделеев
не только предсказал их существование, назвав
экабором (скандий), экаалюминием (галлий) и
экасилицием (германий), но и описал физические и
химические свойства этих элементов, основываясь на
их положении в периодической системе.
Sc
Ga
Ge
17.
Открытие предсказанных элементов• В1875 г франц. Лекоком де
Буабодраном – галлий
(экаалюминий)
• В 1879 г шведом Л. Нильсоном был
открыт «экабор» (скандий).
• В1886 г немцем К. Винклером
«экасилиций» (германий)
18.
Виды таблиц• Периодическая система элементов является
графическим (табличным) выражением
периодического закона.
• Известно более 500 форм изображения
периодического закона, наиболее широко
используются только три:
• короткая, 8-клеточная; полудлинная,
• 18 клеточная; длиннопериодная,
• 32-клеточная.
• Принципиальный подход к построению таблиц
единый – элементы располагаются в порядке
возрастания заряда ядер их атомов.
19.
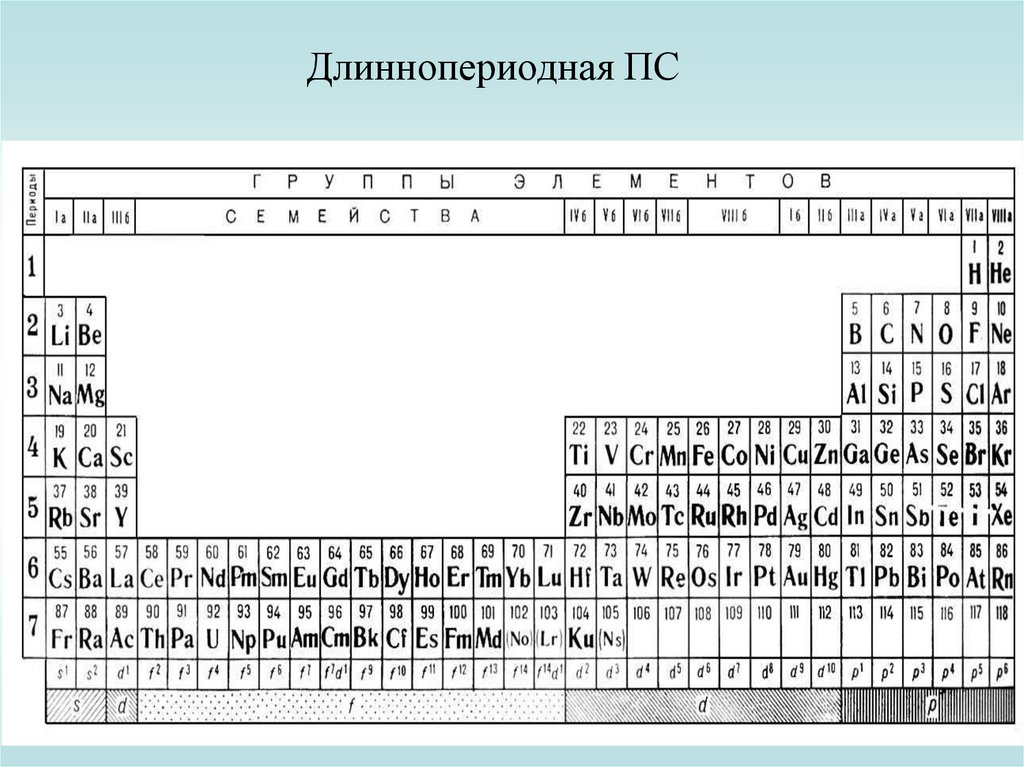
Длиннопериодная ПС20.
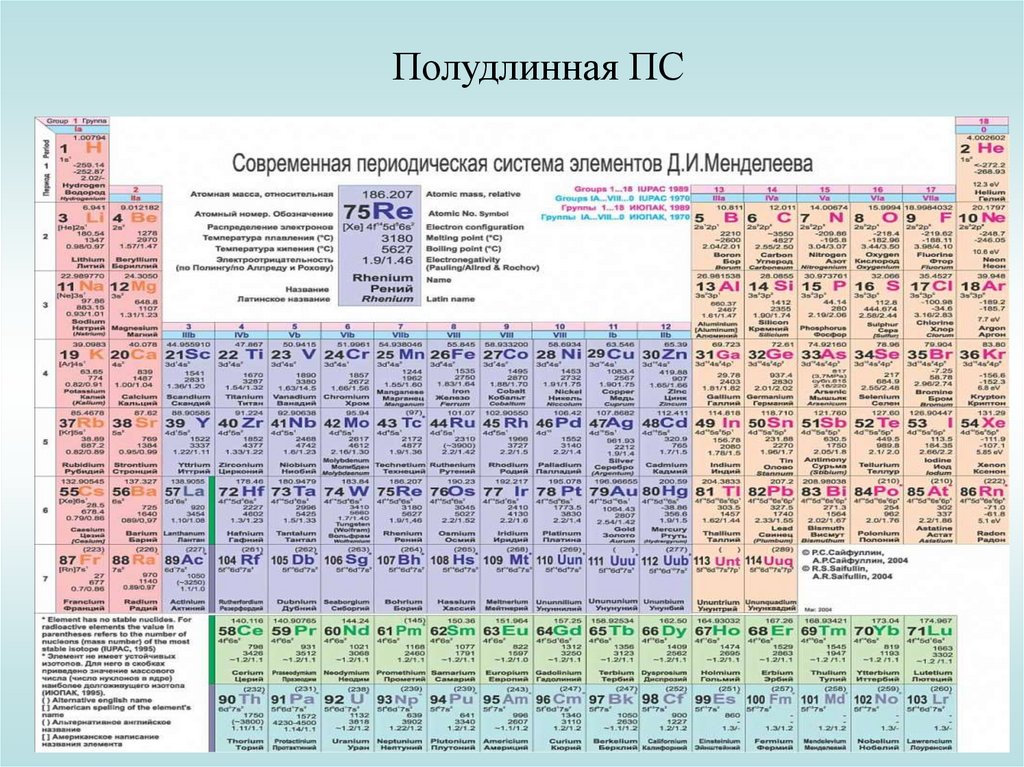
Полудлинная ПС21.
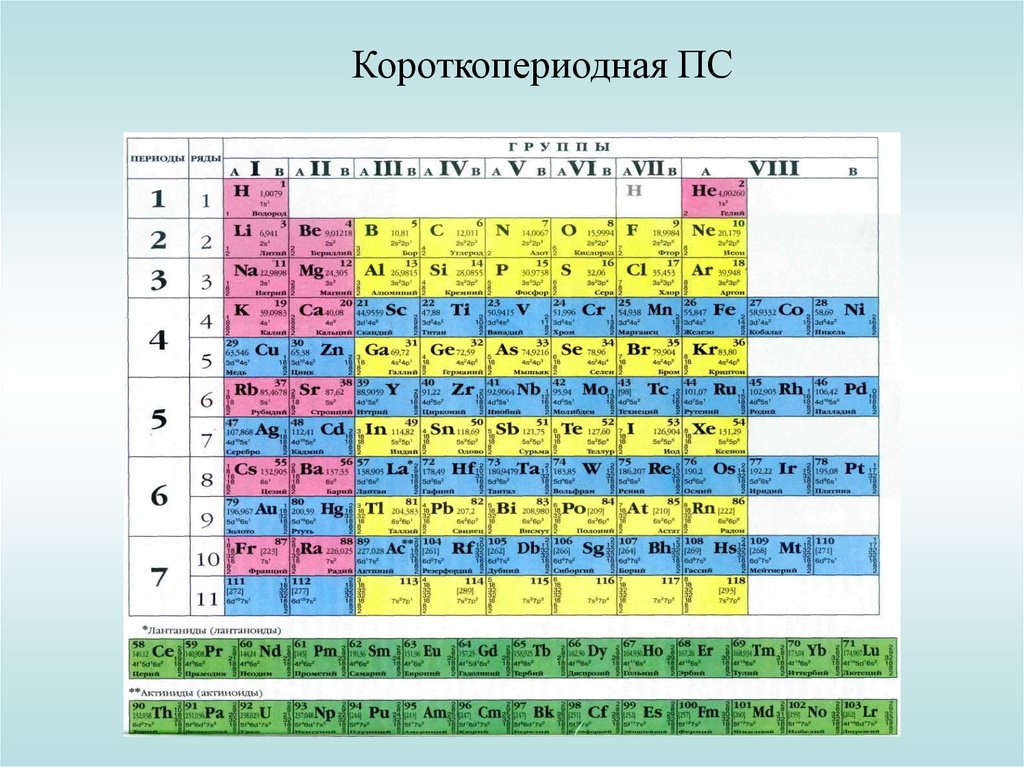
Короткопериодная ПС22.
https://ptable.com/#%D0%A1%D0%B2%D0%BE%D0%B9%D1%81%D1%82%D0%B
2%D0%B0
















 Химия
Химия








