Похожие презентации:
Кристаллизация аморфных ортофосфатов церия (IV) в гидротермальных условиях
1.
Министерство науки и высшего образования РоссийскойФедерации
ФГБОУ ВО «Российский химико-технологический
университет
имени Д. И. Менделеева»
Факультет естественных наук
Кафедра общей и неорганической химии
Кристаллизация аморфных ортофосфатов
церия(IV) в гидротермальных условиях
Биричевская Карина Вячеславовна
Научный руководитель: н.с., к.х.н. Козлова Т.О.
Лаборатория синтеза функциональных материалов и переработки
минерального сырья ИОНХ им. Н.С. Курнакова Российской академии наук
Москва, 2021
2.
Ортофосфаты церияНахождение в природе
Монацит
Рабдофан
CePO4
CePO4·xH2O
Получение кристаллических ортофосфатов церия(IV) в лабораторных условиях:
• Соосаждение из водных растворов
• Высокотемпературная обработка
Се(III)
• Гидротермальная обработка
Се(IV)
Кристаллический
ортофосфат
церия(IV)
2
3.
Постановка цели и задачЦель
• Исследование закономерностей формирования кристаллических
ортофосфатов церия(IV) из аморфных гелей в среде растворов
различных электролитов в гидротермальных условиях.
Задачи
• Получение кристаллических ортофосфатов церия(IV) методом
гидротермальной
обработки
аморфных
церийсодержащих
фосфорнокислых гелей
• Анализ
полученных
продуктов
при
помощи
различных
современных физико-химических методов анализа
3
4.
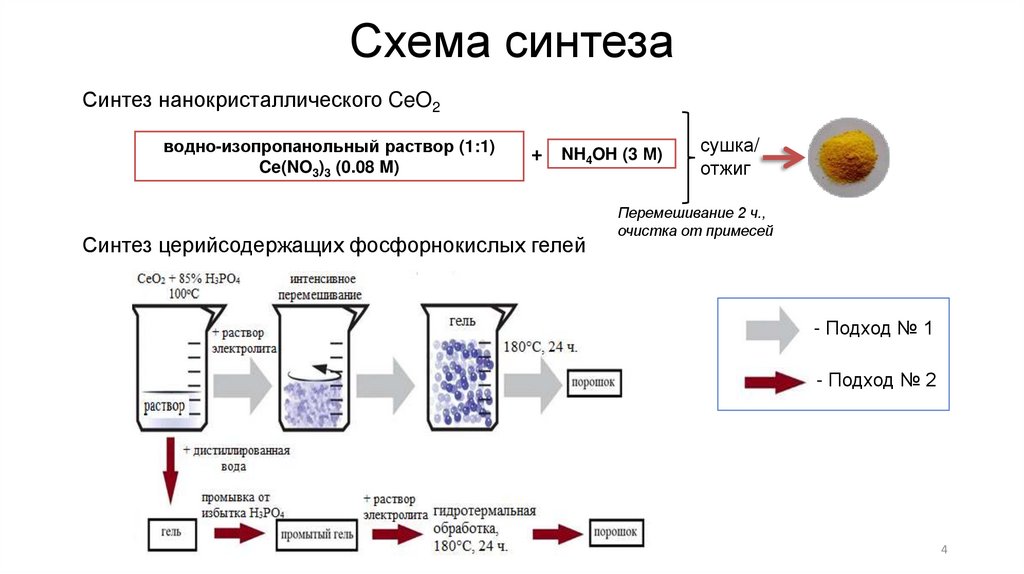
Схема синтезаСинтез нанокристаллического CeO2
водно-изопропанольный раствор (1:1)
Ce(NO3)3 (0.08 M)
+
NH4OH (3 М)
Синтез церийсодержащих фосфорнокислых гелей
сушка/
отжиг
Перемешивание 2 ч.,
очистка от примесей
- Подход № 1
- Подход № 2
4
5.
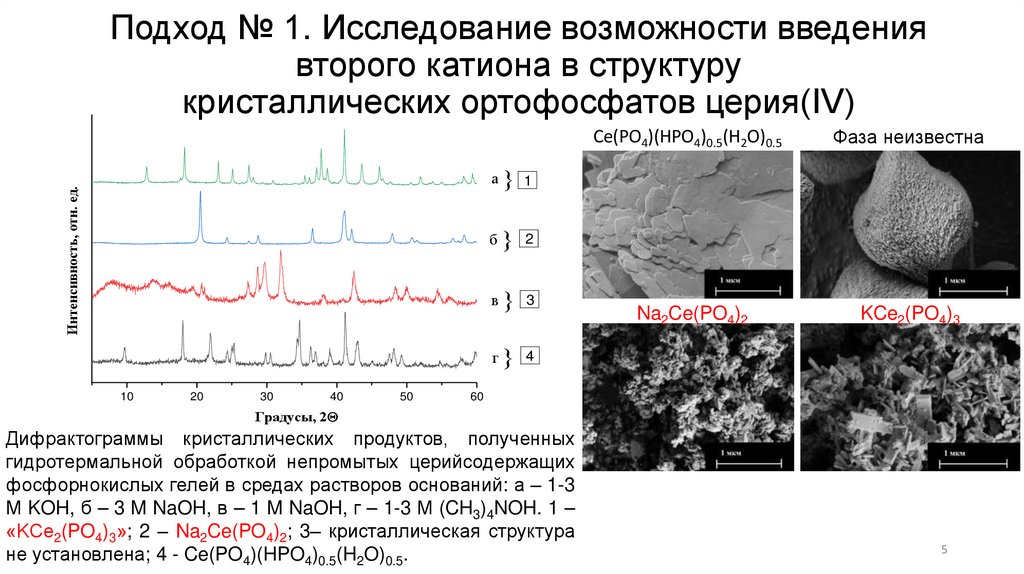
Подход № 1. Исследование возможности введениявторого катиона в структуру
кристаллических ортофосфатов церия(IV)
Ce(PO4)(HPO4)0.5(H2O)0.5
Фаза неизвестна
Na2Ce(PO4)2
KCe2(PO4)3
Интенсивность, отн. ед.
а 1
б 2
в 3
г 4
10
20
30
40
50
60
Градусы, 2
Дифрактограммы кристаллических продуктов, полученных
гидротермальной обработкой непромытых церийсодержащих
фосфорнокислых гелей в средах растворов оснований: а – 1-3
М KOH, б – 3 M NaOH, в – 1 M NaOH, г ‒ 1-3 М (CH3)4NOH. 1 –
«KCe2(PO4)3»; 2 ‒ Na2Ce(PO4)2; 3– кристаллическая структура
не установлена; 4 - Ce(PO4)(HPO4)0.5(H2O)0.5.
5
6.
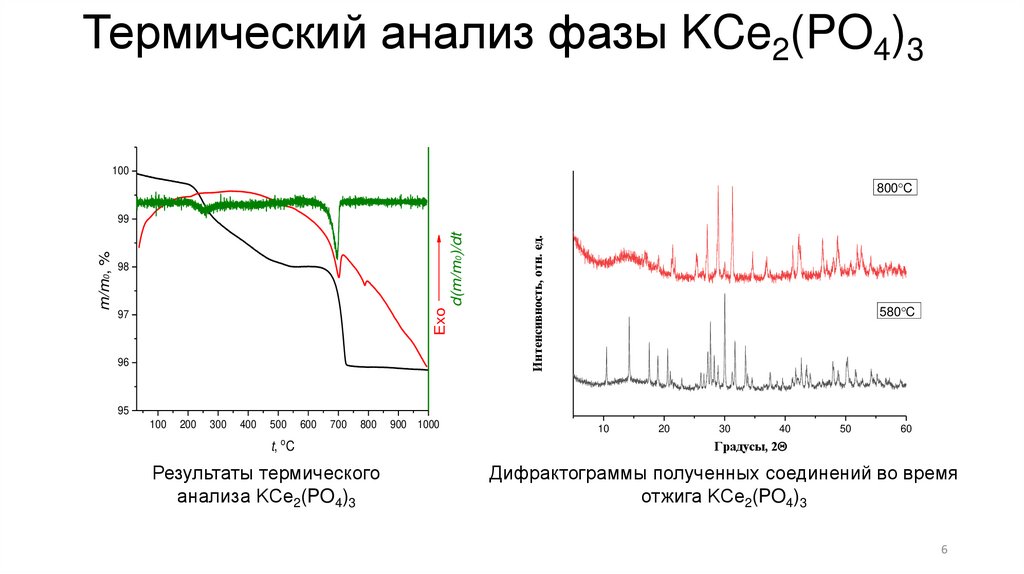
Термический анализ фазы KCe2(PO4)3100
800 C
97
96
Интенсивность, отн. ед.
d(m/m0)/dt
98
Exo
m/m0, %
99
580 C
95
100
200
300
400
500
600
700
800
o
t, C
Результаты термического
анализа KCe2(PO4)3
900 1000
10
20
30
40
50
60
Градусы, 2
Дифрактограммы полученных соединений во время
отжига KCe2(PO4)3
6
7.
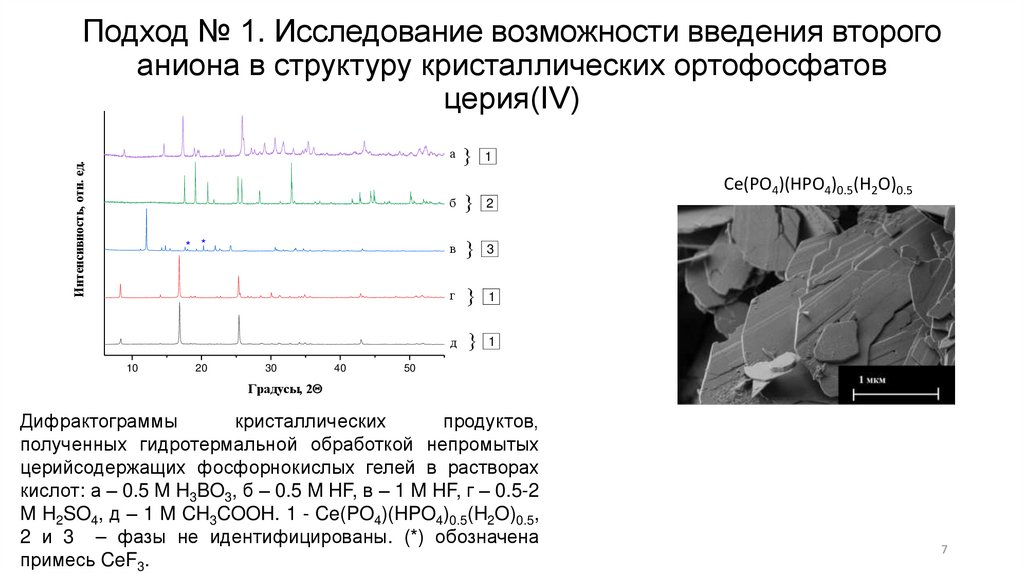
Подход № 1. Исследование возможности введения второгоаниона в структуру кристаллических ортофосфатов
церия(IV)
Интенсивность, отн. ед.
а
* *
10
20
30
40
1
б
2
в
3
г
1
д
1
Ce(PO4)(HPO4)0.5(H2O)0.5
50
Градусы, 2
Дифрактограммы
кристаллических
продуктов,
полученных гидротермальной обработкой непромытых
церийсодержащих фосфорнокислых гелей в растворах
кислот: а – 0.5 M H3BO3, б – 0.5 M HF, в – 1 M HF, г – 0.5-2
M H2SO4, д – 1 M CH3COOH. 1 - Ce(PO4)(HPO4)0.5(H2O)0.5,
2 и 3 – фазы не идентифицированы. (*) обозначена
примесь CeF3.
7
8.
Подход№
1.
Исследование
возможности
одновременного введения катиона и аниона в
структуру кристаллических ортофосфатов церия(IV)
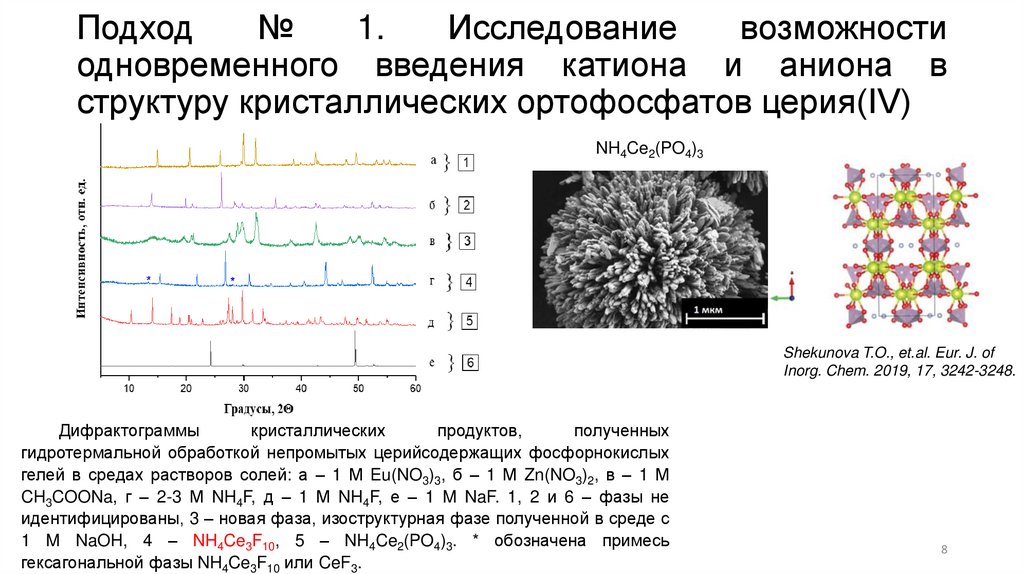
NH4Ce2(PO4)3
Shekunova T.O., et.al. Eur. J. of
Inorg. Chem. 2019, 17, 3242-3248.
Дифрактограммы
кристаллических
продуктов,
полученных
гидротермальной обработкой непромытых церийсодержащих фосфорнокислых
гелей в средах растворов солей: а – 1 М Eu(NO3)3, б – 1 М Zn(NO3)2, в – 1 М
CH3COONa, г – 2-3 М NH4F, д – 1 М NH4F, е – 1 M NaF. 1, 2 и 6 – фазы не
идентифицированы, 3 – новая фаза, изоструктурная фазе полученной в среде с
1 M NaOH, 4 – NH4Ce3F10, 5 – NH4Ce2(PO4)3. * обозначена примесь
гексагональной фазы NH4Ce3F10 или CeF3.
8
9.
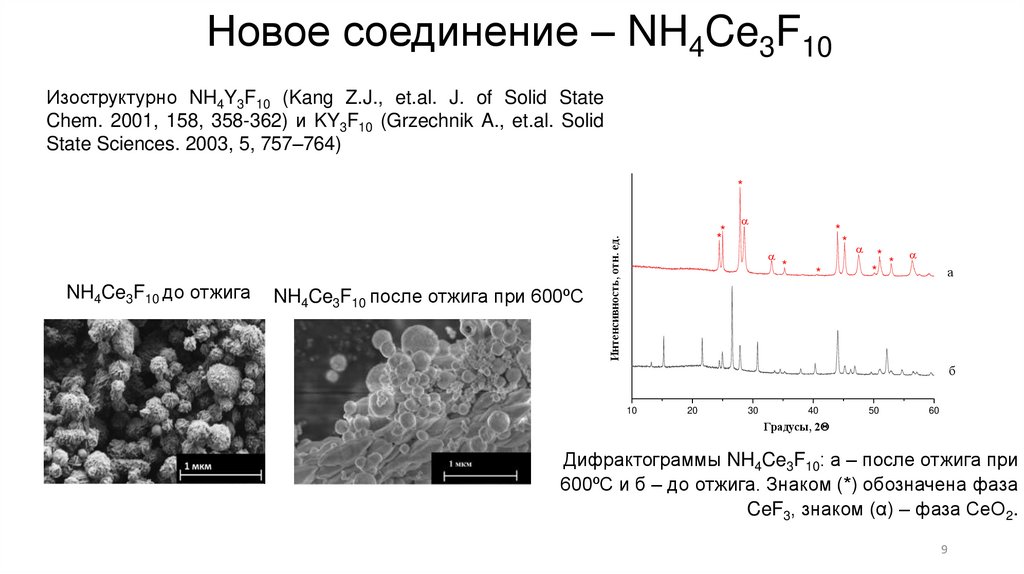
Новое соединение – NH4Ce3F10Изоструктурно NH4Y3F10 (Kang Z.J., et.al. J. of Solid State
Chem. 2001, 158, 358-362) и KY3F10 (Grzechnik A., et.al. Solid
State Sciences. 2003, 5, 757–764)
*
NH4Ce3F10 после отжига при 600ºС
Интенсивность, отн. ед.
NH4Ce3F10 до отжига
*
*
*
*
*
*
*
*
*
а
б
10
20
30
40
50
60
Градусы, 2
Дифрактограммы NH4Ce3F10: а – после отжига при
600ºС и б – до отжига. Знаком (*) обозначена фаза
CeF3, знаком (α) – фаза СеО2.
9
10.
Подход № 2. Исследование возможности введениявторого катиона в структуру кристаллических
ортофосфатов церия(IV)
*
*
Интенсивность, отн. ед.
*
*
а
*
*
*
*
б
10
20
30
40
50
60
Градусы, 2
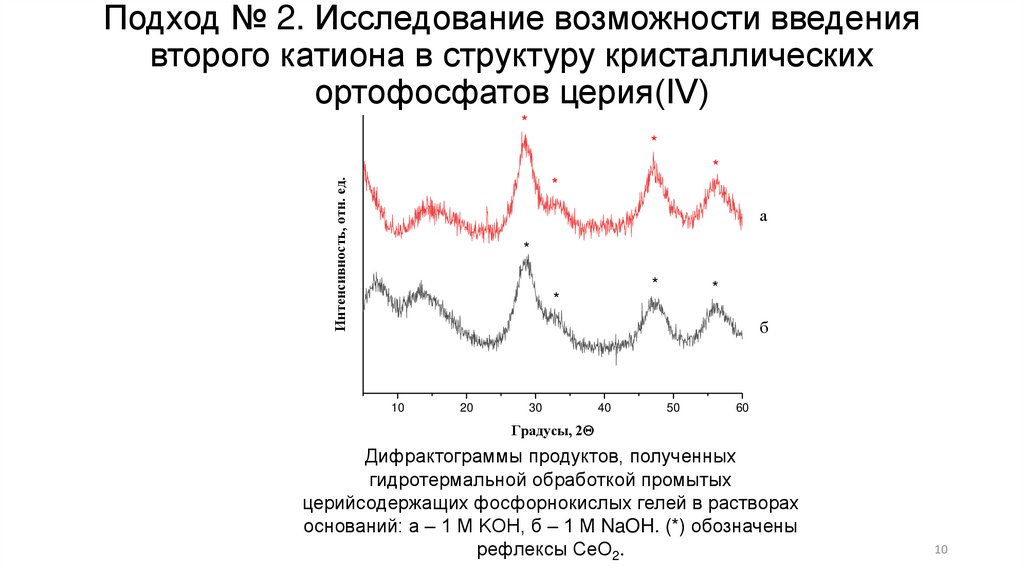
Дифрактограммы продуктов, полученных
гидротермальной обработкой промытых
церийсодержащих фосфорнокислых гелей в растворах
оснований: а – 1 M KOH, б – 1 М NaOH. (*) обозначены
рефлексы CeO2.
10
11.
Подход № 2. Исследование возможности введениявторого аниона в структуру кристаллических
ортофосфатов церия(IV)
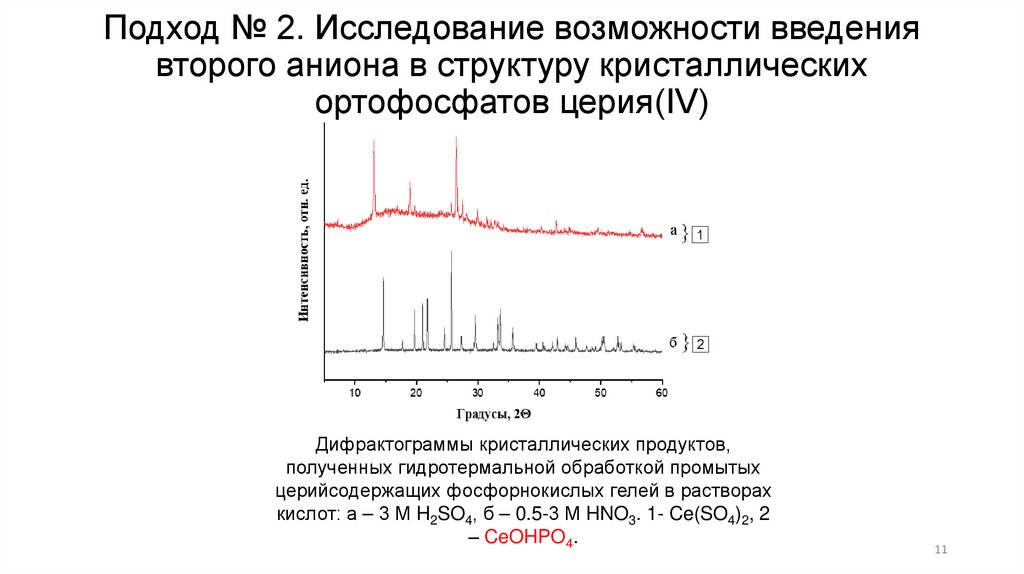
Дифрактограммы кристаллических продуктов,
полученных гидротермальной обработкой промытых
церийсодержащих фосфорнокислых гелей в растворах
кислот: а – 3 М H2SO4, б – 0.5-3 М HNO3. 1- Ce(SO4)2, 2
– CeOHPO4.
11
12.
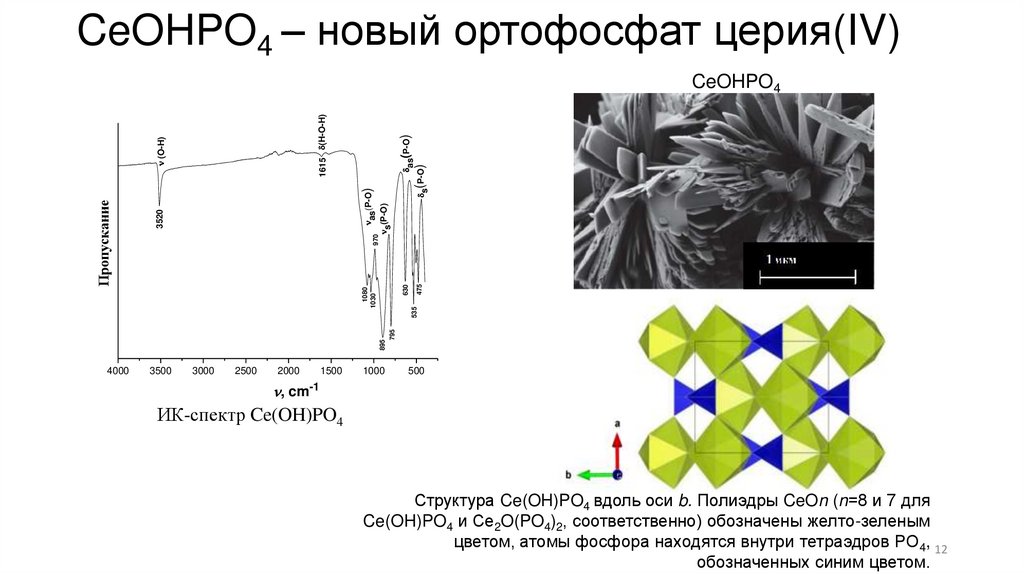
CeOHPO4 – новый ортофосфат церия(IV)s(P-O)
as(P-O)
as(P-O)
s(P-O)
475
895
795
535
1080
1030
630
970
3520
Пропускание
(O-H)
1615 (H-O-H)
CeOHPO4
4000
3500
3000
2500
2000
1500
1000
500
, cm-1
ИК-спектр Ce(OH)PO4
Структура Ce(OH)PO4 вдоль оси b. Полиэдры CeOn (n=8 и 7 для
Ce(OH)PO4 и Ce2O(PO4)2, соответственно) обозначены желто-зеленым
цветом, атомы фосфора находятся внутри тетраэдров PO4, 12
обозначенных синим цветом.
13.
Термический анализ CeOHPO496
0,0
94
d(m/m0)/dt
m/m0, %
98
Интенсивность, отн. ед.
5,0x10-4
100
92
90
100
200
300
400
500
600
700
800
-5,0x10-4
900 1000
10
20
30
40
50
60
70
Градусы, 2
t, o C
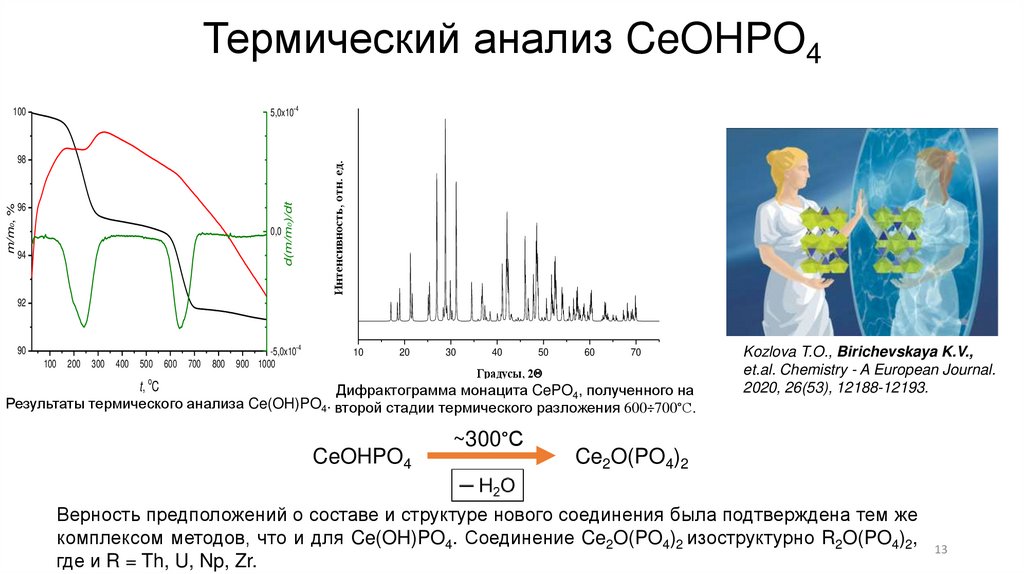
Дифрактограмма монацита CePO4, полученного на
Результаты термического анализа Ce(OH)PO4. второй стадии термического разложения 600÷700°С.
CeOHPO4
~300°С
Kozlova T.O., Birichevskaya K.V.,
et.al. Chemistry - A European Journal.
2020, 26(53), 12188-12193.
Ce2O(PO4)2
Верность предположений о составе и структуре нового соединения была подтверждена тем же
комплексом методов, что и для Ce(OH)PO4. Соединение Ce2O(PO4)2 изоструктурно R2O(PO4)2,
где и R = Th, U, Np, Zr.
13
14.
Подход № 2. Исследование возможностиодновременного введения катиона и аниона в
структуру кристаллических ортофосфатов церия(IV)
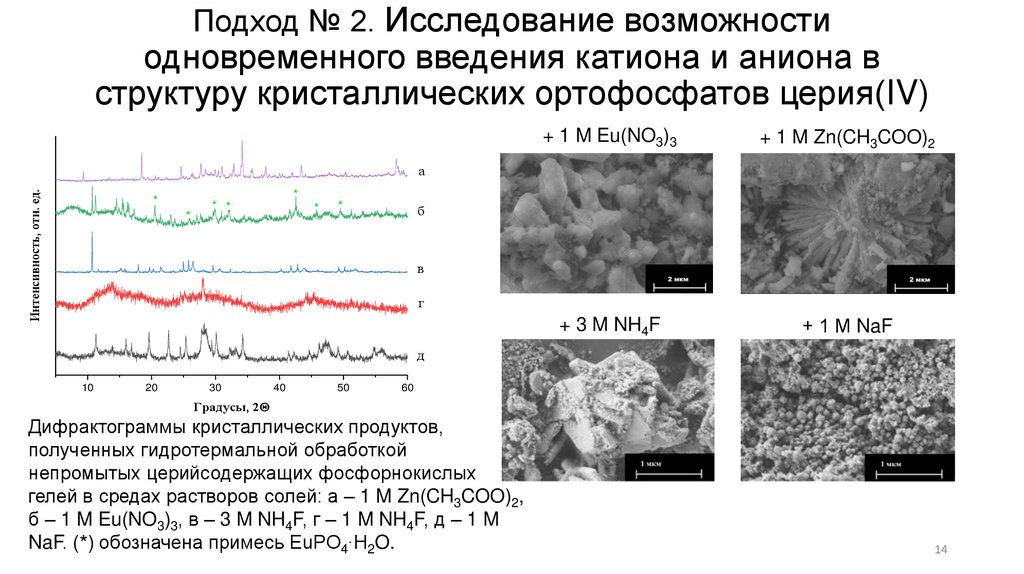
+ 1 M Eu(NO3)3
+ 1 M Zn(CH3COO)2
+ 3 M NH4F
+ 1 М NaF
Интенсивность, отн. ед.
а 1
*
*
*
* *
*
*
б
2
в
3
г
4
д
10
20
30
40
50
5
60
Градусы, 2
Дифрактограммы кристаллических продуктов,
полученных гидротермальной обработкой
непромытых церийсодержащих фосфорнокислых
гелей в средах растворов солей: а – 1 M Zn(CH3COO)2,
б – 1 M Eu(NO3)3, в – 3 M NH4F, г – 1 M NH4F, д – 1 M
NaF. (*) обозначена примесь EuPO4∙H2O.
14
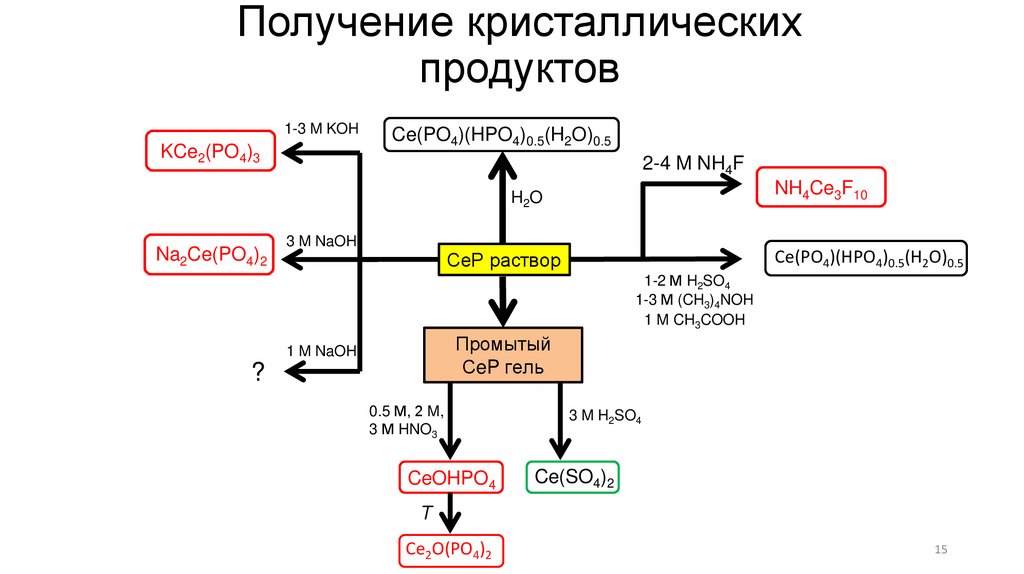
15.
Получение кристаллическихпродуктов
1-3 M KOH
KCe2(PO4)3
Ce(PO4)(HPO4)0.5(H2O)0.5
2-4 M NH4F
NH4Ce3F10
H2O
Na2Ce(PO4)2
3 M NaOH
Ce(PO4)(HPO4)0.5(H2O)0.5
СеР раствор
1-2 М H2SO4
1-3 М (CH3)4NOH
1 M CH3COOH
Промытый
СeP гель
1 M NaOH
?
0.5 М, 2 M,
3 М HNO3
CeOHPO4
3 M H2SO4
Ce(SO4)2
Т
Ce2O(PO4)2
15
16.
Выводы1.
Показано, что маршрут гидротермальной кристаллизации церийсодержащих фосфорнокислых
гелей в водных растворах электролитов (солей, кислот и оснований) в существенной степени
определяется содержанием в реакционной среде ортофосфат-анионов.
2.
Выявлено,
что
проведение
синтеза
в
реакционной
среде,
содержащей
избыток
ортофосфорной кислоты, позволяет варьировать состав получаемых однофазных продуктов
за счет изменения концентрации водного раствора электролита, используемого для
гелирования. Данный подход позволил селективно получить новые двойные ортофосфаты
церия(IV) состава KCe2(PO4)3, Na2Ce(PO4)2 и предположительно NaCe2(PO4)3.
3.
Обнаружено, что присутствие фторид-анионов в реакционной среде также определяет
фазовый состав продуктов гидротермальной обработки и может приводить к кристаллизации
фаз, не содержащих ортофосфат-анионов, даже при проведении синтеза в условиях избытка
ортофосфорной кислоты. В частности, получен новый двойной фторид аммония - церия
NH4Ce3F10, изоструктурный соединению NH4Y3F10.
4.
Показано,
что
использование
гидротермальной
обработки
очищенных
от
избытка
ортофосфорной кислоты церийсодержащих фосфорнокислых гелей также может служить
успешным подходом для получения смешанных ортофосфатов церия(IV). В случае
применения в качестве водного раствора электролита растворов азотной кислоты независимо
от концентрации (0.5-3 М) был получен смешанный ортофосфат церия(IV) Ce(OH)PO4, в ходе
отжига которого формировалось структурно ему близкое соединение состава Cе2O(PO4)2.
16




 Химия
Химия








