Похожие презентации:
Физические свойства металлов
1.
Физические свойства металлов2.
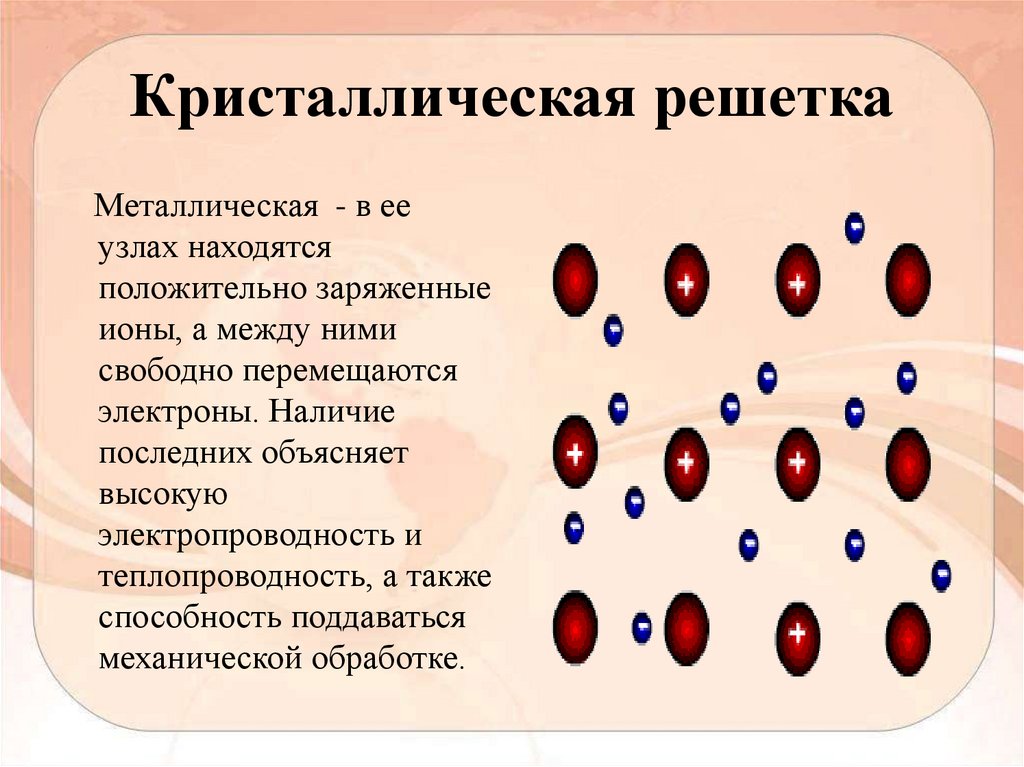
Кристаллическая решеткаМеталлическая - в ее
узлах находятся
положительно заряженные
ионы, а между ними
свободно перемещаются
электроны. Наличие
последних объясняет
высокую
электропроводность и
теплопроводность, а также
способность поддаваться
механической обработке.
3.
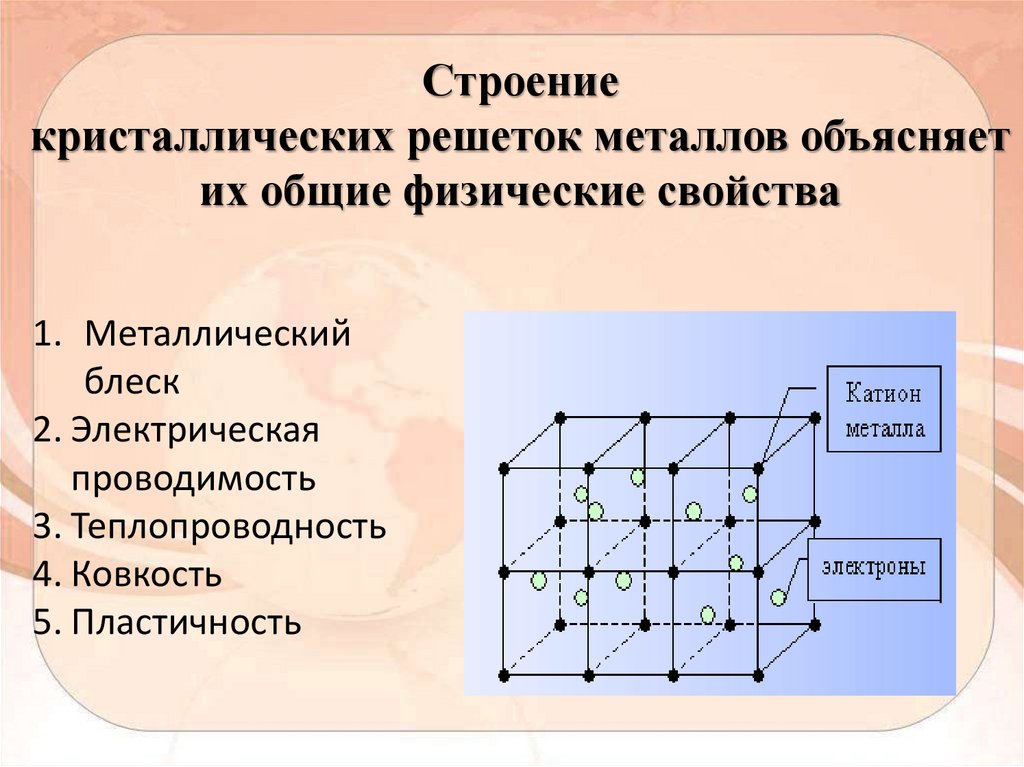
Строениекристаллических решеток металлов объясняет
их общие физические свойства
1. Металлический
блеск
2. Электрическая
проводимость
3. Теплопроводность
4. Ковкость
5. Пластичность
4.
Агрегатное состояниеВсе металлы твердые,
исключение ртуть единственный жидкий
металл.
5.
КовкостьИзготовление различных изделий из железа
в кузнице.
6.
Способность намагничиваться - железо,кобальт, никель. Находит применение при
изготовлении магнитов.
7.
ПластичностьСпособность изменять
свою форму при ударе,
прокатываться в
тонкие листы,
вытягиваться в
проволоку: золото,
серебро, медь,
алюминий. Из 1г
золота можно
вытянуть проволоку
длиной 2 км.
8.
ПластичностьВсем известна
алюминиевая фольга.
Алюминиевая фольга это тонкий слой
алюминия, в котором
отлично сохраняются
продукты питания,
кофе, чай, лекарства,
корма для
домашних животных
и многое другое.
9.
Пластичность• Оловянная фольга, которая используется
для заворачивания лучших сортов
шоколада.
10.
Металлический блескСветовые лучи падают
на поверхность
металла и
отталкиваются от неё
свободными
электронами, создавая
эффект
металлического
блеска.
11.
Металлический блескЗеркало состоит из
гладкого стекла, на
которое наносят очень
тонкий слой металла.
Часто зеркала
покрывают серебром,
потому что оно
прекрасно отражает
свет.
12.
Электропроводность• Высокая электропроводность уменьшается
в ряду металлов:
Аg Сu Аu Аl Мg Zn Fе РЬ Hg
• При нагревании уменьшается, т.к.
колебание ионов затрудняет движение
электронов.
13.
ТеплопроводностьХорошая
теплопроводность,
уменьшается в ряду
металлов:
Аg Сu Аu Аl Мg Zn
Fе РЬ Hg
14.
Все металлы делятся на две большиегруппы:
Черные металлы : Имеют темно-серый
цвет, большую плотность, высокую
температуру плавления и относительно
высокую твердость. Типичным
представителем черных металлов является
железо.
15.
Цветные металлы:• Имеют характерную
окраску: красную,
желтую, белую;
обладают большой
пластичностью, малой
твердостью,
относительно низкой
температурой
плавления.
Типичным
представителем цветных
металлов является медь.
16.
Плотность• В зависимости от своей плотности металлы
делятся на:
Легкие (плотность не более 5 г/см3 )К
легким металлам относятся: литий , натрий
, калий , магний , кальций , цезий ,
алюминий , барий.
Самый легкий металл — литий, плотность
0.534 г/см3.
17.
Плотность• Тяжелые (плотность больше 5 г/см3).К
тяжелым металлам относятся: цинк , медь ,
железо , олово , свинец , серебро , золото ,
ртуть и др.
Самый тяжелый металл — осмий ,
плотность 22,5 г/см3.
18.
Твёрдость• Металлы различаются по своей твердости:
— мягкие: режутся даже ножом (натрий ,
калий , индий );
— твердые: металлы сравниваются по
твердости с алмазом, твердость которого
равна 10. Хром — самый твердый металл,
режет стекло.
19.
Температура плавления• В зависимости от температуры плавления
металлы условно делятся на:
Легкоплавкие (температура плавления до
1539°С).
К самым легкоплавким металлам
относятся: ртуть — температура плавления
—38,9°С; галлий — температура плавления
30°С; цезий — температура плавления
28,6°С
20.
Температура плавленияТугоплавкие (температура
плавления выше 1539 С).
К тугоплавким металлам
относятся: хром — температура
плавления 1890°С; молибден —
температура плавления 2620°С;
ванадий — температура
плавления 1900°С; тантал —
температура плавления 3015°С;
и многие другие металлы.
Самый тугоплавкий металл
вольфрам — температура
плавления 3410°С.
21.
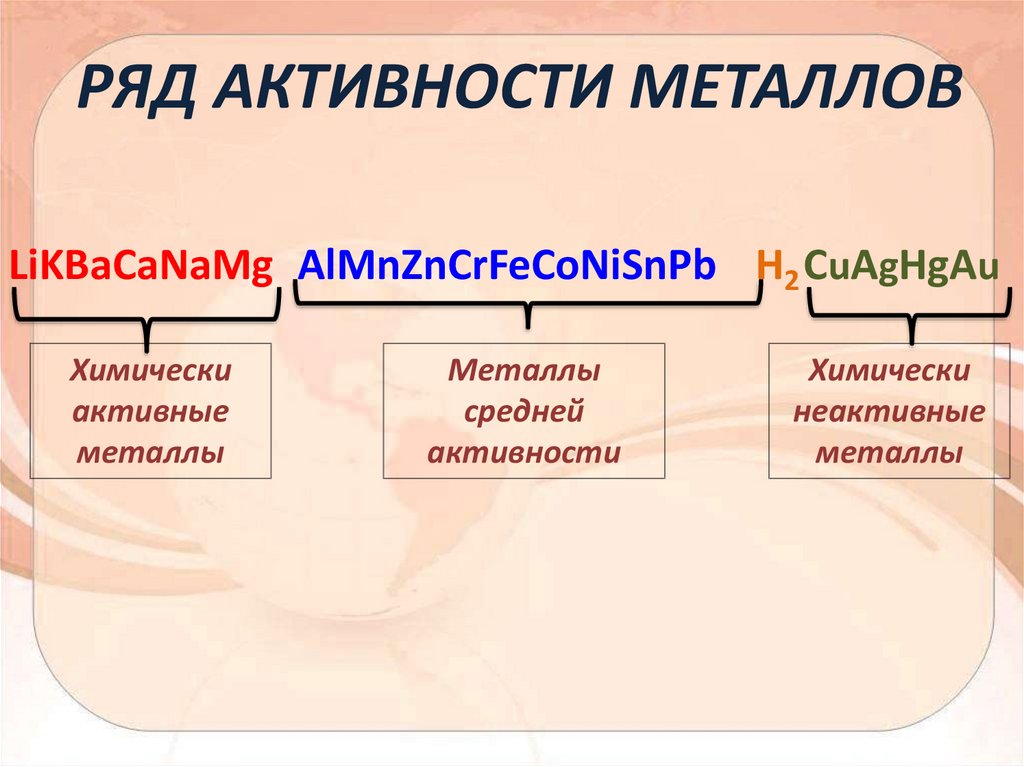
РЯД АКТИВНОСТИ МЕТАЛЛОВLiKBaCaNaMg AlMnZnCrFeCoNiSnPb H2 CuAgHgAu
Химически
активные
металлы
Металлы
средней
активности
Химически
неактивные
металлы
22.
Химически активные металлы ( до AL )Химически активные металлы в природе
встречаются только в виде солей:
Хлоридов NaCL; KCL
Сульфатов Na2SO4 10 H2O, CaSO4 2H2O
Нитратов NaNO3; KNO3
Карбонатов CaCO3 ; MgCO3
23.
Металлы средней активности(от AL до Pв)Металлы средней активности в
природе встречаются в виде оксидов
и сульфидов:
• Fe3O4
• Fe2O3* nH2O
• SnO2
• ZnS
• PbS
• …
24.
ХИМИЧЕСКИ НЕАКТИВНЫЕ И БЛАГОРОДНЫЕметаллы
Благородные металлы встречаются как в свободном
виде, так и в виде солей:
Ag2S; AgCL; PtS…
Pt
Ag
Au




















 Физика
Физика Химия
Химия








