Похожие презентации:
Система менеджмента качества. Базовые требования. Сертификация, консультационные услуги, обучение
1.
Качество менеджмента – Ваш путь к успеху!Большая ошибка казаться себе большим,
чем ты есть на самом деле,
и ценить себя меньше, чем ты стоишь.
И.В. Гете
Сертификация
Консультационные услуги
Обучение
1
2.
«Система менеджмента качества.Базовые требования».
ISO 13485:2016/ГОСТ ISO 13485-2017
По завершении семинара по курсу слушатели должны уметь:
описать требования стандарта ГОСТ ISO 13485-2017,
объяснить взаимоотношения между разделами стандарта ГОСТ ISO 13485-2017;
описать круг обязанностей внутреннего аудитора и роль внутреннего аудита в
функционировании и совершенствовании СМК,
описать в рамках цикла PDCA и процессной модели СМК цель и структуру
стандарта ГОСТ ISO 13485-2017,
планировать, проводить и отчитываться по внутреннему аудиту части СМК в
соответствии со стандартом ISO 19011:2018.
описать новые требования, сформулированные в стандарте ISO 13485:2016/
ГОСТ ISO 13485-2017
Сертификация
Консультационные услуги
Обучение
2
3. Качество – это…
«Система менеджмента качества.Базовые требования».
ISO 9000:2005
Качество – это…
Сертификация
Консультационные услуги
Обучение
3
4. ISO 9000:2015
«Система менеджмента качества. Базовые требования».ISO 9000:2015
3.5.1 Система - совокупность взаимосвязанных и взаимодействующих
элементов.
3.3.3 Менеджмент – скоординированная деятельность руководству и
управлению организацией
3.5.3 Система менеджмента - совокупность взаимосвязанных и
взаимодействующих элементов организации для разработки политик, целей
и процессов достижения этих целей.
ПРИМЕЧАНИЕ. Система менеджмента организации может включать
различные системы менеджмента, такие как
• система менеджмента качества,
• система менеджмента финансовой деятельности или
• система менеджмента охраны окружающей среды
Сертификация
Консультационные услуги
Обучение
4
5.
«Система менеджмента качества. Базовые требования».ISO 9000:2015
3.5.4 Система менеджмента качества – часть системы менеджмента
применительно к качеству.
(Система менеджмента качества - совокупность взаимосвязанных и
взаимодействующих элементов для разработки политики и целей в
области качества и достижения этих целей посредством
скоординированной деятельности (работ) по выбору ее направления и
управлению организацией (3.3.1) применительно к качеству (3.1.1)).
Сертификация
Консультационные услуги
Обучение
5
6. 3.6.2 Качество – степень соответствия совокупности присущих характеристик объекта требованиям.
«Система менеджмента качества.Базовые требования».
ISO 9000:2015
3.6.2 Качество – степень соответствия совокупности присущих характеристик
объекта требованиям.
Собственные
характеристики
Качество
Требования
(3.6.4)
3.10.1 Характеристика - отличительное свойство
3.6.4 Требование - потребность или ожидание, которое установлено,
обычно предполагается или является обязательным.
Сертификация
Консультационные услуги
Обучение
6
7.
«Система менеджмента качества.Базовые требования».
ISO 9000:2015
3.7.11. Результативность – степень реализации запланированной
деятельности и достижения запланированных результатов.
3.7.10 Эффективность – связь между достигнутым результатом и
использованными ресурсами.
3.3.2 Постоянное (непрерывное) улучшение - повторяющаяся
деятельность по улучшению результатов деятельности.
Сертификация
Консультационные услуги
Обучение
7
8.
«Система менеджмента качества.Базовые требования».
ISO 9000:2015
3.2.1 Организация – лицо или группа людей, связанные
определёнными
отношениями,
имеющие
ответственность,
полномочия и выполняющие свои функции для достижения их целей.
организация
группа
необходимых
и
работников
средств
с распределением ответственности,
полномочий и взаимоотношений
Сертификация
Консультационные услуги
Обучение
8
9.
«Система менеджмента качества.Базовые требования».
ISO 9000:2015
Владельцы
поставщик
организация
Personnel
потребитель
Personnel
Общество. Заинтересованные стороны
Сертификация
Консультационные услуги
Обучение
9
10.
«Система менеджмента качества.Базовые требования».
ISO 9000:2015
3.2.4 Потребитель – лицо или организация, которые могут
получать или получают продукцию или услугу,
предназначенные или требуемые этим лицом или
организацией
ПРИМЕРЫ – Клиент, заказчик, конечный пользователь, розничный
продавец , бенефициар и покупатель.
ПРИМЕЧАНИЕ. Потребитель может быть внутренним или внешним
по отношению к организации.
3.2.5 Поставщик – организация, предоставляющая
продукцию или услугу
ПРИМЕРЫ – Производитель, дистрибьютер, предприятие розничный
торговли или продавец продукции или услуг
Сертификация
Консультационные услуги
Обучение
10
11.
«Система менеджмента качества.Базовые требования».
ISO 9000:2015
Заинтересованная сторона лицо, или группа,
заинтересованные в деятельности
или успехе организации (3.3.1)
ПРИМЕРЫ – Потребители
(3.3.5), владельцы, работники
организации, поставщики (3.3.6),
банкиры, ассоциации, партнеры
или общество.
ПРИМЕЧАНИЕ. Группа может
состоять из организации, ее
части или из нескольких
организаций.
Сертификация
Примеры заинтересованных
сторон :
Внешние:
потребители
поставщики, в том числе –
подрядчики
инвесторы
общественность
профсоюзы
общественные организации
надзорные органы
Внутренние:
администрация
персонал
профсоюзная организация
Консультационные услуги
Обучение
11
12.
«Система менеджмента качества.Базовые требования».
ISO 9000:2005
ISO 9000:2015
Предисловие
Международный стандарт ISO 9000:2005 был разработан Техническим
комитетом ISO/ТК 176 «Менеджмент качества и обеспечение качества».
Подкомитет ПК1 «Понятия и терминология».
ГОСТ ISO 13485-2017
Предисловие
Стандарт был разработан Федеральным государственным унитарным
предприятием "Всероссийский научно-исследовательский институт
стандартизации и сертификации в машиностроении" (ВНИИНМАШ)
Сертификация
Консультационные услуги
Обучение
12
13. Другие специфические системы менеджмента в организации
«Система менеджмента качества.Базовые требования ГОСТ ISO 13485-2017
».
Другие специфические системы менеджмента в организации
Системы экологического менеджмента - по стандарту ISO 14001:2015;
Системы менеджмента профессиональной безопасности и охраны труда - по
стандарту ISO 45001:2018;
Системы менеджмента качества в автомобильной промышленности и
организациях, производящих соответствующие запасные части - по стандарту IATF ISO
16949;
Системы менеджмента безопасности пищевых продуктов - по стандарту ISO
22000;
Системы менеджмента информационной безопасности - по стандарту ISO 27001;
Системы менеджмента качества в аэрокосмической промышленности – по
стандарту EN 9100;
Системы менеджмента качества в нефтяной, нефтехимической и газовой отраслях
промышленности - по стандарту ISO/ ТУ 29001;
Системы менеджмента качества в органах местного самоуправления - по
стандарту IWA 4
Сертификация
Консультационные услуги
Обучение
13
14.
«Система менеджмента качества.Базовые требования».
ГОСТ ISO 13485-2017
3.2.1 Организация - группа работников и необходимых средств с
распределением ответственности, полномочий и
взаимоотношений.
организация
группа
необходимых
и
работников
средств
с распределением ответственности,
полномочий и взаимоотношений
Сертификация
Консультационные услуги
Обучение
14
15.
«Система менеджмента качества.Базовые требования».
ГОСТ ISO 13485-2017
Владельцы
поставщик
организация
Personnel
потребитель
Personnel
Общество. Заинтересованные стороны
Сертификация
Консультационные услуги
Обучение
15
16.
«Система менеджмента качества.Базовые требования».
ГОСТ ISO 13485-2017
3.2.4 Потребитель - организация или лицо, получающие
продукцию)
ПРИМЕРЫ – Клиент, заказчик, конечный пользователь, розничный
торговец, бенефициар (рантье, владелец земельного участка) и
покупатель.
ПРИМЕЧАНИЕ. Потребитель может быть внутренним или внешним по
отношению к организации.
3.2.5 Поставщик - организация или лицо, предоставляющие
продукцию
ПРИМЕРЫ – Производитель, оптовик, предприятие розничный торговли
или продавец продукции, исполнитель услуги, поставщик информации.
ПРИМЕЧАНИЕ 1. Поставщик может быть внутренним или внешним по
отношению к организации.
ПРИМЕЧАНИЕ 2. В контрактной ситуации поставщика иногда называют
«подрядчиком».
Сертификация
Консультационные услуги
Обучение
16
17.
«Система менеджмента качества.Базовые требования».
ГОСТ ISO 13485-2017
3.2.3 Заинтересованная сторона
- лицо, или группа,
заинтересованные в деятельности
или успехе организации (3.3.1)
ПРИМЕРЫ – Потребители
(3.3.5), владельцы, работники
организации, поставщики (3.3.6),
банкиры, ассоциации, партнеры
или общество.
ПРИМЕЧАНИЕ. Группа может
состоять из организации, ее
части или из нескольких
организаций.
Сертификация
Примеры заинтересованных
сторон :
Внешние:
потребители
поставщики, в том числе –
подрядчики
инвесторы
общественность
профсоюзы
общественные организации
надзорные органы
Внутренние:
администрация
персонал
профсоюзная организация
Консультационные услуги
Обучение
17
18.
3.1 пояснительное уведомление (advisory notice): Уведомление,выпущенное организацией после поставки медицинского изделия,
содержащее дополнительную информацию и/или рекомендации о том,
какие действия должны быть предприняты при:
- применении медицинского изделия;
- модификации медицинского изделия;
- возврате медицинского изделия организации, которая его поставила;
- утилизации медицинского изделия.
Примечание - Выпуск пояснительного уведомления может требоваться в
соответствии с применимыми регулирующими требованиями.
Сертификация
Консультационные услуги
Обучение
19.
3.2 уполномоченный представитель (authorized representative): Физическое или юридическоелицо, которое определено законодательством страны или региона, получившее письменное
назначение от изготовителя действовать от его имени для выполнения определенных задач в
отношении обязанностей изготовителя, установленных законодательством конкретной страны
или региона.
[GHTF/SG1/N055:2009, пункт 5.2]
3.3 клиническая оценка (clinical evaluation): Анализ и оценивание клинических данных в
отношении медицинского изделия с целью верификации безопасности и функциональных
характеристик изделия при его клиническом применении, как предназначено изготовителем.
[GHTF/SG5/N4:2010, раздел 4]
3.4 претензия (complaint): Письменное, электронное или устное сообщение о недостатках,
связанных с идентификацией, качеством, сроком службы, надежностью, безопасностью или
функциональными характеристиками медицинского изделия, вышедшего из-под управления
организацией, а также в отношении связанного с ним обслуживания, которое влияет на
функциональные характеристики таких медицинских изделий.
Примечание - Это определение "претензии" отличается от определения, данного в ISO
9000:2015.
Сертификация
Консультационные услуги
Обучение
20.
3.11 медицинское изделие (medical device): Инструмент, аппарат, прибор, устройство,оборудование, имплантат, in vitro реагент, программное обеспечение, материал или иные
подобные или связанные с ними изделия, предназначенные изготовителем для применения к
человеку по отдельности или в комбинации:
- диагностики, профилактики, мониторинга, лечения или облегчения заболеваний;
- диагностики, мониторинга, лечения, облегчения или компенсации последствий травмы;
- исследования, замещения или изменения анатомического строения или физиологических
процессов;
- жизнеобеспечения или поддержания жизненных функций;
- управления зачатием;
- дезинфекции медицинских изделий;
- получения информации посредством исследования in vitro проб, взятых из тела человека,
а также не достигающие своего первичного предназначенного воздействия на организм
человека за счет фармакологических, иммунологических или метаболических средств, но
функции которых могут поддерживаться такими средствами.
[GHTF/SG1/N071:2012, пункт 5.1]
Примечание - Некоторые изделия в отдельных юрисдикциях могут рассматриваться как
медицинские, но в их отношении еще не выработан единый подход. Такими изделиями могут
быть:
- дезинфицирующие вещества;
- вспомогательные средства для лице ограниченными возможностями;
- изделия, включающие ткани животных или человека;
- изделия для экстракорпорального оплодотворения и репродуктивных технологий.
Сертификация
Консультационные услуги
Обучение
21.
3.12 семейство медицинских изделий (medical device family): Группамедицинских изделий, производимых одной и той же или для одной и той
же организации и имеющих одинаковую базовую конструкцию и
функциональные характеристики в отношении безопасности,
предназначенного применения и функционирования.
3.13 оценивание функциональных характеристик (performance
evaluation): Оценка и анализ данных для установления или проверки
способности изделия для диагностики in vitroдостигать своего назначения.
3.14 послепродажное наблюдение (post-market surveillance):
Систематический процесс сбора и анализа опыта, полученного в отношении
медицинских изделий, выпущенных на рынок.
3.16 закупаемая продукция (purchased product): Продукция,
предоставленная какой-либо стороной, находящейся вне системы
менеджмента качества организации.
Примечание - Предоставление продукции не всегда сопровождается
коммерческими или финансовыми соглашениями.
Сертификация
Консультационные услуги
Обучение
22.
3.17 риск (risk): Сочетание вероятности причинения вреда и тяжести этоговреда.
[ISO 14971:2007, пункт 2.16]
Примечание - Это определение "риска" отличается от определения,
данного в ISO 9000:2015.
3.18 менеджмент риска (risk management): Систематическое применение
политики, процедур и практических методов менеджмента для решения
задач анализа, оценивания, управления и мониторинга риска. [ISO
14971:2007, пункт 2.22]
Сертификация
Консультационные услуги
Обучение
23. Большинство моделей систем управления строится на модели PDCA, введенной Шуxaртом и Демингом. Модель основана на концепции
«Система менеджмента качества.Базовые требования».
ГОСТ ISO 13485-2017
Большинство моделей систем управления строится на модели PDCA, введенной Шуxaртом и
Демингом. Модель основана на концепции непрерывного совершенствования.
ГОСТ ISO 13485-2017
0.2 Процессный подход
… ко всем процессам СМК может применяться
методология, известная как цикл "Plan-Do-Check-Act"
(PDCA). Цикл PDCA можно кратко описать так:
PLAN
ACT
УЛУЧШЕНИЕ
CHECK
Сертификация
DO
Планирование (plan): разработайте цели и
процессы, необходимые для достижения
результатов в соответствии с требованиями
потребителей и политикой организации;
Осуществление (do): внедрите процессы;
Проверка (check): постоянно контролируйте и
измеряйте процессы и продукцию в сравнении с
политикой, целями и требованиями на продукцию и
сообщайте о результатах;
Действие (act): предпринимайте действия по
постоянному улучшению показателей процессов.
Консультационные услуги
"
Обучение
23
24.
«Система менеджмента качества.Базовые требования».
ISO 9000:2015
Высшее руководство - лицо или группа
работников, осуществляющих направление
деятельности и управление организацией на
высшем уровне
Сертификация
Консультационные услуги
Обучение
24
25. ПРИНЦИПЫ МЕНЕДЖМЕНТА КАЧЕСТВА
«Система менеджмента качества.Базовые требования».
ISO 9000:2015
ПРИНЦИПЫ МЕНЕДЖМЕНТА КАЧЕСТВА
а) Ориентация на потребителя
Организации зависят от своих потребителей, и поэтому им
следует понимать их текущие и будущие потребности,
выполнять их требования и стремиться превзойти их
ожидания.
b) Лидерство руководителя
Руководители обеспечивают единство цели и направления
деятельности организации. Им следует создавать и
поддерживать внутреннюю среду, в которой работники могут
быть полностью вовлечены в решение задач организации.
Сертификация
Консультационные услуги
Обучение
25
26. Ориентация на потребителя
• Организации зависят от своих потребителей, и поэтомудолжны понимать их текущие и будущие потребности,
выполнять их требования и стремиться превзойти их
ожидания.
«Нам совершенно недостаточно иметь потребителя,
который просто удовлетворен… Прибыль в бизнесе
приходит от постоянных покупателей, потребителей,
которые хвастаются вашим продуктом или услугой и
которые приводят к вам своих друзей»
Э. Деминг
Сертификация
Консультационные услуги
Обучение
27.
«Система менеджмента качества.Базовые требования».
ISO 9000:2015
c) Лидерство.
Вовлечение работников
Работники всех уровней составляют основу организации, и
их полное вовлечение дает возможность организации с
выгодой использовать их способности.
Организационная структура - распределение
ответственности, полномочий и взаимоотношений между
работниками.
Сертификация
Консультационные услуги
Обучение
27
28.
«Система менеджмента качества.Базовые требования».
ISO 9000:2015
d) Процессный подход
Желаемый результат достигается
эффективнее, когда деятельностью и
соответствующими ресурсами управляют
как процессом.
Сертификация
Консультационные услуги
Обучение
28
29. 3.4.1 Процесс (ISO 9000:2015 ) - совокупность взаимосвязанных и взаимодействующих видов деятельности, преобразующая входы в
«Система менеджмента качества.Базовые требования».
ISO 9000:2015
3.4.1 Процесс (ISO 9000:2015 ) - совокупность взаимосвязанных и
взаимодействующих видов деятельности, преобразующая входы в выходы.
Любая деятельность или комплекс деятельности, управляемая и использующая
ресурсы для преобразования входов в выходы, рассматривается как процесс.
УПРАВЛЯЮЩИЕ ВОЗДЕЙСТВИЯ
ВХОДЫ
ПРОЦЕСС
ИЗМЕРЕНИЕ
ВЫХОДЫ
ИЗМЕРЕНИЕ
Ресурсы
Сертификация
Консультационные услуги
Обучение
29
30.
«Система менеджмента качества.Базовые требования».
ISO 9000:2015
Виды процессов в
организации
Основной процесс
организации (бизнеспроцесс) - полный цикл
получения конечного
результата – продукции.
Обеспечивающие
(вспомогательные)
процессы - циклы
управления ресурсами
организации.
Сертификация
Выход одного процесса образует
непосредственно вход следующего.
Процессный подход - применение в
организации системы процессов наряду
с их идентификацией и
взаимодействием, а также менеджмент
процессов.
Преимущество процессного подхода
состоит в непрерывности управления,
которое он обеспечивает на стыке
между отдельными процессами в
рамках системы процессов, а также при
их комбинации и взаимодействии.
Консультационные услуги
Обучение
30
31. Описание процесса
«Система менеджмента качества.Базовые требования».
ISO 9000:2015
Описание процесса
Руководитель процесса
(ответственный за процесс,
владелец процесса,
«хозяин» процесса) –
должностное лицо,
наделенное
соответствующими
полномочиями и несущее
ответственность за
организацию, надлежащее
функционирование и
результаты процесса.
Сертификация
Руководитель процесса
идентифицирует подпроцессы и
вспомогательные процессы,
необходимые для функционирования
руководимого им процесса.
Для каждого процесса определяют:
• внутренних или внешних потребителей
каждого процесса и их требования ;
• характеристики намеренных и
ненамеренных результатов процессов
(выходы процессов);
• входы процессов;
• управляющие воздействия;
• необходимые ресурсы, в т.ч. - персонал;
• необходимую документацию.
Консультационные услуги
Обучение
31
32. РЕЗУЛЬТАТИВНОСТЬ ПРОЦЕССА
«Система менеджмента качества.Базовые требования».
ISO 9000:2015
РЕЗУЛЬТАТИВНОСТЬ ПРОЦЕССА
Результативность – степень
реализации запланированной
деятельности и достижения
запланированных результатов.
Полученные
Button
результаты
Результативность
процесса
=
Запланированные
Button
результаты
Сертификация
Консультационные услуги
Обучение
32
33. Блок-схема управления процессом
«Система менеджмента качества.Базовые требования».
ISO 9000:2015
Идентификация
процесса
Блок-схема
Установление
критериев
оценки процесса
управления
Измерение
процесса
процессом
нет
да
Контроль
(сравнение)
Корректирующие
действия
нет
Результативность
корректирующих
действий
да
Эксплуатация и
мониторинг
Сертификация
Консультационные услуги
Обучение
33
34. Примерная структура процессов СМК промышленного предприятия
Последовательность и взаимодействие процессов СМКУправление политикой и
целями в области качества
Анализ СМК со стороны
руководства
Планирование СМК
Процессы управления ресурсами
Управление
инфраструктурой
Управление
персоналом
Процессы управления
документацией и записями
Управление производственной средой
Управление
документацией
Управление
закупками
Управление
производственным
оборудованием и СИ
Требования
потребителя
к продукции
Процессы управления производственной деятельностью
Изучение и анализ
требований
потребителя
Планирование
производства
Верификация
закупленной
продукции
Управление
записями
Производство
Продукция
Процессы ответственности руководства области качества
Процессы измерения, анализа и улучшения
Оценка удовлетворенности
потребителей
Мониторинг и измерение
процессов
Мониторинг и измерение
продукции
Предупреждающие действия
Сертификация
Консультационные услуги
Внутренний аудит
Управление несоответствующей
продукцией
Корректирующие действия
Обучение
35.
4 Система менеджмента качества4.1 Общие требования
4.1.2 Организация должна:
a) определять процессы, необходимые для системы менеджмента
качества, и их применение в организации с учетом ролей, принятых на
себя;
b) применять риск-ориентированный подход к управлению
соответствующими процессами, необходимыми для системы
менеджмента качества;
c) определять последовательность и взаимодействие этих процессов.
4.1.3 Для каждого процесса в системе менеджмента качества
организация должна:
a) определять критерии и методы, необходимые для обеспечения
результативности, как при осуществлении, так и при управлении этими
процессами;
b) обеспечивать наличие ресурсов и информации, необходимых для
поддержки функционирования и мониторинга этих процессов;
c) осуществлять действия, необходимые для достижения
запланированных результатов и поддержания результативности этих
процессов
Сертификация
Консультационные услуги
Обучение
35
36.
d) осуществлять мониторинг, измерение, если целесообразно, и анализэтих процессов;
e) определять и поддерживать в рабочем состоянии записи для
демонстрации соответствия требованиям настоящего стандарта и
применимым регулирующим требованиям (4.2.5).
4.1.4 Организация должна осуществлять менеджмент этих процессов
системы менеджмента качества в соответствии с требованиями
настоящего стандарта и применимыми регулирующими требованиями.
Изменения, вносимые в эти процессы, должны:
4.1.5 Если организация решает передать на сторону выполнение какого-либо
процесса, влияющего на соответствие продукции требованиям, она должна
осуществлять мониторинг и обеспечивать со своей стороны управление такими
процессами. Организация сохраняет ответственность за соответствие такого
процесса требованиям настоящего стандарта, требованиям потребителя и
применимым регулирующим требованиям. Управление должно быть
пропорционально риску, связанному с возможностью внешней стороны
обеспечить соответствие требованиям пункта 7.4. Управление должно включать
письменные соглашения по качеству.
Сертификация
Консультационные услуги
Обучение
36
37.
4.2 Требования к документации4.2.1 Общие положения
4.2.2 Руководство по качеству
4.2.3 Файл медицинского изделия
4.2.4 Управление документами
Для определения необходимых средств управления должна быть разработана
документированная процедура, предусматривающая:
a) анализ и официальное одобрение документов с точки зрения их адекватности до их
выпуска;
b) анализ и актуализацию, по мере необходимости, и повторное официальное
одобрение документов;
c) обеспечение идентификации изменений и статуса пересмотра документов;
d) обеспечение наличия соответствующих версий документов в местах их применения;
e) обеспечение сохранения документов четкими и легко идентифицируемыми;
f) обеспечение идентификации документов внешнего происхождения, определенных
организацией как необходимые для планирования и функционирования системы
менеджмента качества, и управление их рассылкой;
g) предотвращение порчи или потери документов;
h) предотвращение непреднамеренного использования устаревших документов и
применение соответствующей идентификации к ним.
Сертификация
Консультационные услуги
Обучение
37
38. Обязательные документированные процедуры по ГОСТ ISO 13485-2017
«Система менеджмента качества.Базовые требования».
ГОСТ ISO 13485-2017 СМК Требования.
Обязательные документированные процедуры
по ГОСТ ISO 13485-2017
1.
2.
3.
4.
Управление документацией - п. 4.2.3
Управление записями - п. 4.2.4
Инфраструктура- п.6.3
Соответствие закупленной продукции установленным требованиям к
закупке- п.7.4.1
5. Наличие документированных процедур, рабочих инструкций измеренияп.7.5.1
6. Валидация процессов стерилизации- п.7.5.2
7. Внутренние аудиты - п.8.2.2
8. Управление несоответствующей продукцией - п. 8.3
9. Корректирующие действия - п. 8.5.2
10. Предупреждающие действия - п. 8.5.3
Сертификация
Консультационные услуги
Обучение
38
39. Движение документов
«Система менеджмента качества.Базовые требования».
ГОСТ ISO 13485-2017 СМК Требования.
Движение документов
Руководящие
документы
Высший
уровень
Средний
уровень
Отчетные,
информационные
документы
Низовой
уровень
Проекты документов.
Информационные
документы
Сертификация
Консультационные услуги
Обучение
39
40.
4.2.5 Управление записямиЗаписи должны поддерживаться в рабочем состоянии для предоставления свидетельств
соответствия требованиям и результативного функционирования системы менеджмента
качества. Организация должна документировать процедуры для определения средств
управления, необходимых для идентификации, хранения, безопасности и целостности,
восстановления, включая определения сроков хранения, и порядка изъятия записей.
Организация должна определить и внедрить методы защиты конфиденциальной информации о
здоровье, содержащейся в записях, в соответствии с применимыми регулирующими
требованиями.
Записи должны оставаться четкими, легко идентифицируемыми и восстанавливаемыми.
Изменения в записях должны быть идентифицируемыми.
Организация должна хранить записи в течение, по крайней мере, срока службы медицинского
изделия, определенного организацией, но не менее двух лет с момента выпуска медицинского
изделия организацией или в соответствии с применимыми регулирующими требованиями.
Сертификация
Консультационные услуги
Обучение
40
41. Цикл PDСA главы 5 ГОСТ ISO 13485-2017
«Система менеджмента качества.Базовые требования».
ГОСТ ISO 13485-2017 СМК Требования.
Цикл PDСA главы 5 ГОСТ ISO 13485-2017
5.1 Обязательства руководства
5.2 Ориентация на потребителя
5.3 Политика в области качества
5.4 Планирование СМК
PLAN
5.6 Анализ со
стороны
руководства
ACT
Непрерывное
улучшение
DO
5.5 Ответственность,
полномочия и
информирование
CHECK
8 Измерение,
анализ, улучшение
Сертификация
Консультационные услуги
Обучение
41
42.
5 Ответственность руководства5.1 Обязательства руководства
5.2 Ориентация на потребителя
5.3 Политика в области качества
5.4 Планирование
5.4.1 Цели в области качества
5.4.2 Планирование системы менеджмента качества
5.5 Ответственность, полномочия и обмен информацией
5.5.1 Ответственность и полномочия
5.5.2 Представитель руководства
5.5.3 Внутренний обмен информацией
5.6 Анализ со стороны руководства
5.6.1 Общие положения
5.6.2 Входные данные для анализа
5.6.3 Выходные данные для анализа
Сертификация
Консультационные услуги
Обучение
42
43.
5.3 Политика вобласти качества
5.4.1 Цели в
области качества
5.4.2 Планирование
СМК
7.1 Планирование
производства
продукции
7.3.1 Планирование
проектирования и
разработки
8.2.2 (Планирование
внутренних проверок)
Сертификация
Консультационные услуги
Обучение
43
44.
«Система менеджмента качества.Базовые требования».
ГОСТ ISO 13485-2017 СМК Требования.
Положение Политики в
области качества
Цель для предприятия
Цель для
участка
Мы постоянно
повышаем качество
наших услуг
Снижение
числа жалоб
через год на 20%
Снижение числа жалоб
через год на 40%
Анализ СМК
Мероприятия по улучшению
Сертификация
Консультационные услуги
Обучение
44
45.
6 Менеджмент ресурсов6.1 Обеспечение ресурсами
6.2 Человеческие ресурсы
6.3 Инфраструктура
6.4 Производственная среда и контроль загрязнения
6.4.1 Производственная среда
6.4.2 Контроль загрязнения
Сертификация
Консультационные услуги
Обучение
45
46.
«Система менеджмента качества.Базовые требования».
ГОСТ ISO 13485-2017 СМК Требования.
7.1 Планирование
производства продукции
7.2 Процессы, связанные
с потребителем
7.3 Проектирование и
разработка
PLAN
8.3 Управление
несоответствующей
продукцией
8.5.2 Корректирующие
действия
8.5.3 Предупреждающие
действия
ACT
УЛУЧШЕНИЕ
DO
7.4 Закупки
7.5 Обеспечение
производства и
обслуживания
CHECK
7.6 Управление
оборудованием для
монторинга и измерений
8.2.4 Мониторинг и
измерение продукции
Сертификация
Консультационные услуги
Обучение
46
47.
7 Процессы жизненного цикла продукции7.1 Планирование процессов жизненного цикла продукции
7.2 Процессы, связанные с потребителями
7.2.1 Определение требований, относящихся к продукции
7.2.2 Анализ требований, относящихся к продукции
7.2.3 Связь с потребителями
Сертификация
Консультационные услуги
Обучение
47
48. Цикл PDCA для п.7.3 стандарта ГОСТ ISO 13485-2017
«Система менеджмента качества.Базовые требования».
ГОСТ ISO 13485-2017 СМК Требования.
Цикл PDCA для п.7.3 стандарта ГОСТ ISO 13485-2017
7.3.1 Планирование
проектирования и
разработки
7.3.7 Управление
изменениями проекта
и разработки
7.3.2 Входные
данные для
проектирования и
разработки
PLAN
ACT
УЛУЧШЕНИЕ
CHECK
7.3.3 Выходные
данные
проектирования
и разработки
DO
7.3.4 Анализ
проекта и
разработки
7.3.5 Верификация
проекта и разработки
7.3.6 Валидация
проекта и разработки
Сертификация
Консультационные услуги
Обучение
48
49.
7.3 Проектирование и разработка7.3.1 Общие положения
7.3.2 Планирование проектирования и разработки
7.3.3 Входные данные проектирования и разработки
7.3.4 Выходные данные проектирования и разработки
7.3.5 Анализ проектирования и разработки
7.3.6 Верификация проектирования и разработки
7.3.7 Валидация проектирования и разработки
7.3.8 Передача проекта и разработки
7.3.9 Управление изменениями проектирования и разработки
7.3.8 Передача проекта и разработки
7.3.9 Управление изменениями проектирования и разработки
7.3.10 Файлы проектирования и разработки
Сертификация
Консультационные услуги
Обучение
49
50.
7.4 Закупки7.4.1 Процесс закупок
7.4.2 Информация по закупкам
7.4.3 Верификация закупаемой продукции
7.5 Производство и обслуживание
7.5.1 Управление производством и обслуживанием
7.5.2 Чистота продукции
7.5.3 Деятельность по монтажу
7.5.4 Деятельность по обслуживанию
7.5.5 Специальные требования к стерильным медицинским изделиям
7.5.6 Валидация процессов производства и обслуживания
7.5.7 Специальные требования к валидации процессов стерилизации и
системам барьеров стерильности
7.5.8 Идентификация
Сертификация
Консультационные услуги
Обучение
50
51. Цикл PDCA для главы 8 ГОСТ ISO 13485-2017
«Система менеджмента качества.Базовые требования».
ГОСТ ISO 13485-2017 СМК Требования.
Цикл PDCA для главы 8 ГОСТ ISO 13485-2017
8.1 Общие
положения
PLAN
8.5 Улучшение
ACT
Непрерывное
улучшение
DO
8.2 Мониторинг и
измерения
8.3 Управление
несоответствую
щей продукцией
CHECK
8.4 Анализ
данных
Сертификация
Консультационные услуги
Обучение
51
52.
7.5.9 Прослеживаемость7.5.9.1 Общие положения
7.5.9.2 Специальные требования к имплантируемым медицинским изделиям
7.5.10 Собственность потребителей
7.5.11 Сохранение соответствия продукции
7.6 Управление оборудованием для мониторинга и измерений
8 Измерение, анализ и улучшение
8.1 Общие положения
8.2 Мониторинг и измерение
8.2.1 Обратная связь
8.2.2 Рассмотрение претензий
8.2.3 Отчетность в регулирующие органы
8.2.4 Внутренний аудит
8.2.6 Мониторинг и измерение продукции
Сертификация
Консультационные услуги
Обучение
52
53.
«Система менеджмента качества.Базовые требования».
ГОСТ ISO 13485-2017 СМК Требования.
Планирование аудитов
Разработка
Программы аудитов
Обучение аудиторов
План
Проведение
аудитов
Анализ несоответствий
Записи
результатов
Разработка и проведение
корректирующих
мероприятий
Сертификация
Консультационные услуги
Обучение
53
54.
8.3 Управление несоответствующей продукцией8.3.1 Общие положения
8.3.2 Действия в отношении несоответствующей
продукции, обнаруженной до поставки
8.3.3 Действия в отношении несоответствующей продукции,
обнаруженной после поставки
8.3.4 Переделка
8.4 Анализ данных
8.5 Улучшение
8.5.1 Общие положения
8.5.2 Корректирующие действия
8.5.3 Предупреждающие действия
Сертификация
Консультационные услуги
Обучение
54
55.
Контроль процессаАнализ несоответствия
и определение их причин
нет
Необходимо
воздействие?
да
Разработка
корректирующих действий
Осуществление
воздействия
Записи
результатов
Анализ воздействия
Сертификация
Консультационные услуги
Обучение
55
56. Управление процессом (1)
«Система менеджмента качества.Базовые требования».
ГОСТ ISO 13485-2017 СМК Требования.
Управление процессом (1)
8.5.2
8.3
вход
процесс
выход
8.2.3
8.2.3
ресурсы
Сертификация
Консультационные услуги
Обучение
56
57.
«Система менеджмента качества.Базовые требования».
ГОСТ ISO 13485-2017 СМК Требования.
ДП
Разработка процесса
Установление
потенциальных
несоответствий
Разработка
предупреждающих
действий
Проведение
предупреждающих
действий
Записи
результатов
Анализ воздействия
на процесс
Сертификация
Консультационные услуги
Обучение
57
58. Управление процессом (2)
«Система менеджмента качества.Базовые требования».
ГОСТ ISO 13485-2017 СМК Требования.
Управление процессом (2)
8.2
8.4
вход
8.5.3
процесс
8.2.3
выход
8.2.3
ресурсы
Сертификация
Консультационные услуги
Обучение
58
59.
Генеральный Директор5.3 Политика 5.4 Планирование
5.5 Ответственность, полномочия
5.6 Анализ со стороны рук-ва.
7.4 информация по
поставщикам
5.6.2 Входные данные для
анализа
МЕНЕДЖЕР ПРОЦЕССА
8.5.2 Корректирующие
8.5.3 Предупреждающие
действия
Потребители
6.2 Людские ресурсы
6.3 Инфраструктура
6.4 Среда
7.2
требования
7.2
требования
8.5.1 Постоянное
улучшение
8.4 Анализ
данных
4.1 Требования к
процессам СМК
7. 1 Планирование
процессов
8.2.2 Внутренние
проверки
8.2.1 Удовлетворенность
потребителя
8.2.3 Мониторинг процесса
8.2.4 Мониторинг и измерение
продукции
7 Процесс (технология процесса)
Выпуск продукции (услуги) - (операции, функции,
работы)
8.3 Управление несоответствующей
продукцией
выход1
В
Верификация
В
7.5.1, 8.2.4 В – выпуск продукции
Сертификация
Консультационные услуги
Обучение
выход2
Потребитель процесса
5.6.3 Выходные
данные анализа
59
60.
ГОСТ ISO 14971-2021 Изделия медицинские. Применениеменеджмента риска к медицинским изделиям
3.1 сопроводительная документация (accompanying documentation): Документы, прилагаемые
к медицинскому изделию (3.10) и содержащие информацию для пользователя или лиц, ответственных за
установку, применение, техническое обслуживание, вывод из эксплуатации и утилизацию медицинского
изделия (3.10), особенно в отношении безопасного применения.
Примечания
1 Сопроводительная документация может состоять из инструкции по эксплуатации, технического описания,
руководства по установке, краткого справочного руководства и т.д.
2 Сопроводительная документация не обязательно является письменным или печатным документом и
может включать звуковые, визуальные или тактильные материалы и различные типы носителей информации
3.2 польза (benefit): Положительное влияние или предпочтительный результат применения медицинского
изделия (3.10) на здоровье человека или положительное влияние на ведение пациента или общественное
здоровье.
Примечание - Польза может включать положительное влияние на клинический исход, качество жизни
пациента, результаты, связанные с точным определением диагноза, положительное влияние применения
изделий для диагностики на клинические результаты или положительное влияние на общественное здоровье.
3.3 вред (harm): Травма или ущерб здоровью людей, а также ущерб имуществу или окружающей среде.
[ISO/IEC 63:2019, пункт 3.1]
3.4 опасность (hazard): Потенциальный источник вреда (3.3).
[ISO/IEC 63:2019, пункт 3.2]
3.5 опасная ситуация (hazardous situation): Обстоятельства, при которых люди, имущество или окружающая
среда подвергаются одной или нескольким опасностям (3.4).
Сертификация
Консультационные услуги
Обучение
61.
СертификацияКонсультационные услуги
Обучение
62.
Примечания1 Физическое или юридическое лицо несет конечную юридическую ответственность за обеспечение выполнения применимых
регулирующих требований стран или юрисдикций в отношении медицинских изделий, для реализации в которых они
предназначены, если только иное не установлено специальными требованиями регулирующего органа (РО) в пределах его
юрисдикции.
2 Ответственность изготовителя описана в руководящих документах GHTF. Эта ответственность включает в себя как
ответственность по выполнению требований до выпуска в обращение, так и послепродажных требований, таких как
сообщения о неблагоприятных событиях и уведомления о корректирующих действиях.
3 "Проектирование и/или производство" могут включать в себя разработку спецификаций, продукции, производство,
изготовление, сборку, обработку, упаковку, переупаковку, маркировку, перемаркировку, стерилизацию, монтаж или
восстановление медицинского изделия, а также объединение изделий, возможно с другой продукцией, в единый набор для
медицинского назначения.
4 Лицо, осуществляющее в соответствии с инструкцией по применению сборку и регулировку медицинского изделия,
выпущенного в обращение иным лицом и предназначенного для применения конкретным пациентом, не является
изготовителем, если сборка и регулировка не изменяют предусмотренного применения медицинского изделия.
5 Лицо, изменяющее предусмотренное назначение медицинского изделия или модифицирующее медицинское изделие без
согласия
изготовителя
для
выпуска
изделия
под
собственным
именем,
следует
рассматривать
как изготовителя модифицированного медицинского изделия.
6 Уполномоченный представитель, дистрибьютор или импортер, который только добавляет свой адрес и контактные данные
на медицинское изделие или на его упаковку, без удаления или изменения оригинальной маркировки, не
является изготовителем.
7 Если принадлежности попадают под регулирующие требования к медицинскому изделию, лица, ответственные за
проектирование и/или производство таких принадлежностей, являются изготовителями.
Сертификация
Консультационные услуги
Обучение
63.
3.10 медицинское изделие (medical device): Инструмент, аппарат, прибор, устройство, оборудование, имплантат, invitro реагент, программное обеспечение, материал или иные подобные или связанные с ними изделия, предназначенные
изготовителем для применения к человеку по отдельности или в комбинации для одной или нескольких конкретных
медицинских целей:
- диагностики, профилактики, мониторинга, лечения или облегчения заболеваний;
- диагностики, мониторинга, лечения, облегчения или компенсации последствий травмы;
- исследования, замещения или изменения анатомического строения или физиологических процессов;
- жизнеобеспечения или поддержания жизненных функций;
- управления зачатием;
- дезинфекции медицинских изделий (3.10);
- получения информации посредством исследования in vitro проб, взятых из тела человека,
а также не достигающие своего первичного предназначенного воздействия на организм человека за счет
фармакологических, иммунологических или метаболических средств, но функции которых могут поддерживаться такими
средствами.
Примечание - Некоторая продукция в отдельных юрисдикциях может рассматриваться как медицинские изделия, но не
являться таковой в других, например:
- дезинфицирующие вещества;
- вспомогательные средства для людей с ограниченными возможностями;
- изделия, содержащие ткани животных и/или человека;
- изделия для экстракорпорального оплодотворения или репродуктивных технологий.
[ISO/IEC 63:2019, пункт 3.7]
3.11 объективное свидетельство (objective evidence): Данные, подтверждающие существование или истинность чеголибо.
Примечание - Объективное свидетельство может быть получено посредством наблюдения, измерения, испытания или
другими способами.
[ISO 9000: 2015, пункт 3.8.3, изменено - примечание 2 удалено]
3.12 постпроизводство (post-production): Часть жизненного цикла (3.8) медицинского изделия (3.10) после завершения
проектирования и изготовления медицинского изделия (3.10).
Пример - Транспортирование, хранение, монтаж, применение продукции, техническое обслуживание, ремонт,
изменение продукции, вывод из эксплуатации и утилизация.
3.13 процедура (procedure): Установленный способ осуществления деятельности или процесса (3.14).
Примечание - Процедуры могут быть документированными или недокументированными.
[ISO 9000:2015, пункт 3.4.5]
Сертификация
Консультационные услуги
Обучение
64.
3.14 процесс (process): Совокупность взаимосвязанных или взаимодействующих видов деятельности, использующих входныеданные для достижения намеченного результата.
Примечания
1 Будет ли "намеченный результат" процесса называться выходными данными, продукцией или услугой, зависит от исходного
контекста.
2 Входные данные для процесса, как правило, являются выходными данными других процессов, а выходные
данные процесса, как правило, являются входными данными для других процессов.
3 Процессом также можно назвать два взаимосвязанных и взаимодействующих последовательных процесса или более.
[ISO 9000:2015, пункт 3.4.1, изменено - примечания 4, 5 и 6 удалены]
3.15 обоснованно прогнозируемое неправильное применение (reasonably foreseeable misuse): Применение продукции или
системы способом, не предусмотренным изготовителем (3.9), но который может быть результатом легко предсказуемого
поведения человека.
Примечания
1 Легко предсказуемое поведение человека включает в себя поведение всех типов пользователей, как профессиональных, так
и непрофессиональных.
2 Обоснованно прогнозируемое неправильное применение может быть преднамеренным или непреднамеренным.
[ISO/IEC 63:2019, пункт 3.8]
3.16 запись (record): Документ, предоставляющий свидетельства осуществленной деятельности или достигнутых результатов.
Примечания
1 Записи могут применяться, например, для формирования прослеживаемости и предоставления свидетельств верификации,
корректирующих и предупреждающих действий.
2 Как правило, записи не должны находиться под управлением изменениями.
[ISO 9000:2015, пункт 3.8.10]
3.17 остаточный риск (residual risk): Риск, остающийся после выполнения мер по управлению риском (3.21).
[ISO/IEC 63:2019, пункт 3.9]
3.18 риск (risk): Сочетание вероятности причинения вреда (3.3) и тяжести (3.27) этого вреда (3.3).
[ISO/IEC 63:2019, пункт 3.10, изменено - примечание 1 удалено]
3.19
анализ
риска
(risk
analysis):
Систематическое
использование
имеющейся
информации
для
идентификации опасностей (3.4) и определения риска (3.18).
[ISO/IEC 63:2019, пункт 3.11]
3.20 оценка риска (risk assessment): Полный процесс (3.14) анализа риска (3.19) и оценивания риска (3.20).
Сертификация
Консультационные услуги
Обучение
65.
3.21 управление риском (risk control): Процесс (3.14), в ходе которого принимают решения и выполняют меры,посредством которых риски (3.18) снижаются до установленных уровней или поддерживаются в пределах
установленных уровней.
[ISO/IEC 63:2019, пункт 3.12]
3.22 определение риска (risk estimation): Процесс (3.14), используемый для присвоения значений вероятности
наступления вреда (3.3) и тяжести (3.27) этого вреда.
[ISO/IEC 63:2019, пункт 3.13]
3.23 оценивание риска (risk evaluation): Процесс (3.14) сравнения риска (3.18), который уже определен, с
установленными критериями риска (3.18) для определения допустимости риска (3.18).
[ISO/IEC 63:2019, пункт 3.14]
3.24 менеджмент риска (risk management): Систематическое применение политики, процедур (3.13) и
практических методов менеджмента для решения задач анализа, оценивания, управления и
мониторинга риска (3.18).
[ISO/IEC 63: 2019, пункт 3.15]
3.25 файл менеджмента риска (risk management file): Совокупность записей (3.16) и других документов,
создаваемых в процессе менеджмента риска (3.24).
3.26 безопасность (safety): Отсутствие недопустимого риска (3.18).
[ISO/IEC 63:2019, пункт 3.10]
3.27 тяжесть (severity): Мера возможных последствий опасности (3.4).
[ISO/IEC 63:2019, пункт 3.17]
3.28 современное состояние науки и техники (state of the art): Стадия технического потенциала,
разработанного на данный момент времени в отношении продукции, процессов (3.14) и услуг на основании
соответствующих консолидированных выводов науки, техники и опыта.
Примечание - Современное состояние науки и техники воплощает в себе то, что в настоящее время
повсеместно принято как передовой опыт в области технологии и медицины. Современное состояние науки и
техники не обязательно подразумевает наиболее перспективное с технологической точки зрения решение.
Описанное здесь современное состояние науки и техники можно назвать "общепризнанное современное
состояние науки и техники".
[ISO/IEC 63:2019, пункт 3.18]
3.29 высшее руководство (top management): Лицо или группа лиц, осуществляющих руководство и
управление изготовителем (3.9) на высшем уровне.
Сертификация
Консультационные услуги
Обучение
66.
[ISO 9000:2015, пункт 3.1.1, изменено - термин "организация" заменен на термин "изготовитель", примечания удалены]3.30 ошибка применения (use error): Выполнение или невыполнение действия пользователем при
применении
медицинского
изделия
(3.10),
приводящее
к
результату,
отличающемуся
от
предусмотренного изготовителем (3.9) или ожидаемого пользователем.
Примечания
1 Ошибка применения включает в себя неспособность пользователя выполнить задачу.
2 Ошибки применения могут быть вызваны несоответствием между характеристиками пользователя,
пользовательского интерфейса, задачи или среды применения.
3 Пользователи могут знать или не знать, что произошла ошибка применения.
4 Непредвиденная физиологическая реакция пациента сама по себе не считается ошибкой применения.
5 Неправильное функционирование медицинского изделия, которое приводит к непредвиденному результату, не
считается ошибкой применения.
[МЭК 62366-1:2015, пункт 3.21, изменено - примечание 6 удалено]
3.31 верификация (verification): Подтверждение на основе предоставления объективных свидетельств (3.11) того, что
установленные требования выполнены.
Примечания
1 Объективное свидетельство, необходимое для верификации, может быть результатом проверки или других форм
определения, таких как выполнение альтернативных расчетов или изучение документов.
2 Деятельность, осуществляемая в целях верификации, иногда называется процессом квалификации.
3 Термин "верифицировано" используется для обозначения соответствующего статуса.
[ISO/IEC 63:2019, пункт 3.19]
Сертификация
Консультационные услуги
Обучение
67.
СертификацияКонсультационные услуги
Обучение
68.
СертификацияКонсультационные услуги
Обучение
69.
СертификацияКонсультационные услуги
Обучение
70.
СертификацияКонсультационные услуги
Обучение
71.
СертификацияКонсультационные услуги
Обучение
72.
СертификацияКонсультационные услуги
Обучение
73.
СертификацияКонсультационные услуги
Обучение
74.
СертификацияКонсультационные услуги
Обучение
75.
СертификацияКонсультационные услуги
Обучение
76.
СертификацияКонсультационные услуги
Обучение
77.
СертификацияКонсультационные услуги
Обучение
78.
СертификацияКонсультационные услуги
Обучение
79.
СертификацияКонсультационные услуги
Обучение
80.
СертификацияКонсультационные услуги
Обучение
81.
СертификацияКонсультационные услуги
Обучение
82.
• АудитAUDIO (лат.) – «слушать»
НЕ ПОИСК НЕСООТВЕТСТВИЯ И НАКАЗАНИЕ
ВИНОВНОГО,
А ПОИСК ПОДТВЕРЖДЕНИЯ СООТВЕТСТВИЯ И
ВОЗМОЖНЫХ ОБЛАСТЕЙ УЛУЧШЕНИЯ СМ
Сертификация
Консультационные услуги
Обучение
82
83. Термины и определения (1)
Аудит - систематический, независимый и документальнооформленный процесс для
получения аудиторских свидетельств и их объективной оценки
для определения степени, в которой
выполняются критерии аудита системы менеджмента,
установленные организацией
Примечание: Во многих случаях, например в маленьких организациях,
независимость может быть продемонстрирована отсутствием
ответственности за аудитируемую деятельность
Сертификация
Консультационные услуги
Обучение
83
84. Термины и определения (2)
Аудиты:– Первой стороны – выполняется организацией в своих
собственных целях (= внутренний аудит)
– Второй стороны – выполняется по заказу заинтересованной
организации (например, потребителем у своего существующего
или потенциального поставщика)
– Третьей стороны – выполняется полностью независимой
организацией (обычно в целях сертификации
Сертификация
Консультационные услуги
Обучение
84
85.
«Аудитор Системы менеджмента»Принципы проведения аудитов
Относящиеся к аудиторам
Надлежащая
профессиональная
тщательность
Относящиеся к процессу аудита
Независимость
Беспристпастное
представление
результатов
Риск-ориентированный
подход
Конфиденциальность
Подход, основанный
на свидетельствах
Честность-основа
профессионализма
Сертификация
Консультационные услуги
Обучение
85
86. Термины и определения (3)
Область аудита - содержание и границы аудитаКритерии аудита - совокупность политик, процедур или
требований
Свидетельства аудита - записи, изложение фактов или другая
информация, которая связана с критериями аудита и может
быть проверена
Результаты аудита - результаты оценки собранных свидетельств
аудита в сравнении с критериями аудита
Заключение по результатам аудита - выходные данные аудита,
предоставленные аудиторской командой с учетом целей аудита
и всех результатов аудита
ГОСТ Р ИСО 19011-2021
Сертификация
Консультационные услуги
Обучение
86
87. Процесс проведения аудита – общая информация
ОпределитеОБЛАСТЬ
аудита (т.е.
границы)
Установите
КРИТЕРИИ
проведения
аудита
Сертификация
Соберите
СВИДЕТЕЛЬ
СВА
(Положит. и
отрицательн
ые)
Консультационные услуги
Оцените
свидетельства,
чтобы получить
РЕЗУЛЬТАТЫ
Составьте
ЗАКЛЮЧЕНИЕ
по
результатам
Обучение
87
88. Термины и определения (4)
Программа аудита - совокупность одного илинескольких аудитов, запланированных на конкретные
сроки и направленных на достижение определенной
цели
План аудита - описание деятельности и мероприятий
аудита
ГОСТ Р ИСО 19011-2021
Сертификация
Консультационные услуги
Обучение
88
89. Термины и определения
Аудитор - лицо, обладающее компетентностью дляпроведения аудита
Компетентность - продемонстрированные личные
качества и способность применять знания и навыки
ISO 9000
Какими личными качествами, по вашему мнению, должен
(не должен) обладать аудитор?
Сертификация
Консультационные услуги
Обучение
89
90. Принципы аудита
Этичное поведение– Доверие, честность, конфиденциальность и рассудительность
Справедливое представление результатов
– Результаты аудита, аудиторские заключения и отчет достоверно
и точно отражают деятельность в рамках аудита
Профессионализм
– Аудиторы с должной тщательностью относятся к важности
выполняемой ими задачи и доверию к ним со стороны
руководства
Независимость
– Отражение потребности в объективности, описанной выше.
Подход на основе доказательств
– Свидетельства аудита должны поддаваться проверке
Сертификация
Консультационные услуги
Обучение
90
91. Зачем проводить аудит?
Требование стандарта ГОСТ ISO13485-2017(п.8.2.4).Оценка соответствия требованиям
Оценка результативности внедрения и функционирования
Определение потребности в обучении
Выделение сильных и слабых сторон
Выявление и исправление несоответствий
Предоставление информации руководству
Определение направлений для улучшения
Сертификация
Консультационные услуги
Обучение
91
92. Результаты аудита
Несоответствие:– Невыполнение установленных требований
• процедур и инструкций СМ
• законодательных и нормативных документов
• договорных документов
Уведомление
• потенциальная проблема
• риск
• не самая лучшая практика
• недопонимание
Хорошая практика
• высокая мотивация
• хорошие знания
• значительные улучшения
Сертификация
Консультационные услуги
Обучение
92
93. Этапы проведения аудита
Инициирование аудитаАнализ документации
План аудита
Рабочие документы
Подготовка
Проведение аудита
Представление отчетов
Последующие мероприятия
Сертификация
Назначение руководителя группы
Определение целей, области и критериев
Выбор группы аудиторов
Проверка документации соответствующей
системы менеджмента, включая записи
Вводное совещание
Сбор информации
Формирование свидетельств и результатов
Заключительное совещание
Подготовка и распространение отчетов
Проверка результативности предпринятых мер
Консультационные услуги
Обучение
93
94. ГОСТ Р ИСО 19011-2021 Подготовка к проведению аудита
Внедрение системыэкологического менеджмента
на основе ISO 9001:2015
ГОСТ Р ИСО 19011-2021
Подготовка к проведению
аудита
Сертификация
Консультационные услуги
Обучение
94
95. Инициирование аудита
Назначение руководителя аудиторской команды– с учетом целей, области и критериев аудита
– на основе информации о компетентности аудиторов
Определение целей, критериев и области аудита
– согласно программе аудита
Определение возможности проведения аудита
Подбор аудиторской команды
– аудиторы, стажеры
– технические эксперты
Установление контакта с проверяемой стороной
– сроки, язык аудита, состав команды
– требуемые ресурсы и информация
– безопасность, конфиденциальность
– аудит не должен быть «сюрпризом»
Сертификация
Консультационные услуги
Обучение
95
96. Анализ документации
Цель:– сбор информации, необходимой для проведения аудита
– оценка соответствия документации СМ критериям аудита
По возможности – до проведения аудита
– процедуры, инструкции
– записи, результаты предыдущих аудитов
– цели, задачи
Если в документации найдены несоответствия:
– сообщить проверяемой стороне и заказчику аудита
– принять решение о возможности проведения аудита
Сертификация
Консультационные услуги
Обучение
96
97. Подготовка плана аудита (1)
На основе:– программы, целей, области и критериев аудита
– информации, полученной от проверяемой стороны
Состав (если применимо):
– цели, область, критерии
– сроки проведения аудита
– состав аудиторской команды
– информация о представителе проверяемой стороны и
сопровождающих
– место проведения аудита
– график проведения аудита
– методы проведения аудита
– язык аудита
Сертификация
Консультационные услуги
Обучение
97
98. Подготовка плана аудита (2)
Планирование:– от «входа» к «выходу» проверяемой области
– в зависимости от сложности проверяемой области
– должна быть возможность внесения изменений в план
– предусмотреть время на:
• вступительное совещание
• промежуточные совещания аудиторской команды
• промежуточные совещания с проверяемой стороной
• резервное время для дополнительных проверок
• время на подготовку к заключительному совещанию
Согласование плана:
– с аудиторской командой
– с заказчиком аудита
– с проверяемой стороной
Сертификация
Консультационные услуги
Обучение
98
99. Подготовка рабочих документов (1)
Контрольные вопросы (чек-листы):– служат напоминанием
– гарантируют рассмотрение всех основных вопросов
– обеспечивают рассмотрение процессов во взаимодействии
– обеспечивают всесторонний охват при проведении аудита
– управление временем
– помогают регистрировать данные
– являются частью отчета о проведении аудита
НЕ помогают:
– при возникновении дополнительных вопросов
– при изучении областей, не указанных в чек-листе
Аудитом управляет аудитор, а не перечень вопросов!
Сертификация
Консультационные услуги
Обучение
99
100. ГОСТ Р ИСО 19011-2021 Проведение аудита
СертификацияКонсультационные услуги
Обучение
100
101. Порядок проведения аудита
Вступительноесовещание
Сбор данных
Промежуточные
совещания
Подготовка к
заключительному
совещанию
Заключительное
совещание
Сертификация
Консультационные услуги
Обучение
101
102. Вступительное совещание
Цель – подтверждение договоренностей:– подтверждение целей, области и критериев аудита
– представление аудиторской команды и проверяемой стороны
– обсуждение плана аудита и изменений
– методы проведения аудита
– возможные результаты аудита
– способы связи между аудиторами и проверяемой стороной
– подтверждение наличия необходимых ресурсов
– подтверждение соблюдения требований безопасности и
конфиденциальности
– условия для досрочного прекращения аудита
– порядок обжалования результатов аудита
Проводит ведущий аудитор
Присутствует вся аудиторская команда
Сертификация
Консультационные услуги
Обучение
102
103. Методы сбора данных
ИнтервьюСвидетельства
аудита
Анализ данных
Наблюдение за
деятельностью
Могут применяться совместно или раздельно
Сертификация
Консультационные услуги
Обучение
103
104. Интервью (1)
Место проведения интервью:– на рабочем месте проверяемого
– располагайтесь так, чтобы не мешать проверяемому
– начинать лучше с руководства, затем переходить
к сотрудникам подразделения
Время проведения интервью
– времени всегда не хватает
– не планируйте интервью в периоды пиковой нагрузки
– не приходите раньше или позже назначенного времени,
если это не согласовано заранее
– не опаздывайте
– учитывайте перерывы и время окончания работы
– следите за соблюдением запланированного времени интервью
Сертификация
Консультационные услуги
Обучение
104
105. Интервью (2)
Подготовка к интервью:– выберите сотрудника для интервью
– представьтесь
– поясните цель визита и порядок проведения интервью
– цель аудита – оценка соответствия, а не поиск виновных и
проблем
– поясните, что проверяете не конкретного человека,
а работу СМ
– поясните смысл ведения записей в ходе интервью
– 2-3 минуты – разговор «ни о чем»
– найдите, за что похвалить собеседника
– «вы готовы?» («давайте начинать?»)
Средства аудио- и видеозаписи с согласия проверяемых!
Сертификация
Консультационные услуги
Обучение
105
106. Интервью (3)
Во время интервью:– не превращайте беседу в допрос
– говорите с сотрудником на его языке
– дайте время на обдумывание вопроса и ответа
– разрешите пользоваться документами
– следуйте плану аудита
– не давайте увести себя в сторону
– поясняйте свои вопросы
– непонятно – переспросите
– просите подтверждения слов на практике
– используйте приемы «активного слушания»
– не давайте рекомендаций
Сертификация
Консультационные услуги
Обучение
106
107. Интервью (4)
Во время интервью:– дружелюбно, но профессионально
– сообщайте о найденных результатах
– дайте возможность исправиться
– ничего личного при интервью
Получение информации – задача аудитора
Следите за состоянием собеседника:
– поза
– жесты
– голос
– интонации
– выражения
Сертификация
Консультационные услуги
Обучение
107
108. Процесс общения осуществляется через:
СертификацияКонсультационные услуги
Обучение
108
109. Интервью (5)
Виды вопросов:– открытые
• «что…?», «как…?», «почему…?»
• предполагают развернутый ответ
– закрытые
• «правда ли, что…?»
• однозначный ответ «да» или «нет»
– альтернативные
• «или… или»
• возможность выбора варианта ответа
– гипотетические
• «что делать, если…»
• действия в предполагаемой ситуации
– завершающие
• «что-нибудь еще?»
Сертификация
Консультационные услуги
Обучение
109
110. Интервью (6)
Обратите внимание:– открытые
• «что…?», «как…?», «почему…?»
• предполагают развернутый ответ
– закрытые
• «правда ли, что…?»
• однозначный ответ «да» или «нет»
– альтернативные
• «или… или»
• возможность выбора варианта ответа
– гипотетические
• «что делать, если…»
• действия в предполагаемой ситуации
– завершающие
• «что-нибудь еще?»
Сертификация
Консультационные услуги
Обучение
110
111. Интервью (7)
Воронка вопросов:Общая
информация
Открытые вопросы
Закрытые
Альтернативные
Гипотетические
Завершающие
вопросы
Сертификация
Конкретная
информация
Консультационные услуги
Обучение
111
112. Интервью (8)
Обратите внимание:– Не делайте скоропалительных выводов!
– Не судите по первому впечатлению!
– Убедитесь, что у вас достаточно доказательств!
– Убедитесь, что доказательства объективны!
– Если сомневаетесь, изучите ситуацию!
– Определите направление дальнейшего изучения
Сертификация
Консультационные услуги
Обучение
112
113. Интервью (9)
Завершение интервью:– в соответствии с графиком
– дополнительное интервью – согласуйте время и место
– поблагодарите за участие
– подведите итоги (особенно по несоответствиям)
– добейтесь согласия с итогами интервью
– сообщите о порядке обжалования результатов
Сертификация
Консультационные услуги
Обучение
113
114. Интервью (10)
Конфликты:– уход от темы аудита
• «… давайте продолжим»
• «… покажите мне»
– длительное отсутствие сотрудника на месте
• согласовать время отсутствия \ паузы в интервью
• зафиксировать в отчете
– конфликты внутри подразделения
• не вмешиваться
– нежелание участвовать в интервью
• сообщить руководителю сотрудника \
ведущему аудитору
• зафиксировать в отчете
– угроза жизни и здоровью
• сообщить ведущему аудитору
• прервать аудит
Сертификация
Консультационные услуги
Обучение
114
115. Наблюдение за деятельностью
Предупредите проверяемогоНе мешайте в ходе наблюдения
Непонятно – спросите
Сообщите о результатах наблюдения
Что проверять:
– Соответствие деятельности требованиям СМ;
– Применение соответствующих инструментов, материалов,
методов работы
– Наличие средств защиты
– Наличие необходимой информации на рабочем месте
Сертификация
Консультационные услуги
Обучение
115
116.
«Система экологического менеджмента..Внутренний аудитор СМ».
Советы аудитору
Демонстрируйте позитивное отношение,
Используйте понятную терминологию,
Прослеживайте конкретный проект (заказ, программу…),
Фиксируйте объективные свидетельства,
Отмечайте улучшения,
Не навязывайте свое мнение,
Ведите записи
Сертификация
Консультационные услуги
Обучение
116
117. Анализ данных (1)
Данные выбирает аудитор:– «покажите мне…»
– процедуры и инструкции
– журналы, отчеты, протоколы
– базы данных
Объем выборки определяет аудитор на основе:
– результатов предыдущих аудитов
– результатов анализа документации при подготовке к аудиту
– информации от участников аудиторской команды
– информации о деятельности
– собственной компетентности
– полученных результатов
Сертификация
Консультационные услуги
Обучение
117
118. Анализ данных (2)
Проверка:– наличие и доступность
– читаемость
– соответствие требованиям СМ
– соответствие сроков и содержания
Данные нужны аудитору
Если данных нет на месте проверки – согласовать время и
место передачи данных
Сертификация
Консультационные услуги
Обучение
118
119. Ведение записей в ходе сбора данных
ПИШИТЕ!!!Подробно
– для несоответствий
• дата, номер чертежа, номер документа,
нарушенное требование
• описание нарушения
• источник данных о нарушении
Кратко
– для наблюдений
• краткое описание
• возможные последствия
– для хороших практик
Аккуратно и разборчиво
Сертификация
Консультационные услуги
Обучение
119
120. Оформление отчетов о несоответствиях (1)
Несоответствие:– удостоверьтесь в том, что оно действительно есть;
– рассматривайте несоответствие как очередную возможность для
улучшения
Формулировка несоответствия:
– «Требование»: описание нарушенного требования с указанием
его источника (№ документа, пункт, содержание…)
– «Нарушение»: описание нарушения (подробно)
– «Свидетельство»: источник информации о несоответствии
(журнал, база данных, интервью…)
Сертификация
Консультационные услуги
Обучение
120
121. Оформление отчетов о несоответствиях (2)
Не изобретайте требованияИзбегайте расплывчатых формулировок
Сомневаешься в несоответствии – пиши наблюдение
Сомнения – в пользу проверяемой стороны
Требования к отчету о несоответствии:
– Четкость и точность
– Краткость и тщательность
– Всесторонний охват
– Описание проблемы
– Разъяснение требований
– Ссылка на доказательство
Сертификация
Консультационные услуги
Обучение
121
122.
НЕСООТВЕТСТВИЯ невыполнение установленных требованийУведомления
(Наблюдения)
Значительные
Незначительные
Серьёзный недостаток,
который отрицательно
воздействует на
качество работ - не
выполняется
требование к СМ
Упущения в
выполнении
отдельных пунктов
требований к СМ
Сертификация
Консультационные услуги
Могут быть
положены в основу
действий по улучшению функционирования СМ
Обучение
122
123. Обмен информацией в ходе аудита
Внутри аудиторской команды:– Результаты аудита
– Дополнительная информация для проверки
С проверяемой стороной
– Промежуточные итоги аудита
– Дополнительная информация
С внешними сторонами
– Промежуточные итоги аудита (при необходимости)
Если результат выходит за область аудита:
– сообщить ведущему аудитору
Сертификация
Консультационные услуги
Обучение
123
124. Подготовка к заключительному совещанию
Цель:– анализ полученных данных с точки зрения целей и критериев
аудита
– согласование результатов аудита с проверяемой стороной
– устранение разногласий
– подготовка рекомендаций (если необходимо)
– обсуждение действий после аудита
Проведение:
– в виде совещания аудиторской команды
– после завершения всех этапов сбора данных согласно плану
аудита
Сертификация
Консультационные услуги
Обучение
124
125. Заключительное совещание (1)
Цель:– информирование о результатах аудита и степени соответствия
области аудита критериям
– информирование о возникших конфликтных ситуациях
– обсуждение порядка дальнейших действий после аудита
Участники:
– аудиторская команда
– представители проверяемой стороны
– заказчик аудита (при необходимости)
Формальный или неформальный подход к проведению
совещания
Председатель – ведущий аудитор
Сертификация
Консультационные услуги
Обучение
125
126. Заключительное совещание (2)
Повестка совещания:– благодарность участникам аудита
– цели, область и критерии аудита
– степень выполнения плана аудита
– возникшие конфликтные ситуации
– упоминание о выборочности аудита
– методы проведения аудита
– полученные результаты
– заключение о степени соответствия области аудита критериям
– порядок подготовки и распространения отчета
– порядок действий после завершения аудита
Сертификация
Консультационные услуги
Обучение
126
127. ГОСТ Р ИСО 19011-2021 Подготовка отчета и последующие действия по результатам аудита
СертификацияКонсультационные услуги
Обучение
127
128. Подготовка отчета об аудите
Без отчета нет аудитаТочная, сжатая и понятная информация об аудите
Содержание отчета:
– цели аудита;
– область аудита (подразделения, функции, процессы)
– состав аудиторской команды и проверяемой стороны
– места проведения аудита
– критерии аудита
– результаты и свидетельства аудита
– заключения по аудиту
– заявление о степени соответствия
области аудита критериям
– расхождения во мнениях между аудиторами
и проверяемой стороной…
Сертификация
Консультационные услуги
Обучение
128
129. Рассылка отчета об аудите
В установленные срокиПолучатели:
– проверяемая сторона
– заказчик аудита
– заинтересованные стороны по согласованию с заказчиком и
проверяемой стороной
Конфиденциальность
Управление отчетом - запись
Сертификация
Консультационные услуги
Обучение
129
130. Действия после аудита
Проверяемая сторона– анализ отчета об аудите и отчетов о несоответствиях
– анализ причин несоответствий
– разработка КД и ПД (возможно, совместно с аудиторами)
– согласование мероприятий с ведущим аудитором
– проведение КД и ПД
– информирование о результатах
Ведущий аудитор:
– согласование КД и ПД (возможно, совместно с аудиторами)
– планирование оценки результативности
– оценка результативности КД и ПД
– информирование о результативности заинтересованных сторон
– принятие решения о закрытии несоответствия
– принятие решения о завершении аудита
Сертификация
Консультационные услуги
Обучение
130
131. ГОСТ Р ИСО 19011-2021 Компетентность и оценка аудиторов
СертификацияКонсультационные услуги
Обучение
131
132.
Метод оценкиЦели
Примеры
Анализ записей
Проверка квалификации аудитора
Анализ записей об образовании,
обучении, производственном опыте и
опыте по аудиту
Обратная связь
Обеспечивает информацией о том, как
воспринимается деятельность аудитора
Инспектирование деятельности,
опросы, резюме, рекомендации,
жалобы, оценка деятельности,
отзывы коллег
Собеседование
Оценка личных качеств и коммуникационных
навыков, проверка информации и знаний по
тестам и получение дополнительной
информации
Персональное собеседование
Наблюдение
Оценка личных качеств и способности
применения знаний и навыков
Ролевые игры, наблюдения в
процессе аудита, деятельность на
рабочем месте
Тестирование
Оценка личных качеств, знаний, навыков и их
применение
Устные и письменные экзамены,
психометрическое тестирование
Анализ
деятельности
после аудита
Получение информации о работе аудитора во
время выполнения действий по аудиту,
определение его сильных сторон и недостатков
Анализ отчета по аудиту, опросы и
обсуждение с руководителем группы по
аудиту, членами группы по аудиту и, при
необходимости, использование
обратной связи для получения
информации от проверяемой
организации
Сертификация
Консультационные услуги
Обучение
133.
Личные качества аудитораСАМОСТОЯТЕЛЬНЫЙ, т.е.
ЭТИЧНЫЙ, т.е.
справедливый,
правдивый, искренний,
честный и тактичный
способный действовать и
работать независимо, при
этом эффективно
сотрудничать с другими
НАСТОЙЧИВЫЙ, т.е.
постоянно нацеленный на
достижение целей
ШИРОКИХ ВЗГЛЯДОВ, т.е.
готовый рассмотреть
альтернативные идеи или
точки зрения
РЕШИТЕЛЬНЫЙ, т.е.
своевременно приходящий к
заключениям, основанным на
логичном рассуждении и
анализе
АУДИТОР
ГИБКИЙ, т.е.
способный быстро
приспосабливаться к
различным ситуациям
ДИПЛОМАТИЧНЫЙ, т.е.
тактичный в обращении с
людьми
НАБЛЮДАТЕЛЬНЫЙ, т.е.
живо воспринимающий
окружающую
действительность
ПРОНИЦАТЕЛЬНЫЙ, т.е.
интуитивно осознающий и
способный понять ситуацию
ТАКОГО НЕ БЫВАЕТ,
НО СТРЕМИТЬСЯ К ЭТОМУ НАДО !
Сертификация
Консультационные услуги
Обучение
133
134. Вопросы
«Система менеджмента качества. Базовые требования.Аудитор СМК».
Вопросы
Сертификация
Консультационные услуги
Обучение
134













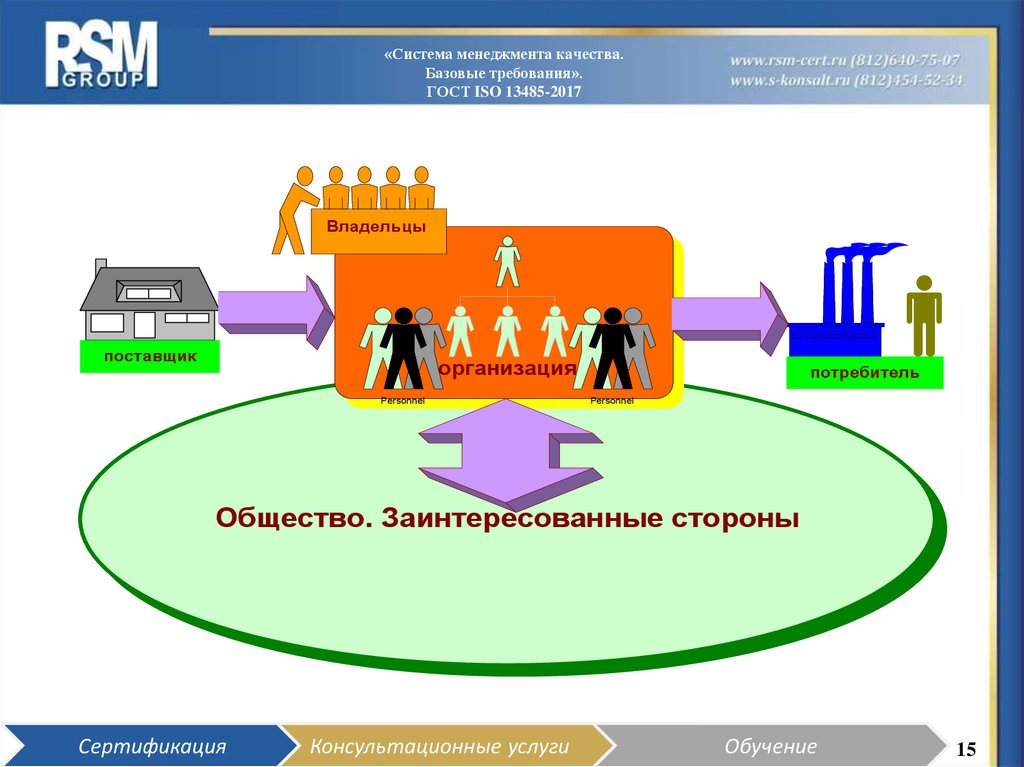

















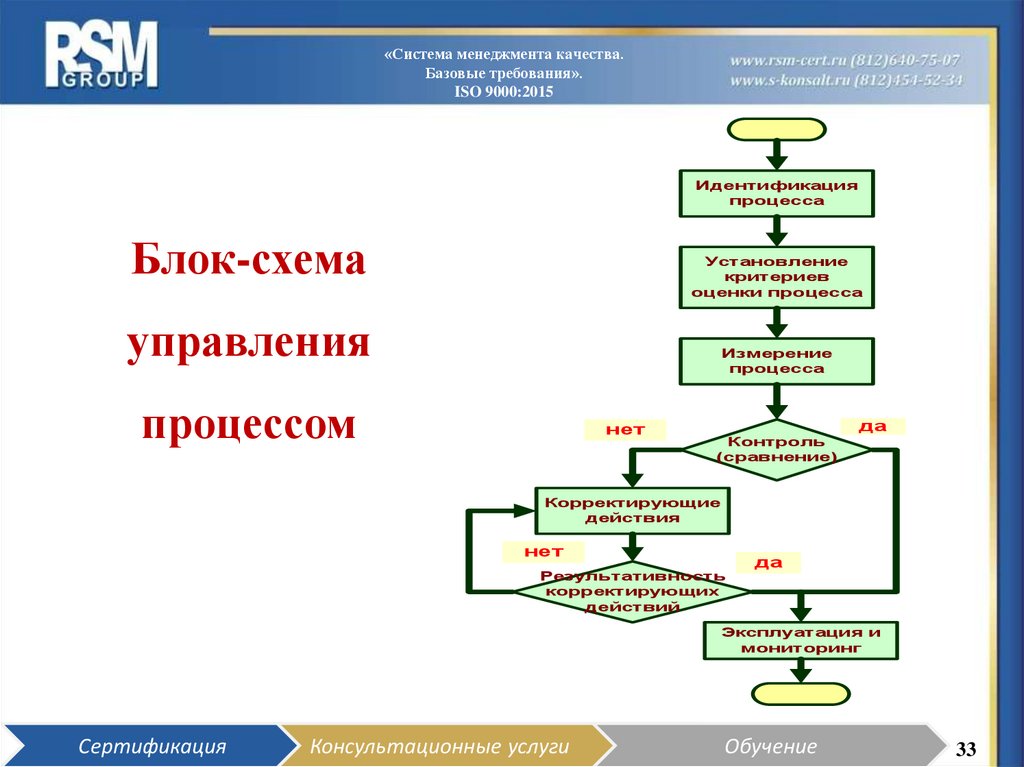
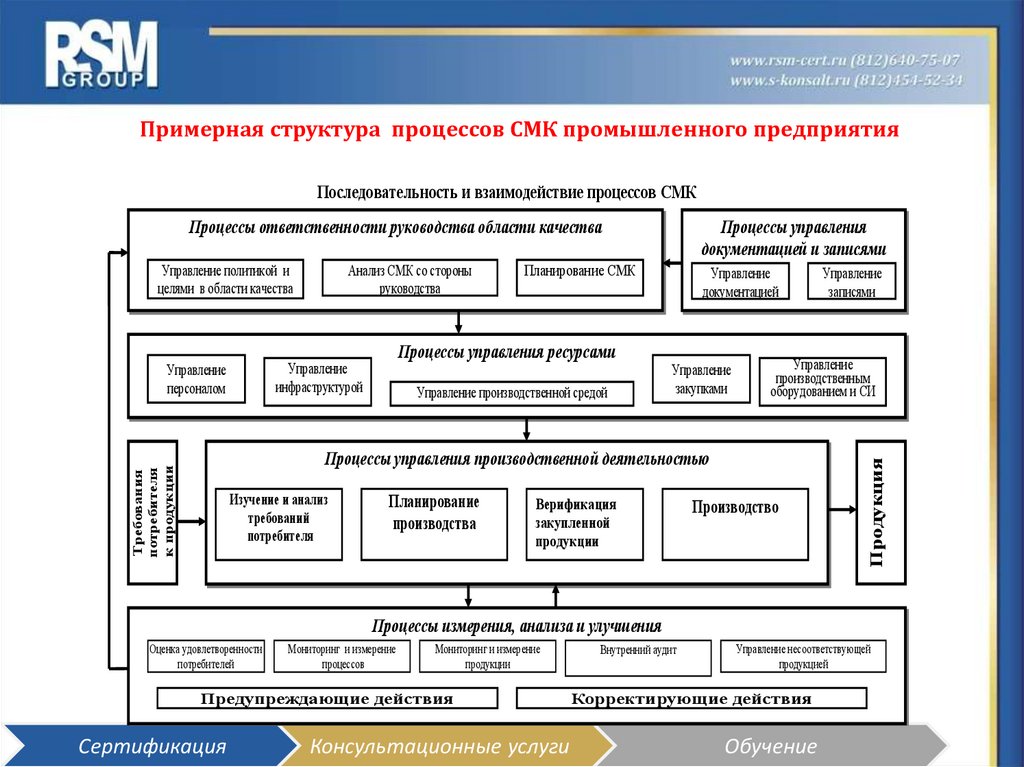




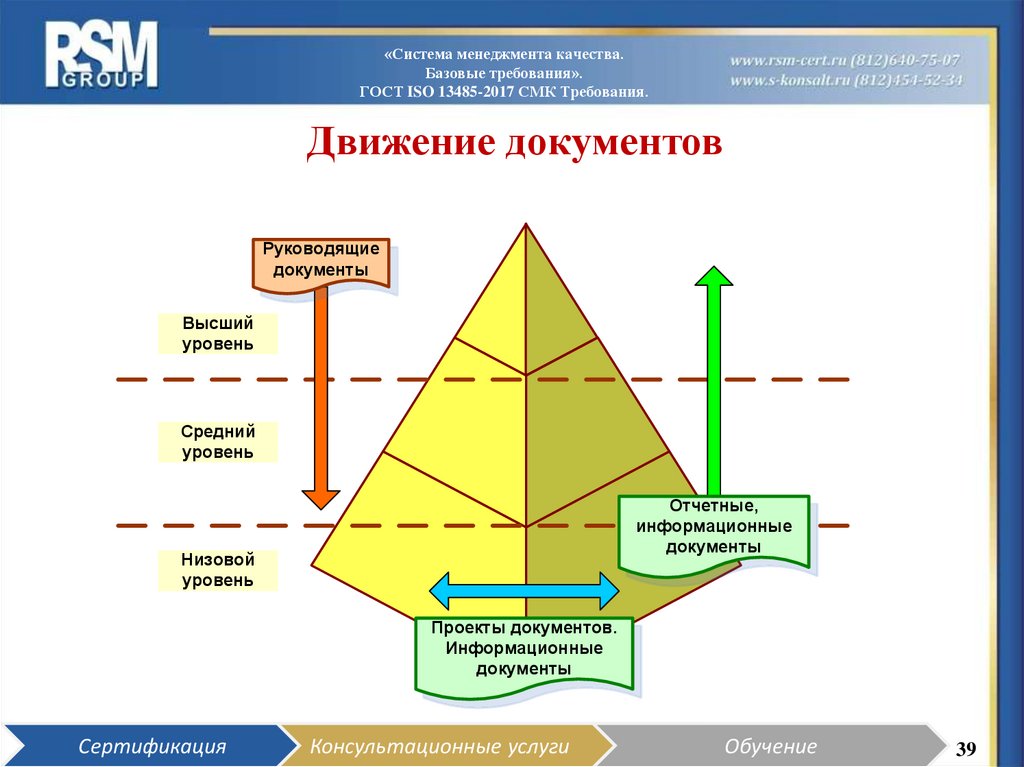




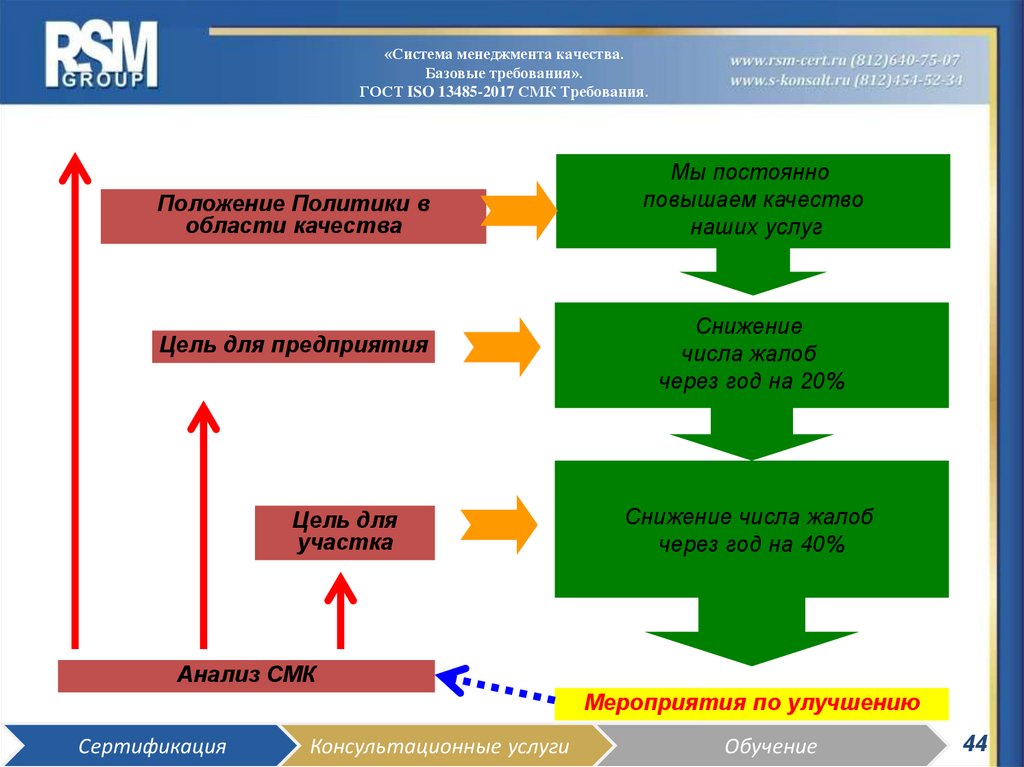

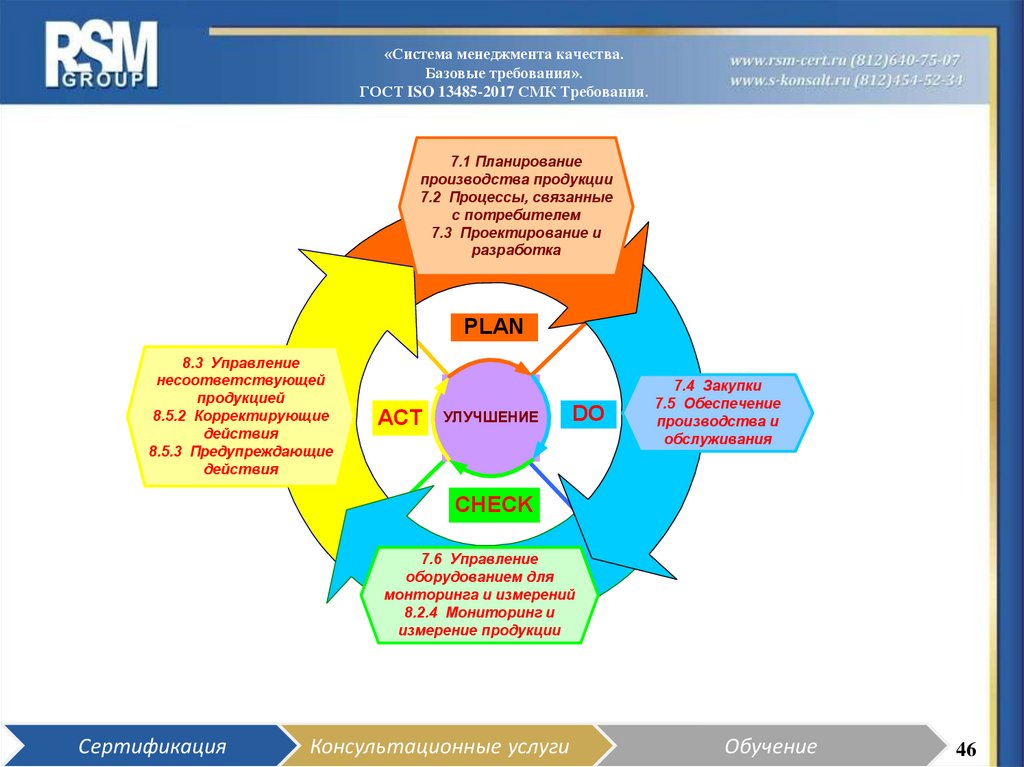

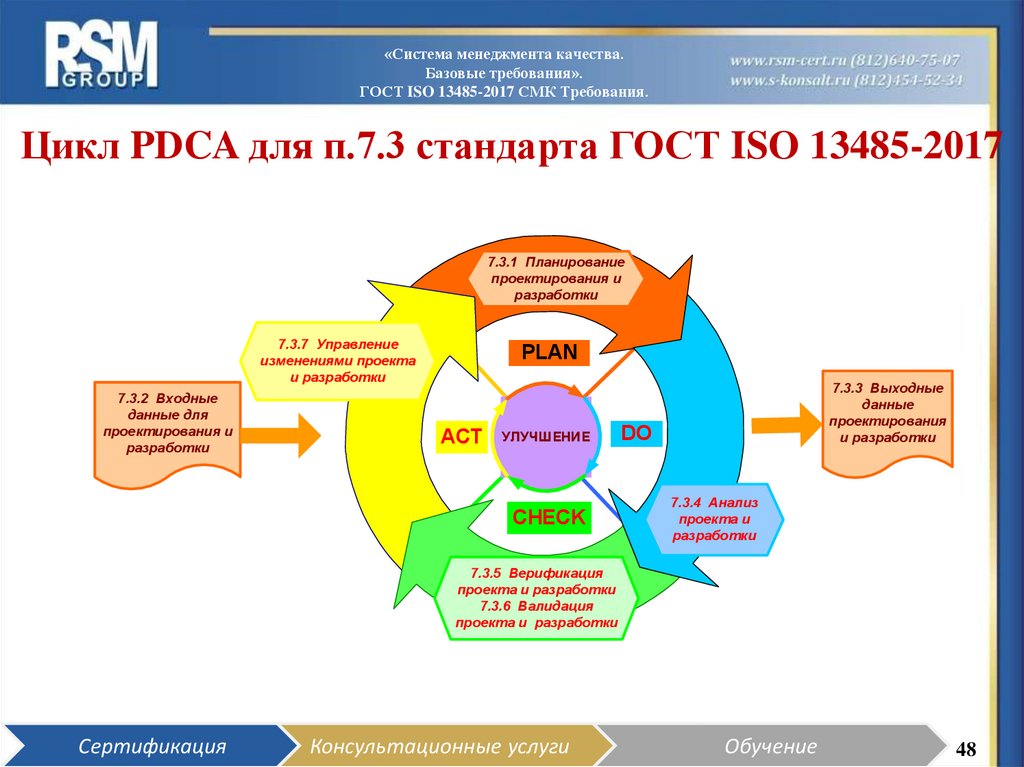


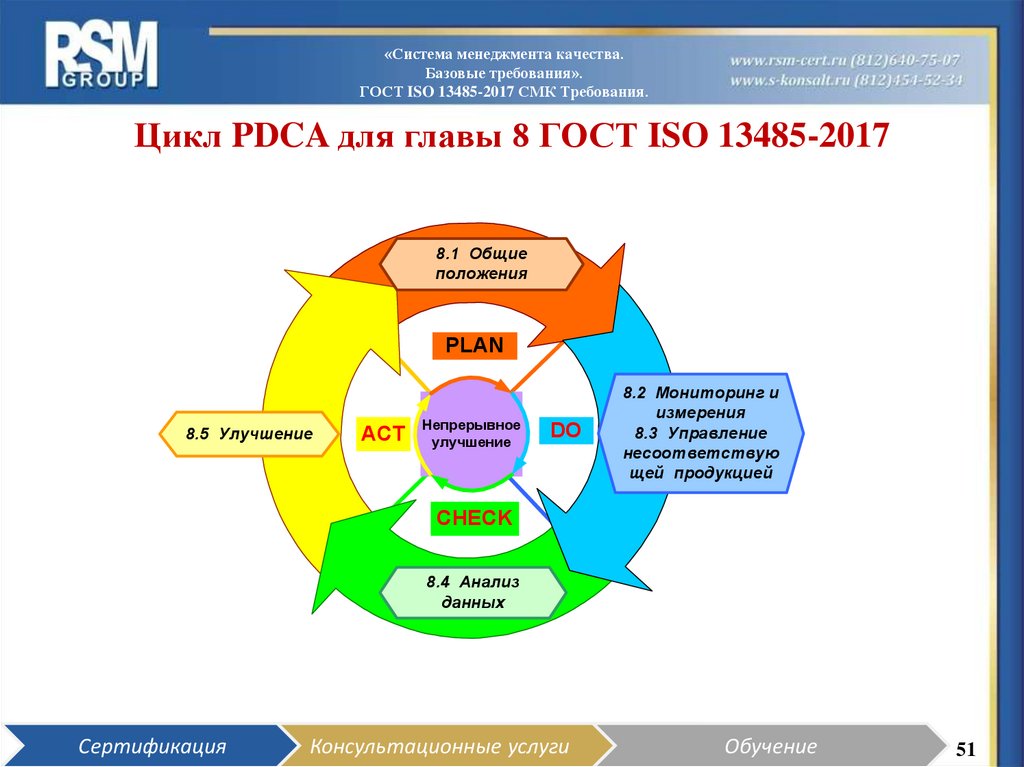

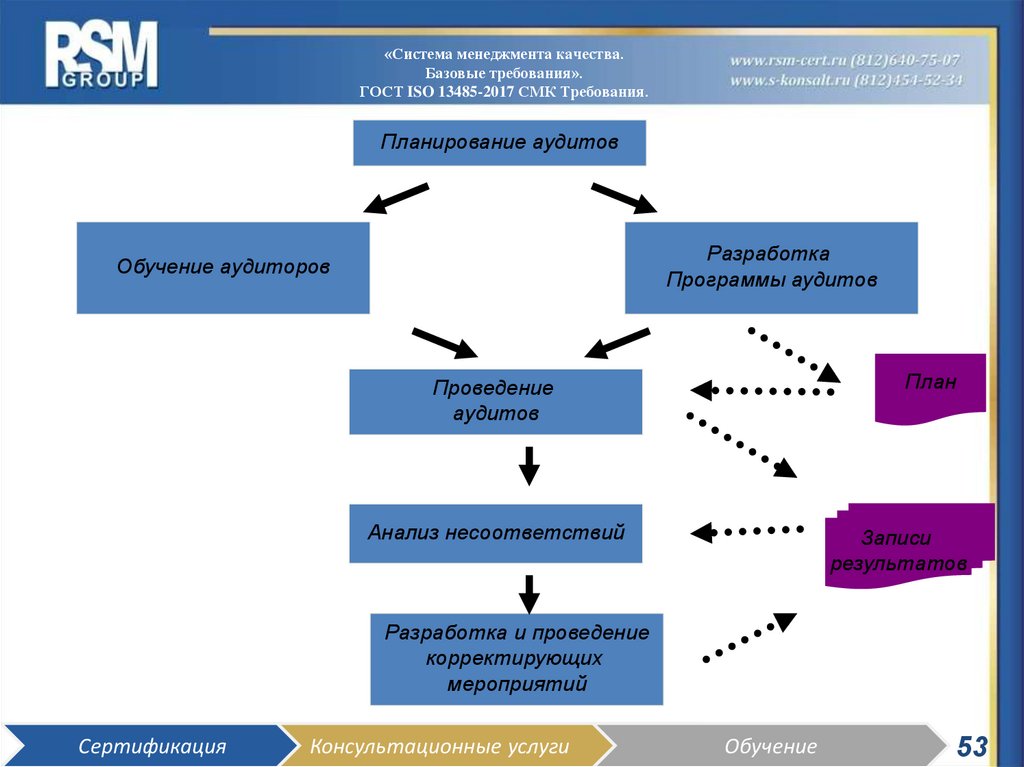

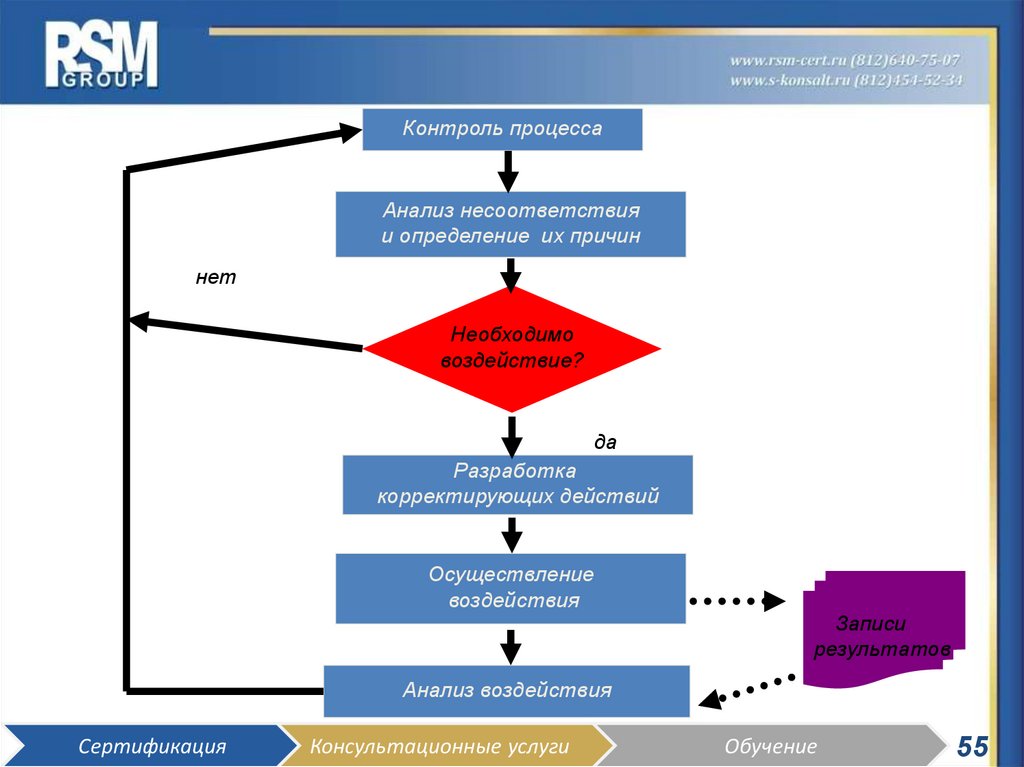
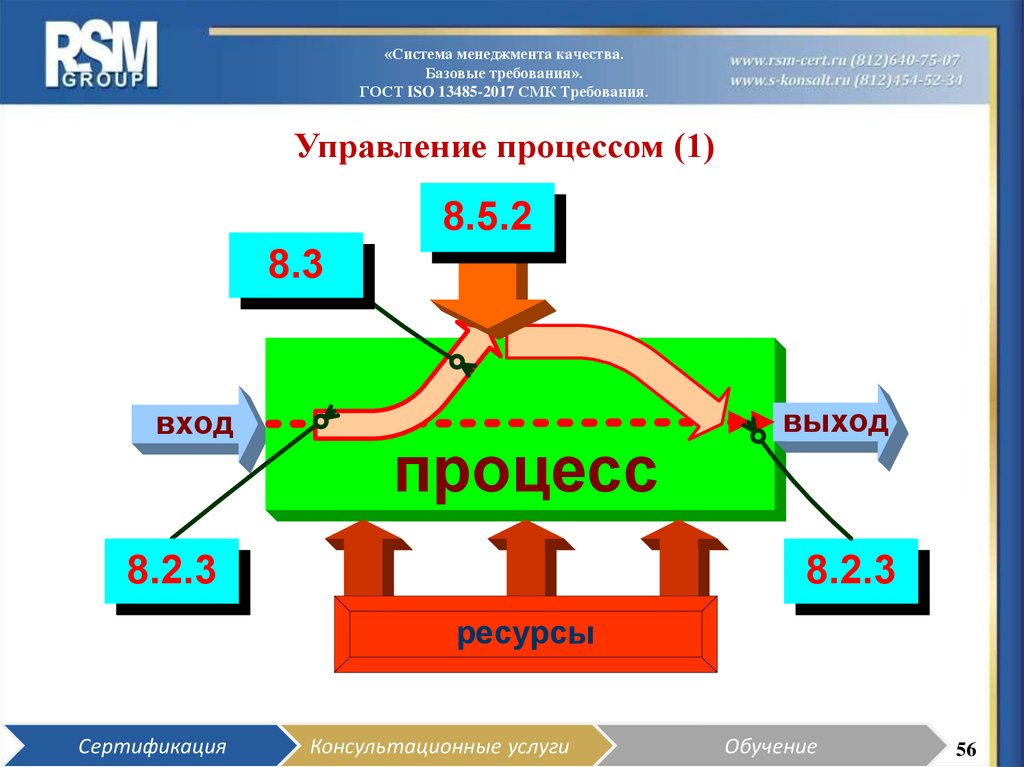
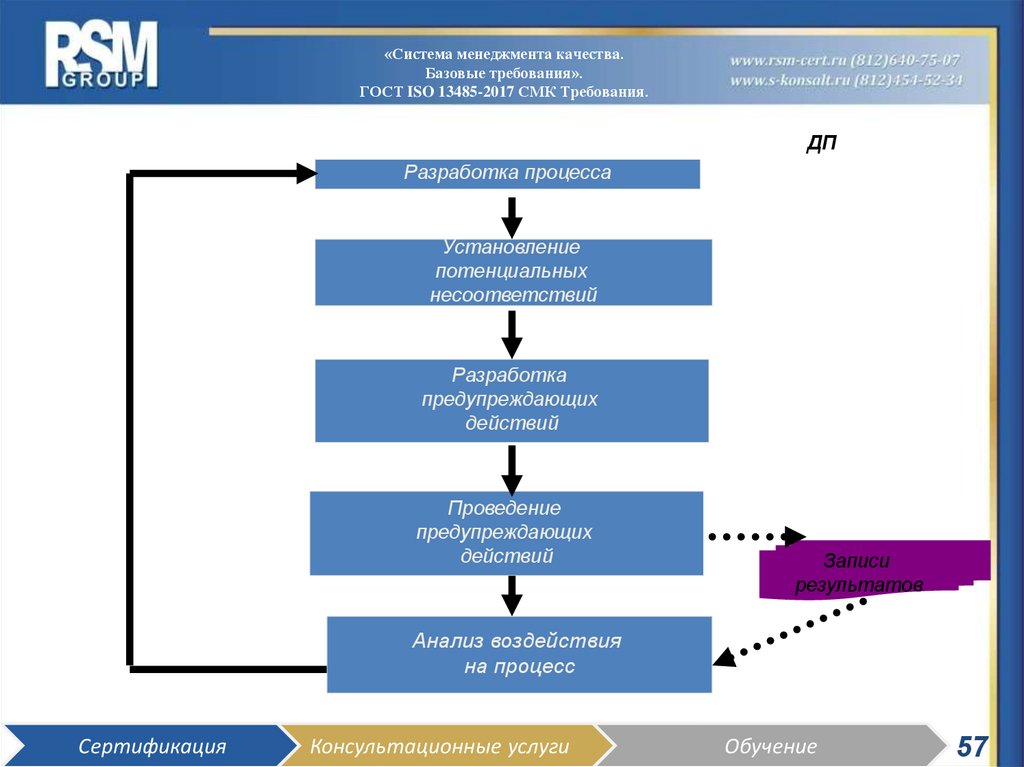
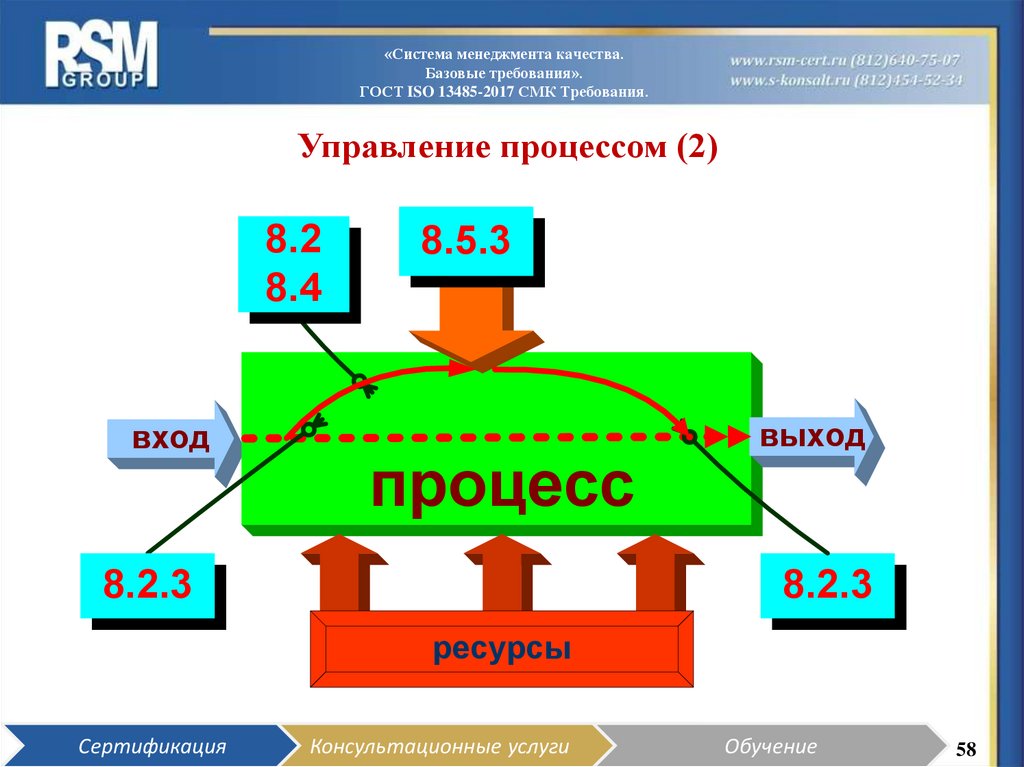










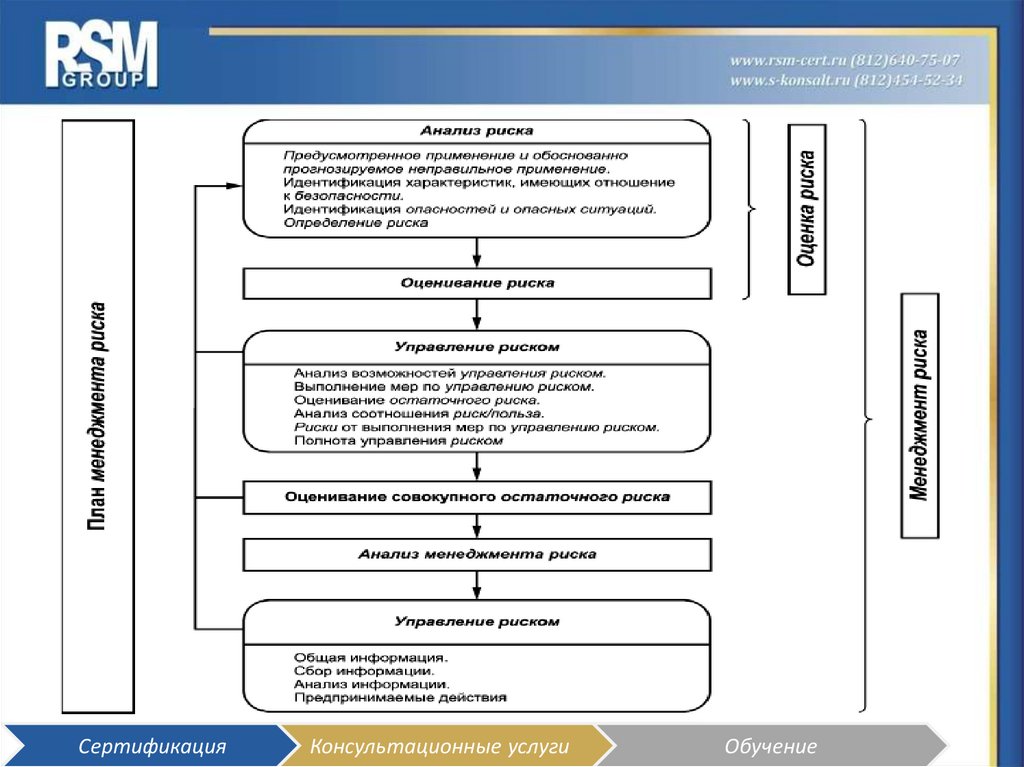



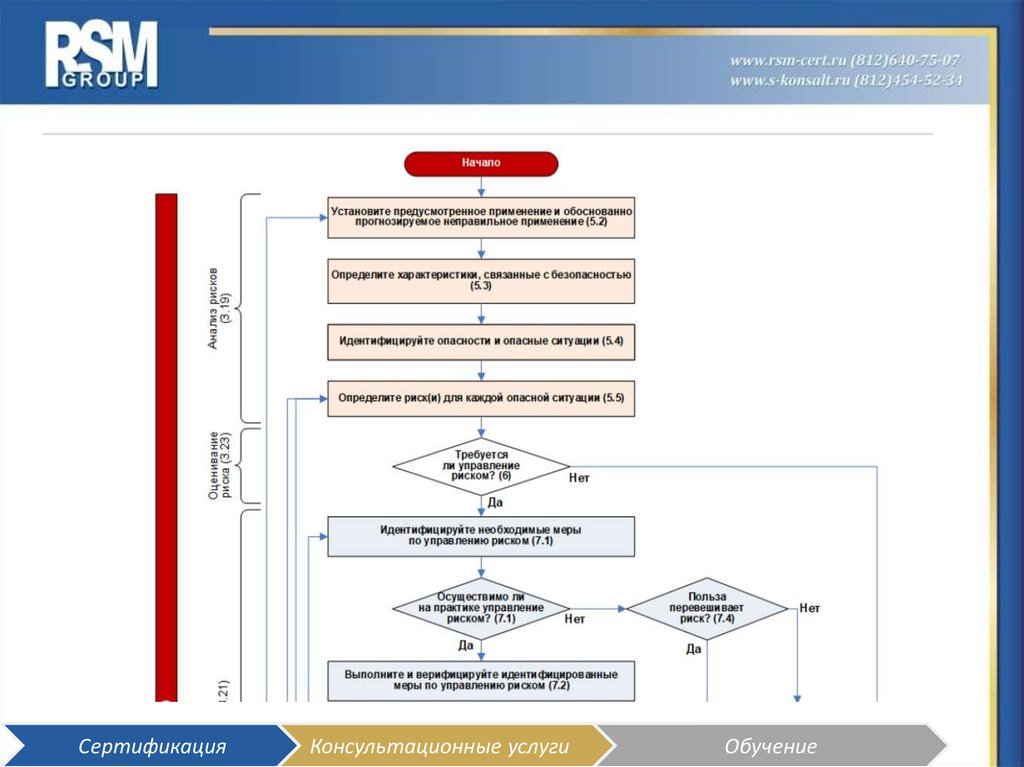

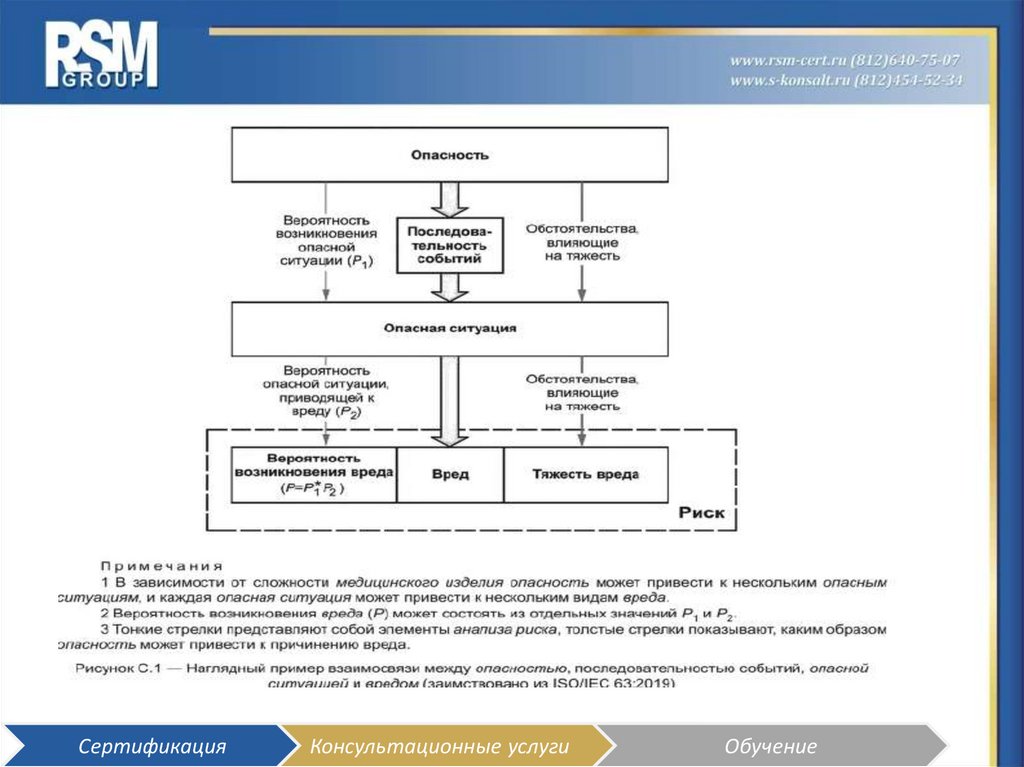









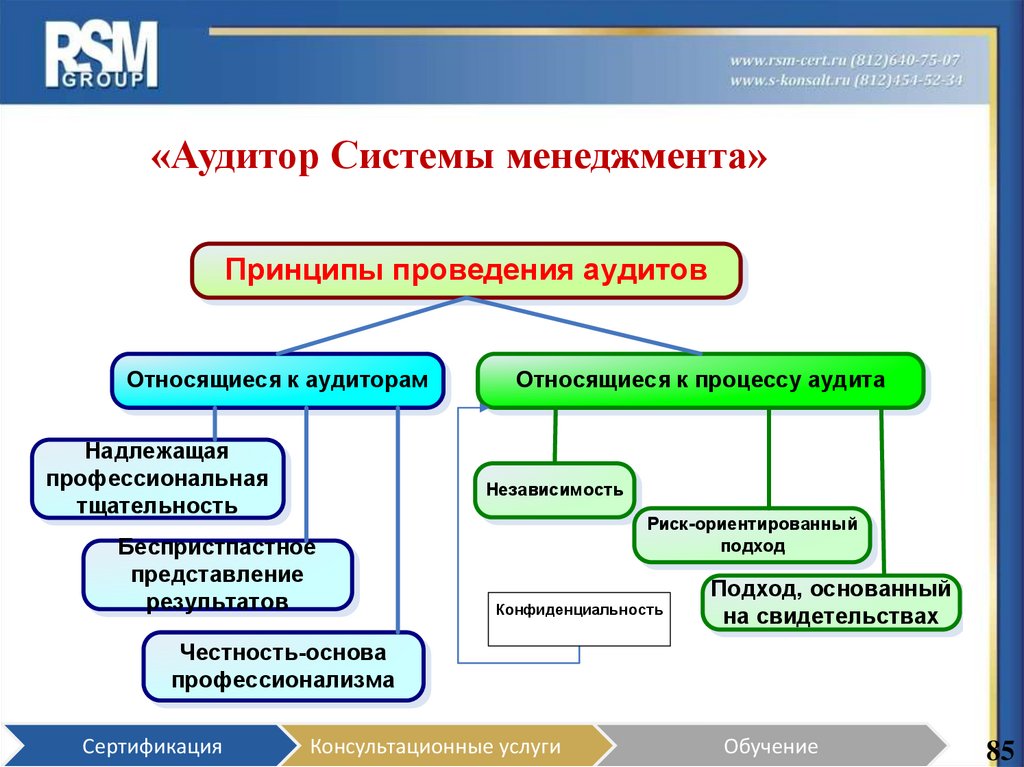

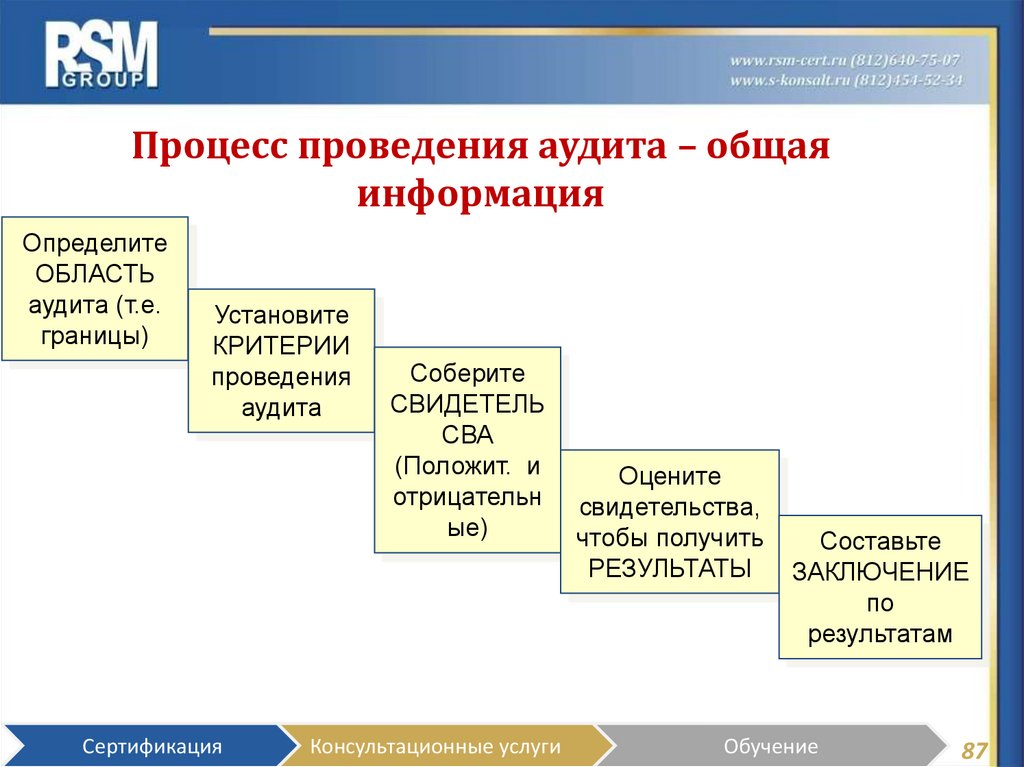















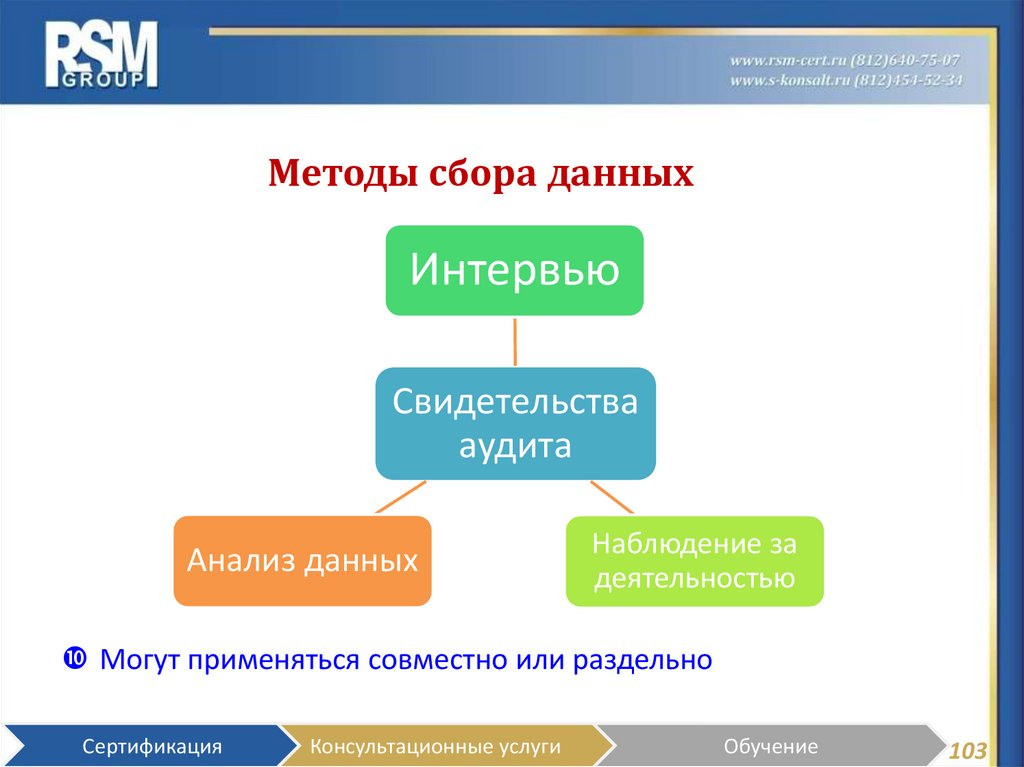































 Менеджмент
Менеджмент








