Похожие презентации:
Программа развития универсальных учебных действий
1.
Рыбакова Л.Ю.,учитель химии
МОУ «СОШ п. Динамовский
Новобурасского района»
2.
Программа развития универсальных учебныхдействий
Выделяют четыре блока УУД:
Личностные – формирование личности
Регулятивные – поведение личности
Познавательные – развитие личности
Коммуникативные – общение личности
Каждый учебный предмет в зависимости от
предметного содержания и способов организации
учебной деятельности учащихся раскрывает
определенные возможности для формирования УУД.
3.
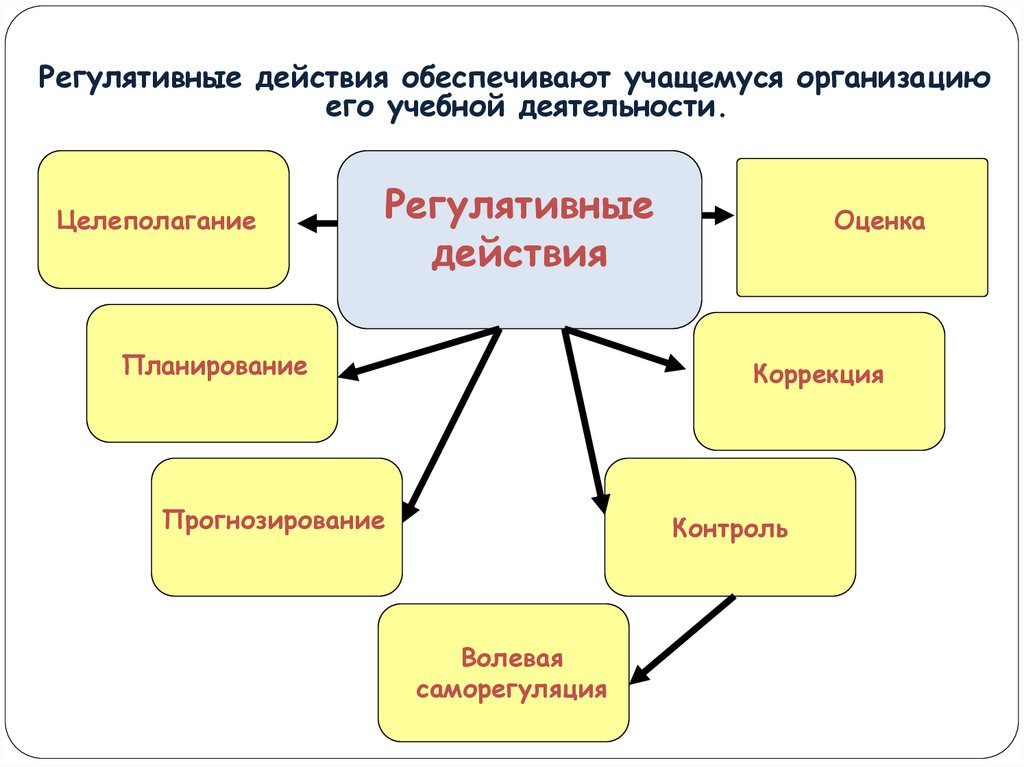
Регулятивные действия обеспечивают учащемуся организациюего учебной деятельности.
Целеполагание
Регулятивные
действия
Планирование
Оценка
Коррекция
Прогнозирование
Контроль
Волевая
саморегуляция
4.
ЦелеполаганиеПриемы целеполагания строятся на диалоге,
поэтому важно грамотно сформулировать
вопросы, учить детей отвечать на них, и задавать
свои.
Цель (как совокупность ожидаемых результатов в
области предмета, метапредметности) необходимо
записать на доске.
В конце урока необходимо вернуться к этой
записи и предложить учащимся не только
проанализировать, что им удалось достичь на
уроке, но и в зависимости от этого –
сформулировать свои образовательные задачи.
Процесс целеполагания – это коллективное
действие.
5.
Приемы целеполаганияТема-вопрос
Работа над понятием
Ситуация яркого пятна
Исключение
Домысливание
Проблемная ситуация
Группировка
Мозговой штурм
Подводящий диалог
Собери слово
Исключение
Проблема
предыдущего урока.
6.
7.
Ночевала тучка золотаяНа груди утёса-великана ...
М. Лермонт ов
На рукомойнике моём
Позеленела медь…
А.Ахмат ова
А за окошком в первом инее
Лежат поля из алюминия.
А.Вознесенский
Сегодня сидишь,
Сердце в железе ...
В. Маяковский
8.
Явления9.
«Собака Баскервиллей»“...Да! Это была собака, огромная, черная, как смоль. Но такой
собаки еще никто из нас, смертных, не видывал. Из ее отверстой
пасти вырывалось пламя, глаза метали искры, по морде и
загривку переливался мерцающий огонь. Ни в чьем воспаленном
мозгу не могло возникнуть видение более страшное, более
омерзительное, чем это адское существо, выскочившее на нас из
тумана...»
Как вы считаете, почему, светится маска на морде чудовища?
Какое простое вещество обладает таким свойством светиться в
темноте? О каком химическом элементе идет речь?
Но могло ли быть такое в действительности, имеет ли фосфор
такие свойства, прав ли был А.Конан-Дойл?
Какая тема урока сегодня?
Что мы рассмотрим сегодня на уроке, какой план изучения вы
можете предложить?
10.
Проблемная ситуацияУченикам предлагается вспомнить, что им
известно о свойствах растворов водородных
соединений неметаллов VI и VII групп, а также
сравнить окраску индикатора лакмуса в водных
растворах водородных соединений хлора и азота.
Что удивило?
Что предполагали увидеть?
Проблемная ситуация: почему растворы имеют
разную среду, хотя оба образованны атомами
неметаллов?
11.
ПланированиеУчащиеся должны выбрать способ достижения
поставленной цели, строят план достижения цели и
определяют средства – алгоритмы, модели, учебник
и т.д.
Для формирования УУД планирования собственной
учебной деятельности эффективны следующие
приёмы:
обсуждение готового плана решения учебной задачи;
работа с деформированным планом решения
учебной задачи;
использование плана с недостающими или
избыточными пунктами;
составление своего плана решения учебной задачи.
12.
Прогнозирование -предвосхищениерезультата
Задачи:
с недостающими и лишними данными
Ответы на вопросы:
«Как думаешь, какой результат может получиться?»,
«Как думаешь, достаточно знать… для выполнения задания?»,
«Какие трудности могут возникнуть и почему?»
При прогнозировании необходимо
уметь
.
проводить анализ и синтез;
применять усвоенные знания в новых нестандартных условиях;
осуществлять обоснование (доказательство);
делать выводы
13.
Пример №1Не прибегая к опыту, определите, какой из двух металлов –
медь или железо – будет реагировать с соляной кислотой.
Пример №2
Определите способ получения, характерные свойства и области
применения гидроксида бария.
Пример №3
Определите элемент, группу и подгруппу, в которой он
находится, а также строение атома, если известно, что
степень его окисления +1, атомная масса наименьшая по
сравнению с другими элементами данной подгруппы. Кроме
того, основный характер его гидроксида выражен наиболее
слабо.
14.
Контроль - сличение способа действия и егорезультата с заданным эталоном с целью
обнаружения отклонений и отличий от эталона
Типовые задания:
«Проверь: прав ли он?»,
«Такой ли получен результат, как в образце?»,
«Правильно ли это делается?»;
«Сможешь доказать?..»,
«Поменяйтесь тетрадями, проверьте работу друг у друга»,
«Проверь по таблице…», «Проверь вывод по…
Прием «Корректор»
При расстановке коэффициентов в следующих записях
допущены ошибки. Исправьте их цветным карандашом (это
может быть текст с ошибками).
а) 4HgO = 4Hg + 2O2
б) 2Al(OH)3 = Al2O3 + 6H2O
в) SO2 + 2O2 = 2SO3
15.
Коррекция - внесение необходимых дополнений и коррективв план и способ действия в случае расхождения эталона,
реального действия и его результата
Типовые задания:
«Помоги исправить ошибки»
«Установи правильный порядок предложений в тексте»
«Помоги восстановить правильный порядок событий»
16.
Оценка -выделение и осознаниеучащимися того, что уже усвоено и что еще нужно усвоить, осознание
качества и уровня усвоения
Закончите предложения и оцените свою
работу:
1)
А вы знаете, что сегодня на уроке я…
2)
Больше всего мне понравилось…
3)
Самым интересным сегодня на уроке
было…
4)
Самым сложным для меня сегодня
было…
5)
Сегодня на уроке я почувствовал
6)
Сегодня я понял…
7)
Сегодня я научился…
8)
Сегодня я задумался….
9)
Сегодняшний урок показал мне
10) На будущее мне надо иметь в виду
Критерии самооценки:
«2» - учебный материал
воспроизвести не могу
«3» – я знаю и понимаю
учебный материал, могу
воспроизвести при
сопровождении
преподавателя.
«4» – я умею и выполняю
самостоятельно учебную
работу по индивидуальной
траектории .
«5» – я исследую учебную
проблему, оформляю
итоги индивидуальной
работы и представляю
(презентую) их публично.
17.
Требования к системе оцениванияИспользование критериальной системы оценивания;
Включение учащихся в контрольно-оценочную деятельность;
Применение дифференцированных оценок;
Использование разнообразных форм оценивания;
Позволять Досдать, ПЕРЕсдать.
* Выполнение тестового задания - максимум 5 баллов.
* Выполнение текстового задания - максимум 3 балла.
* Выполнение карточки – задания - максимум 3 балла.
* Тест - максимум 5 баллов
*
Итого: максимум - 16 баллов.
Ключ к оценке:
* 16-15 баллов - оценка "5";
* 14-11 - оценка "4";
* 10-6 баллов - оценка "3"
18.
Технологии, формирующие РУУД1.
Проблемно – диалогическая технология;
2.
Технология продуктивного чтения;
3.
Технология оценивания учебных успехов;
4.
Технология метода проектов;
5.
Исследовательская деятельность;
6.
Проблемное обучение.
19.
Показатель сформированностирегулятивных УУД
Ученик умеет составлять план действий
Ученик может внести необходимые дополнения и коррективы
в план и способ действия в случае необходимости
Ученик осознает то, что уже усвоено и что еще подлежит
усвоению, а также качество и уровень усвоения
Ученик может поставить учебную задачу на основе соотнесения
того, что уже известно и освоено учащимся, и того. что еще
неизвестно
Ученик способен к волевому усилию
Ученик владеет навыками результирующего, процессуального и
прогностического самоконтроля
У ученика сформирован внутренний план действий
Ученик перед тем, как начать действовать определяет
последовательность действий
Ребенок может адекватно реагировать на трудности и не
боится сделать ошибку
20.
Тема«ОБНАРУЖЕНИЕ ИОНОВ ПРИ ПОМОЩИ КАПЕЛЬНЫХ
РЕАКЦИЙ»
Задача. В четырёх пронумерованных
пробирках находятся хлорид, сульфат
и карбонат натрия. Соединения могут
отсутствовать или повторяться.
Определите, в какой пробирке какое
вещество находится, используя
реактивы. Напишите краткие ионные
уравнения реакции.
Реактивы. Проба; растворы HNO3 ,
AgNО3 , Ва(NOз)2
Оборудование. Пробирки, штатив
для пробирок, ёмкость для
дистиллированной воды, ёмкость для
слива.
Задача1
Дан раствор хлорида магния.
Прилейте поочередно растворы:
а) гидроксида натрия,
б) карбоната натрия, в) нитрата
серебра, г) фосфата калия.
Запишите уравнения реакций в
молекулярном, полном ионном и
сокращенном ионном видах.
21.
Тема«ОБНАРУЖЕНИЕ ИОНОВ ПРИ ПОМОЩИ КАПЕЛЬНЫХ
РЕАКЦИЙ»
На основе таблицы
растворимости
составляют таблицу
ожидаемых
взаимодействий,
вписав в клетки
сокращённые ионные
уравнения реакции и
обязательно
отмечают выпадение
осадка и выделение
Вещества
HN03реакция
AgN03
Ва(NOз)
газа . Если
не2
идётИоны
— ставят
Н+
Ag+
Ва2+
прочерк..
NaCl
СlТаблица ожидаемых
взаимодействий (с указанием
СОз2осадков и газов)
Na2СОз
Na2S04
S042-
Регулятивные УД
- планирование
-прогнозирование
Познавательные УД
(общеучебные УД)
-выбор наиболее
эффективных
способов решения
задачи в зависимости
от конкретных
условий
-смысловое чтение с
целью извлечения
необходимой
информации
Коммуникативные УД
-управление
поведением партнера





















 Образование
Образование








