Похожие презентации:
Неметаллы. Азот
1. НЕМЕТАЛЛЫ
АЗОТ - «Безжизненныйэлемент, но важная
составная часть жизни».
2. ЦЕЛИ :
Сформировать представлениео строении атома и молекулы
азота.
Рассмотреть физические и
химические свойства азота.
Показать значение азота как
биогенного элемента.
3. ПЛАН УРОКА
История открытияНахождение в природе
Строение и свойства атома и молекулы
Физические свойства
Химические свойства
Получение
Применение
4. ДЕВИЗ УРОКА :
«Нет жизни без азота, ибо онявляется непременной
составной частью белков.»
Д.Н.Прянишников
5. ИСТОРИЯ ОТКРЫТИЯ
К.Шееле и Г.Кавендиш получили азот1772г. Д.Резерфорд описал получение и
свойства
1787г. Лавуазье предложил название азот –
«безжизненный» (а – нет, зоэ – жизнь)
Многочисленные названия: нечистый газ,
удушливый газ, испорченный воздух, огорюченный
воздух, селитрород, гнилотвор, смертельный газ,
нитроген и др.
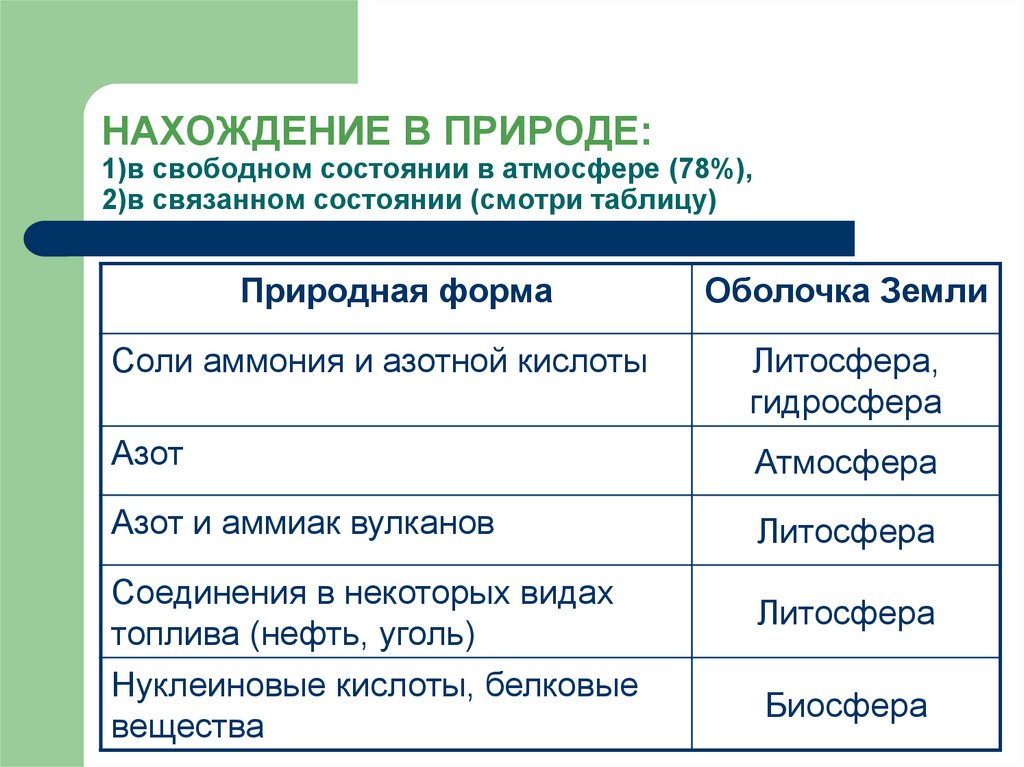
6. НАХОЖДЕНИЕ В ПРИРОДЕ: 1)в свободном состоянии в атмосфере (78%), 2)в связанном состоянии (смотри таблицу)
Природная формаОболочка Земли
Соли аммония и азотной кислоты
Литосфера,
гидросфера
Азот
Атмосфера
Азот и аммиак вулканов
Литосфера
Соединения в некоторых видах
топлива (нефть, уголь)
Нуклеиновые кислоты, белковые
вещества
Литосфера
Биосфера
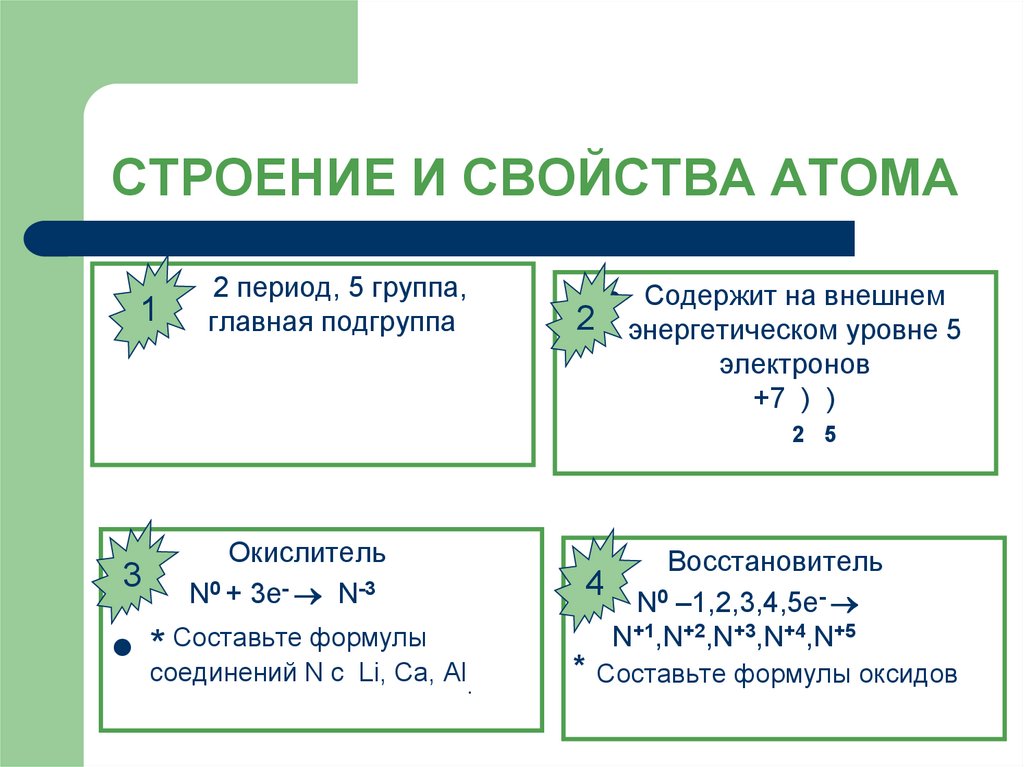
7. СТРОЕНИЕ И СВОЙСТВА АТОМА
12 период, 5 группа,
главная подгруппа
2
Содержит на внешнем
энергетическом уровне 5
электронов
+7 ) )
2 5
3
Окислитель
N0 + 3e- N-3
* Составьте формулы
соединений N с Li, Са, Al.
Восстановитель
4 N0 –1,2,3,4,5e-
N+1,N+2,N+3,N+4,N+5
* Составьте формулы оксидов
8. Проверь себя
Li3N, Ca3N2, AlN, H3NN2O, NO, N2O3, NO2, N2O5.
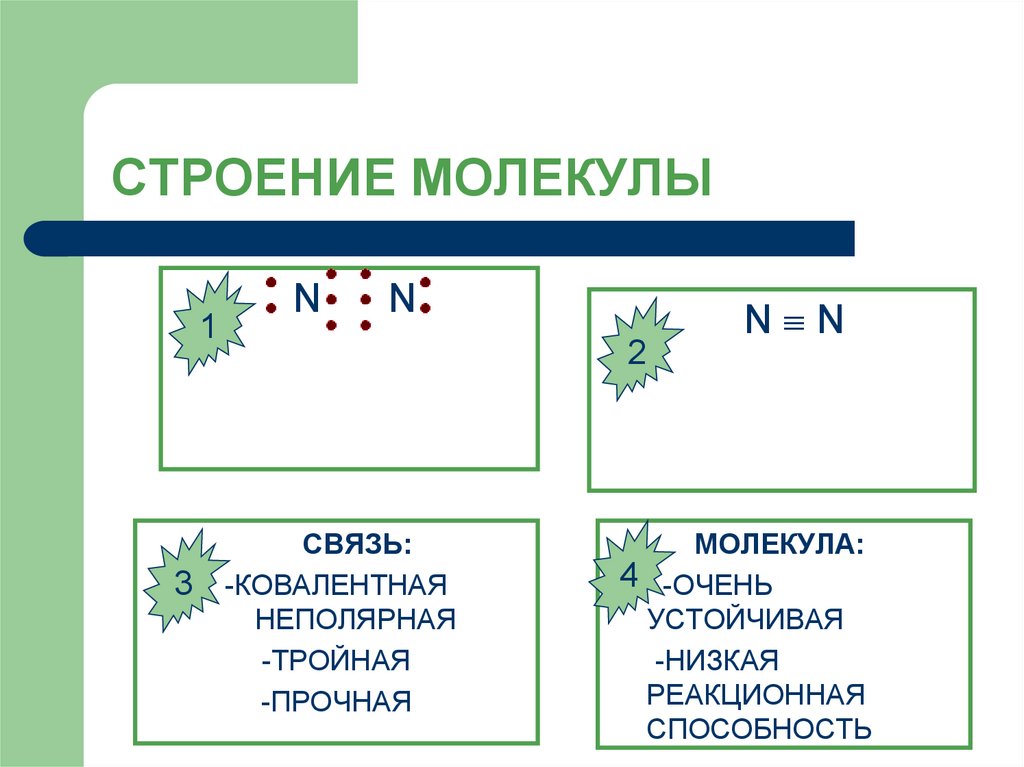
9. СТРОЕНИЕ МОЛЕКУЛЫ
13
N
N
2
СВЯЗЬ:
-КОВАЛЕНТНАЯ
НЕПОЛЯРНАЯ
-ТРОЙНАЯ
-ПРОЧНАЯ
N N
МОЛЕКУЛА:
4 -ОЧЕНЬ
УСТОЙЧИВАЯ
-НИЗКАЯ
РЕАКЦИОННАЯ
СПОСОБНОСТЬ
10. ФИЗИЧЕСКИЕ СВОЙСТВА.
Газ без цвета, запаха и вкусаПлохо растворим в воде
Немного легче воздуха, плотность 1,2506
кг/м3
Tºпл.= -210ºС
Tºкип.= -196ºС
Не поддерживает дыхание и горение
11. ХИМИЧЕСКИЕ СВОЙСТВА Задание: составить уравнения химических реакций.
ОкислительныеN20
2N-3
При нагревании с
другими
металлами(Ca, Al, Fe)
При комнатной tº
только с Li
*При высокой tº, р, kat
(Fe, оксиды Al, K) с H2
Восстановительные
N20
2N+2
*При
tº электрической
дуги (3000 - 4000ºС) с
О2
12. ПРИМЕНЕНИЕ АЗОТА
ПрименениеПолучение аммиака и азотной
кислоты.
Создание инертной атмосферы в
металлургии.
Производство азотных удобрений.
Производство взрывчатых веществ.
Жидкий азот в медицине.
Насыщение поверхности стали для
повышения прочности
13. Получение азота
ПолучениеВ промышленности – из
жидкого воздуха
В лаборатории –
разложением неустойчивых
соединений азота
14. Вопросы для самоконтроля
1.2.
3.
4.
5.
6.
7.
8.
9.
10.
Газ без цвета , вкуса и запаха
Молекула двухатомна
Содержание в воздухе 78 %
В лаборатории получают разложением KMnO4 и
H2O2
В промышленности – из жидкого воздуха
Химически малоактивен
Взаимодействует почти со всеми простыми
веществами
С ним связаны процессы дыхания и фотосинтеза
Является составной частью белков
Участвует в круговороте веществ в природе
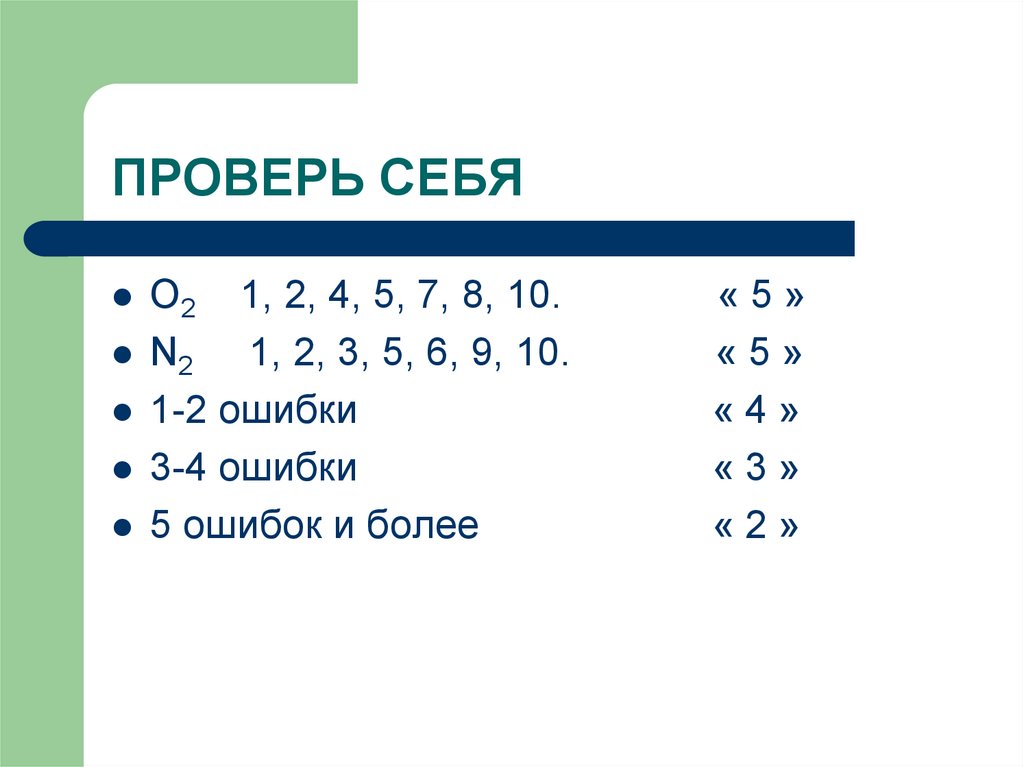
15. ПРОВЕРЬ СЕБЯ
O2 1, 2, 4, 5, 7, 8, 10.N2 1, 2, 3, 5, 6, 9, 10.
1-2 ошибки
3-4 ошибки
5 ошибок и более
«5»
«5»
«4»
«3»
«2»
16. Домашнее задание
Параграф №23 , выполнить задания 1,3 настранице 111
Составить рассказ на тему: «Путешествие азота в
природе»
Ответить на вопросы: Как можно доказать
опытным путём, что в воздухе есть азот? Для
перевозки овощей и фруктов на дальние
расстояния используют рефрижераторы, в которых
в качестве хладоагента используют жидкий АЗОТ.
На каких свойствах это основано?












 Химия
Химия








