Похожие презентации:
Кислоты. Определение
1.
Презентация для учащихся8 – 9 классов
Учитель : Касимова С.П.
2.
1.Определение
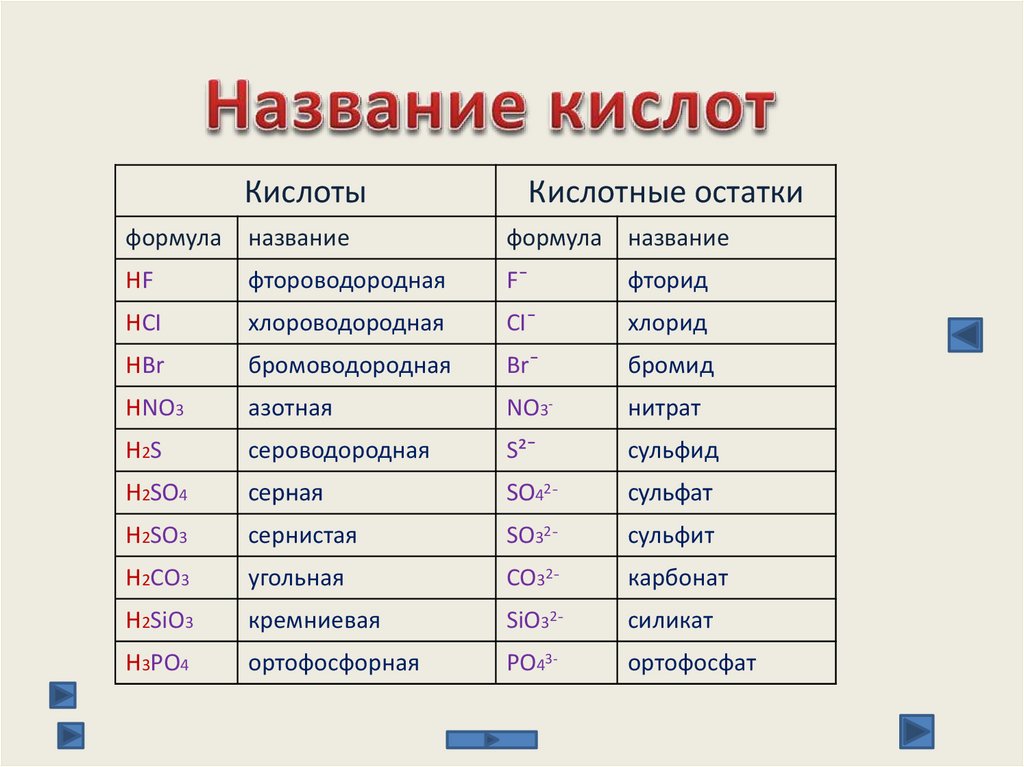
2. Название кислот
3. Определение степени окисления
кислотного остатка
4. Задание №1
5. Лабораторная работа
6. Изменение окраски индикатора
7. Классификация кислот
8. Задание №2
9. Кислоты в природе
10. Кислоты в организме человека
11. Домашнее задание
3.
Кислоты – это сложныевещества, состоящие из ионов
водорода и кислотного остатка
Например:
HCI H2SO4 H3PO4
Кислотный остаток
4.
КислотыКислотные остатки
формула
название
формула название
HF
фтороводородная
F¯
фторид
HCI
хлороводородная
CI¯
хлорид
HBr
бромоводородная
Br¯
бромид
HNO3
азотная
NO3-
нитрат
H2S
сероводородная
S²¯
сульфид
H2SO4
серная
SO42¯
сульфат
H2SO3
сернистая
SO32¯
сульфит
H2CO3
угольная
CO32¯
карбонат
H2SiO3
кремниевая
SiO32¯
силикат
H3PO4
ортофосфорная
PO43-
ортофосфат
5.
Определение степениокисления кислотного остатка
Степень окисления кислотного
остатка определяется по числу
атомов водорода в молекуле
данной кислоте
6.
Подчеркнуть кислотный остаток иопределить его степень окисления:
HNO3 H2SO4 H3PO4
7.
Найти соответствиеОксиды:
Кислоты:
СО2
Н2SO4
P2O5
H2CO3
SO3
H2SO3
SO2
H3PO4
8.
Используя имеющиеся индикаторыопределить кислоту среди
выданных соединений
9.
ИндикаторОкраска
индикатора в
нейтральной среде
Окраска
индикатора в
кислотной среде
10.
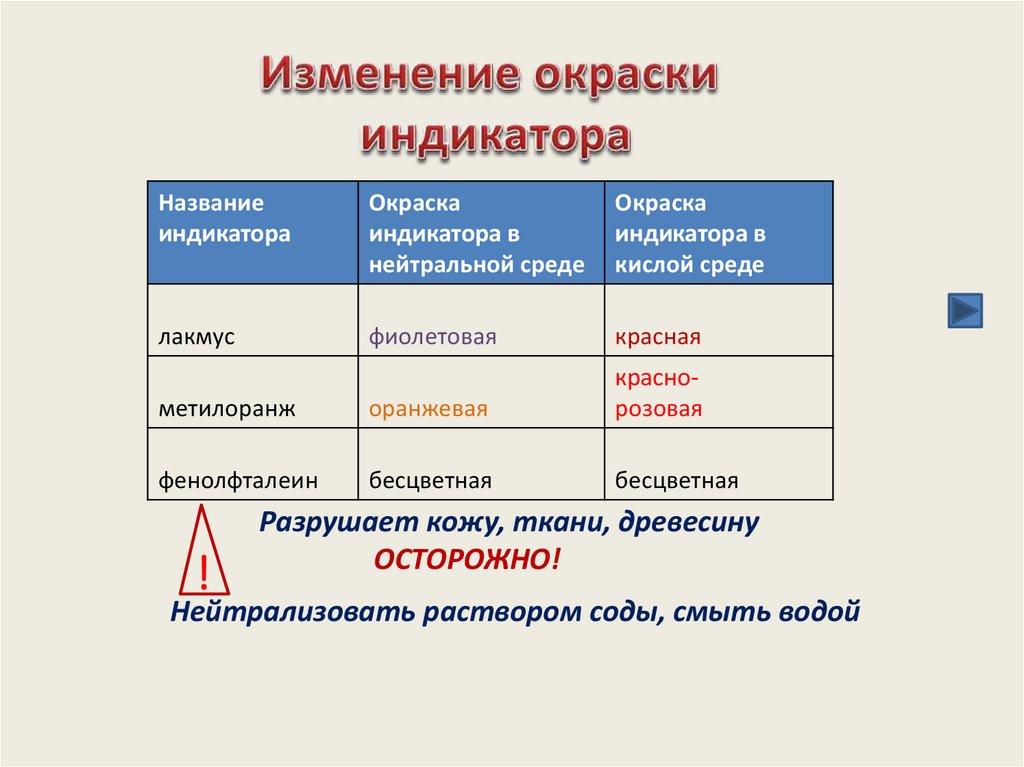
Названиеиндикатора
Окраска
индикатора в
нейтральной среде
Окраска
индикатора в
кислой среде
лакмус
фиолетовая
красная
метилоранж
оранжевая
краснорозовая
фенолфталеин
бесцветная
бесцветная
!
Разрушает кожу, ткани, древесину
ОСТОРОЖНО!
Нейтрализовать раствором соды, смыть водой
11.
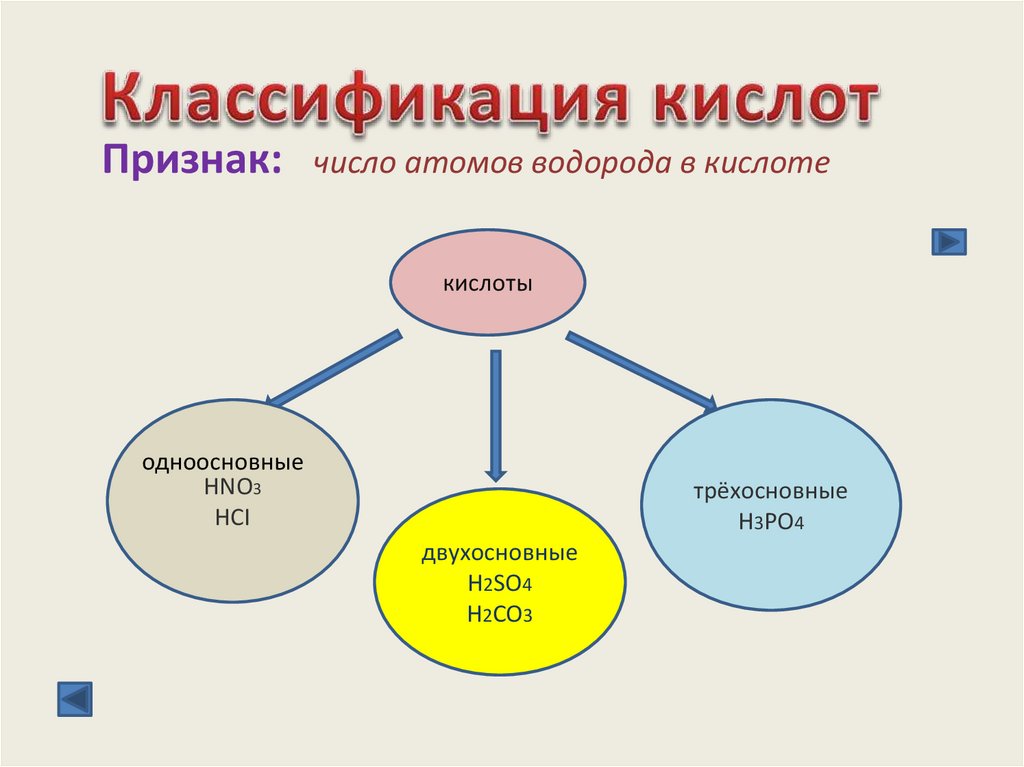
Признак:число атомов водорода в кислоте
кислоты
одноосновные
HNO3
HCI
трёхосновные
H3PO4
двухосновные
H2SO4
H2CO3
12.
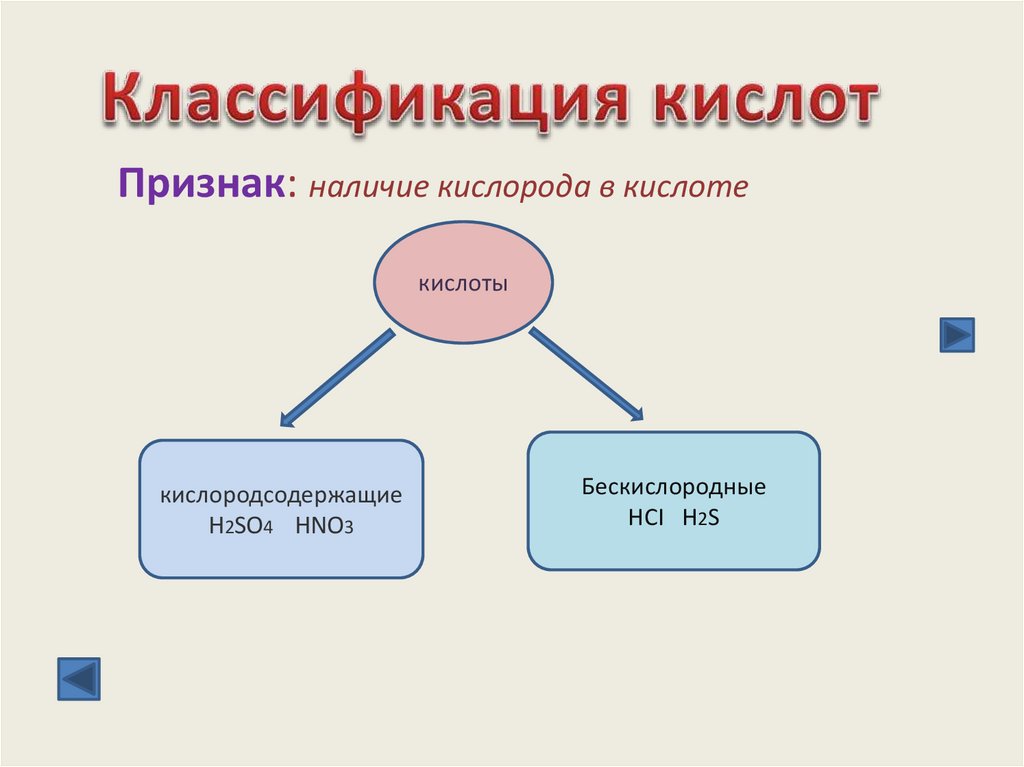
Признак: наличие кислорода в кислотекислоты
кислородсодержащие
H2SO4 HNO3
Бескислородные
HCI H2S
13.
Среди представленных формулкислот: H2SO4 HNO3 H2S H3PO4
выбрать
одноосновную кислородсодержащую
двухосновную бескислородную
14.
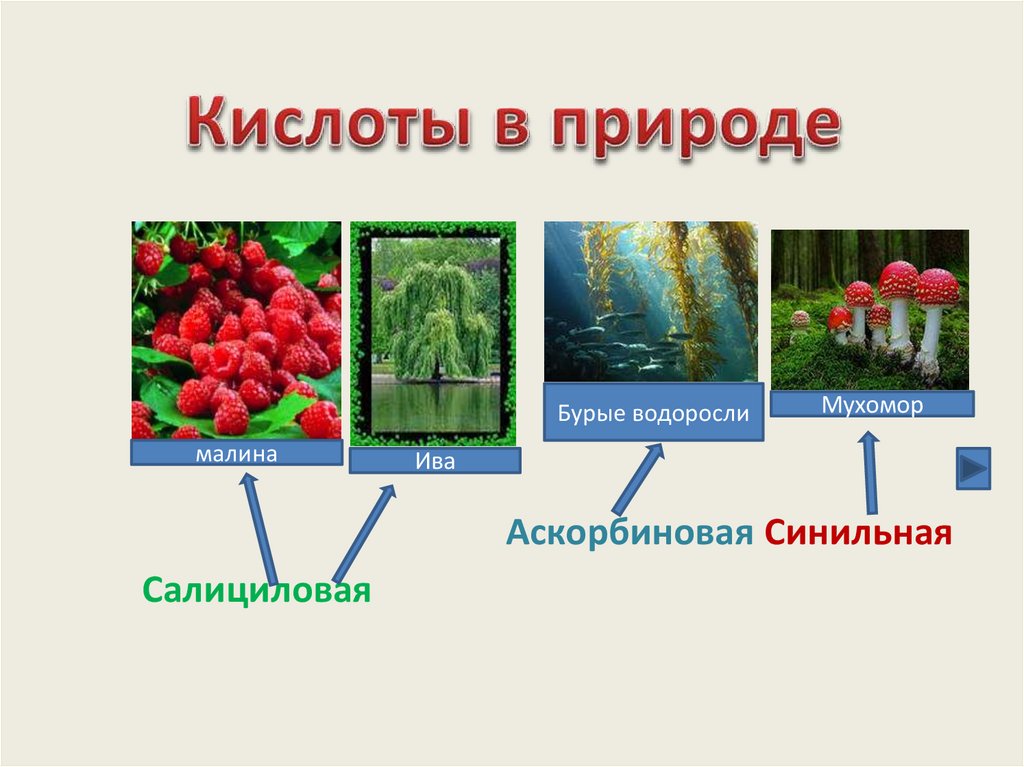
Бурые водорослималина
Мухомор
Ива
Аскорбиновая Синильная
Салициловая
15.
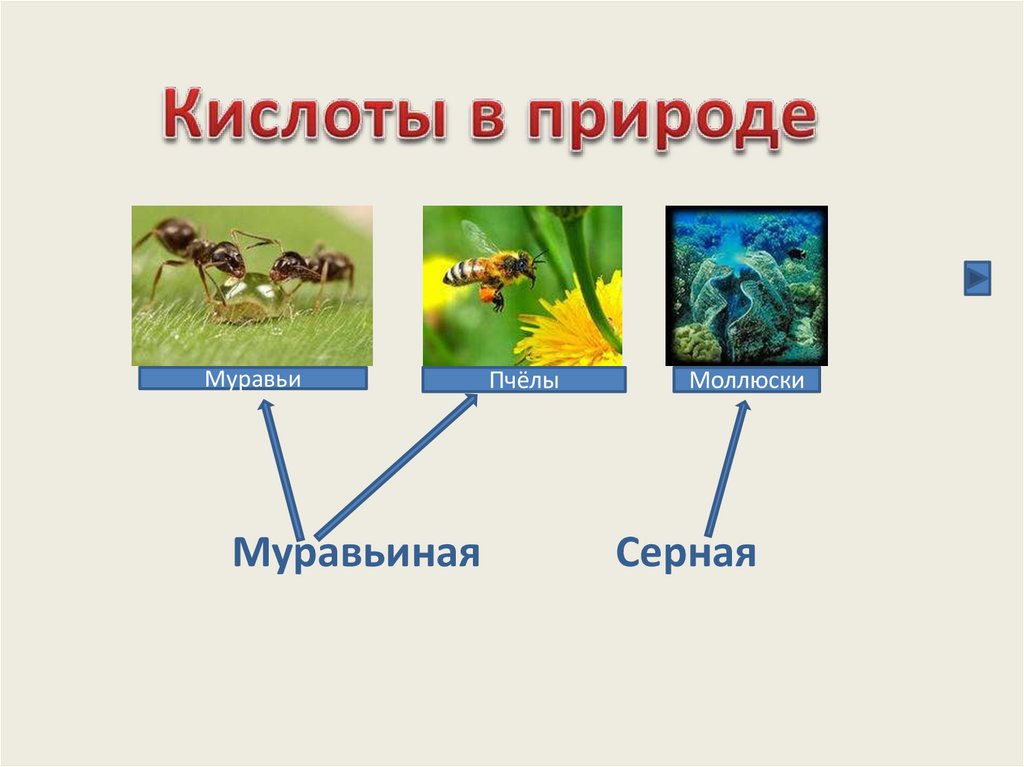
МуравьиМуравьиная
Пчёлы
Моллюски
Серная
16.
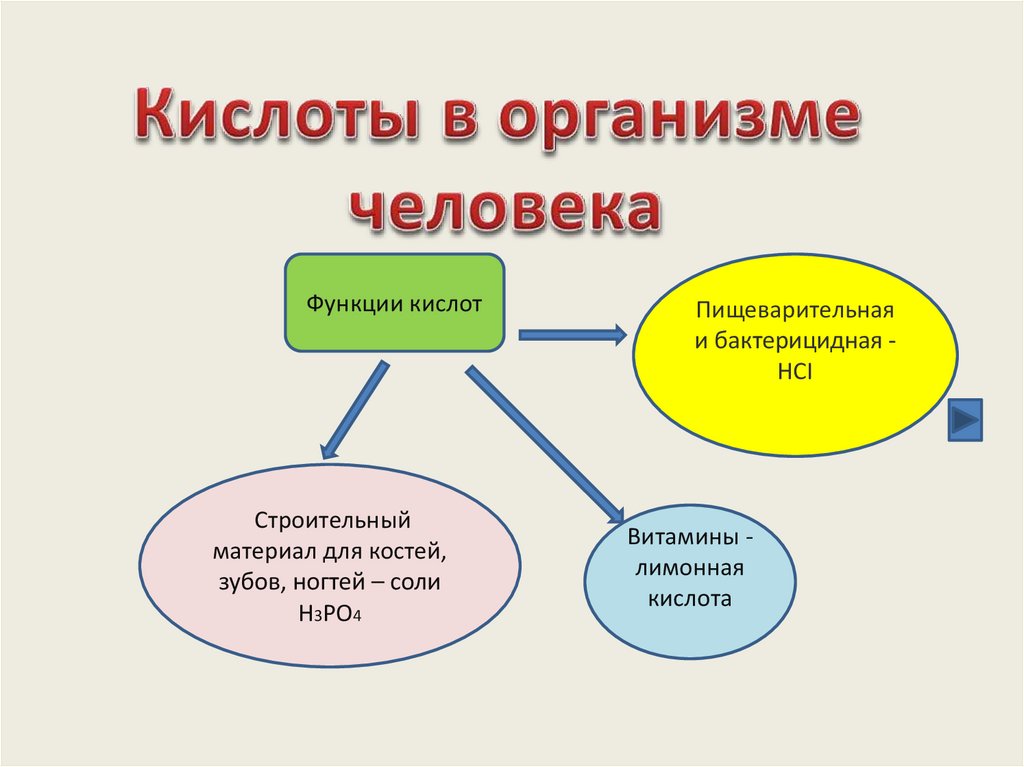
Функции кислотCтроительный
материал для костей,
зубов, ногтей – соли
H3PO4
Пищеварительная
и бактерицидная HCI
Витамины лимонная
кислота
17.
Разрушение памятников культурыЗакисление почв
Гибель лесов
18.
Металлургические ихимические
предприятия
автотранспорт
Извержение вулканов
Авиация
Теплоэлектростанции
19.
Общее : § 20 с.107 № 1По выбору:
1. Небольшое интересное
сообщение о какой-либо
кислоте или презентация
2. Составить кроссворд












 Химия
Химия








