Похожие презентации:
Урок открытия новых знаний. Химия. 9 класс
1.
Урокоткрытия
новых
знаний
Химия 9 класс
Подготовила:
2021год
Пряхина Е.А.
учитель химии
и биологии
2.
• Изучение какого-либопроцесса, происходящего в
природе или в лаборатории,
тесно связано с
химическими реакциями.
Вот и мы сегодня не просто
будем говорить о
природном явлении, но и
будем проводить опыты.
Тему нашего изучения мы
узнаем в процессе урока.
3.
Работа у демонстрационногостола:
-Растворение мыльного
раствора в талой воде и в воде
из под крана.
Вывод:
-В талой воде мыло пенится
хорошо, а в воде из под крана
плохо.
4.
Почему в воде из подкрана мыло пенится
плохо?
• Вода из-под крана имеет
примеси…. Они обуславливают
особое свойство воды жесткость. А в жесткой воде
мыло не мылится.
5.
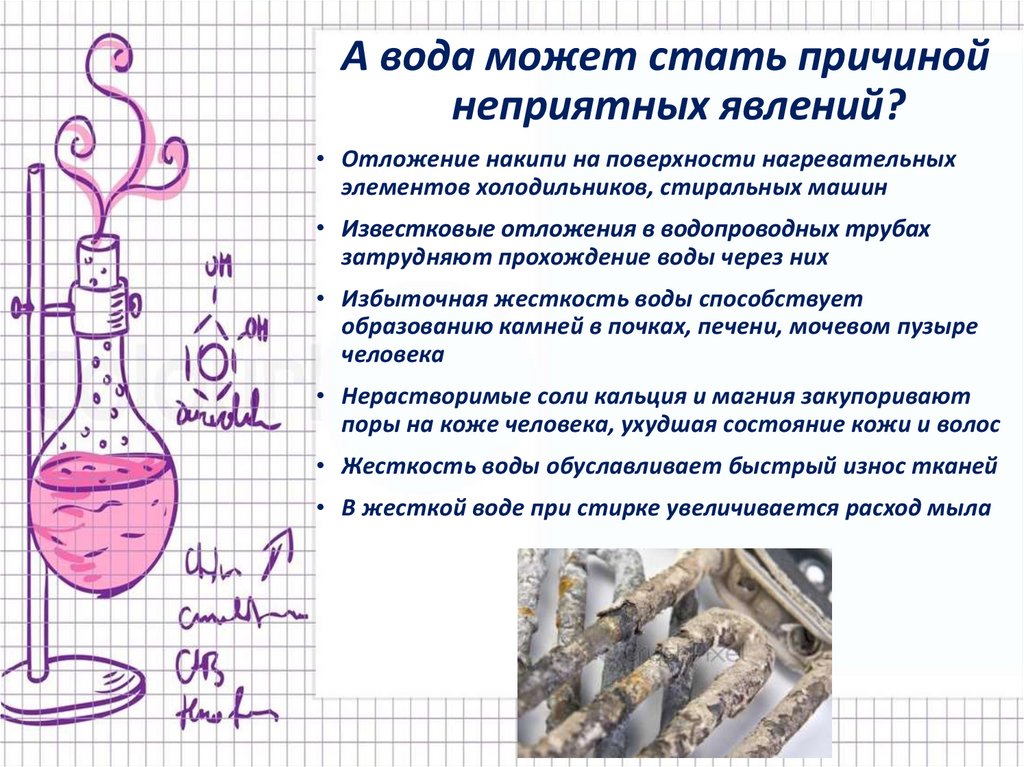
А вода может стать причинойнеприятных явлений?
• Отложение накипи на поверхности нагревательных
элементов холодильников, стиральных машин
• Известковые отложения в водопроводных трубах
затрудняют прохождение воды через них
• Избыточная жесткость воды способствует
образованию камней в почках, печени, мочевом пузыре
человека
• Нерастворимые соли кальция и магния закупоривают
поры на коже человека, ухудшая состояние кожи и волос
• Жесткость воды обуславливает быстрый износ тканей
• В жесткой воде при стирке увеличивается расход мыла
6.
Чтобы разобраться спонятием жесткость воды,
поставим цели на сегодняшний
урок:
1. Изучить природу жёсткости
воды
2. Узнать о способах устранения
жесткости воды
3. Познакомиться с видами
жесткости
7.
1. Природа жесткостиR-COONa = R-COO- + Na+
Повышенное содержание Са2+ и
Mg2+ придаёт воде
отрицательное качество,
называемое жёсткостью.
2R-COO- + Са2- = (R-COO)2Са
8.
• Жесткость может быть вызвананаличием в воде растворимых
средних солей кальция и магния –
хлоридов или сульфатов
Ca Cl2, MgSO4
• Но не только средние
растворимые соли кальция и
магния являются причиной
жесткости воды, но и их кислые
соли:
Ca(HCO3)2 = Ca2+ + 2HCO3 -
9.
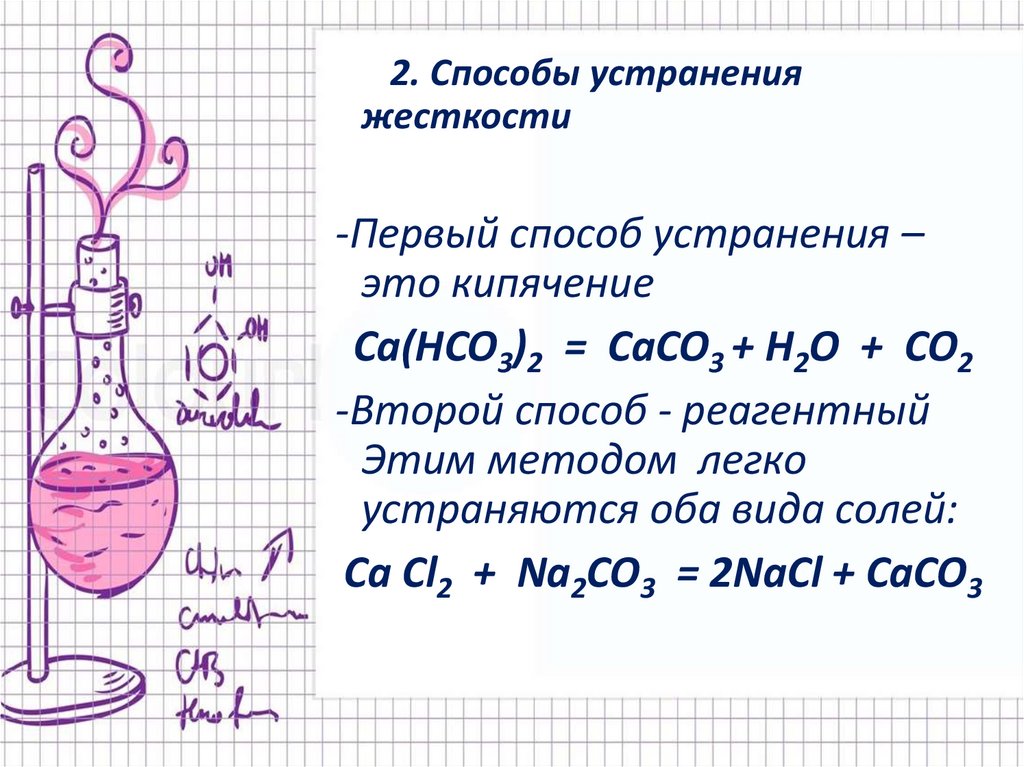
2. Способы устраненияжесткости
-Первый способ устранения –
это кипячение
Ca(HCO3)2 = CaCO3 + H2O + CO2
-Второй способ - реагентный
Этим методом легко
устраняются оба вида солей:
Ca Cl2 + Na2CO3 = 2NaCl + CaCO3
10.
3. Виды жесткости:- Жесткость, обусловленная
содержанием в ней
гидрокарбонатов кальция и
магния, устраняемая
кипячением - временная
жесткость
- Жесткость, обусловленная
содержанием в ней других
соединений кальция и магния
(хлоридов и сульфатов) и не
устраняемая кипячением постоянная жесткость
11.
• Какая самая жесткая вода вприроде?
• А какая самая мягкая?
• Соли, необходимые для нашего
организма поступают с
минеральной водой ( если 1 г/л
и более). Разные источники
содержат разный набор
ионов. Наиболее известен
район Кавказских
Минеральных Вод (Нарзан в
Кисловодске 2-3 г/л).
12.
13.
Приготовьте три пробирки с жесткой водой –налейте по 2 мл в каждую:
1. В первую добавьте 1 мл мыльного раствора, закройте
пробирку и встряхните. Что наблюдаете? Почему?
2. Вторую пробирку закрепите в пробиркодержателе и
нагрейте над пламенем спиртовки (равномерно
прогреваем), доводим до кипения. Объясните
наблюдаемое явление. Какой тип жесткости
устраняется кипячением? Какие соли ее вызывают?
Напишите реакцию.
3. В третью пробирку добавьте 1-2 мл раствора соды.
Также объясните наблюдаемое явление. Какой тип
жесткости устраняется добавлением реагентов
(соды). Напишите реакции с солями, которые
вызывают эту жесткость.
14.
1. Наблюдаем образование хлопьевидного осадка.Объясняется это тем, что в воде присутствуют
ионы кальция и магния. Мыло это растворимые
соли жирных кислот, а магний и кальций образует
с ними в растворе нерастворимые осадки. Пока
они в растворе, мыло не будет мылиться.
2. Наблюдаем выпадение осадка. Объясняется это
тем, что в воде имеются кислые соли магния и
кальция, которые обуславливают временную
жесткость воды. Её можно устранить
кипячением
Ca(HCO3)2 = CaCO3 + H2O + CO2
3. При добавлении соды также выпадает осадок,
так как идет реакция с хлоридами и сульфатами
магния и кальция, которые обуславливают
постоянную жесткость воды
Ca Cl2 + Na2CO3 = 2NaCl + CaCO3
MgSO4 + Na2CO3 = Na2SO4 + MgCO3
15.
Какие бываютвиды жесткости?
Как устранить
жесткость воды?
К каким
последствиям
приводит жесткая
вода?
16.
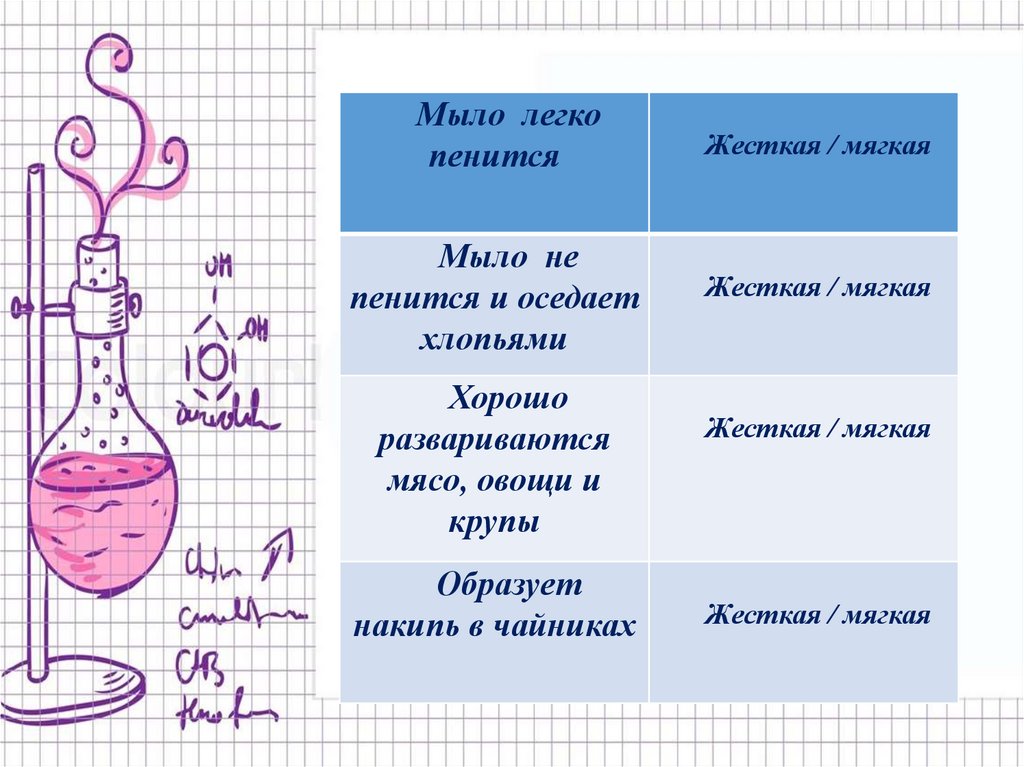
Мыло легкопенится
Мыло не
пенится и оседает
хлопьями
Хорошо
развариваются
мясо, овощи и
крупы
Образует
накипь в чайниках
Жесткая / мягкая
Жесткая / мягкая
Жесткая / мягкая
Жесткая / мягкая
17.
Супер! Все очень понятно)Я хорошо усвоил эту тему)
Не всё понятно, но я старался)
Я ничего не понял(
18.
Параграф 32, отвечать навопросы, выучить новые
понятия
Спасибо за
работу)))















 Химия
Химия








