Похожие презентации:
Что скрывается в этих тезисах?
1.
Что скрывается в этих тезисах?Это вещество было описано арабским
химиком в VIII веке Джабиром ибн Хайяном
(Гебер) в его труде «Ямщик мудрости», а с ХV
века это вещество добывалось для
производственных целей
Благодаря этому веществу русский учёный
В.Ф. Петрушевский в 1866 году впервые
получил динамит
2.
Что скрывается в этих тезисах?Это вещество является компонентом
ракетного топлива, его использовали для
двигателя первого в мире советского
реактивного самолёта БИ – 1
Это вещество – прародитель большинства
взрывчатых веществ (например, тротила, или
тола)
3.
Что скрывается в этих тезисах?Это вещество в смеси с соляной кислотой
растворяет платину и золото, признанное
«царём» металлов. Сама смесь, состоящая из
1-ого объёма этого вещества и 3-ёх объёмов
соляной кислоты, называется «царской
водкой».
4.
Так что мы сегодня будем изучатьна уроке?
Тема «Азотная кислота»
5.
Строение и свойства молекулыазотной кислоты:
• «дымится на воздухе», на свету
желтеет, т. к. подвергается
разложению
•Сильная кислота – сильный
окислитель (ст/о = +5)
• Mr(HNO3)
= 63
• жидкость;
4HNO3 = 2H2O +4NO2 + O2
6.
Лабораторный опыт «Определение реакции средыазотной кислоты».
уравнение диссоциации:
HNO3 H+ + NO3-.
Гипотеза:
Азотной кислоте должны быть
характерны общие свойства кислот!
7.
1 группа:провести реакцию раствора азотной кислоты
и оксида меди (II), записать уравнение
реакции, определить ее тип.
При необходимости можно нагреть для
увеличения скорости химической реакции.
CuO + 2 HNO3 = Cu(NO3)2 + H2O
реакция ионного обмена,
необратимая
CuO + 2H+ + 2 NO3- = Cu2+ + 2 NO3- + H2O
CuO + 2H+ = Cu2+ + H2O
8.
2 группа:провести реакцию растворов азотной кислоты и
гидроксида натрия в присутствии фенолфталеина,
записать уравнение реакции, определить ее тип.
HNO3 + NaOH = NaNO3 + H2O
реакция ионного обмена, необратимая
H+ + NO3- + Na+ + OH- = Na+ + NO3- + H2O
H+ + OH- = H2O
Реакция нейтрализации; в результате раствор
щелочи, подкрашенный индикатором,
обесцветился
9.
3 группа:получить нерастворимое основание Cu(OH)2; провести
реакцию раствора азотной кислоты и гидроксида меди
(II); записать уравнение реакции, определить ее тип.
CuCl2 + 2 NaOH = Cu(OH)2 + 2 NaCl
Cu(OH)2 + 2 HNO3 = Cu(NO3)2 + 2 H2O
реакция ионного обмена, необратимая
Cu(OH)2 + 2H+ + 2 NO3- = Cu2+ + 2 NO3- + 2 H2O
Cu(OH)2 + 2H+ = Cu2+ + 2 H2O
Признак реакции – растворение голубого осадка
Cu(OH)2.
10.
4 группа:провести реакцию растворов азотной кислоты и
карбоната натрия, записать уравнение реакции,
определить ее тип
• 2 HNO3 + Na2CO3 = 2 NaNO3 + H2O + CO2
• реакция ионного обмена, необратимая
2 H+ + 2NO3- + 2 Na+ + CO3 2- = 2 Na+ +NO3- + H2O
+ CO2
• 2 H+ + CO3 2- = H2O + CO2
• Признак реакции – характерное
«вскипание».
11.
Так в чём же причина необычногоповедения азотной кислоты?
• с раствором серной кислоты
окислителем является протон
водорода, а в случаях с азотной
кислотой окислитель - атом азота
нитрат-аниона.
12.
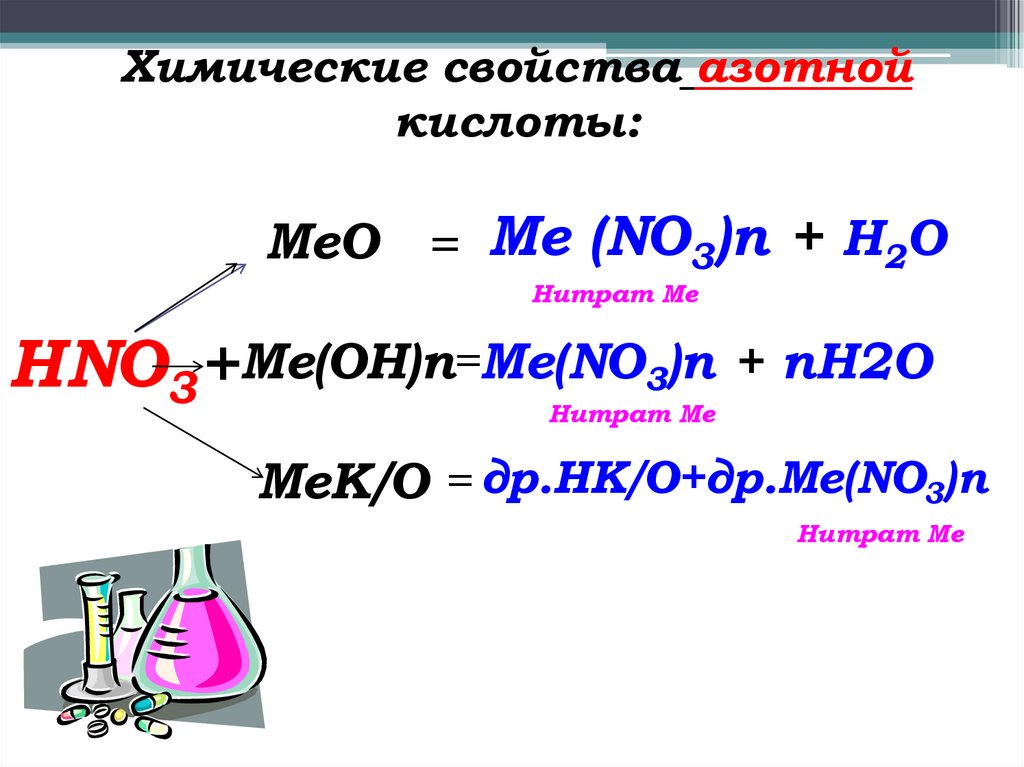
Химические свойства азотнойкислоты:
MeO = Me (NO3)n + H2O
Нитрат Ме
HNO3+Me(OH)n=Me(NO3)n + nH2O
Нитрат Ме
MeК/О = др.HK/O+др.Me(NO3)n
Нитрат Ме
13.
Специфические химическиесвойства концентрированной
азотной кислоты
Fe , Al + HNO3 ---- НЕ ВЗАИМОДЕЙСТВУЮТ,
т.к. образуют защитную пленку ==
ПАССИВИРОВАНИЕ
хранение и
транспортировка азотной кислоты.
Au + HNO3 + 3HCL = AuCl3 + NO + 2H2O
« царская водка»
14.
Свойстваконцентрированной
азотной кислоты:
Cu + 4HNO3 = Cu(NO3)2+2H2O + 2NO2
( конц.)
бурый
Cu
0
N
+5
---2 e
-------- Cu
+1 е
-------- N
+2
+4
15.
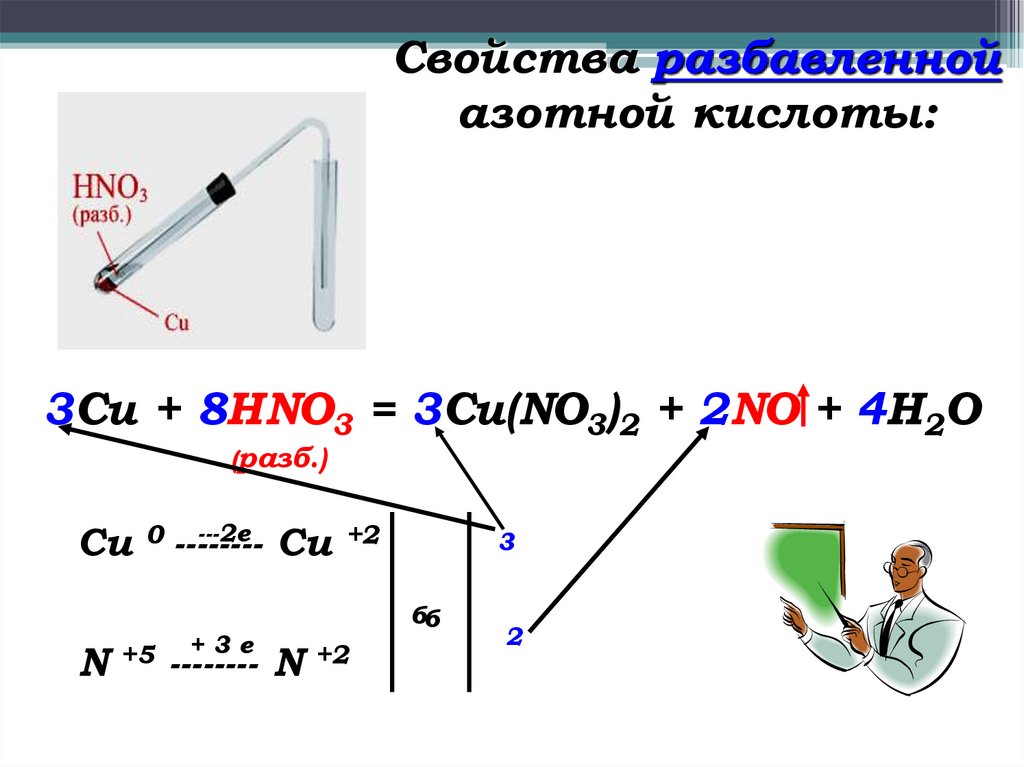
Свойства разбавленнойазотной кислоты:
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O
(разб.)
Cu
N
0
+5
---2e
-------Cu
+3e
-------- N
+2
3
66
+2
2
16.
вывод:азотная кислота взаимодействовала с
медью, т.к. она особенная, за счёт
атома азота нитрат иона.
17.
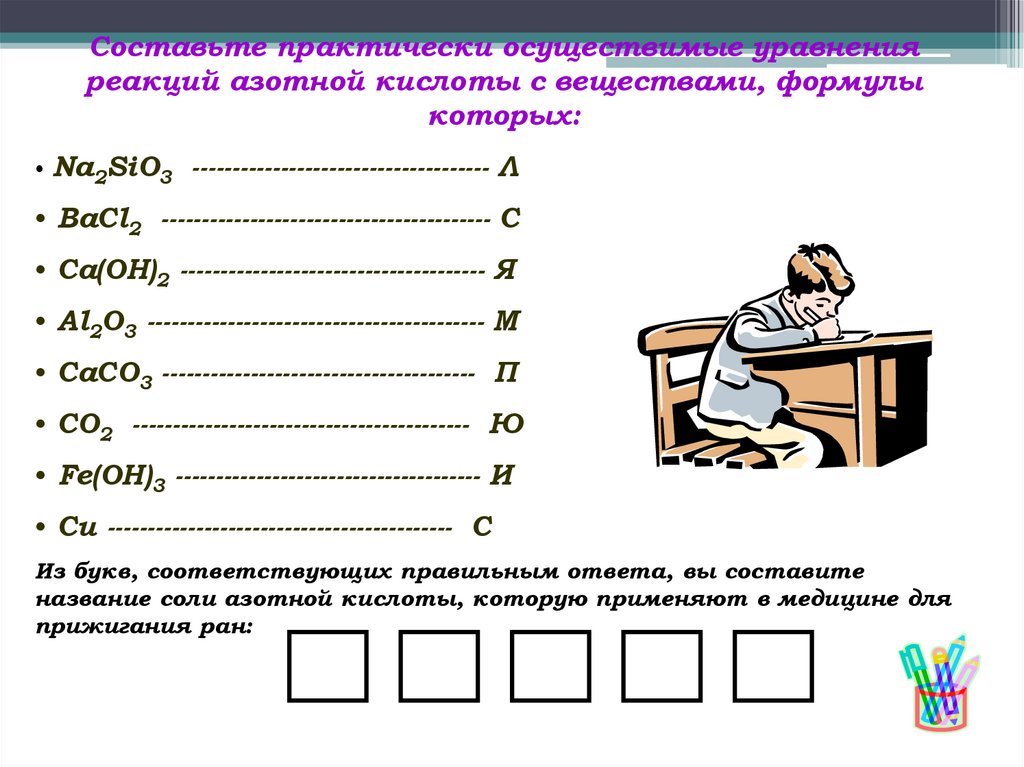
Составьте практически осуществимые уравненияреакций азотной кислоты с веществами, формулы
которых:
Na2SiO3 ------------------------------------- Л
• BaCl2 ----------------------------------------- С
• Ca(OH)2 -------------------------------------- Я
• Al2O3 ------------------------------------------ М
• CaCO3 --------------------------------------- П
• CO2 ------------------------------------------ Ю
• Fe(OH)3 -------------------------------------- И
• Cu ------------------------------------------- С
Из букв, соответствующих правильным ответа, вы составите
название соли азотной кислоты, которую применяют в медицине для
прижигания ран:














 Химия
Химия








