Похожие презентации:
Признаки химических реакций
1.
*Тема: «Признакихимических
реакций»
2.
*Цель: Закрепить на практике знания учащихся о
признаках химических реакций
Задачи:
Обучающие – экспериментально исследовать
некоторые из признаков химических реакций.
Продолжить умение работать с лабораторным
оборудованием, реактивами.
Развивающие – развить мышление, умение делать
логические выводы из наблюдений по опыту.
Воспитывающие – воспитать наблюдательность,
аккуратность при выполнении практической работы с
соблюдением техники безопасности.
3.
* План урока:1.
2.
3.
4.
5.
6.
Организационный момент. Вводное слово
учителя о целях и задачах урока.
Повторение признаков химических реакций.
Просмотр видеоопытов. Составление
химических уравнений реакций и определение
их типов.
Правила техники безопасности.
Выполнение практической работы.
Оформление полученных результатов и выводов
экспериментов.
Подведение итогов.
4.
*«Ни одна наука не нуждается вэксперименте такой степени
как химия. Её основные законы,
теории и выводы опираются на
факты. Поэтому постоянный
контроль опытом необходим»
Майкл Фарадей
5.
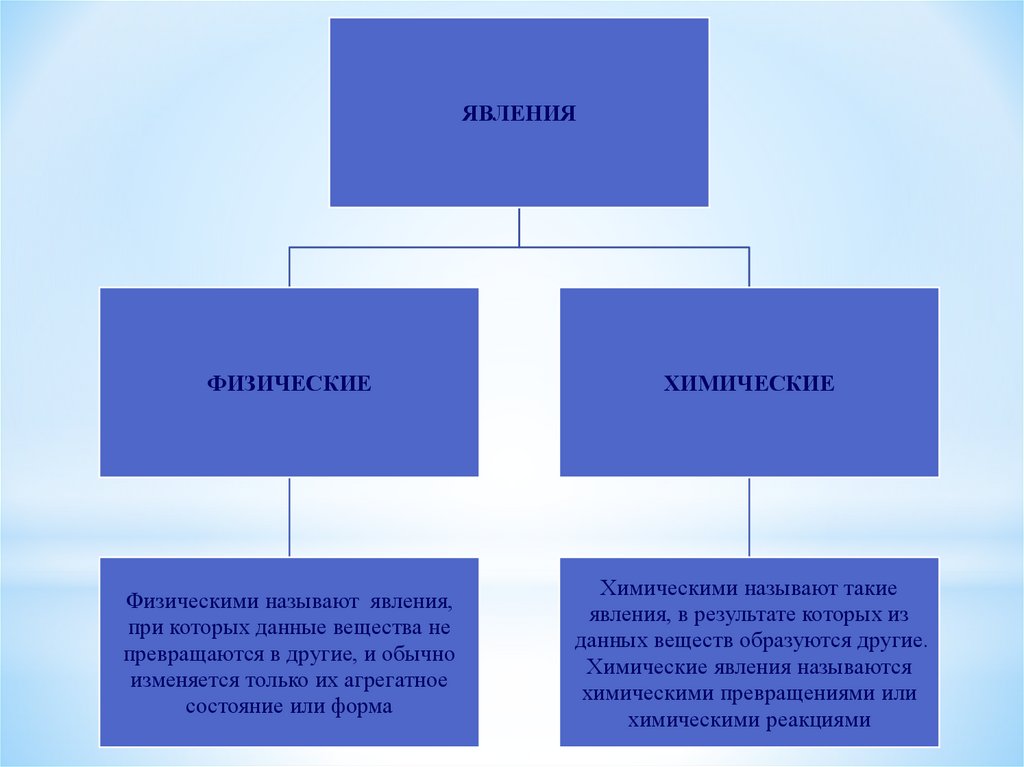
ЯВЛЕНИЯФИЗИЧЕСКИЕ
ХИМИЧЕСКИЕ
Физическими называют явления,
при которых данные вещества не
превращаются в другие, и обычно
изменяется только их агрегатное
состояние или форма
Химическими называют такие
явления, в результате которых из
данных веществ образуются другие.
Химические явления называются
химическими превращениями или
химическими реакциями
6.
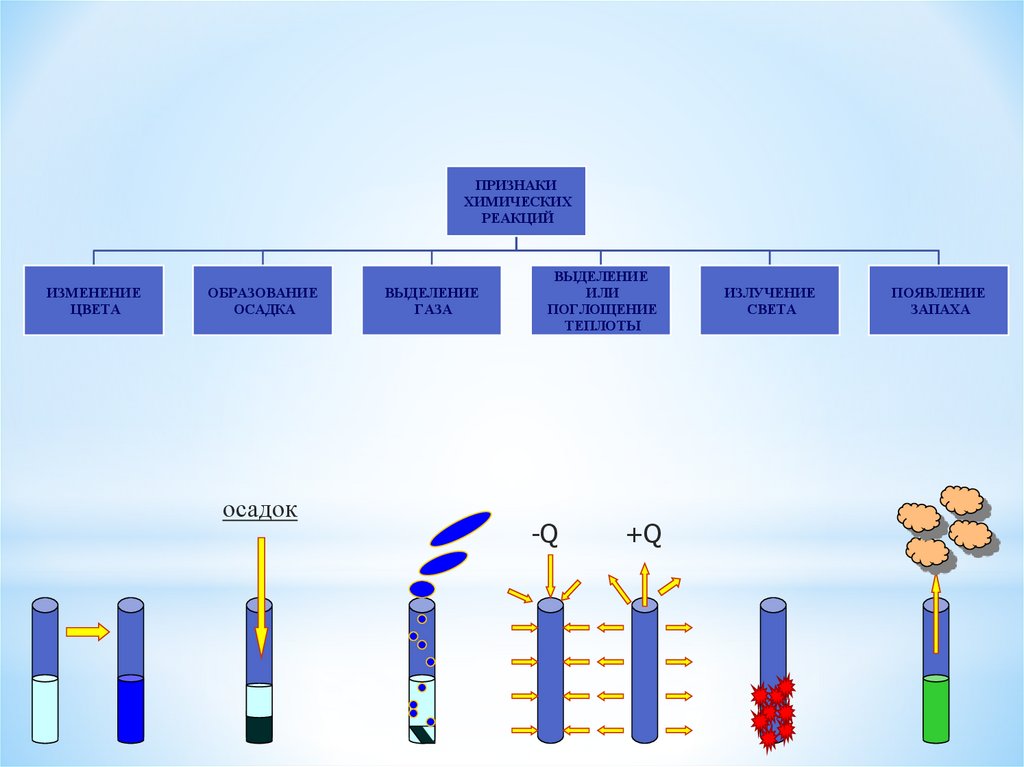
ПРИЗНАКИХИМИЧЕСКИХ
РЕАКЦИЙ
ИЗМЕНЕНИЕ
ЦВЕТА
ОБРАЗОВАНИЕ
ОСАДКА
осадок
ВЫДЕЛЕНИЕ
ГАЗА
ВЫДЕЛЕНИЕ
ИЛИ
ПОГЛОЩЕНИЕ
ТЕПЛОТЫ
-Q
+Q
ИЗЛУЧЕНИЕ
СВЕТА
ПОЯВЛЕНИЕ
ЗАПАХА
7.
*ИЗМЕНЕНИЕЦВЕТА
?CuO + ?H2 → ? … + ?...
CuO + H = Cu + H O
2
2
(реакция замещения)
https://youtu.be/6iDuKLfnzWc
8.
*ОБРАЗОВАНИЕОСАДКА
?Na3PO4+?AgNO3 →?…+ ?...
Na3PO4+3AgNO3 = Ag3PO4↓ + 3NaNO3
(реакция обмена)
https://youtu.be/69roC_P4pLg
9.
*ВЫДЕЛЕНИЕГАЗА
?Zn + ?HCl → ? …+ ?...
Zn +2HCl = ZnCl2 + H2↑
(реакция замещения)
https://youtu.be/TT6JkVr83PE
10.
* ВЫДЕЛЕНИЕТЕПЛОТЫ И ГАЗА
?Na + ?Н2О → ? …
2Na +2Н2О= 2NaОН+Н2↑
(реакция замещения)
https://yandex.ru/video/preview/?filmId=
11.
*ИЗЛУЧЕНИЕСВЕТА
?Р + ?О2 → ? …
4Р + 5O2 = 2Р2O5
(реакция соединения)
https://yandex.ru/video/preview/?filmId
12.
*ПОЯВЛЕНИЕЗАПАХА
?Аl+ ?Br2 → ? …
2Аl + 3Br2 = 2AlBr3
(реакция соединения)
https://yandex.ru/video/preview/?filmId=
13.
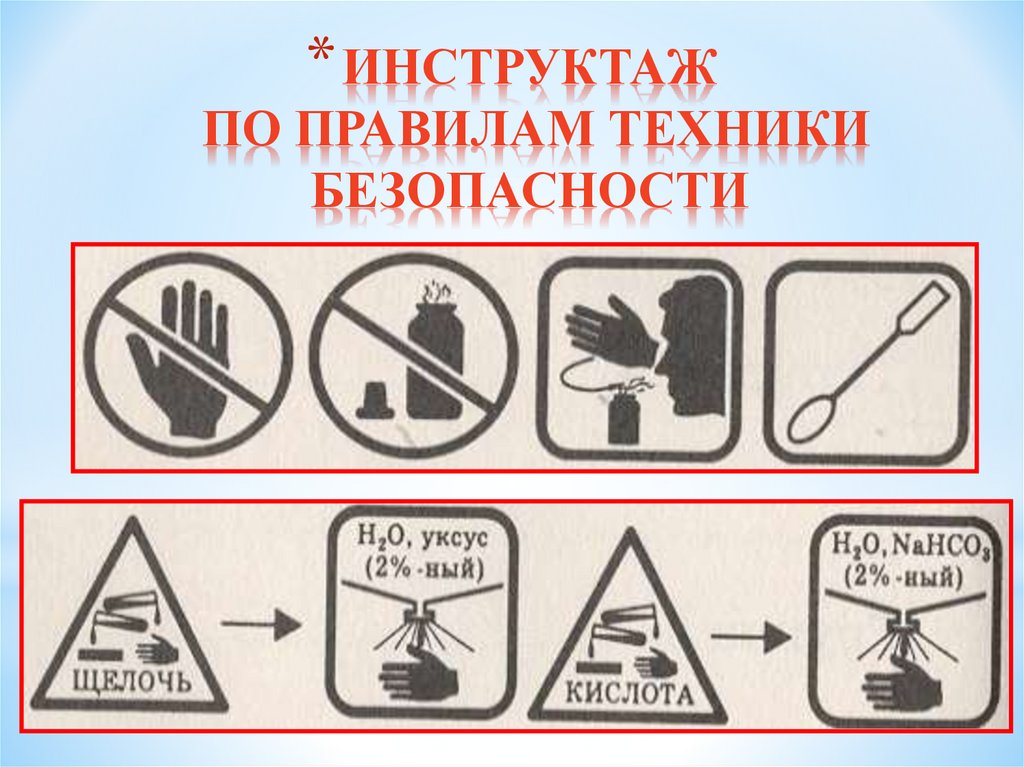
* ИНСТРУКТАЖПО ПРАВИЛАМ ТЕХНИКИ
БЕЗОПАСНОСТИ
14.
* Практическая работа«Признаки химических реакций»
Правила техники безопасности (ТБ)
Опыт №1. Взаимодействие мрамора с соляной кислотой.
• Положите в пробирку 1 – 2 кусочка мрамора.
• Прилейте соляную кислоту.
• Какие признаки химических реакций вы наблюдаете?
• Запишите уравнения химической реакции и укажите тип.
https://yandex.ru/video/preview/?filmId=
Опыт №2. Взаимодействие хлорида железа (III) с роданидом калия.
• В пробирку налейте 2 мл раствора хлорида железа (III).
• Добавьте несколько капель раствора роданида калия (KCNS).
• Какие признаки химических реакций вы наблюдаете?
• Запишите уравнения химической реакции и укажите тип.
https://yandex.ru/video/preview/?filmId=
Опыт №3. Взаимодействие сульфата натрия с хлоридом бария.
• В пробирку налейте 2 мл раствора сульфата натрия.
• Добавьте несколько капель раствора хлорида бария.
• Какие признаки химических реакций вы наблюдаете?
• Запишите уравнения химической реакции и укажите тип.
https://youtu.be/Q_LMQeKuy5g
15.
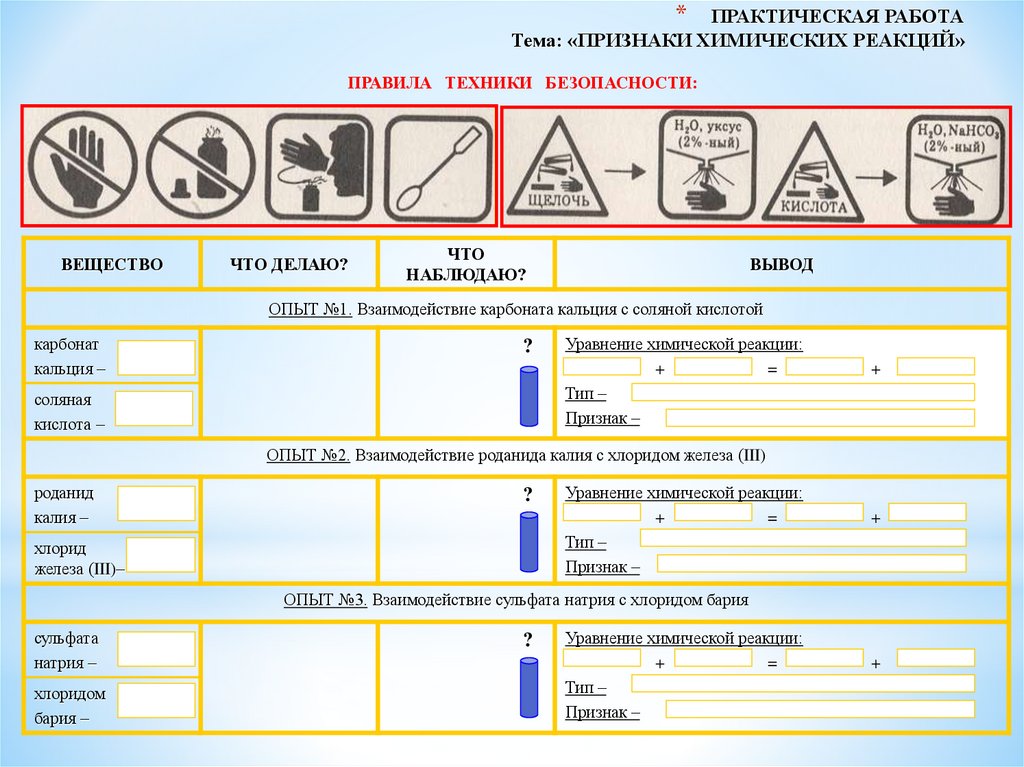
*ПРАКТИЧЕСКАЯ РАБОТА
Тема: «ПРИЗНАКИ ХИМИЧЕСКИХ РЕАКЦИЙ»
ПРАВИЛА ТЕХНИКИ БЕЗОПАСНОСТИ:
ВЕЩЕСТВО
ЧТО ДЕЛАЮ?
ЧТО
НАБЛЮДАЮ?
ВЫВОД
ОПЫТ №1. Взаимодействие карбоната кальция с соляной кислотой
карбонат
кальция –
?
соляная
кислота –
Уравнение химической реакции:
+
=
Тип –
Признак –
+
ОПЫТ №2. Взаимодействие роданида калия с хлоридом железа (III)
роданид
калия –
?
хлорид
железа (III)–
Уравнение химической реакции:
+
=
Тип –
Признак –
+
ОПЫТ №3. Взаимодействие сульфата натрия с хлоридом бария
сульфата
натрия –
хлоридом
бария –
?
Уравнение химической реакции:
+
=
Тип –
Признак –
+
16.
*ПРИЗНАКИ ХИМИЧЕСКИХ РЕАКЦИЙ
ОПЫТ №1
ОПЫТ №2
ОПЫТ №3
УЧЕНИК:
ОЦЕНКА:
ЧИСЛО:
ОПЫТ №4











 Химия
Химия








