Похожие презентации:
Кислород. Промышленный способ (перегонка жидкого воздуха)
1.
2.
Окислород
озон
О2
О3
3.
Газ - без цвета, вкуса и запаха;в 100V H2O растворяется 3V O2
t кип= -183 С;
t пл = -219 C;
Немного тяжелее воздуха
Малорастворим в воде
О2
Струя жидкого кислорода
отклонятся в сильном магнитном поле
4.
Промышленный способ (перегонка жидкого воздуха).Лабораторный способ
(разложение некоторых кислородосодержащих веществ)
2KMnO4 –t K2MnO4 + MnO2 + O2
2KClO3 –t ;MnO2 2KCl + 3O2
2H2O2 –MnO2 2H2O + O2
В природе (процесс фотосинтеза)
5.
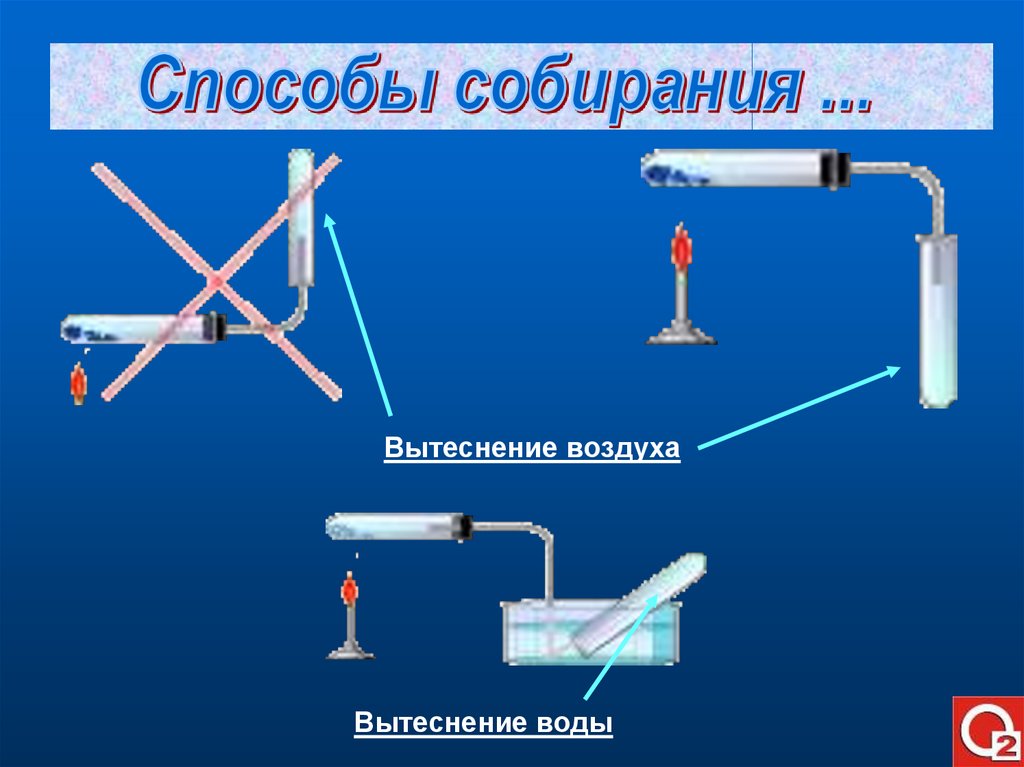
Вытеснение воздухаВытеснение воды
6.
O2KMnO4
O2
O2
H2O
7.
Взаимодействие веществ с кислородом называетсяметаллов
2Mg + O2 2MgO
2Cu + O2 –t 2CuO
окислением.
сложных веществ
2H2S + 3O2 2SO2 + 2H2O
CH4 + 2O2 CO2 + 2H2O
Кислород
поддерживает
горение!
неметаллов
C + O2 CO2
2H2 + O2 2H2O
8.
+ металлкислород
+ неметалл
+ сложное вещество
Оксид металла МеО
Оксид неметалла НеМеО
Оксиды элементов
9.
Получение3O2 2O3
Во время грозы (в природе),
(в лаборатории) в озонаторе
Химические свойства
Неустойчив:
O3 O2 + O
Сильный окислитель:
2KI + O3 + H2O 2KOH + I2 + O2
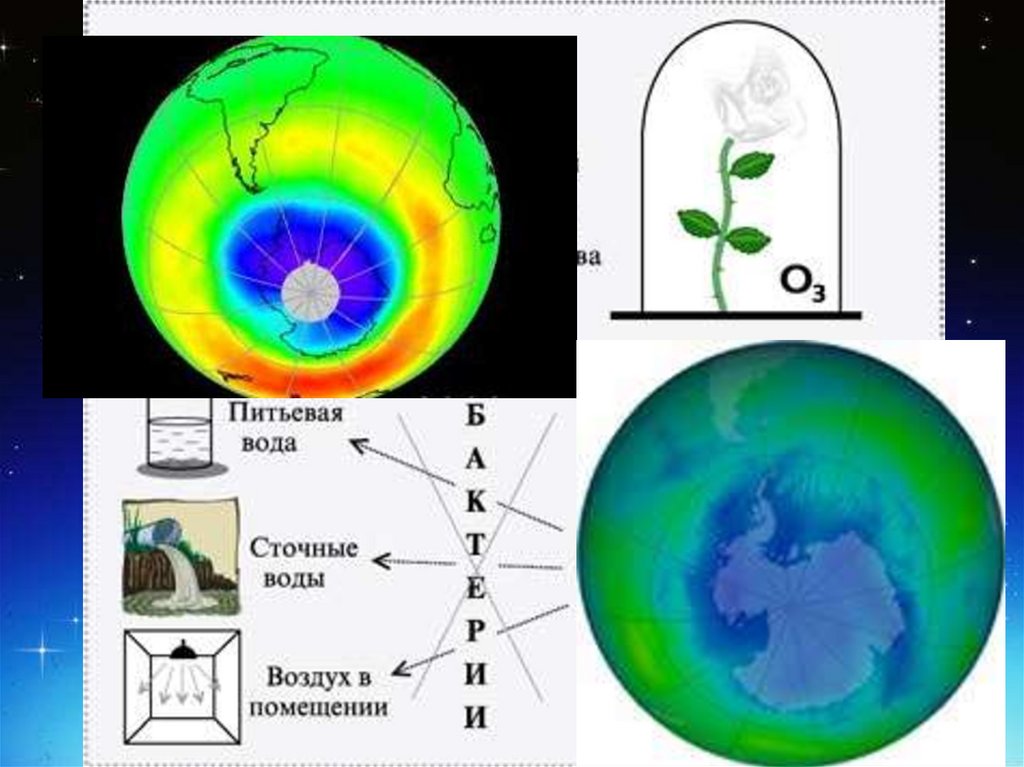
Обесцвечивает красящие вещества,
отражает УФ - лучи, уничтожает
10.
11.
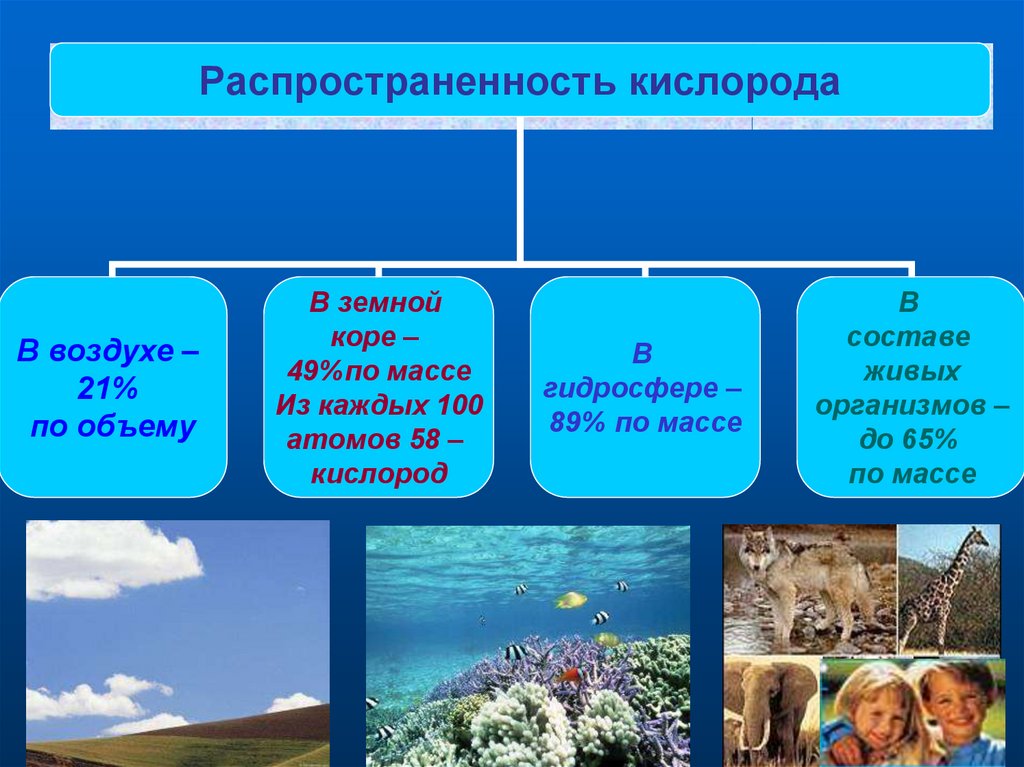
Распространенность кислородаВ воздухе –
21%
по объему
В земной
коре –
49%по массе
Из каждых 100
атомов 58 –
кислород
В
гидросфере –
89% по массе
В
составе
живых
организмов –
до 65%
по массе
12. Применение кислорода
В течение одной минутычеловек в среднем
употребляет 0,5 л кислорода.
Современный пассажирский
самолет при полете в течение
9 ч расходует 50-75 т
кислорода.








 Химия
Химия








