Похожие презентации:
Водород. 9 класс
1. Домашнее задание
Параграф 17,Упражнение 3
2. Водород
Урок химии9 класс
3. План изучения водорода
Химический элемент водород (положение
в ПСХЭ; строение атома)
Простое вещество водород (молекулярная
формула, относительная молекулярная
масса, строение молекулы, получение в
лаборатории, физические свойства,
химические свойства, применение
человеком, открытие водорода)
4. Химический элемент водород
1.2.
3.
4.
5.
Положение в ПСХЭ:
Порядковый номер –
Номер группы –
Подгруппа –
Номер периода –
Относительная атомная масса -
5. Химический элемент водород
1.2.
3.
4.
5.
6.
7.
Строение атома:
Заряд ядра –
Число протонов, нейтронов в ядре –
Число электронов –
Число энергетических уровней –
Число электронов на внешнем уровне –
Высшая степень окисления –
Низшая степень окисления -
6. Простое вещество водород
Молекулярная формула:Н2
Относительная молекулярная масса:
Mr (H2) = 2
7. Простое вещество водород
Строение молекулы:Н(* *)Н
Ковалентная неполярная связь
8. Простое вещество водород
Получение водородаС помощью каких веществ можно получить
водород?
С помощью каких приборов можно получить
водород?
Как собрать водород?
Как проверить водород на чистоту?
Зачем проверять водород на чистоту?
Какими физическими свойствами обладает
водород?
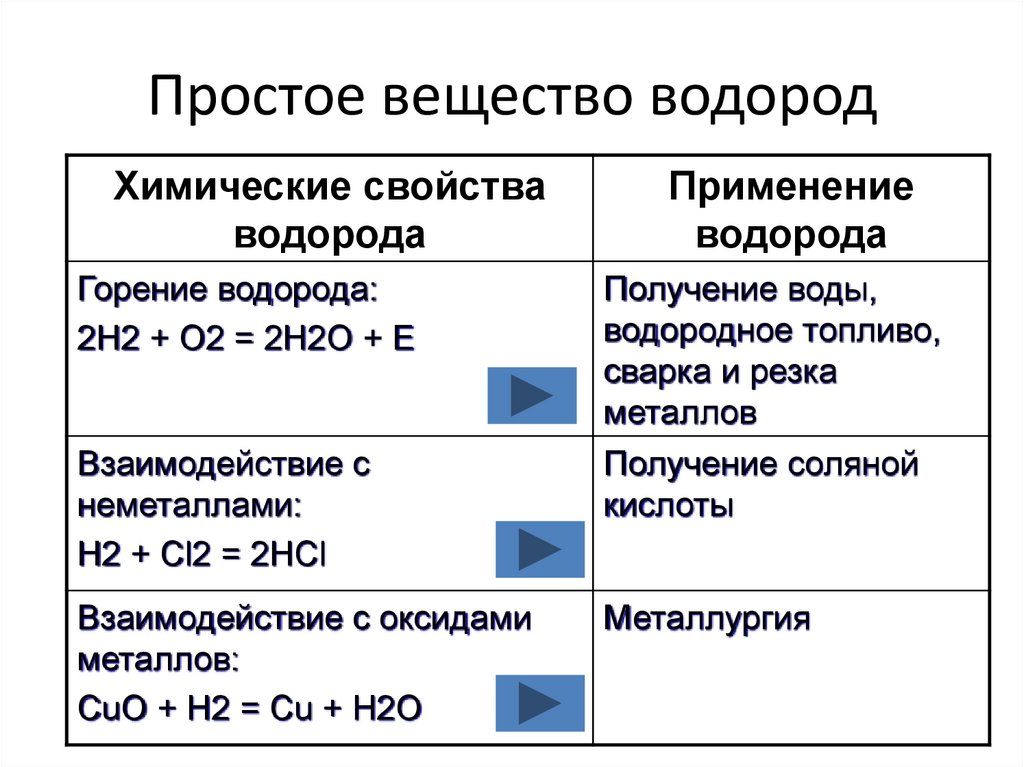
9. Простое вещество водород
Химические свойстваводорода
Горение водорода:
2H2 + O2 = 2H2O + Е
Взаимодействие с
неметаллами:
H2 + Cl2 = 2HCl
Взаимодействие с оксидами
металлов:
CuO + H2 = Cu + H2O
Применение
водорода
Получение воды,
водородное топливо,
сварка и резка
металлов
Получение соляной
кислоты
Металлургия
10. Простое вещество водород
Открытие водородаУчебник – стр. 102
Прочитать!









 Химия
Химия








