Похожие презентации:
Первоначальные представления об органических веществах
1.
Первоначальные представления оборганических веществах
2.
Цели урока:Дать первоначальные понятия об органической
химии и органических веществах.
Познакомить с многообразием органических
веществ, показать познавательное и
народнохозяйственное значение органической
химии.
Ввести новые понятия, определяющие
классификационные группы органических веществ.
Развивать умения учащихся сравнивать, обобщать,
проводить аналогию между органическими и
неорганическими веществами.
3.
Классификация веществI группа.
Неорганические вещества - около 500 тысяч:
1)
2)
Простые –металлы и неметаллы
Сложные:
а) оксиды - основные, кислотные, амфотерные;
б) кислоты (одноосновные и многоосновные,
кислородсодержащие и бескислородные);
в) основания (щелочи и нерастворимые
основания);
г) соли – средние и кислые.
4.
Органическая химия1. Это наука об органических веществах и
законах, которым они подчиняются.
2. Это химия углерода и его соединений.
Что вам известно из жизненного опыта, из
курса биологии об органических веществах?
Где они используются?
5.
Особенности веществОрганические
вещества:
1) встречаются только в
живой природе или
получены
искусственным путем;
2) все содержат
химический элемент
углерод;
3) имеют молекулярную
кристаллическую
решетку;
Неорганические
вещества:
1) встречаются и в живой,
и неживой природе;
2) не все содержат
химический элемент
углерод;
3) могут иметь
молекулярную,
атомную, ионную,
металлическую КР;
6.
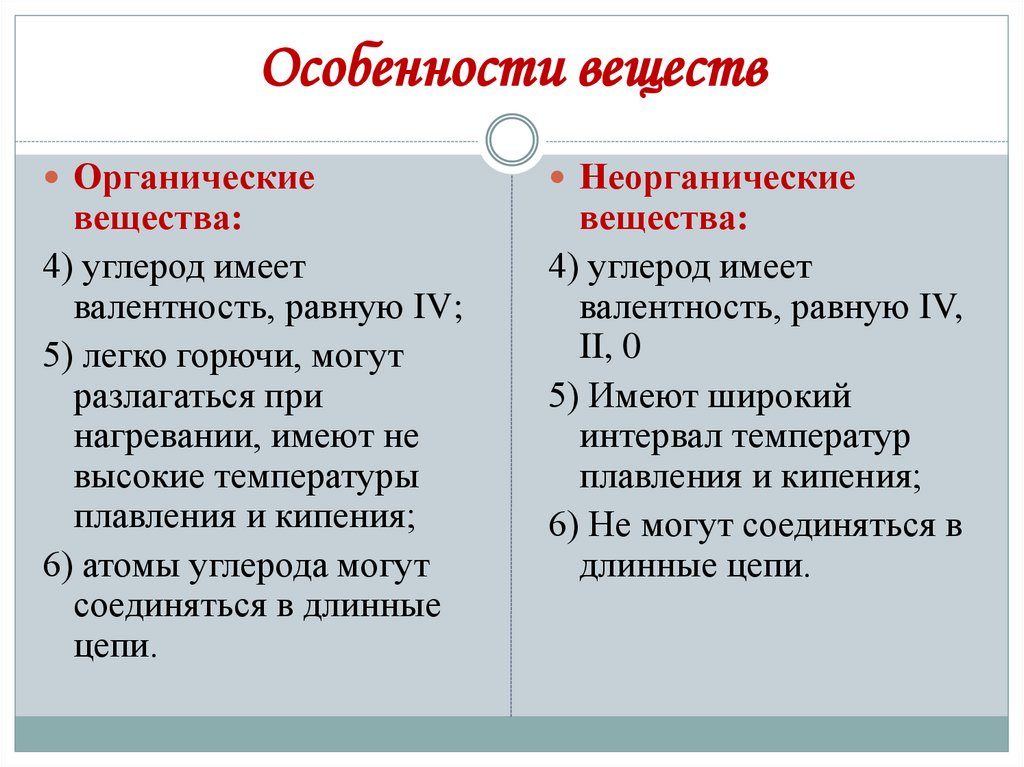
Особенности веществОрганические
вещества:
4) углерод имеет
валентность, равную IV;
5) легко горючи, могут
разлагаться при
нагревании, имеют не
высокие температуры
плавления и кипения;
6) атомы углерода могут
соединяться в длинные
цепи.
Неорганические
вещества:
4) углерод имеет
валентность, равную IV,
II, 0
5) Имеют широкий
интервал температур
плавления и кипения;
6) Не могут соединяться в
длинные цепи.
7.
Сходство органических и неорганических веществСостоят из одних и тех же химических элементов,
которые находятся в ПТХЭ Д.И. Менделеева.
Из неорганических веществ можно получить сложные
органические вещества (фотосинтез), и наоборот, из
сложных органических веществ можно получить
более простые неорганические вещества (гниение,
горение)
8.
Классификация веществII группа
Органические вещества: более 15 миллионов:
1) Углеводороды (предельные и
непредельные);
2) Кислородсодержащие вещества (спирты,
кислоты, жиры, углеводы);
3) Азотсодержащие вещества (аминокислоты
и белки).
9.
УглеводородыЭто органические вещества, которые в своем
составе содержат только атомы углерода и водорода.
Делятся на группы:
1) Предельные углеводороды - метан;
2) Непредельные углеводороды:
а) алкены – этилен;
б) алкины – ацетилен.
Выписать из учебника формулы данных веществ
10.
Кислородсодержащие органические веществаСпирты – это производные углеводородов, в
молекулах которых один или несколько атомов
водорода замещены на гидроксильную группу ОН и
имеют общую формулу R-(ОН)n
Спирты подразделяются на
1) одноатомные – содержат только одну
гидроксильную группу ОН – выпишите из
учебника формулы метанола и этанола;
2) многоатомные содержат 2 и более гидроксильных
групп ОН – глицерин; выпишите из учебника
формулу вещества.
11.
Кислородсодержащие органические веществаКарбоновые кислоты – это производные
углеводородов, в молекулах которых присутствует
карбоксильная группа атомов -СООН
Сложные эфиры – это продукты взаимодействия
карбоновых кислот со спиртами
Жиры – это сложные эфиры глицерина и высших
карбоновых кислот (твердые и жидкие)
Выпишите в тетрадь формулу уксусной кислоты.
Выписать в тетрадь формулу этилацетата.
Выписать общую формулу жира
12.
Выводы по урокуМежду органической и неорганической химией
есть взаимосвязь.
Органические вещества имеют как сходство, так
и отличие от неорганических веществ.
Продукты органической химии имеют большое
значение и применяются во всех отраслях
народного хозяйства.
13.
Домашнее заданиеПараграф 51 читать, учить записи в тетради
Используя параграфы 51-56, выписать формулы
органических веществ, 20 терминов НВ смотреть
1 группу
14.
Основные положения теории химического строения(ТХС) А.М.Бутлерова
Все атомы, образующие молекулы ОВ, соединяются друг с другом
согласно их валентности. Валентность атома углерода в ОВ постоянна
и равна IV
*** Порядок соединения атомов в молекуле называется химическим
строением.
*** Для записи формул ОВ используют структурные формулы (СФ) – это
формулы, в которых черточками показаны химические связи между атомами
в молекуле.
А) полная (развернутая) СФ – в ней черточками показаны химические
связи между всеми атомами в молекуле данного вещества.
Учебник с 180 – формулы этилена, этана, ацетилена
Б) сокращенная СФ - в ней черточками показаны химические связи только
между атомами углерода в молекуле данного вещества.
Н2С = СН2
СН3 – СН3
НС = СН
ЭТИЛЕН
ЭТАН
АЦЕТИЛЕН
1.
Назад
15.
Основные положения теории химического строения(ТХС) А.М.Бутлерова
2. Свойства вещества зависят не только от того, какие атомы и
сколько их входит в состав молекулы ОВ, но и от порядка их
соединения, т.е. от химического строения вещества.
*** Изомерия ОВ – это явление, когда может существовать
несколько ОВ с одной и той же молекулярной формулой
(одинаковый качественный и количественный состав), но при
этом они имеют разное химическое строение, а следовательно,
и разные свойства; такие вещества называют изомерами.
*** Изомеры – это ОВ, у которых одна и та же молекулярная
формула (одинаковый качественный и количественный состав),
но разное химическое строение, а следовательно, и разные
свойства.
16.
Основные положения теории химического строения(ТХС) А.М.Бутлерова
17.
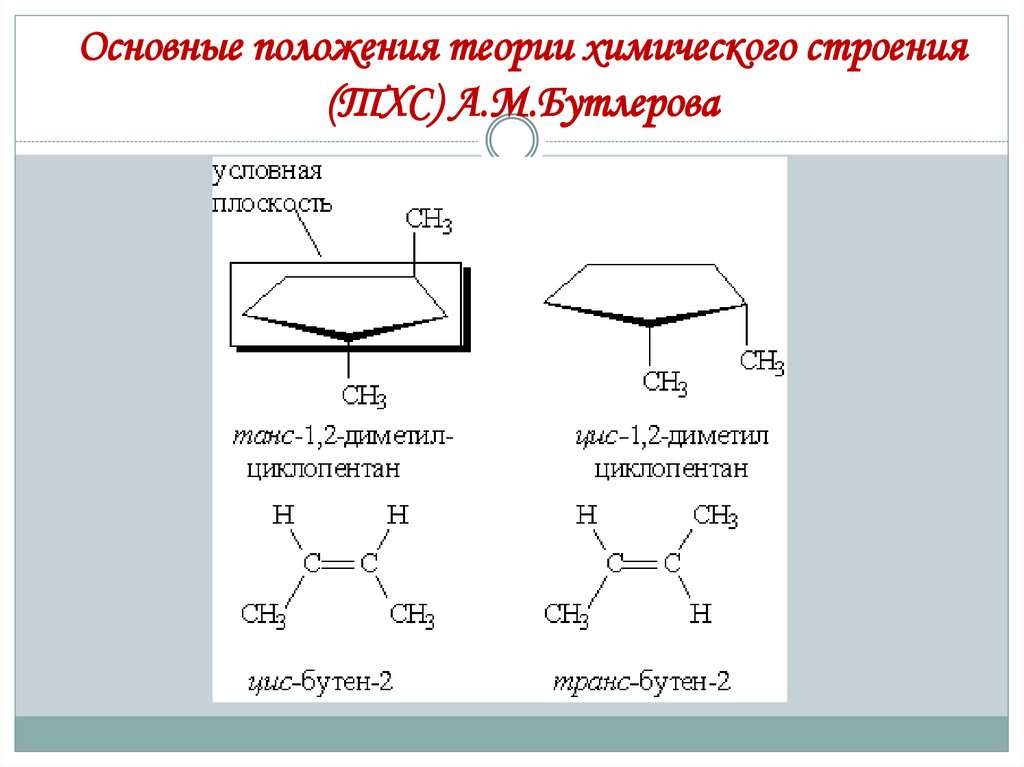
Основные положения теории химического строения(ТХС) А.М.Бутлерова
3. Атомы или группы атомов, образующие молекулы ОВ
взаимно влияют друг на друга.
4. Зная строение ОВ можно предсказать его свойства, и
наоборот, зная свойства ОВ можно предсказать его
строение.
***А.М.Бутлеров доказал, что строение ОВ познаваемо,
его можно изучить с помощью химических методов
анализа и синтеза, а также используя физические методы:
спектроскопию, ЯМР, рентгенографию и другие.
***А.М.Бутлеров предсказал, что ТХС получит свое
дальнейшее развитие и это будет связано а) с
пространственным строением молекул ОВ (стереохимия)
и б) изучение природы химических связей в ОВ.
18.
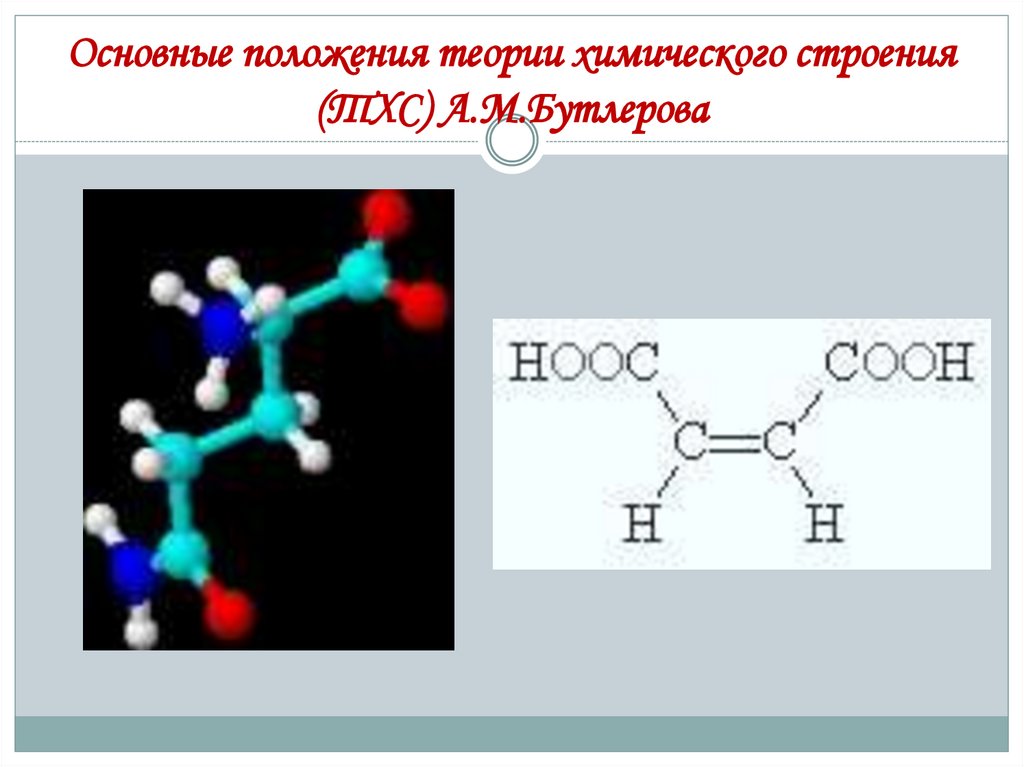
Основные положения теории химического строения(ТХС) А.М.Бутлерова
19.
Основные положения теории химического строения(ТХС) А.М.Бутлерова
Гомологи – это ОВ, которые имеют разные формулы (разный
качественный и количественный состав вещества),
отличаются друг от друга на одну или несколько
гомологических разностей - СН2 , но при этом обладают
сходным химическим строением и сходными свойствами.
Гомологический ряд ОВ – это группа ОВ, имеющих общую
формулу ряда и обладающие сходным строением и
свойствами.
Углевоороды – это ОВ, молекулы которых состоят только из
атомов углерода и водород
Алканы или Предельные углеводороды (Парафины)
СnH2n+2 , где n больше или =1, имеют только одинарные связи
и в своем названии заканчиваются на АН.
• Радикалы - это химически активные частицы, которые
содержат на один атом водорода меньше, чем в самом УВ.
20.
Гомологический ряд Алканов или Предельных УВФормула
Название ПУВ
Формула радикала
Название радикала
CH4
метан
CH3 -
метил
C2H6
этан
C2H5 -
этил
C3H8
пропан
C3H7 -
пропил
C4H10
бутан
C4H9 -
бутил
C5H12
пентан
C5H11 -
пентил
C6H14
гексан
C6H13 -
гексил
C7H16
гептан
C7H15 -
гептил
C8H18
октан
C8H17 -
октил
C9H20
нонан
C9H19 -
нонил
C10H22
(децил)
декан
C10H21 -
декил
21.
Домашнее задание1) Выучить четыре положения ТХС
А.М.Бутлерова
2) Выучить таблицу «АЛКАНЫ»
3) Выучить термины: ОХ (два определения), ОВ
и их особенности (таблица), химическое
строение, структурная формула, развернутая СФ,
сокращенная СФ, изомерия, изомеры, гомологи,
гомологические ряды, радикалы.


















 Химия
Химия








