Похожие презентации:
Оксиды. Номенклатура, классификация, свойства
1. ОКСИДЫ
Номенклатура,классификация, свойства
2. ПЛАН ИЗУЧЕНИЯ ТЕМЫ
1. Состав, определение иноменклатура (название)
оксидов.
2. Классификация оксидов.
3. Физические свойства оксидов.
4. Химические свойства
оксидов.
3. ОПРЕДЕЛЕНИЕ И СОСТАВ ОКСИДОВ
ОКСИДЫ – это сложные вещества, состоящиеиз двух элементов, одним из которых
является кислород
Пример: Al2O3, N2O, Fe2O3, PbO2,
Na2O, Li2O, S2O3, CO2, Ga2O3, Ag2O,
Se2O3, SnO2, P2O5, MgO, B2O3,Cl2O7
ЗАПОМНИ: на I месте – металл
или неметалл,
на II месте – КИСЛОРОД
4. ЕЩЕ РАЗ…
МеО неМе ОЭТО
ОКСИДЫ
5. ВСПОМНИМ О ВАЛЕНТНОСТИ
Валентность – свойство атомов химическогоэлемента присоединять и или замещать
определенное число атомов другого
химического элемента
ВАЛЕНТНОСТЬ соответствует номеру группы
Натрий в какой
В
Валентность равна I
группе?
первой
Цинк в какой
Валентность равна II
Во
группе?
второй
В третьей
Алюминий в
какой группе?Валентность равна III
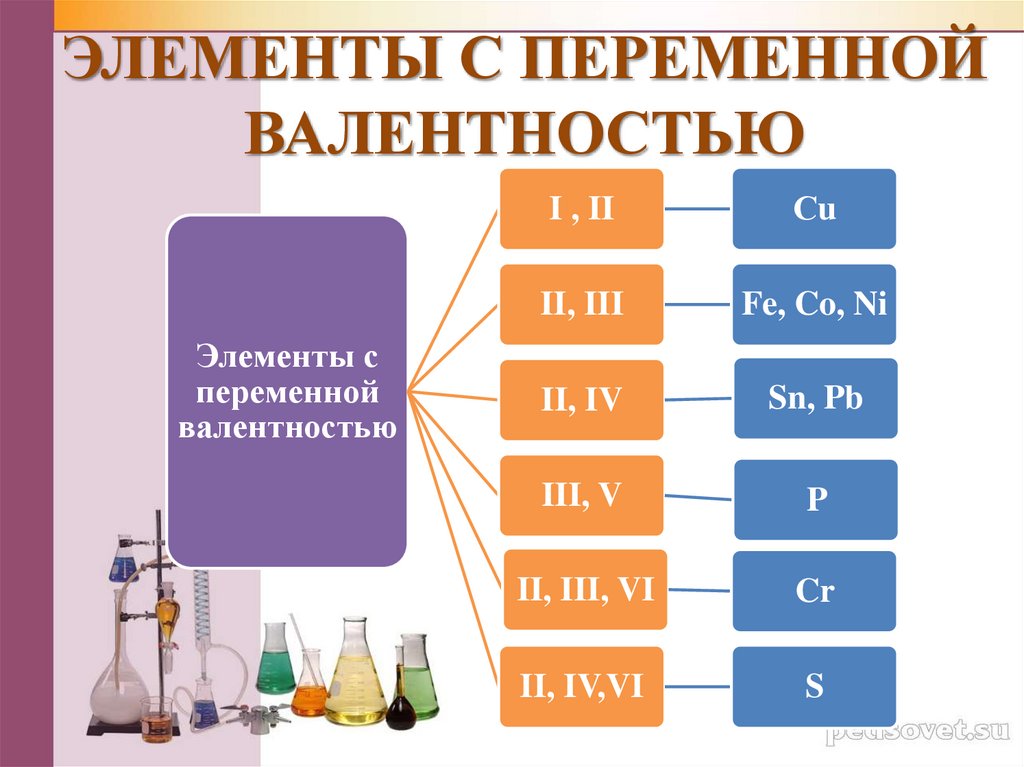
6. ЭЛЕМЕНТЫ С ПЕРЕМЕННОЙ ВАЛЕНТНОСТЬЮ
Элементы спеременной
валентностью
I , II
Сu
II, III
Fe, Co, Ni
II, IV
Sn, Pb
III, V
P
II, III, VI
Cr
II, IV,VI
S
7. НОМЕНКЛАТУРА
Как назвать оксиды?1. на первом месте ставим слово ОКСИД
2. На втором месте добавляем элемент в
родительном падеже. Оксид чего?
3. В скобках указываем переменную
валентность
Например: MgO
Название: оксид (чего?)магния
S2O3 - оксид серы (VI)
8.
ЗАКРЕПИМ ПОЛУЧЕННЫЕЗНАНИЯ
назовите оксиды:
1. MgO - оксид магния
2. P₂O₅ - oксид фосфора (V)
3. Na₂O - оксид натрия
4. Al₂O₃ - оксид алюминия
5.Fe₂O₃ - оксид железа (III)
6. N₂O₅ - оксид азота (V)
9. АЛГОРИТМ ПОСТРОЕНИЯ ФОРМУЛ ОКСИДОВ
ЗАДАНИЕ:напишите формулу оксида
железа (II)
10.
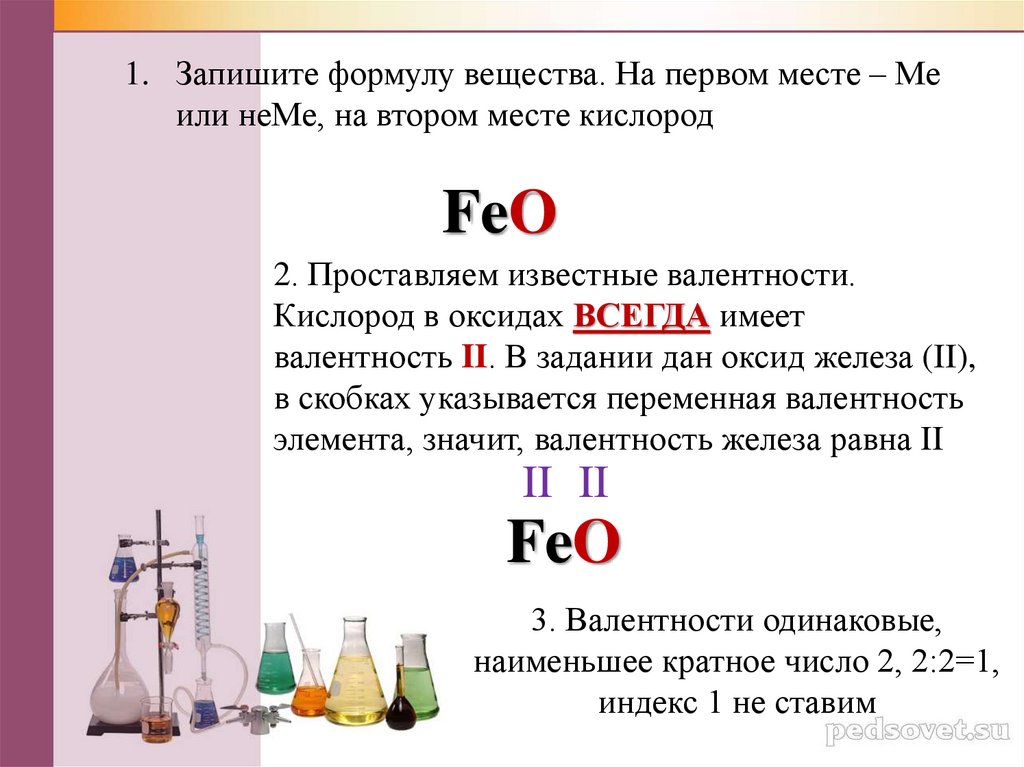
1. Запишите формулу вещества. На первом месте – Меили неМе, на втором месте кислород
FeO
2. Проставляем известные валентности.
Кислород в оксидах ВСЕГДА имеет
валентность II. В задании дан оксид железа (II),
в скобках указывается переменная валентность
элемента, значит, валентность железа равна II
II II
FeO
3. Валентности одинаковые,
наименьшее кратное число 2, 2:2=1,
индекс 1 не ставим
11. Ответ: оксид железа (II) - FeO
Ответ: оксиджелеза (II) FeO
12. АЛГОРИТМ ПОСТРОЕНИЯ ФОРМУЛ ОКСИДОВ
ЗАДАНИЕ:напишите формулу оксида
марганца (VII)
13.
1. Запишите формулу вещества. На первом месте – Меили неМе, на втором месте кислород
МnO
2. Проставляем известные валентности.
Кислород в оксидах всегда имеет валентность
II. В задании дан оксид железа (II), в скобках
указывается переменная валентность элемента,
значит, валентность железа равна II
VII
II
МnO
3. Валентности разные, наименьшее
кратное число (чтобы делились и VII
и II) 14
14.
14VII II
МnO
14:7=2 (индекс марганца),
14:2=7 (индекс кислорода)
Проставляем индексы и получаем формулу:
Мn2O7
15. ЗАКРЕПИМ ПОЛУЧЕННЫЕ ЗНАНИЯ
Некоторый металл образует ряд оксидов,среди которых MeO, MeO3, Me2O3. Укажите,
какой характер (основный, кислотный,
амфотерный) имеет каждый из оксидов.
VI
II
Решение: MeO3 -II валентность
Ме больше IV, значит,
II
кислотный оксид; MeO – валентность Ме II, значит,
III
II
оснОвный оксид; Me2O3 – валентность
Ме III, значит, амфотерный оксид
16. ЗАКРЕПИМ ПОЛУЧЕННЫЕ ЗНАНИЯ
По названиям составьте их формулы:Ag2O
1. Оксид серебра
2. Оксид марганца (IV) MnO2
3. Оксид ванадия (V)
V5O2
4. Оксид галлия
Ga2O3
5. Оксид золота (I) Au2O
6. Оксид хлора (VII) Cl2O7
7. Оксид цинка ZnO
17. ДОМАШНЕЕ ЗАДАНИЕ№ 1
1. Выучить понятия: «валентность»,«оксиды», «номенклатура».
• 2 Выполнить письменно задание
(Слайд 18)
18. ЗАКРЕПИМ ПОЛУЧЕННЫЕ ЗНАНИЯ
ЗАДАНИЕ: составьте формулы оксидов иукажите их характер
Оксид хрома (VI), оксид меди (II), оксид
мышьяка, оксид углерода (II), оксид азота (I),
оксид серы (II), оксид кальция, оксид
бериллия, оксид кремния, оксид серы (IV),
оксид серы (VI), оксид лития, оксид
калия, оксид фосфора (V),
оксид азота (V)
19. КЛАССИФИКАЦИЯ ОКСИДОВ
ОКСИДЫнесолеобразу
ющие
Оксиды
неметаллов с
валентностью
I, II
оснОвные
Оксиды
металлов I и II
группы
амфотерн
ые
кислотные
Оксиды
металлов с
валентностью
III
исключение:
ZnO, BeO, PbO
Оксиды
неметаллов и
металлов с
валентностью IV
и выше
20. Примеры УРАВНЕНИЯ РЕАКЦИЙ
1.CaO + H2O = Ca(OH)22. SO3 + H2O= H2SO4
3. 3Na2O + 2H3PO4 = 2 Na3PO4 + 3H2O
4.CaO + N2O5 = Ca(NO3)2
5.SO3 + 2NaOH = Na2SO4 + H2O
6.N2O3 + H2O = 2HNO2
7.P2O5 + 6KOH = 2K3PO4 + 3H2O
8.MgO + 2HNO3 = Mg(NO3)2 + H2O
9. N2O5 + Ca(OH)2 =
Ca(NO3)2 + H2O
21. ПРОВЕРЯЕМ
НЕСОЛЕОБРАЗУЮЩИЕОСНОВНЫЕ
КИСЛОТНЫЕ
АМФОТЕРНЫЕ
оксид серы (II)
SO,
оксид углерода
(II) CO,
оксид азота (I),
N2O
оксид меди (II)
CuO,
оксид кальция
CaO, оксид лития
Li2O
оксид калия K2O,
Оксид хрома (VI)
CrO3
оксид мышьяка
As2O5, оксид
кремния SiO2,
оксид серы (IV)
SO2 ,
оксид серы (VI)
SO3 ,
оксид фосфора
(V) P2O5, оксид
азота (V) P2O5
Оксид бериллия
BeO
22. ВЫБЕРИТЕ УКАЗАННЫЕ ПОНЯТИЯ
МолодецFeO
Ошибка
Al2O3
Молоде
MgO
ц
Молоде
BaO
ц
Молодец
Li2O
Ошибка
Cl2O7
Молодец
CaO
Ошибка
SO2
Кислотные
оксиды
Молодец
P2O5
Ошибка
NO
Молодец
CL2O5
Молодец
CO2
Ошибка
SrO
Молодец
SeO3
Ошибка
BeO
Молодец
N2O5
Амфотерные
оксиды
Молодец
ZnO
Молодец
Al2O3
Ошибка
FeO
Ошибка
Mn2O7
Молодец
TiO2
Ошибка
N2O3
Молодец
SnO2
Ошибка
CO
Основные
оксиды
23. РАБОТА С УЧЕБНИКОМ
1.24. Химические свойства основных оксидов
CaO +2 HNO3
Ca(NO3)2 + H2O
MgO + N2O5
K2O + H2O
Mg(NO3)2
2KOH
25. Химические свойства кислотных оксидов
P2O5 + 6LiOH2 Li3PO4 + 3H2O
SO3 + CaO
CaSO4
SO2 + H2O
H2SO3
























 Химия
Химия








