Похожие презентации:
Аллотропия. Аллотропные модификации кислорода
1.
Учитель химии МБОУСОШ№4,г. Советский
Казанцева А.Г.
2.
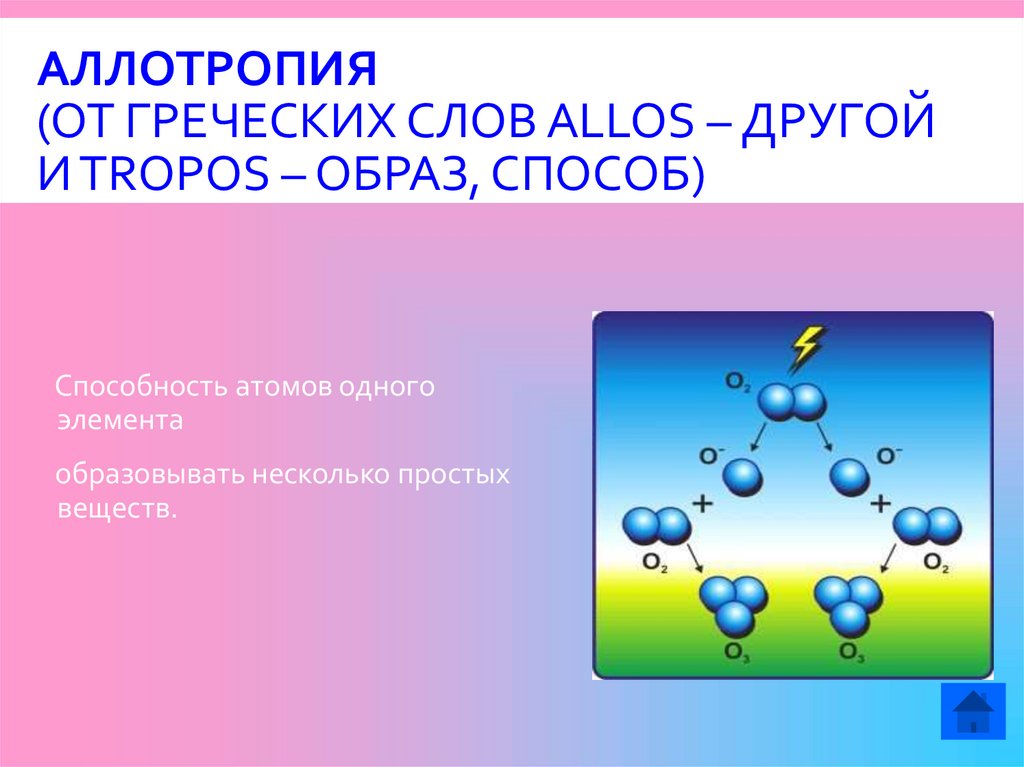
АЛЛОТРОПИЯ(ОТ ГРЕЧЕСКИХ СЛОВ ALLOS – ДРУГОЙ
И TROPOS – ОБРАЗ, СПОСОБ)
Способность атомов одного
элемента
образовывать несколько простых
веществ.
3.
АЛЛОТРОПНЫЕМОДИФИКАЦИИ КИСЛОРОДА.
О2
кислород
(простое вещество)
О3
озон
К. В. Шееле 1772 г.
(простое вещество)
Дж. Пристли 1774 г.
Х. Ф. Шёнбейн 1839 г.
А. Лавуазье 1777г.
«рождающий кислоты»
«пахнущий»
4.
Впервые озон обнаружил в 1785 голландский физикМ. ван Марум по характерному запаху (свежести) и
окислительным свойствам, которые приобретает
воздух после пропускания через него электрических
искр. Однако как новое вещество он описан не был,
ван Марум считал, что образуется особая
«электрическая материя».
5.
НАХОЖДЕНИЕ В ПРИРОДЕ.О2
Воздух – 21% по объёму
23% по массе.
О3
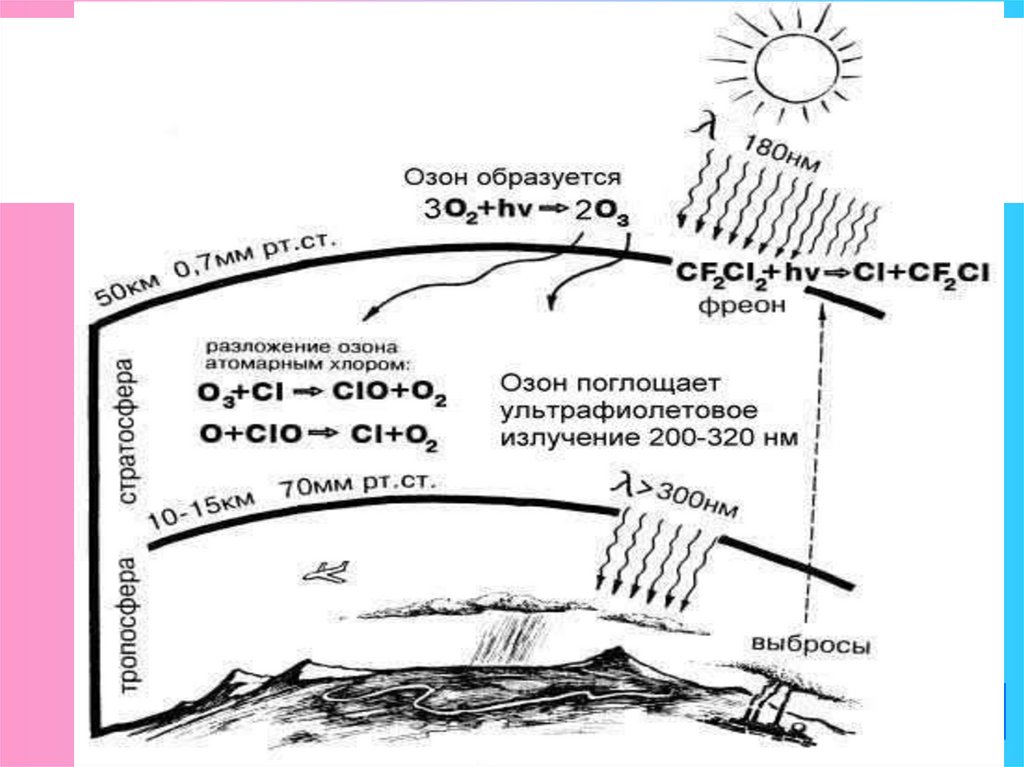
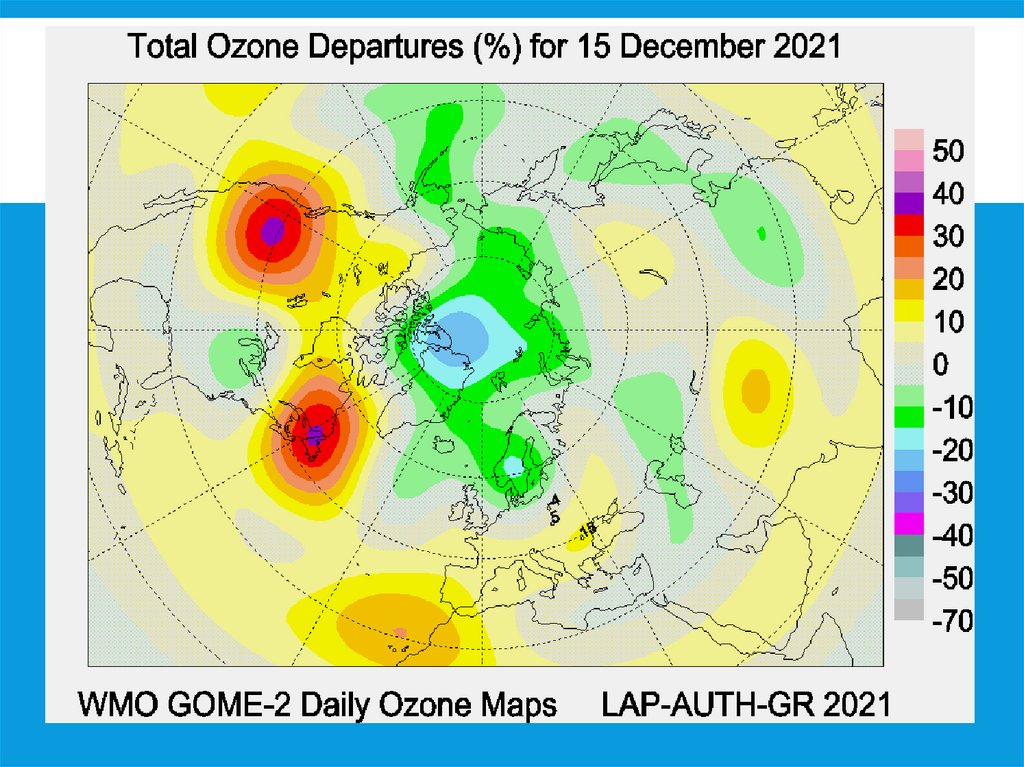
Атмосфера (верхний
слой) – озоновый экран
Земли.
6.
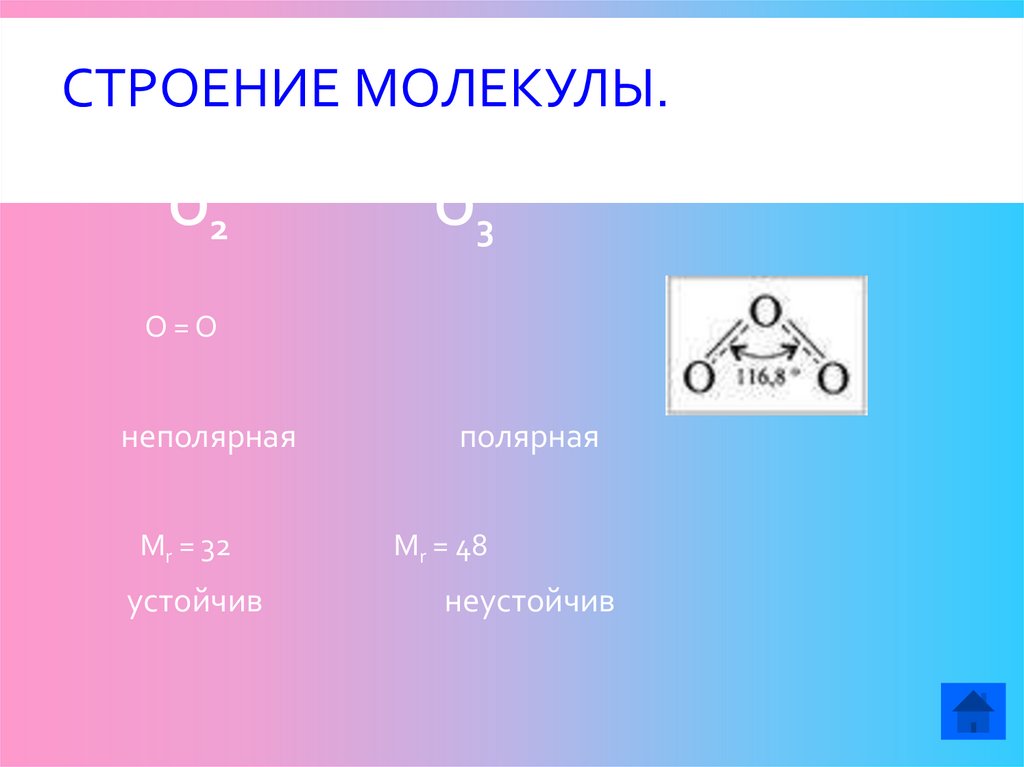
СТРОЕНИЕ МОЛЕКУЛЫ.О2
О3
О=О
неполярная
Mr = 32
устойчив
полярная
Mr = 48
неустойчив
7.
АЛЛОТРОПИЯ КИСЛОРОДА.КИСЛОРОД И ОЗОН
8.
ФИЗИЧЕСКИЕ СВОЙСТВА.Свойства(н.у.)
Агрегатное
состояние
Цвет
Запах
Кислород
Озон
газ
бесцветный
без запаха
газ
голубой
запах
свежести
2,14 г/л
хорошо
растворим
токсичен
Плотность
1,43 г/л
Растворимост малораство ь в воде
рим
Токсичность
нетоксичен
9.
ПОЛУЧЕНИЕ В ПРИРОДЕ.О2
6СО2 + 6Н2О = С6Н12О6 + 6О2
Процесс фотосинтеза.
О3
3О2 ⇄ 2О3
Грозовые разряды.







 Химия
Химия








