Похожие презентации:
Фосфор и его соединения
1. ФОСФОР И ЕГО СОЕДИНЕНИЯ
Урок химиив 9 классе
2. Цели:
изучить фосфор как химический элемент ипростое вещество;
рассмотреть физико-химические свойства
фосфора и его соединений;
определить области его применения.
Этот многоликий фосфор!
3. Открытие фосфора
1669 годГамбургский
алхимик
Хеннинг Бранд
4. Строение атома фосфора
Элемент VA группы имеет электроннуюформулу 1s22s22p63s23p3.
Фосфор – неметалл.
Наиболее характерные степени окисления:
+5, +3, 0, -3.
Оксид имеет кислотные свойства.
Летучее водородное соединение – фосфин
PH3.
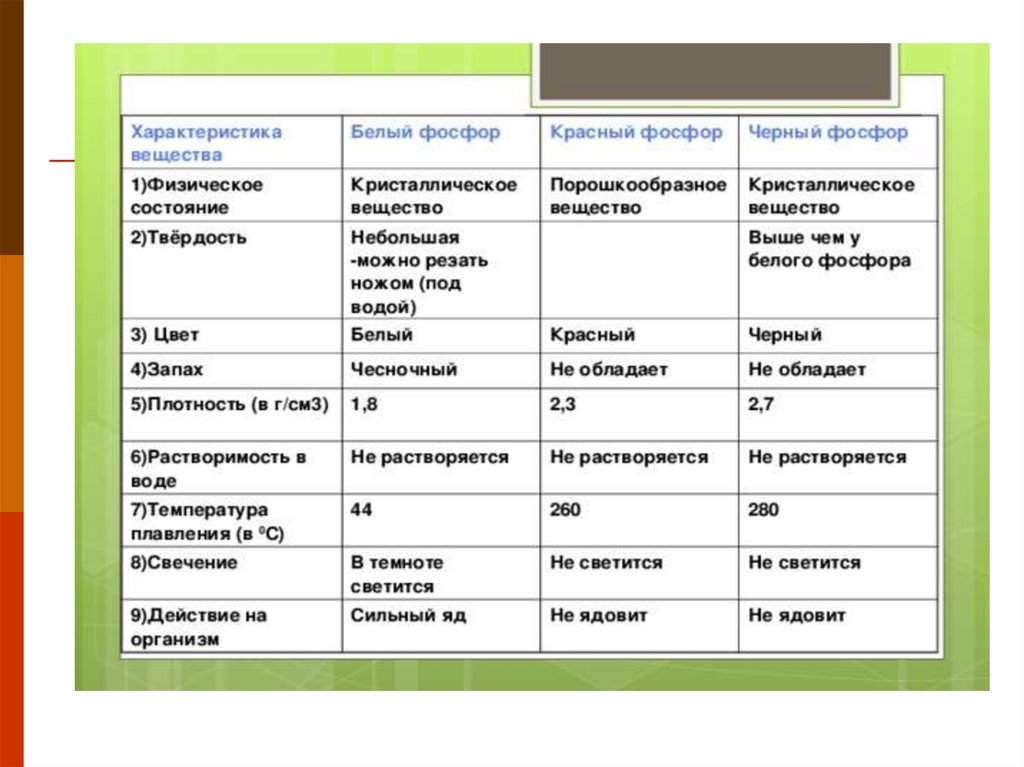
5. Аллотропные модификации фосфора
Кристаллическое веществоБесцветный с желтоватым оттенком
Чесночный запах
Не растворяется в воде
Хорошо растворяется
в сероуглероде
В темноте светится
Сильный яд
Белый фосфор
6. Аллотропные модификации фосфора
Порошкообразное веществоТемно-красный
Без запаха
Не растворяется в воде
Не растворяется
в сероуглероде
Не светится
Не ядовит
Красный фосфор
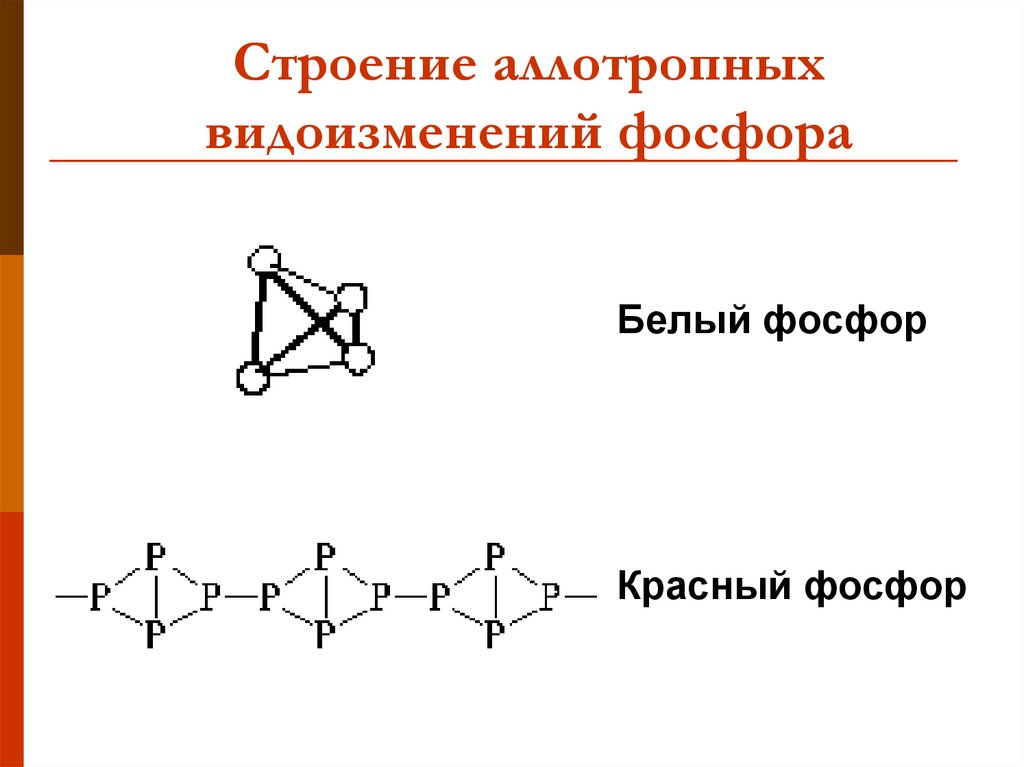
7. Строение аллотропных видоизменений фосфора
Белый фосфорКрасный фосфор
8.
9. Химические свойства фосфора
Фосфор соединяетсясо многими простыми
веществами – кислородом,
галогенами, серой и
некоторыми металлами,
проявляя окислительные и
восстановительные
свойства.
10.
11.
12. Получение фосфора
фосфорит + уголь + песок = фосфор1) Ca3(PO4)2 + 3SiO2 → P2O5 + 3CaSiO3
2) P2O5 + 5C → 2P + 5CO
________________________________________
Ca3(PO4)2 + 5C + 3SiO2 → 2P + 3CaSiO3 + 5CO
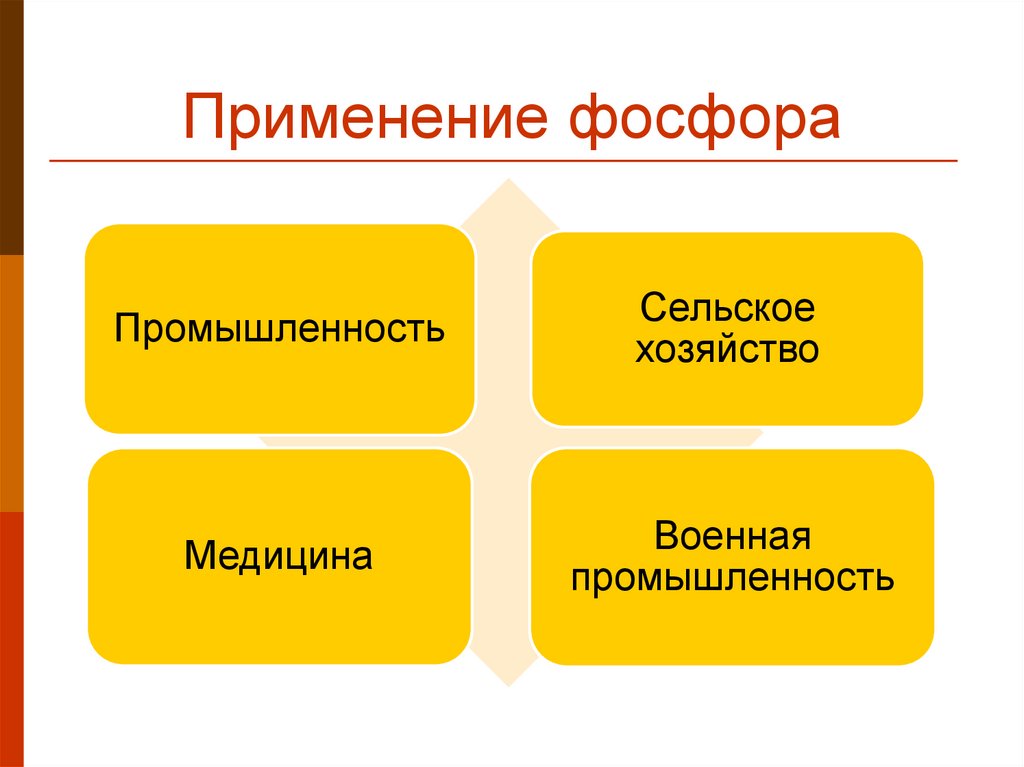
13. Применение фосфора
ПромышленностьСельское
хозяйство
Медицина
Военная
промышленность












 Химия
Химия








