Похожие презентации:
Уравнение Менделеева-Клапейрона
1. Уравнение Менделеева - Клапейрона
2.
46. Температура и тепловоеравновесие. Определение
температуры.
47. Абсолютная температура.
Температура – мера средней
кинетической энергии молекул.
Df. Величины, характеризующие
состояние макроскопических тел
без учета молекулярного строения
тел (V,p,t), называются
макроскопическими параметрами.
3.
4.
Df. Тепловым равновесиемназывают такое состояние, при
котором все макроскопические
параметры сколь угодно долго
остаются неизменными.
Df. Температура характеризует
состояние теплового равновесия
системы тел: все тела системы,
находящиеся друг с другом в
тепловом равновесии, имеют одну
и ту же температуру.
5.
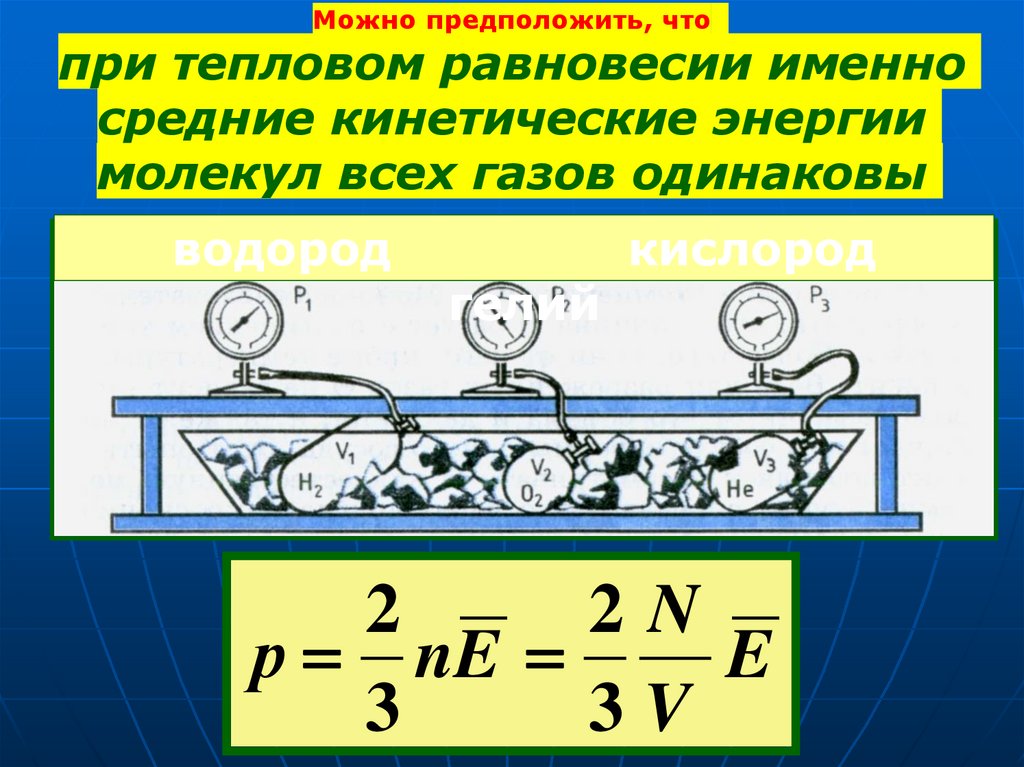
Можно предположить, чтопри тепловом равновесии именно
средние кинетические энергии
молекул всех газов одинаковы
водород
гелий
кислород
2
2N
р nE
E
3
3V
6.
22N
р nE
E
3
3V
рV 2
m
E
N
NA
N 3
M
водород
кислород
гелий
7.
рV21
0 3,76 10 Дж
N
рV
21
100 5,14 10 Дж
N
8. Как всё начиналось
Клапейрон Бенуа Поль Эмиль(26.I.1799–28.I.1864)
Французский физик,
член Парижской АН
Окончил
Политехническую школу
в Париже(1818)
В 1820–30 работал в
Петербурге в институте
инженеров путей
сообщения
9. Его уравнение состояния
Температуру, объем,давление и некоторые
другие параметры
принято называть
параметрами состояния
газа
Клапейрон выводит
уравнение,
устанавливающее
зависимость между
этими параметрами
Его называют
уравнением состояния
идеального газа
10. Его дело продолжено
Менделеев ДмитрийИванович
(8.II.1834–2.II.1907)
Обобщив уравнение
Клапейрона,
в 1874 вывел общее
уравнение состояния
идеального газа
11. Вот что получилось
Подставив вместоkNA
универсальную
газовую
постоянную R,
Менделеев
получил такой
вариант
уравнения,
которое теперь
называется
уравнением
Менделеева Клапейрона
12. Для чего это нужно?
Знатьуравнение
необходимо
при
исследовании
тепловых
явлений, а
конкретно…
13. В термометрах…
• В термометрах…Уравнение
позволяет
определить одну
из величин,
характеризующих
состояние, если
известны две
другие величины
Это используют в
термометрах
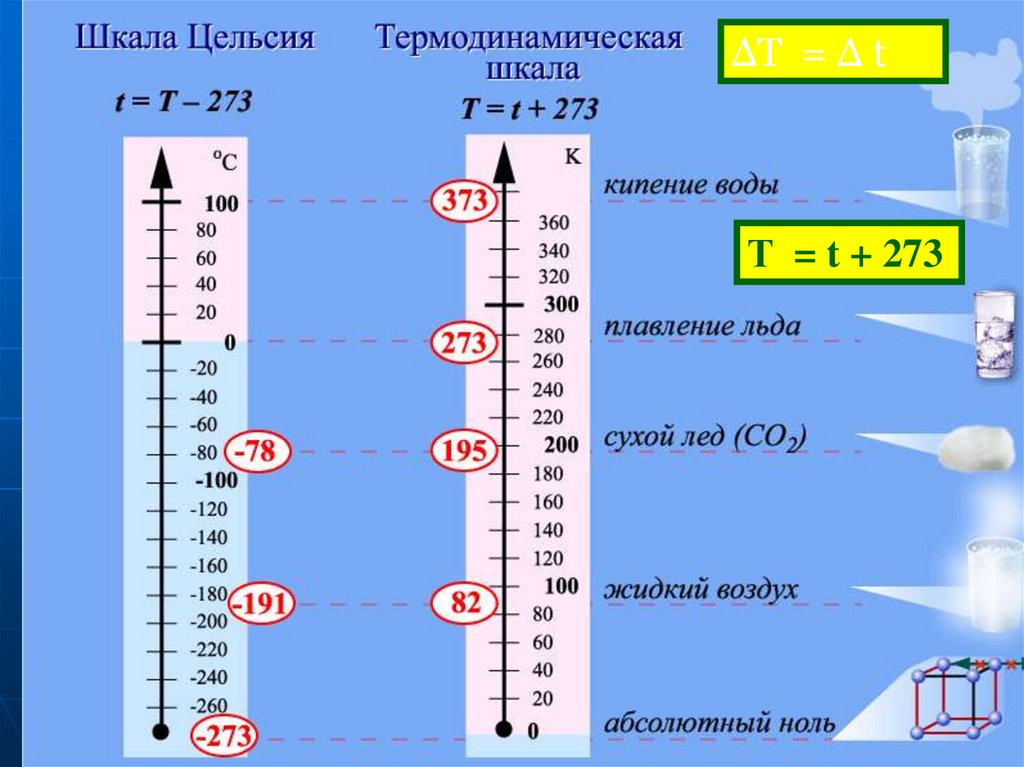
14.
ΔТ = Δ tТ = t + 273
15.
рV 2E kT
N 3
2
E kT
3
температура
–
3
E kT мера средней
2
кинетической
энергии
16. Уравнение Клапейрона
PVconst
T
P1V1 P2V2
T1
T2
17. Уравнение Менделеева-Клапейрона
Уравнение МенделееваКлапейрона18. Универсальная газовая постоянная
Произведение постояннойБольцмана k= 1,38*10 Дж/К и
числа АвогадроN = 6*10 моль
R= 8,31 Дж/ (моль* К)
19. В газовых законах…
• В газовых законах…Зная уравнение
состояния, можно
сказать, как
протекают в
системе процессы
при определённых
внешних условиях
20. В молекулярной физике…
• В молекулярной физике…Зная уравнение
состояния, можно
определить, как
меняется
состояние
системы, если она
совершает работу
или получает
теплоту от
окружающих тел
21. А в целом…
Уравнение Клапейрона-Менделеева показывает, что дляданной массы газа возможно одновременно изменение
трех
параметров,
характеризующих
состояние
идеального газа.
Уравнение Клапейрона-Менделеева представляет собой
уравнение
состояния
идеального
газа,
которое
объединяет закон Бойля — Мариотта, закон ГейЛюссака, закон Шарля и закон Авогадро.
Уравнение Клапейрона-Менделеева — наиболее простое
уравнение состояния, применяемое с определенной
степенью точности к реальным газам при низких
давлениях и высоких температурах, например, к
атмосферному воздуху, когда свойства газов близки к
идеальному газу.
22. Уравнение состояния -
Уравнение состояния Первое из замечательных обобщений вфизике, с помощью которых свойства
разных веществ выражаются через одни и
те же основные величины. Именно к
этому стремиться физика - к нахождению
общих законов, не зависящих от тех или
иных веществ. Газы, существенно простые
по своей природе, дали первый пример
такого обобщения. И в этом большая
заслуга одного из выдающихся учёных –
Дмитрия Ивановича Менделеева.
23. Для чего нужно уравнение состояния?
Уравнение состояния позволяет определитьодну из величин, характеризующих состояние,
например температуру, если известны две
другие величины. Это и используют в
термометрах.
Зная уравнение состояния, можно сказать, как
протекают в системе различные процессы при
определенных внешних условиях: например,
как будет меняться давление газа, если
увеличивать его объем при неизменной
температуре, и т. д.
Зная уравнение состояния, можно определить,
как меняется состояние системы, если она
совершает работу или получает теплоту от
окружающих тел.
24. Задача №1
Газ при давлении 200 кПа итемпературе 17 С имеет объем 5 л.
Чему равен объем (л) этой массы
газа при давлении 100 кПа и
температуре – 3 С?
25. Задача №2
В баллоне вместимостью25,6 л находится 1,04 кг азота при
давлении 3,55 МПа. Определить
температуру газа
26. Задача №3
Какой объем ( в литрах) 1 гводорода занимает при
нормальных условиях
( 273 К, 101 кПа)?





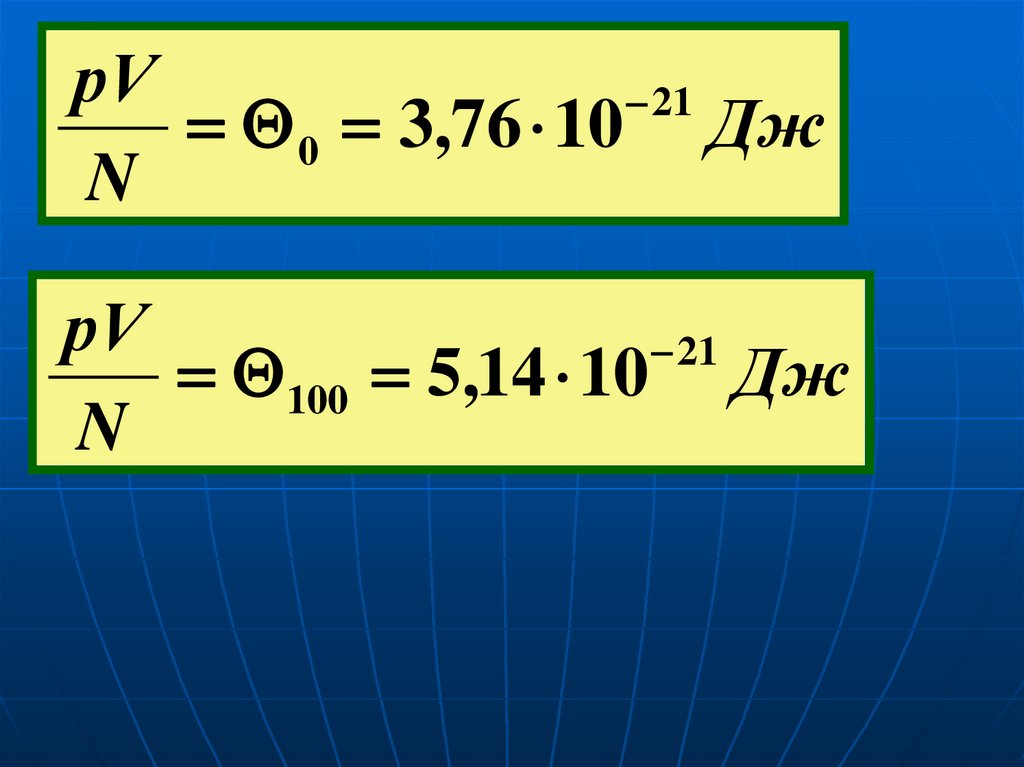


















 Физика
Физика








