Похожие презентации:
Органическая химия. Теория строения органических веществ
1.
Органическая химия.Теория строения
органических веществ
А.М. Бутлерова
Преподаватель Юридического колледжа
Валентина Владимировна Киреева
2.
РЕМОНТВ 1807 году Якоб
Берцелиус предложил
назвать вещества,
получаемые из
организмов,
органическими, а
науку, изучающую
их, - органической
химией.
3.
РЕМОНТТеория
витализма:
для
синтеза
органических веществ необходима особая
«жизненная сила», присущая только
живому, и поэтому их синтез невозможен.
Фридрих Вёлер в 1824 году синтезировал
щавелевую кислоту, а в 1828 году «органическую» мочевину.
В 1845 г. Кольбе синтезировал уксусную кислоту,
в 1854 г. Бертло – жир, в 1861 г. Бутлеров –
сахаристое вещество
4.
РЕМОНТФ. Энгельс: «Благодаря получению
неорганическим путем таких веществ,
которые до того времени порождались
только в живых организмах, было
доказано, что законы химии имеют ту же
силу для органических тел, как и для
неорганических…»
5.
РЕМОНТФормулы органических соединений:
СН4 С3Н6 С2Н5 ОН
СCl4
СF4
6.
РЕМОНТОрганические
вещества
соединения
углерода
(за исключением карбидов,
карбонатов, оксидов углерода и
цианидов)
независимо
от
способа их образования –
естественным
или
искусственным путем
7.
РЕМОНТОрганическая химия - раздел
химии, изучающий соединения
углерода,
их
структуру,
свойства, методы синтеза
8.
РЕМОНТОсновные «противоречия»
органической химии
•Многообразие веществ, образованных небольшим
числом элементов;
•Кажущееся несоответствие валентности в
органических веществах: СН4, С2Н6, С2Н4, С2Н2;
•Различные свойства соединений, имеющих
одинаковую молекулярную формулу (С6Н12О6 –
глюкоза, фруктоза; С4Н10О – бутиловый спирт,
диэтиловый эфир)
9.
РЕМОНТ«Органическая химия может сейчас кого угодно
свести с ума. Она представляется мне дремучим
лесом, полным удивительных вещей, безграничной
чащей, из которой нельзя выбраться, куда не
осмеливаешься проникнуть»
(из письма Ф.Велера к
Й. Берцелиусу)
10.
РЕМОНТБутлеров Александр
Михайлович
(1828-86)
« Нечто о строении
химических
соединений» 1861 год
11.
РЕМОНТОсновные положения теории
химического строения
(Бутлеров А.М., 1861)
12.
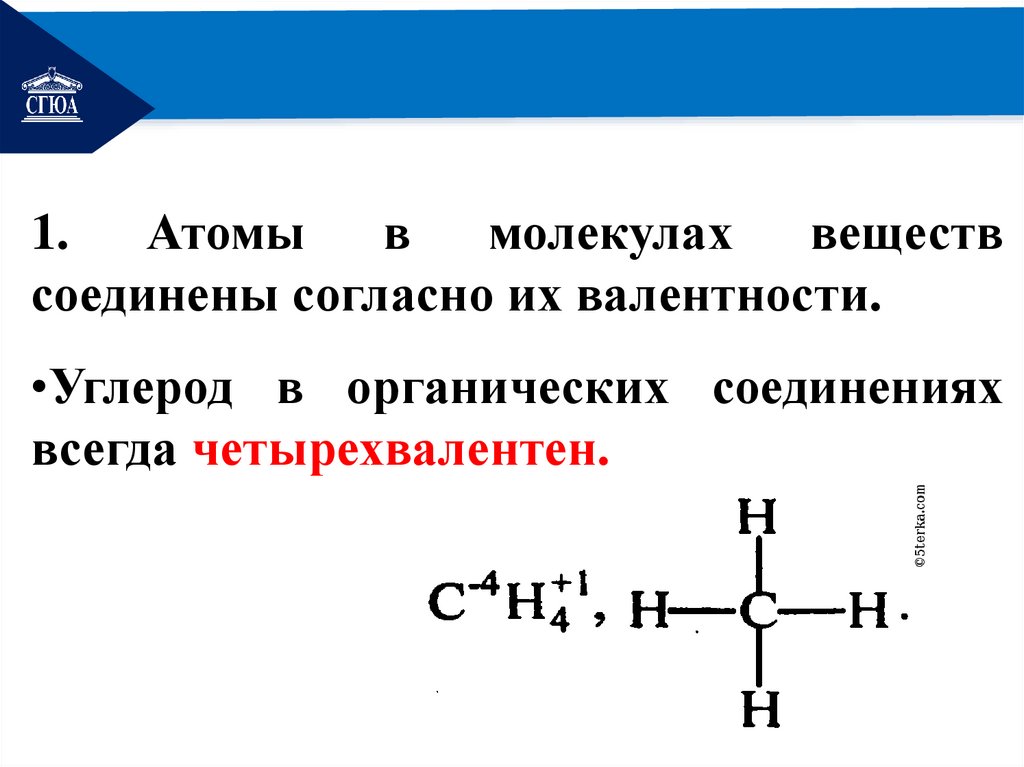
РЕМОНТ1.
Атомы
в
молекулах
веществ
соединены согласно их валентности.
•Углерод в органических соединениях
всегда четырехвалентен.
13.
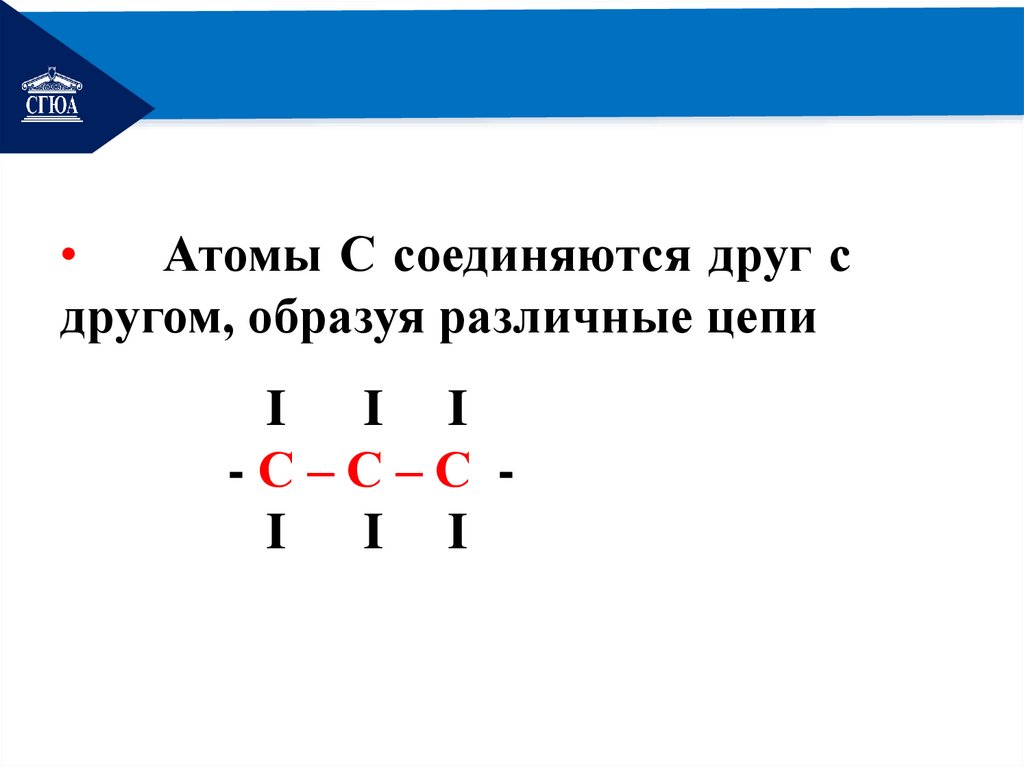
РЕМОНТАтомы С соединяются друг с
другом, образуя различные цепи
I
I I
-С–С–С I
I I
14.
РЕМОНТПорядок соединения атомов в молекулах
может
быть
отображен
при
помощи
структурных формул.
•Написать структурную формулу пропана
С3Н8
1. Составляем
цепочку
(углеродный скелет)
-С–С–С -
из
атомов
С
15.
РЕМОНТ•Доставляем связи у каждого атома С до 4
I I I
-С–С–С I I I
16.
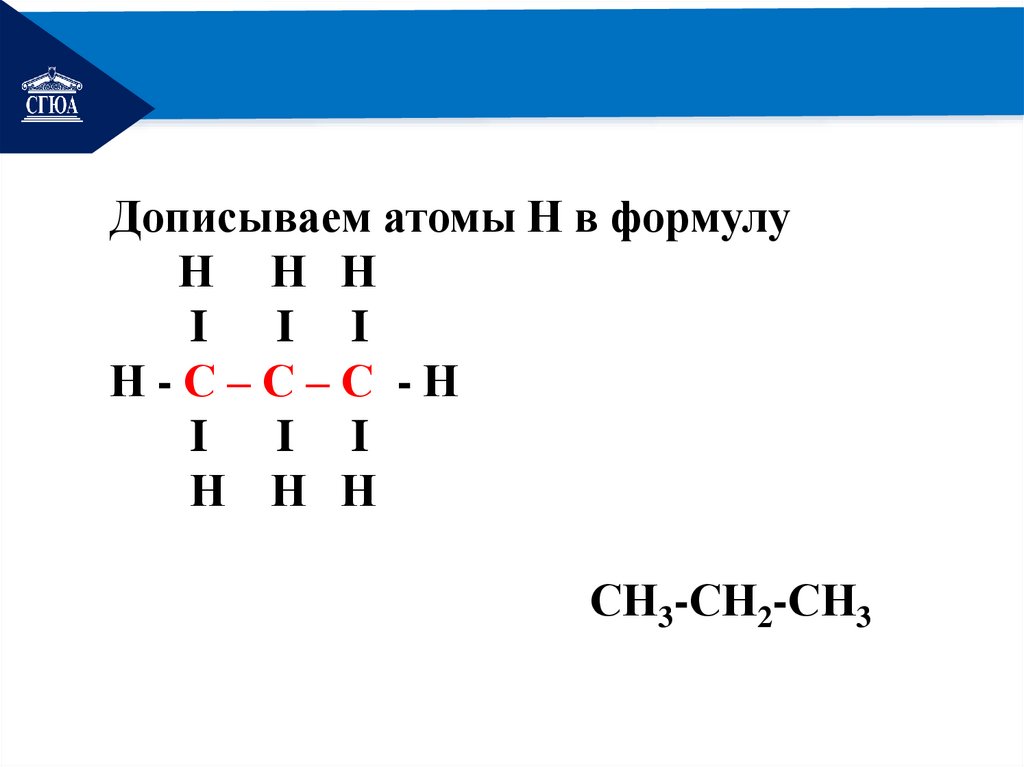
РЕМОНТДописываем атомы Н в формулу
Н Н Н
I I I
Н-С–С–С -Н
I I I
Н Н Н
СН3-СН2-СН3
17.
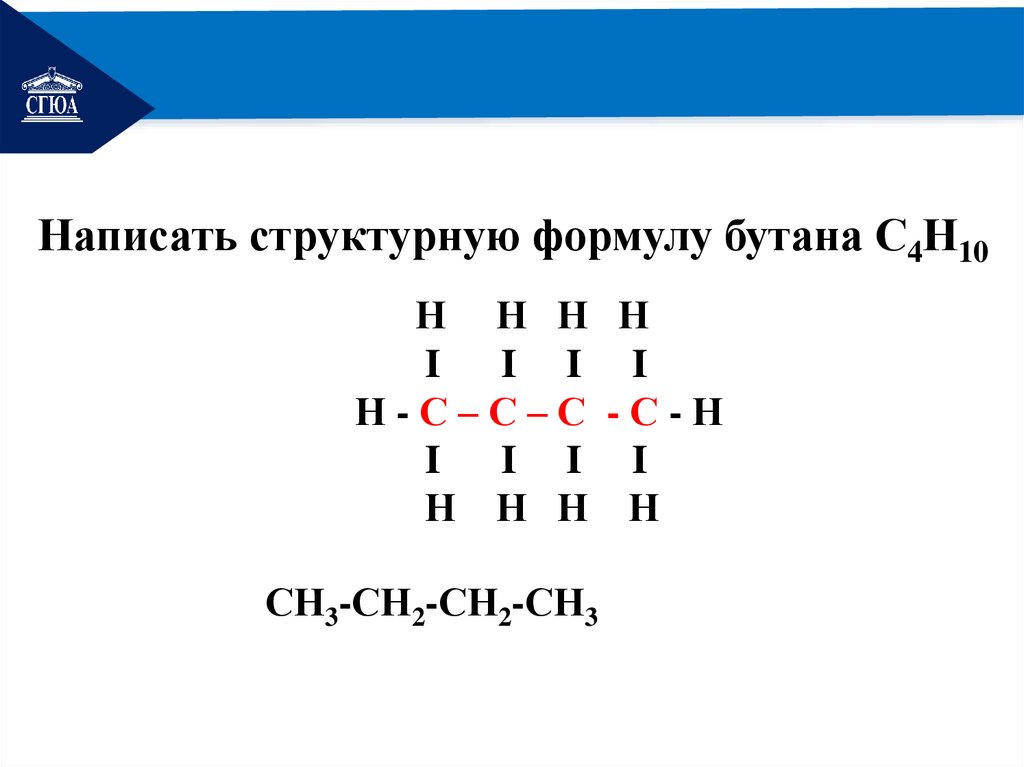
РЕМОНТНаписать структурную формулу бутана С4Н10
Н Н Н Н
I
I I I
Н-С–С–С -С-Н
I
I I I
Н Н Н Н
СН3-СН2-СН2-СН3
18.
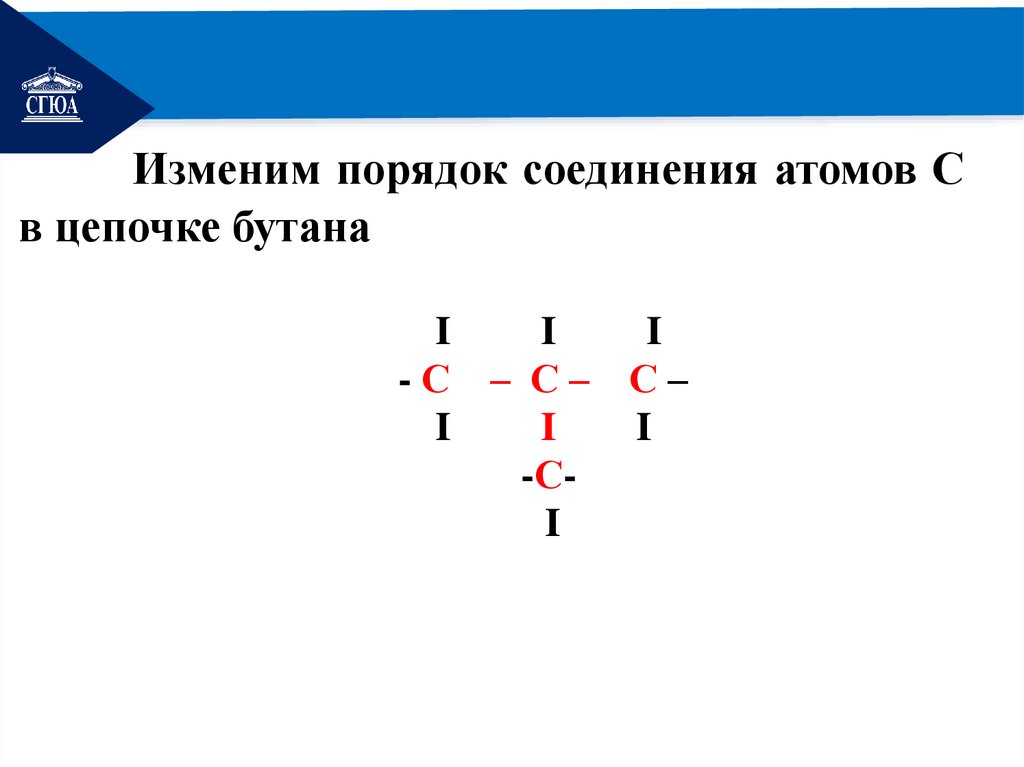
РЕМОНТИзменим порядок соединения атомов С
в цепочке бутана
I
I
-С – С–
I
I
-СI
I
С–
I
19.
РЕМОНТН
Н
Н
I
I
I
Н–С – С– С– Н
I
I
I
Н Н-С-Н Н
I
Н
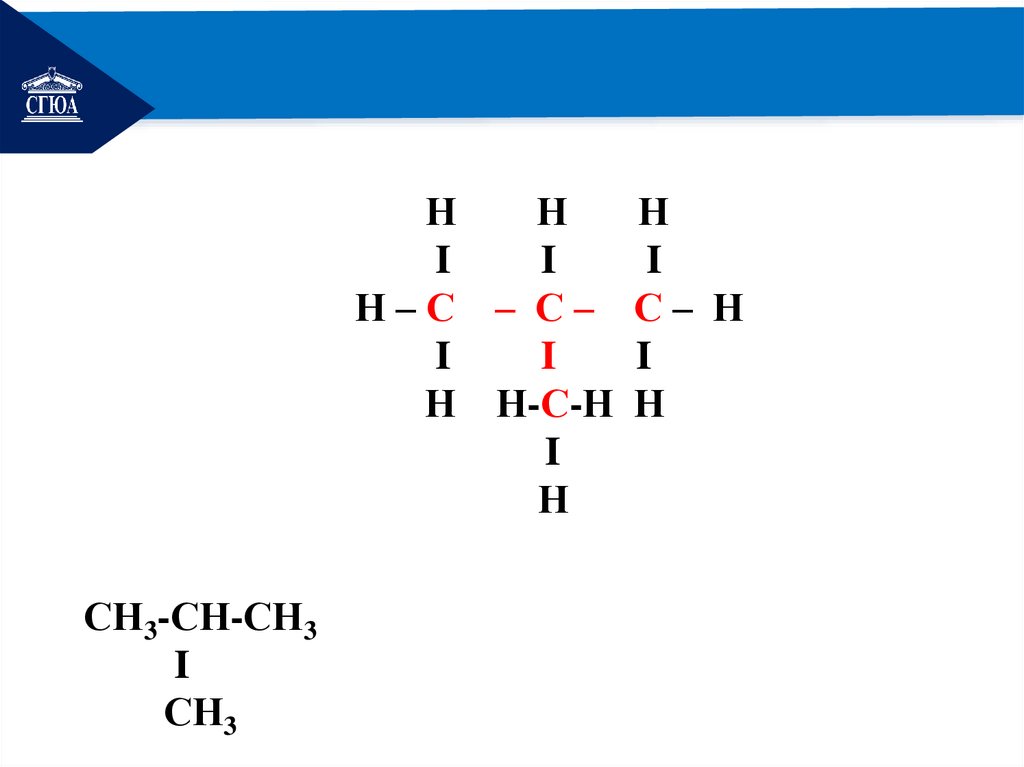
СН3-СН-СН3
I
СН3
20.
РЕМОНТСН3 - СН2
- СН2
- СН3
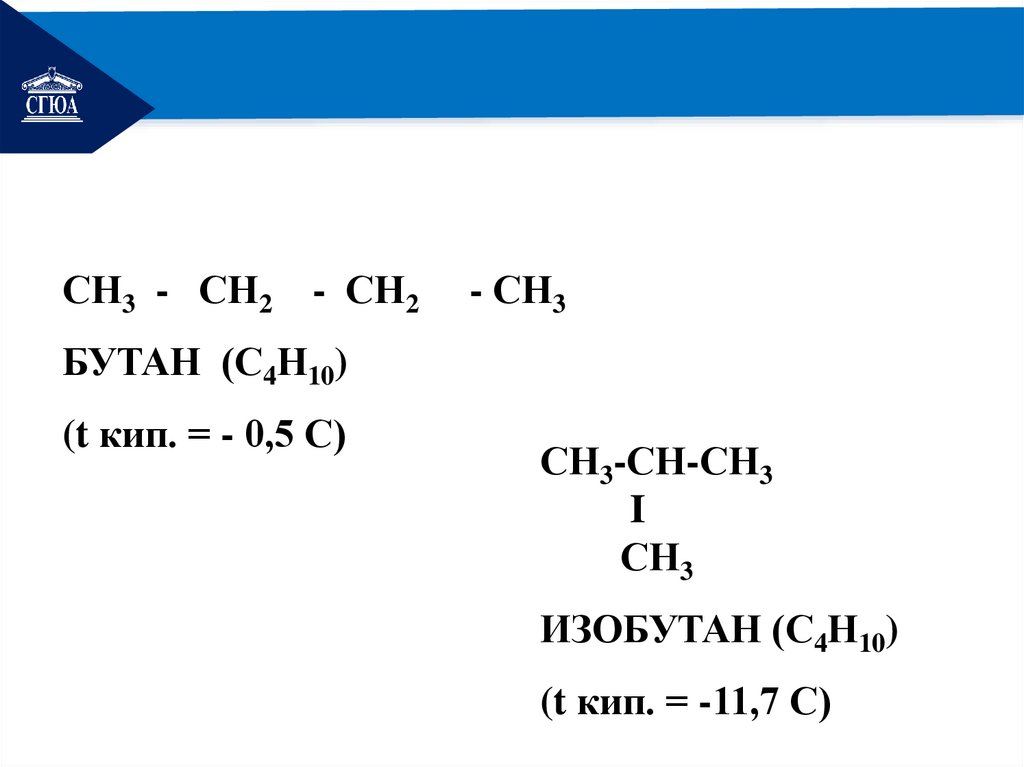
БУТАН (С4Н10)
(t кип. = - 0,5 С)
СН3-СН-СН3
I
СН3
ИЗОБУТАН (С4Н10)
(t кип. = -11,7 С)
21.
РЕМОНТ2.
Свойства
веществ
определяются не только их
качественным
и
количественным составом, но и
порядком соединения атомов в
молекуле,
т.е.
химическим
строением вещества.
22.
РЕМОНТВещества, которые имеют один
и
тот
же
качественный
и
количественный
составы,
но
отличаются по своему строению и
свойствам, называются изомерами, а
явление
существования
таких
веществ носит название изомерии
23.
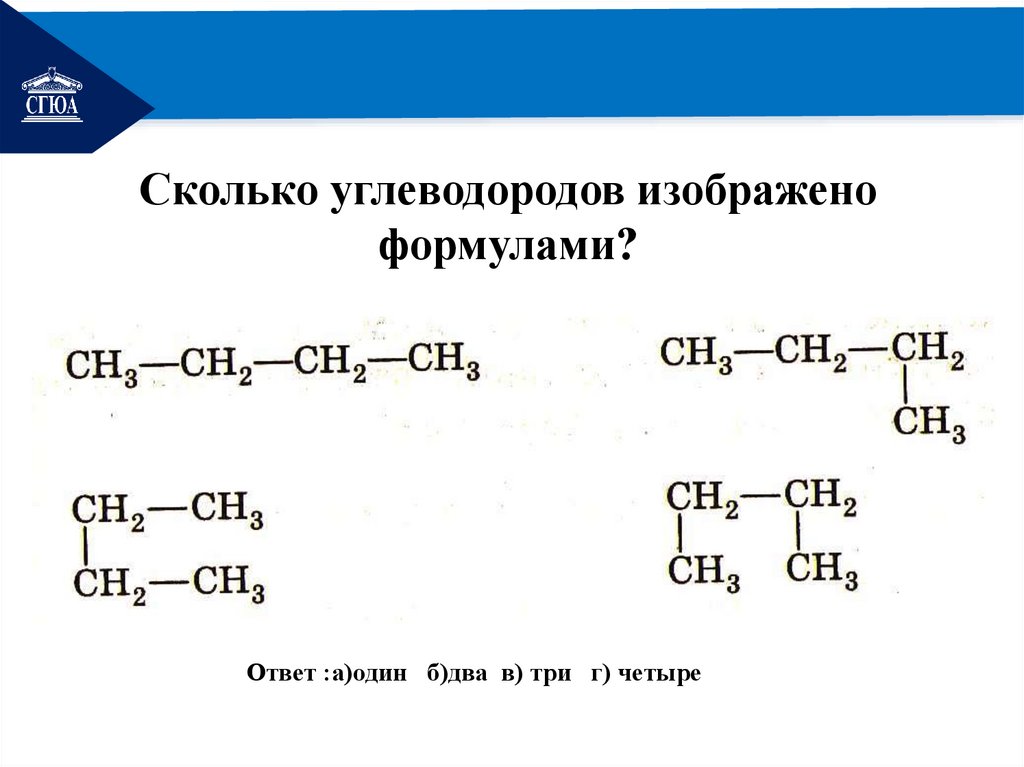
РЕМОНТСколько углеводородов изображено
формулами?
Ответ :а)один б)два в) три г) четыре
24.
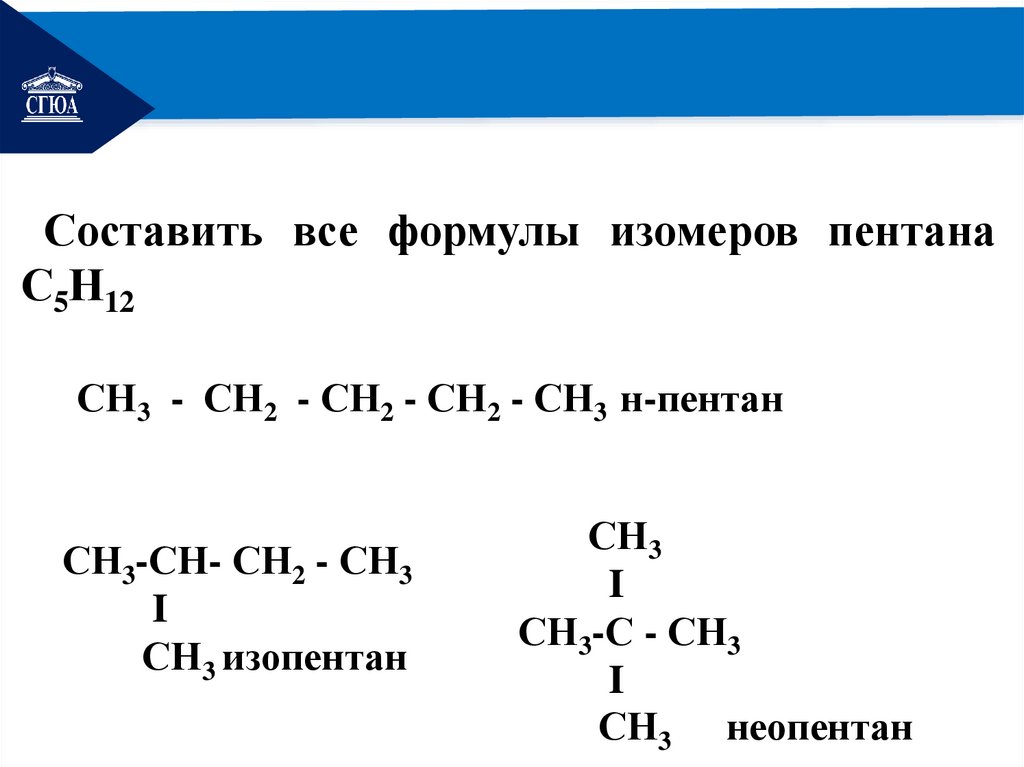
РЕМОНТСоставить все формулы изомеров пентана
С5Н12
СН3 - СН2 - СН2 - СН2 - СН3 н-пентан
СН3-СН- СН2 - СН3
I
СН3 изопентан
СН3
I
СН3-С - СН3
I
СН3 неопентан
25.
РЕМОНТЗадание
Составить формулы изомеров гексана С6Н14
26.
РЕМОНТ3. Свойства органических соединений зависят
от взаимного влияния атомов и групп атомов в
молекуле друг на друга.
27.
РЕМОНТ4. Зная строение вещества, можно
предположить его свойства.
Зная свойства вещества, можно
предположить его строение
СН3 - СН2 - ОН
этиловый спирт
СН3 - О
диметиловый эфир
С2Н6О
- СН3
28.
РЕМОНТ29.
РЕМОНТКлассификация химических реакций
1. Реакции замещения;
2. Реакции присоединения:
- гидрирование – присоединение молекулы Н2;
- галогенирование - присоединение молекулы
галогена;
- гидрогалогенирование
присоединение
молекулы галогеноводорода;
- гидратация - присоединение молекулы Н2О;
- полимеризация
–
образование
высокомолекулярного соединения посредством
многократного соединения низкомолекулярных
соединений.
30.
РЕМОНТРеакции
элиминирования
(отщепления):
- дегидрирование
–
отщепление
молекулы Н2;
- дегидратация
–
отщепление
молекулы Н2О;
- дегидрогалогенирование
–
отщепления
молекулы
галогеноводородов и воды
31.
РЕМОНТ4. Реакция изомеризации - внутримолекулярная
перестройка без изменения состава вещества.
5. Реакции окисления.
6. Реакции конденсации и поликонденсации взаимодействие
нескольких
органических
соединений с образованием нового орг. вещества и
низкомолекулярного соединения.
7. Реакции разложения - процесс расщепления
сложного органического соединения на менее
сложные или простые вещества
32.
СПАСИБО ЗАВНИМАНИЕ!






















 Химия
Химия








