Похожие презентации:
Благородные газы
1.
Благородные газы.2.
Благородные газы.химические элементы, образующие нулевую
группу периодической системы элементов, а
именно: гелий (Не), неон (Ne), аргон (Аr или А),
криптон (Кr), ксенон (X или Хe);
3.
Гелий "He".Химический элемент VIII группы короткой формы первого периода периодической системы
химических элементов, имеет атомный номер
2. Возглавляет группу инертных газов.
Свечение гелия в газорозрядной трубе.
4.
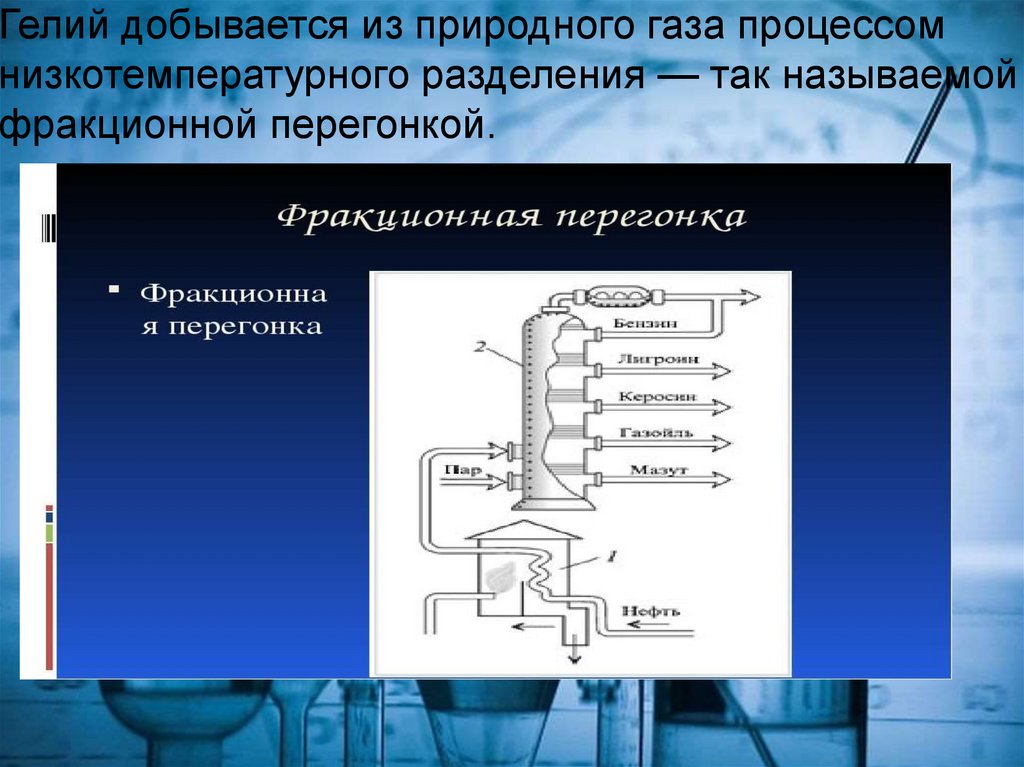
Гелий добывается из природного газа процессомнизкотемпературного разделения — так называемой
фракционной перегонкой.
5.
История открытия.18 августа 1868 года французский учёный Пьер Жансен, находясь во время
полного солнечного затмения в индийском городе Гунтур, впервые исследовал
хромосферу Солнца. Жансену удалось настроить спектроскоп таким образом,
чтобы спектр короны Солнца можно было наблюдать не только при затмении,
но и в обычные дни. На следующий же день спектроскопия солнечных
протуберанцев наряду с линиями водорода — синей, зелено-голубой и красной
— выявила очень яркую жёлтую линию, первоначально принятую Жансеном и
другими наблюдавшими её астрономами за линию D натрия. Жансен
немедленно написал об этом во Французскую академию наук. Впоследствии
было установлено, что ярко-жёлтая линия в солнечном спектре не совпадает с
линией натрия и не принадлежит ни одному из ранее известных химических
элементов.Спустя два месяца, 20 октября, английский астроном Норман Локьер
не зная о разработках французского коллеги, также провёл исследования
солнечного спектра. Обнаружив неизвестную жёлтую линию с длиной волны
588 нм (более точно — 587,56 нм), он обозначил её D3, так как она была очень
близко расположена к фраунгоферовым линиям D1 (589,59 нм) и D2 (588,99 нм)
натрия. Спустя два года Локьер совместно с английским химиком Эдуардом
Франклендом, в сотрудничестве с которым он работал, предложил дать новому
элементу название «гелий» (от др.-греч. ἥλιος — «солнце»).
6.
Физические свойства.Гелий — практически инертный химический элемент.
Простое вещество гелий нетоксично, не имеет цвета, запаха и вкус
He) наименьшая среди всех веществ; твёрдый гелий получен лишь пр
7.
Свойства в газовой сфере.При нормальных условиях гелий ведёт себя практически как идеальный газ.
При всех условиях гелий является моноатомным веществом. обладает
теплопроводностью — бо́льшей, чем у всех других газов, за исключением
водорода, а его удельная теплоёмкость чрезвычайно высока.
Символ элемента, выполненный из газоразрядных трубок, наполненных
гелием.
При пропускании тока через заполненную гелием трубку наблюдаются
разряды различных цветов, зависящих главным образом от давления газа в
трубке. Обычно видимый свет спектра гелия имеет жёлтую окраску. По мере
уменьшения давления происходит смена цветов на розовый, оранжевый,
жёлтый, ярко-жёлтый, жёлто-зелёный и зелёный. Это связано с присутствием
в спектре гелия нескольких серий линий, расположенных в диапазоне между
инфракрасной и ультрафиолетовой частями спектра.
8.
ПрименениеГелий широко используется в промышленности и народном хозяйстве:
в металлургии в качестве защитного инертного газа для выплавки чистых мет
в пищевой промышленности (зарегистрирован в качестве пищевой добавки E9
в качестве хладагента для получения сверхнизких температур (в частности, дл
для наполнения воздухоплавающих судов (дирижабли и аэростаты) — при нез
в дыхательных смесях для глубоководного погружения
для наполнения воздушных шариков и оболочек метеорологических зондов;
для заполнения газоразрядных трубок;
в качестве теплоносителя в некоторых типах ядерных реакторов;
в качестве носителя в газовой хроматографии;
для поиска утечек в трубопроводах и котлах
как компонент рабочего тела в гелий-неоновых лазерах;
в качестве наполнителя в некоторых современных моделях накопителей на жё
для наполнения колб филаментных светодиодных ламп, что позволяет эффек
9.
Неон.Нео́н-химический элемент 8-й группы второго периода
периодической системы с атомным номером 10.Пятый по
распространённости элемент Вселенной после водорода,
гелия, кислорода и углерода. Как простое вещество
представляет собой инертный одноатомный газ без цвета
и запаха. Обнаружен в1898 году путём вывода из жидкого
воздуха водорода,кислорода,аргона и углекислого газа.
Неон в сосуде.
10.
История.Неон открыли в июне 1898 года английские химики Уильям
Рамзай и Морис Траверд. Они выделили этот инертный газ
«методом исключения» после того, как кислород, азот, аргон и
все более тяжёлые компоненты воздуха были сжижены. В
декабре 1910 года французский изобретатель Жорж Клод
создал газоразрядную лампу, заполненную неоном.
Происхождение названия.
Название происходит от греч. νέος — новый.
11.
Физические свойства.Благородные газы — бесцветные одноатомные газы без
вкуса и запаха.Инертные газы обладают более высокой
электропроводностью по сравнению с другими газами и при
прохождении через них тока ярко светятся, в частности,
неон — огненно-красным светом, так как самые яркие его
линии лежат в красной части спектра.Эмиссионный спектр
неона (слева направо: от ультрафиолетовых до
инфракрасных линий. Линии, находящиеся в невидимых
глазом участках спектра, изображены белым цветом).
Насыщенность внешних электронных оболочек атомов
инертных газов обусловливает более низкие точки
сжижения и отвердевания, чем у других газов с близкими
молекулярными массами.
12.
Химические свойства.Все благородные газы имеют завершённую
электронную оболочку, поэтому они химически
инертны. Химическая инертность неона
исключительна, в этом с ним может конкурировать
только гелий. Пока не получено ни одного его
валентного соединения. Даже так называемые
клатратные соединения неона с водой (Ne·6Н2О),
гидрохиноном и другими веществами (подобные
соединения тяжелых благородных газов: радона,
ксенона, криптона и даже аргона — широко
известны) получить и сохранить очень трудно
13.
ПрименениеНеоновая» вывеска
идкий неон используют в качестве охладителя в криогенных
становках. Ранее неон применялся в промышленности в качестве
нертной среды, но был вытеснен более дешёвым аргоном. Неоном
аполняют газоразрядные лампы, сигнальные лампы в
адиотехнической аппаратуре, фотоэлементы, выпрямители. Смесь
еона и гелия используют как рабочую среду в газовых лазерах
елий-неоновый лазер).
рубки, заполненные смесью неона и азота, при пропускании через
их электрического разряда дают красно-оранжевое свечение, в связи
чем они широко используются в рекламе.
14.
Криптон.Крипто́н — химический элемент с атомным номером 36.
Принадлежит к 8-й группе периодической таблицы
химических элементов, находится в четвёртом периоде
таблицы. Атомная масса элемента 83,798. Обозначается
символом Kr (от лат. krypton). Простое вещество
криптон — инертный одноатомный газ без цвета, вкуса
и запаха.
Газовый разряд в криптоне
15.
История
В 1898 году Уильям Рамзай совместно со своим
ассистентом Морисом Уильямом Траверсом
выделил из жидкого воздуха, предварительно
удалив кислород, азот и аргон, смесь, в которой
спектральным методом были открыты два газа:
криптон (от греч. κρυπτός — «скрытый»,
«секретный») и ксенон («чуждый», «необычный»).
16.
Физические свойства
Криптон — инертный одноатомный газ без цвета, вкуса и
запаха (при давлении 6 атмосфер приобретает острый
запах, похожий на запах хлороформа. Плотность при
стандартных условиях в 3 раза тяжелее воздуха. При
нормальном давлении криптон сжижается при температуре
0−153,415 °C, затвердевает при −157,37 °C, образуя
кристаллы кубической сингонии (гранецентрированная
решётка), пространственная группа Fm3m, параметры
ячейки a = 0,572 нм, Z = 4. Таким образом, в жидкой фазе он
существует лишь в диапазоне температур около четырёх
градусов.
17.
Химические свойства
Криптон химически инертен. В жёстких условиях
реагирует со фтором, образуя дифторид криптона.
Относительно недавно было получено первое
соединение со связями Kr−O (Kr(OTeF5)2).
В 1965 году было заявлено о получении соединений
состава KrF4, KrO3·H2O и BaKrO4. Позже их
существование было опровергнуто.
В 2003 году в Финляндии было получено первое
соединение со связью C−Kr (HKrC≡CH —
гидрокриптоацетилен) путём фотолиза криптона и
ацетилена на криптонной матрице
18.
ПрименениеПроизводство сверхмощных эксимерных лазеров (KrF).
Криптон используется для заполнения ламп
накаливания, увеличивая срок службы нити накала.
Как теплоизолятор и шумоизолятор в стеклопакетах.
Фториды криптона предложены в качестве
окислителей ракетного топлива.
В период между 1960 и 1983 годом длина волны
оранжевой линии спектра излучения 86Kr служила
для определения метра.
Рабочее тело для электроракетных двигателей.
19.
Биологическая рольВоздействие криптона на живые организмы изучено
плохо. Исследуются возможности его использования
в водолазном деле в составе дыхательных смесей и
при повышенном давлении как средство для
анестезии.
Физиологическое действие
Большое количество вдыхаемого криптона при
недостаточном количестве кислорода может привести
к удушью.
При вдыхании газовых смесей, содержащих криптон,
при давлении более 3,5 атмосфер наблюдается
наркотический эффект
20.
Радон.86.РадонRnРадо́н-элемент 18-й группы периодической
системы химических элементов Д. И. Менделеева (по
старой классификации-главной подгруппы VIII группы), 6-го
периода, с атомным номером 86. Обозначается символом
Rn (лат. Radon). Простое вещество радон при нормальных
условиях-бесцветный инертный газ; радиоактивен,
стабильных изотопов не имеет, может представлять
опасность для здоровья и жизни. При комнатной
температуре является одним из самых тяжёлых газов.
Наиболее стабильный изотоп (Rn) имеет период
полураспада 3,8 суток.
Внешний вид простого вещества
Бесцветный, слегка флюоресцирующий радиоактивный га
21.
Физические свойства.Растворимость в воде при комнатной температуре составляет 460 мл/л, что
выше, чем растворимость более лёгких инертных газов. В органических
растворителях и в жировой ткани человека растворимость радона в десятки
раз выше, чем в воде. Газ хорошо просачивается сквозь полимерные плёнки.
Химические свойсва.
В химическом отношении радон является наиболее активным из
благородных газов, так как его электроны внешних электронных
оболочек имеют относительную низкую энергию ионизации.Радон
образует химические соединения с фтором. Так, дифторид радона
RnF2 является белым нелетучим кристаллическим
веществом.Фториды радона могут быть получены также под
действием сильных фторирующих агентов (например, фторидов
галогенов.Получены также соединения с катионом.Кроме фтора, радон
может образовывать бинарные соединения с кислородом; в
частности, был получен триоксид радона, однако получение других
оксидов радона не подтверждено.Кроме того, радон может входить в
состав различных клатратов, которые, хотя и имеют постоянный
стехиометрический состав, не образуют химических связей с участием
атомов радона.
22.
История.Открытие радиоактивности и радона совпало с
повышением интереса к биологическим эффектам
радиации. Было установлено, что вода многих
источников минеральных вод богата эманацией
радия (так именовался радон в то время). Вслед за
этим открытием последовала волна моды «на
радиацию». В частности, в рекламе того времени
радиоактивность минеральных вод выдавалась за
главный показатель их полезности и эффективности.
23.
ПрименениеРадон используют в медицине для
приготовления радоновых ванн. Радон
используется в сельском хозяйстве для
активации кормов домашних животных, в
металлургии в качестве индикатора при
определении скорости газовых потоков в
доменных печах, газопроводах. В геологии
измерение содержания радона в воздухе и
воде применяется для поиска
месторождений урана и тория.
24.
Биологическое воздействиеРадон радиотоксичен и канцерогенен. Попадая
в организм человека, он способствует
процессам, приводящим к раку лёгкого. Распад
ядер радона и его дочерних изотопов в
лёгочной ткани вызывает микроожог, поскольку
вся энергия альфа-частиц поглощается
практически в точке распада. Особенно опасно
(повышает риск заболевания) сочетание
воздействия радона и курения. По данным
департамента здравоохранения США радон —
второй по частоте (после курения) фактор,
вызывающий рак лёгких преимущественно
бронхогенного (центрального) типа.
25.
Ксенон.Ксено́н — элемент 18-й группы (по устаревшей
классификации — элемент главной подгруппы VIII группы),
пятого периода периодической системы химических
элементов Д. И. Менделеева, с атомным номером 54.
Обозначается символом Xe (лат. Xenon). Простое вещество
ксенон — благородный одноатомный газ без цвета, вкуса и
запаха.
26.
История.Открыт в 1898 году британскими учёными Уильямом
Рамзаем и Морисом Траверсом, которые подвергли
медленному испарению жидкий воздух и
спектроскопическим методом исследовали его наиболее
труднолетучие фракции. Ксенон был обнаружен как
небольшая примесь к криптону. За открытие инертных
газов (в частности ксенона) и определение их места в
периодической таблице Менделеева Рамзай получил в
1904 году Нобелевскую премию по химии.
Происхождение названия
Рамзай предложил в качестве названия элемента древнегрече
27.
Физические свойстваГранецентрированная кубическая структура ксенона; a = 0,6197
нм
При нормальном давлении температура плавления 161,40 К
(−111,75 °C), температура кипения 165,051 К (−108,099 °C).
Молярная энтальпия плавления 2,3 кДж/моль, молярная
энтальпия испарения 12,7 кДж/моль, стандартная молярная
энтропия 169,57 Дж/(моль·К)
Химические свойства.
Ксенон стал первым инертным газом, для которого были получены настоящие
Первое соединение ксенона было получено Нилом Барлеттом реакцией ксенон
28.
Получение.Ксенон получают как побочный продукт
производства жидкого кислорода на
металлургических предприятиях.
В промышленности ксенон получают как
побочный продукт разделения воздуха на
кислород и азот. После такого разделения,
которое обычно проводится методом
ректификации, получившийся жидкий кислород
содержит небольшие количества криптона и
ксенона
29.
Применение.Несмотря на высокую стоимость, ксенон незаменим
в ряде случаев:
Ксенон используют для наполнения ламп
накаливания, мощных газоразрядных и импульсных
источников света (высокая атомная масса газа в
колбах ламп препятствует испарению вольфрама с
поверхности нити накаливания).
Радиоактивные изотопы применяют в качестве
источников излучения в радиографии и для
диагностики в медицине, для обнаружения течи в
вакуумных установках.
Фториды ксенона используют для пассивации
металлов.
30.
Применение.Ксенон как в чистом виде, так и с небольшой
добавкой паров цезия-133, является
высокоэффективным рабочим телом для
электрореактивных двигателей космических
аппаратов. В 2020 году Роскосмос заявил о начале
строительства космического аппарата «Нуклон» с
ядерной силовой установкой. Ксенон будет
использоваться в качестве рабочего тела
реактивного двигателя.
В наши дни ксенон проходит апробацию в лечении
зависимых состояний
31.
Применение.Жидкий ксенон иногда используется как рабочая среда
лазеров.
Ксенон используется для наполнения ячейки Голея в
детекторах терагерцевого излучения.
Для транспортировки фтора, проявляющего сильные
окисляющие свойства.
32.
Биологическая роль.Газ ксенон нетоксичен, но способен вызвать
наркоз (по физическому механизму), а в
больших концентрациях (более 80 %)
вызывает асфиксию.
Заполнение ксеноном лёгких и выдыхание
при разговоре приводит к значительному
понижению тембра голоса (эффект, обратный
эффекту гелия).
Фториды ксенона ядовиты, ПДК в воздухе —
0,05 мг/м³
33.
Аргон.Арго́н — химический элемент 8й группы периодической
таблицы химических элементов третьего периода
периодической системы химических элементов Д. И.
Менделеева, с атомным номером 18. Обозначается символом
Ar (лат. Argon). Третий по распространённости элемент в
земной атмосфере (после азота и кислорода) — 0,93 % по
объёму. Простое вещество аргон — инертный одноатомный
газ без цвета, вкуса и запаха.
34.
Происхождение названия.По предложению доктора Медана (председателя
заседания, на котором был сделан доклад об
открытии) Рэлей и Рамзай дали новому газу имя
«аргон» (от др.-греч. ἀργός — ленивый, медленный,
неактивный). Это название подчёркивало
важнейшее свойство элемента — его химическую
неактивность.
35.
Физические свойства.Аргон — одноатомный газ с температурой кипения
(при нормальном давлении) −185,9 °C (немного
ниже, чем у кислорода, но немного выше, чем у
азота). В 100 мл воды при 20 °C растворяется 3,3 мл
аргона, в некоторых органических растворителях
аргон растворяется значительно лучше, чем в воде.
Плотность при нормальных условиях составляет
1,7839 кг/м3.
36.
Химические свойства.Пока известны только 2 химических соединения
аргона — гидрофторид аргона и CU(Ar)O, которые
существуют при очень низких температурах. Кроме
того, аргон образует эксимерные молекулы, то есть
молекулы, у которых устойчивы возбуждённые
электронные состояния и неустойчиво основное
состояние.
37.
Изотропы.Аргон представлен в земной атмосфере тремя
стабильными изотопами.Почти вся масса тяжёлого
изотопа 40Ar возникла на Земле в результате
распада радиоактивного изотопа калия 40K . Распад
радиоактивного калия идёт по двум направлениям
одновременно.
38.
Применение.
в аргоновых лазерах;
внутри ламп накаливания и при заполнении
внутреннего пространства стеклопакетов;
в качестве защитной среды при сварке, как
металлов (например, титана), так и неметаллов;
в качестве плазмаобразователя в плазматронах при
сварке и резке
39.
Биологическая роль
Аргон не играет никакой заметной
биологической роли.
Физиологическое действие
Инертные газы обладают физиологическим
действием, которое проявляется в их
наркотическом воздействии на организм.
Наркотический эффект от вдыхания аргона
проявляется только при барометрическом
давлении свыше 0,2 МПа







































 Химия
Химия








