Похожие презентации:
Иммобилизованные ферменты
1. Иммобилизованные ферменты
2. План
• 1. Преимущества и недостатки иммобилизованныхферментов.
• 2.
Влияние иммобилизации на состояние
фермента.
• 3. Стабильность иммобилизованных ферментов.
• 4. Основной принцип конструирования ферментных
электродов и их рабочие параметры.
• 5. Ферментные электроды и их использование в
научно-исследовательских
и
технологических
процессах.
3.
• Иммобилизация ферментов – этоперевод
их
в
нерастворимое
состояние с сохранением (частичным
или
полным)
каталитической
активности.
4.
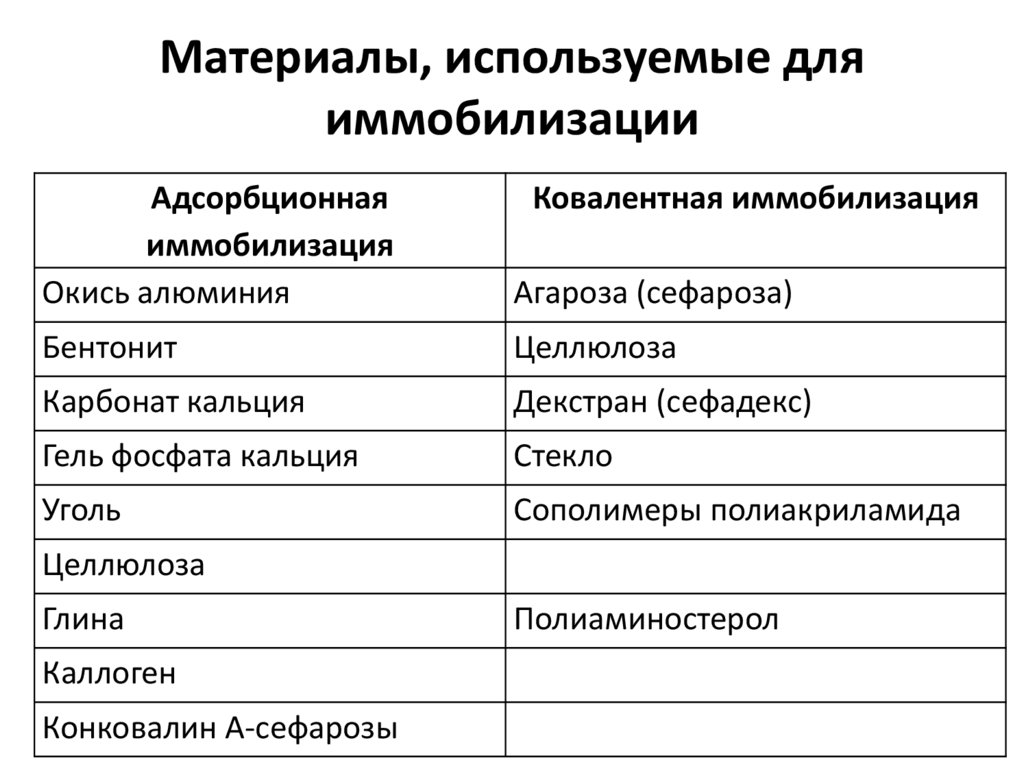
5. Материалы, используемые для иммобилизации
Адсорбционнаяиммобилизация
Окись алюминия
Ковалентная иммобилизация
Агароза (сефароза)
Бентонит
Целлюлоза
Карбонат кальция
Декстран (сефадекс)
Гель фосфата кальция
Стекло
Уголь
Сополимеры полиакриламида
Целлюлоза
Глина
Каллоген
Конковалин А-сефарозы
Полиаминостерол
6. Кинетические параметры катализа иммобилизованных ферментов
• Cкорость(V)
катализируемой
ферментативной
реакции
подчиняется
уравнению
Михаэлиса
–
Ментен,
предложенному еще в начале XX века:
kкат [Е] [S]
V=
Км + [S]
где [Е], [S] – концентрация фермента и субстрата в
системе соответственно; kкат – каталитическая константа
ферментативной реакции; Км – константа Михаэлиса.
7.
Vначальный
наклон = Е/Км
V = 0,5
[S]
0
Км
а
1/V
наклон = Км/[Е]
1/[Е]
1/[S]
0
–1/Км
б
Зависимость начальной скорости (0) от концентрации субстрата
(S): а, б – в обычных и обратных координатах соответственно
8.
Факторы вызывающие инактивациюсвободных ферментов
• Физические (нагревание или охлаждение,
облучение
(γ-рентгеновские
лучи),
ультразвук, сорбцию и т. д. )
• Химические (действие щелочи, кислоты,
ПАВ, окислителей и т. д. )
9. Основные инактивационные механизмы
• 1. Агрегация.• 2. Изменение первичной структуры.
• 3. Десорбция кофактора из активного
центра фермента.
10.
Три причины изменения стабильности врезультате иммобилизации:
• 1.
Изменение
конформации
иммобилизованного
фермента
по
сравнению с нативной структурой.
• 2. Изменение микроокружения ферментной
молекулы.
• 3. Ужесточение нативной конформации
белковой глобулы.
11.
ФерментБиофункциональный
реагент
Активный центр
а
б
Схематическое изображение иммобилизованных
подходов к стабилизации ферментов:
а – многоточечное ковалентное связывание;
б – сшивание биофункциональными реагентами;
в – включение в поры носителя.
в
12. Ферментные электроды
• Ферментный электрод – это комбинациядатчика, основанного на использовании
ионселективного
электрода,
с
иммобилизованным
ферментом,
обеспечивающая высокоселективный и
высокочувствительный метод определения
данного субстрата.
13.
1962 г. - первые сообщения об измеренииконцентрации глюкозы в биологических растворах и
тканях
с
помощью
электрода,
в
котором
использовали глюкозооксидазу, иммобилизованную в
геле
на
поверхности
полярографического
кислородного электрода
14. Электродные датчики, используемые для конструирования ферментных электродов
ДатчикиОпределяемое вещество
Датчики для потенциометрических электродов
NH3
Мочевина, аминокислоты, глутамин, нитрат и др.
CO2
Мочевина, аминокислоты,
декарбоксилирования
pH
Пенициллин, РНК, ДНК, глюкоза и др.
ферментные
системы
Датчики для амперометрических электродов
O2
Pt или С
Глюкоза, аминокислоты, спирты, мочевая кислота,
холестерол, фосфат, ферменты – катализирующие
поглощение О2
Окислительно-восстановительные ферменты, сульфат,
холестерол, спирты, глюкоза, органические кислоты и
др.













 Биология
Биология








