Похожие презентации:
Идеальный газ. Основное уравнение МКТ идеального газа. Температура. Формула Больцмана
1.
Идеальный газ.Основное уравнение МКТ
идеального газа. Температура.
Формула Больцмана.
Преподаватель физики
Костенкова С.С.
ГБПОУ КДПИ им. К. Фаберже
2016
2.
Идеальный газИзвестно, что частицы в газах, в отличие от
жидкостей и твердых тел, располагаются друг
относительно друга на расстояниях, существенно
превышающих их собственные размеры.
В этом случае взаимодействие
между молекулами пренебрежимо
мало и кинетическая энергия
молекул много больше энергии
межмолекулярного
взаимодействия.
Для выяснения наиболее
общих свойств, присущих всем
газам, используют упрощенную
модель реальных газов – идеальный газ
3.
Идеальный газ(модель)
1. Совокупность большого числа молекул
массой m0, размерами молекул
пренебрегают (принимают молекулы
за материальные точки).
2. Молекулы находятся на больших
расстояниях друг от друга и движутся
хаотически.
3. Молекулы взаимодействуют по
законам упругих столкновений ,
силами притяжения между
молекулами пренебрегают.
4. Скорости молекул разнообразны, но
при определенной температуре
средняя скорость молекул остается
постоянной.
Реальный газ
1. Молекулы реального газа не
являются точечными
образованиями, диаметры
молекул лишь в десятки раз
меньше расстояний между
молекулами.
2. Молекулы не взаимодействуют по законам
упругих столкновений.
4.
Основное уравнение МКТидеального газа
5.
m0 масса атомаp
давление газа
средняя квадратичная
скорость движения
молекул
6.
• Давление газа обусловлено ударами молекул остенки сосуда, поэтому с помощью МКТ его
можно выразить через концентрацию молекул,
• средние скорости молекул и массу одной
молекулы. Это было сделано немецким
физиком Рудольфом Клаузисом в середине 19
века.
1
2
p m0 n
3
7.
Связь давления со среднейкинетической энергией
8.
m0 VЕ
2
2
Средняя кинетическая
энергия поступательного
движения молекулы
m
V
2
2
1
0
2
nE
n
P m0 nV
3
2
2
3
2
9.
Связь давления с плотностью газа.m0 n
Масса молекулы
Плотность газа
2
1
P m0 n V
3
Концентрация
молекул
10.
Задача№1• Каково давление азота, если средняя квадратичная
скорость его молекул 500 м/с, а его плотность
3
1,35 кг / м ?
11.
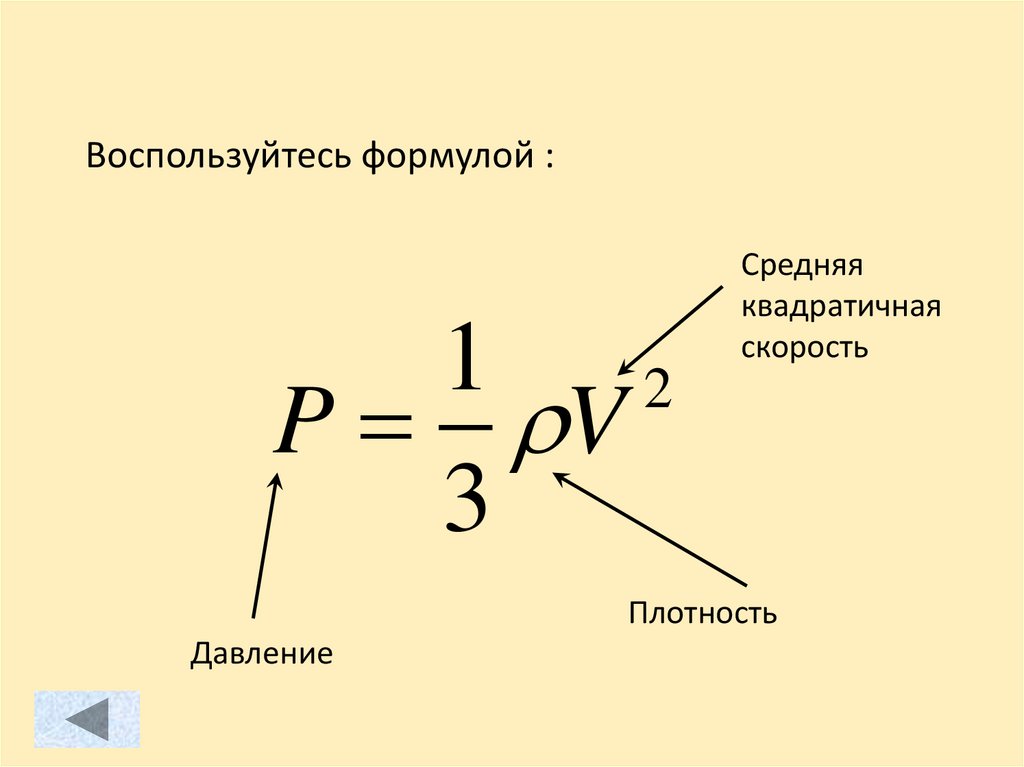
Воспользуйтесь формулой :1
2
P V
3
Средняя
квадратичная
скорость
Плотность
Давление
12.
Дано :V 500 м / с
1,35кг / м
Найти :
Р ?
Решение:
3
1
2
P V
3
1
2
P 1,35 500
3
112500 Па
112,5кПа
Ответ: 112,5кПа
13.
Задача №2• Какова средняя квадратичная скорость
движения молекул газа, если имея массу 6 кг,
он занимает объем 5 кПа при давлении
200кПа?
14.
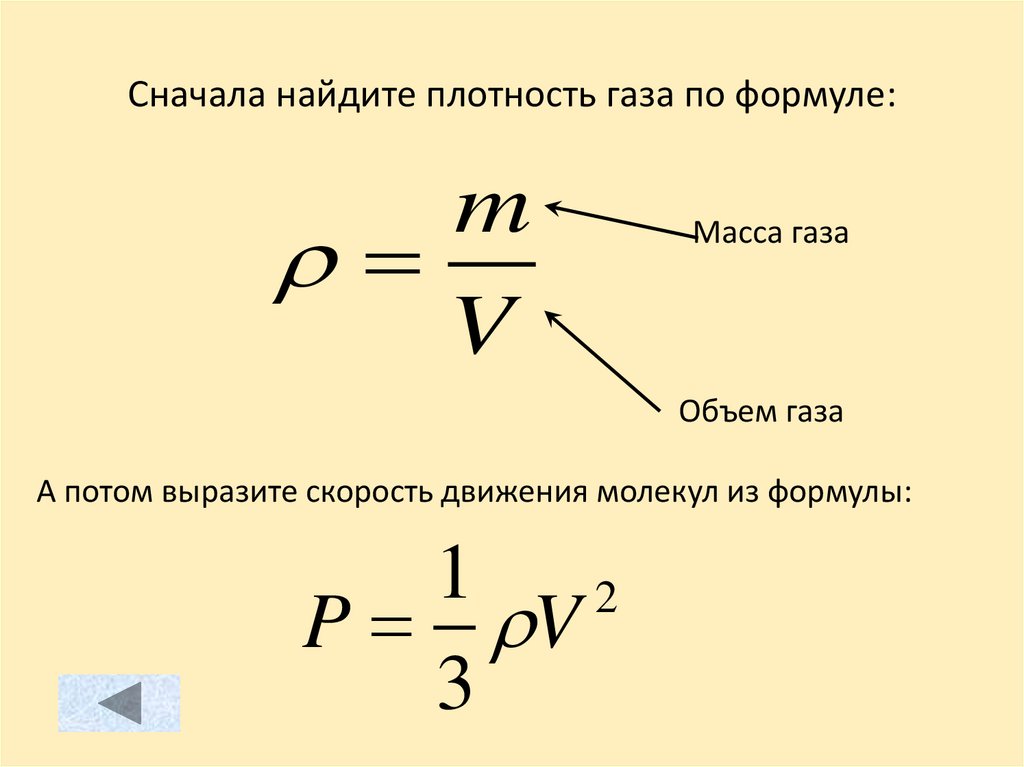
Сначала найдите плотность газа по формуле:m
V
Масса газа
Объем газа
А потом выразите скорость движения молекул из формулы:
1
2
P V
3
15.
Решение:Дано :
m 6кг
V 5м
6
m
5
V
3
1, 2 кг / м
3
P 2 10 Па
Найти :
5
V=?
V=
3P
3 2 10
1, 2
707 м / с
Ответ: 707 м/с
5
16.
ТЕМПЕРАТУРА. АБСОЛЮТНАЯТЕМПЕРАТУРА – МЕРА СРЕДНЕЙ
ЭНЕРГИИ МОЛЕКУЛ.
17.
Определение• Температура — скалярная физическая
величина, характеризующая состояние
теплового равновесия (среднюю кинетическую
энергию частиц макроскопической системы).
• Тела находящиеся в тепловом равновесии
имеют одинаковую температуру.
18.
Измерение температурыДля измерения термодинамической температуры выбирается
некоторый термодинамический параметр
термометрического вещества.
Изменение этого параметра однозначно связывается с
изменением температуры. Классическим примером
термодинамического термометра
может служить газовый термометр,
в котором температуру определяют
методом измерения давления газа в
баллоне постоянного объема.
19.
Единицы и шкала измерениятемпературы
Из того, что температура — это
кинетическая энергия молекул,
ясно, что наиболее естественно
измерять её в энергетических
единицах
(то есть системе СИ в джоулях).
Однако измерение
температуры началось задолго
до создания молекулярнокинетической теории, поэтому
практические шкалы измеряют
температуру в единицах —
градусах
20.
Шкала температур КельвинаПонятие абсолютной
температуры было введено У.
Томсоном (Кельвином), в связи
с чем шкалу абсолютной
температуры называют
шкалой Кельвина или
термодинамической
температурной шкалой.
Единица абсолютной
температуры — кельвин (К).
21.
Абсолютная шкалатемпературы называется
так, потому что мера
основного состояния
нижнего предела
температуры —
абсолютный ноль, то
есть наиболее низкая
возможная температура,
при которой в принципе
невозможно извлечь из
вещества тепловую
энергию.
Абсолютный ноль
определён как 0 K, что равно
−273.15 °C (точно).
Шкала температур
Кельвина — это шкала, в
которой начало отсчёта
ведётся от абсолютного
нуля.
22.
Шкала Цельсия• В технике, медицине,
метеорологии и в быту
используется шкала Цельсия, в
которой температура тройной
точки воды равна 0,008 °C, и,
следовательно, точка замерзания
воды при давлении в 1 атм равна
0 °C..
• Шкала Цельсия практически
очень удобна, поскольку вода
очень распространена на нашей
планете и на ней основана наша
жизнь. Ноль Цельсия — особая
точка для метеорологии,
поскольку связана с
замерзанием атмосферной воды.
Шкала предложена Андерсом
Цельсием в 1742 г.
23.
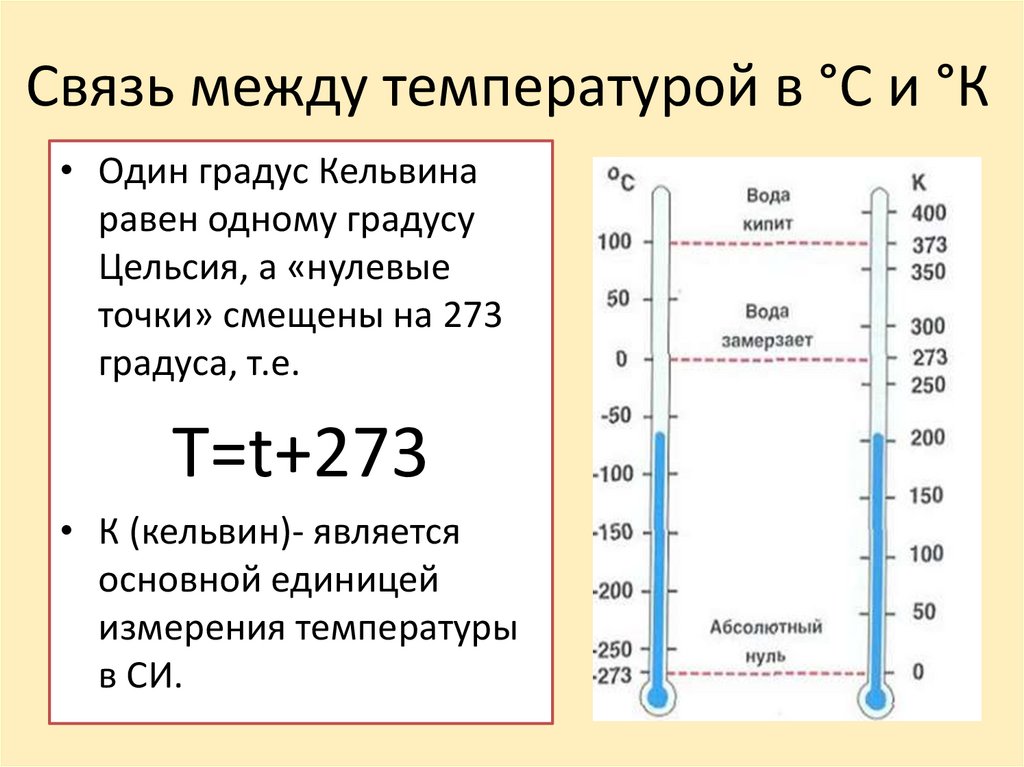
Связь между температурой в °С и °К• Один градус Кельвина
равен одному градусу
Цельсия, а «нулевые
точки» смещены на 273
градуса, т.е.
T=t+273
• К (кельвин)- является
основной единицей
измерения температуры
в СИ.
24.
Домашнее задание( ответить на вопросы)• 1. Как связано понятие температуры с понятием
теплового равновесия?
• 2.Как определяют шкалу температур по Цельсию?
• 3.Что такое абсолютная температура?
• 4.Какое соотношение связывает абсолютную
температуру с температурой по шкале Цельсия?
• 5.Что такое идеальный газ? Перечислить его свойства.
• 6. Какой вид имеет основное уравнение молекулярнокинетической теории идеального газа?
• 7. Как определяют шкалу температур по Фаренгейту и
где она применяется? Формула перевода «градусов»
Фаренгейта в «градусы» Цельсия.







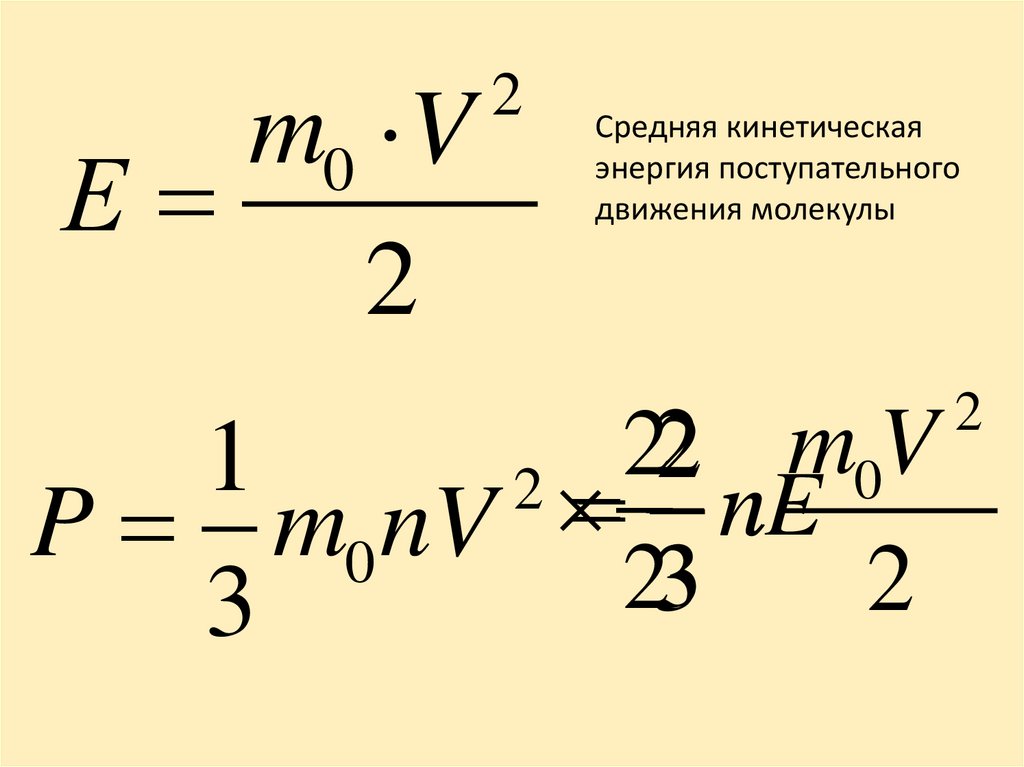













 Физика
Физика








