Похожие презентации:
Получение и химические свойства кислотных, основных и амфотерных оксидов
1.
2.
ОТВЕТЬТЕ НА ВОПРОСЫ:• Какие вещества называются простыми?
Приведите примеры.
• Какие вещества называются сложными?
Приведите примеры.
• Что такое оксид.
• Какие оксиды называются основными?
• Какие оксиды называются амфотерными?
• Какие оксиды называются кислотными?
3.
О КАКОМ ОКСИДЕ ИДЁТ РЕЧЬ?В земной коре находятся глина - оксид…..
Драгоценный камень рубин – оксид…
Песок – оксид….
Этот оксид содержится в красном железнякеВодная оболочка Земли, это –
Газ необходимый для фотосинтеза, газ образующийся в
процессе дыхания это –
В результате хозяйственной деятельности человека
образуются вещества, загрязняющие атмосферу:
угарный газ – оксид….
сернистый газ – оксид….
4.
ОксидыКислоты
Основания
Соли
5.
Бинарные соединения,состоящие из двух
элементов, одним из
которых является
кислород
6.
СолеобразующиеНесолеобразующие
Это оксиды, которые
взаимодействуют с
кислотами или со щелочами
с образованием солей и воды:
N2O5, CO2, CaO, Na2O
Это оксиды, которые не
взаимодействуют ни с
кислотами, ни с основаниями и
не образуют солей. Оксиды
образованы атомами
неметаллов:
CO, NO, N2O, SiO2
7.
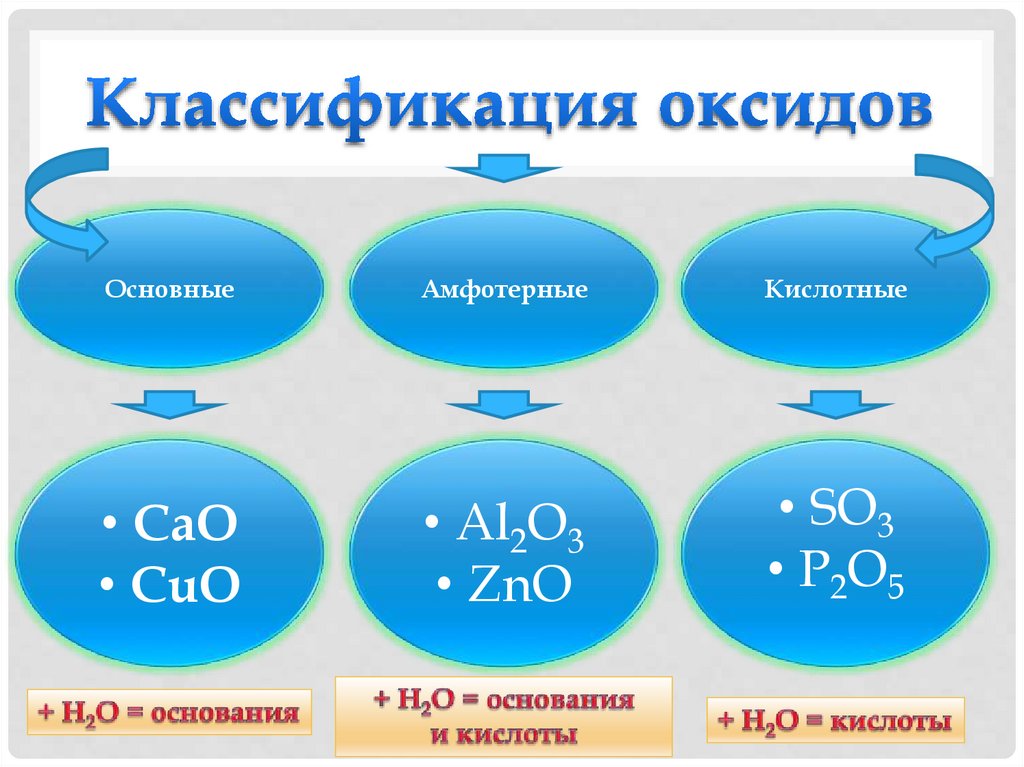
ОсновныеАмфотерные
Кислотные
• CaO
• CuO
• Al2O3
• ZnO
• SO3
• P2O5
8.
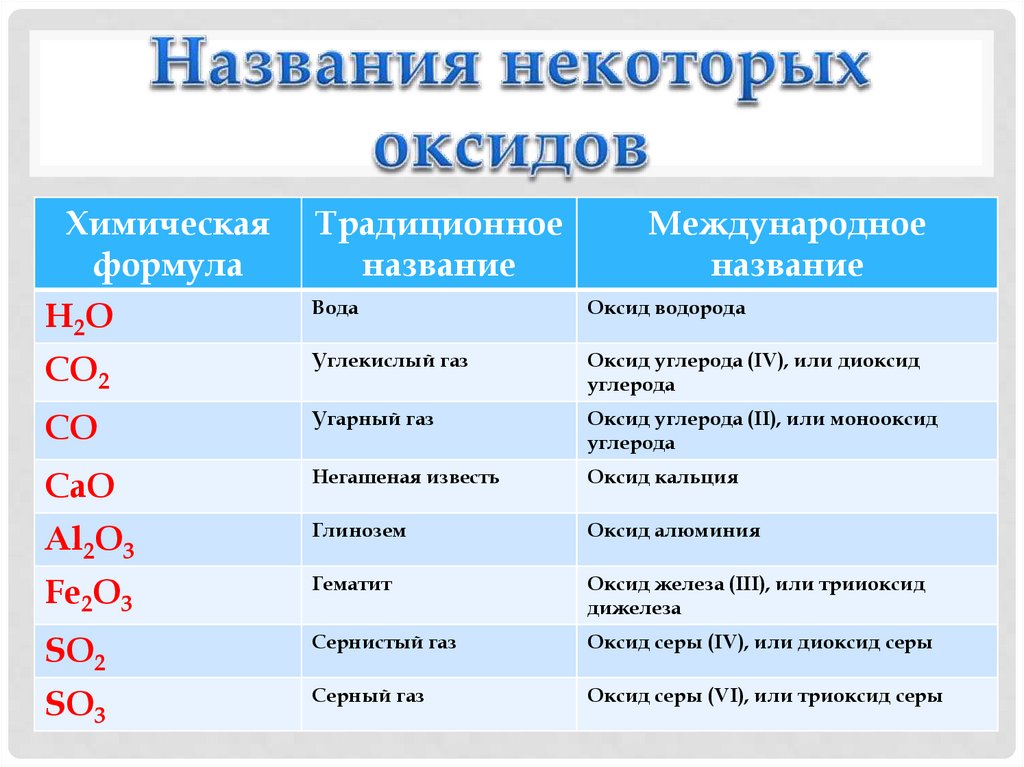
Химическаяформула
Традиционное
название
Международное
название
Н2О
Вода
Оксид водорода
CO2
Углекислый газ
Оксид углерода (IV), или диоксид
углерода
CO
Угарный газ
Оксид углерода (II), или монооксид
углерода
CaO
Негашеная известь
Оксид кальция
Al2O3
Глинозем
Оксид алюминия
Fe2O3
Гематит
Оксид железа (III), или трииоксид
дижелеза
SO2
Сернистый газ
Оксид серы (IV), или диоксид серы
SO3
Серный газ
Оксид серы (VI), или триоксид серы
9.
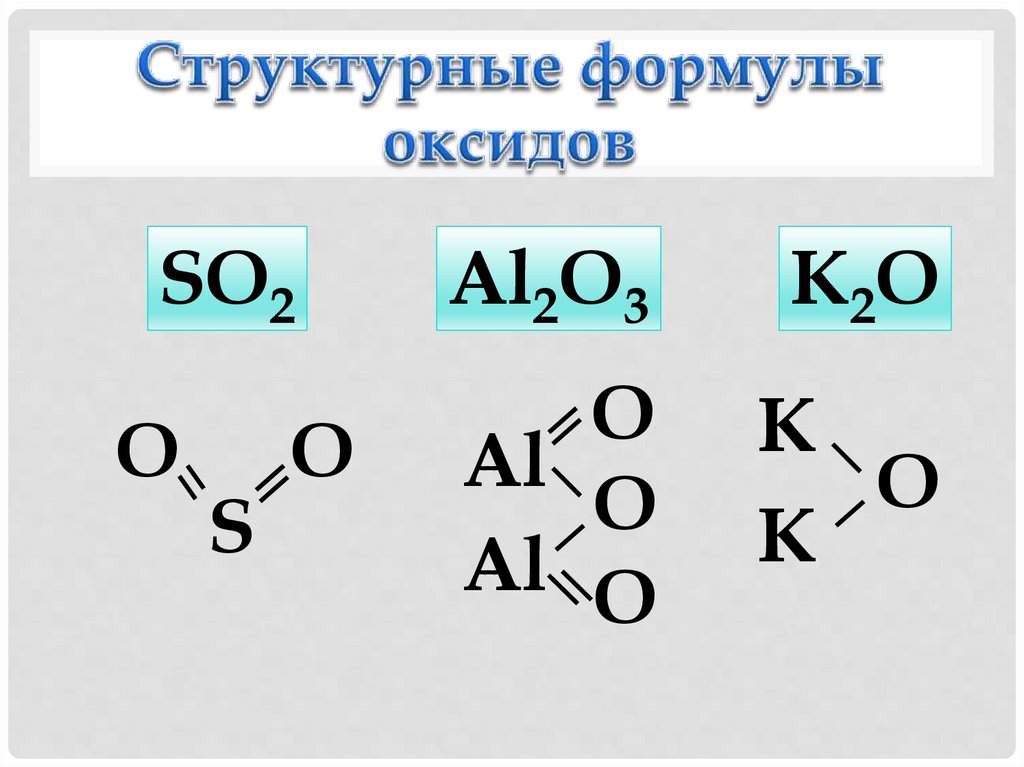
SO2Al2O3
К2O
О
О
Al
О
Al О
К
О
К
S
О
10.
С + O2 = CO22 Cu + O2 =2 CuO
2 Ca + O2 =2 CaO
11.
Получение оксидовCH4 +2 O2 = CO2 +2 H2O
Метан
12.
Получение оксидов4FeO + O2 =2 Fe2O3
2 CO + O2 =2 CO2
13.
Получение оксидовMg(OH)2 = MgO + H2O
2Fe(OH)3 = Fe2O3 +3 H2O
14.
Получение оксидовCaCO3 = CaO + CO2
CaSO4 = CaO + SO3
15.
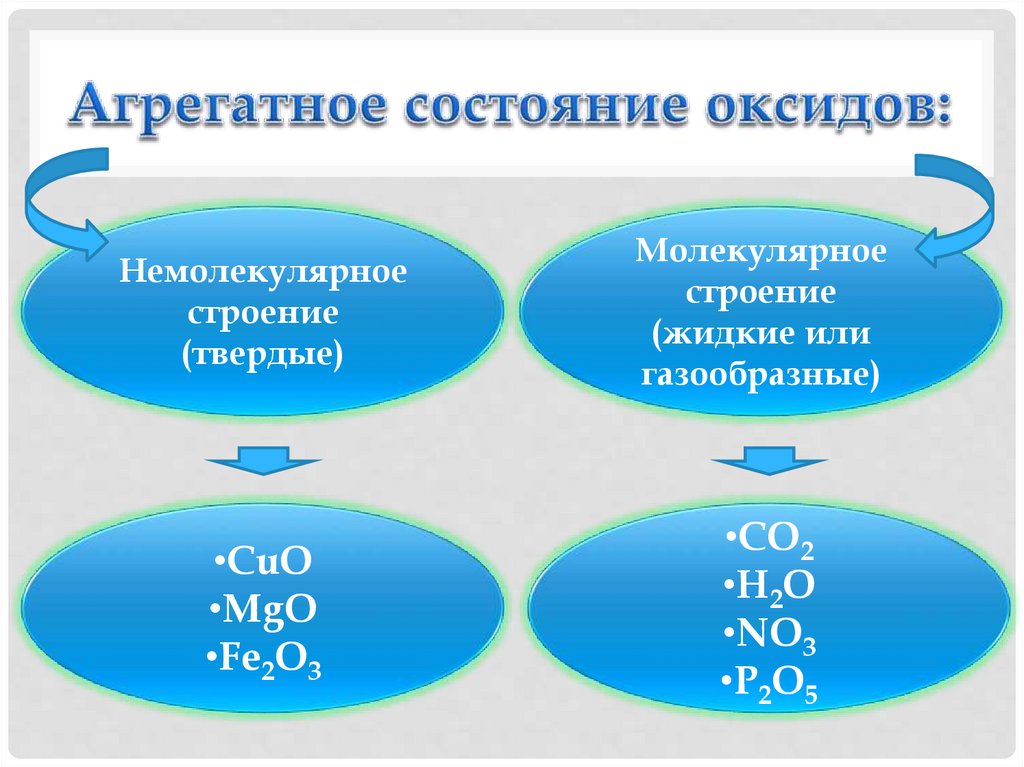
Немолекулярноестроение
(твердые)
Молекулярное
строение
(жидкие или
газообразные)
•CuO
•MgO
•Fe2O3
•CO2
•H2O
•NO3
•P2O5
16.
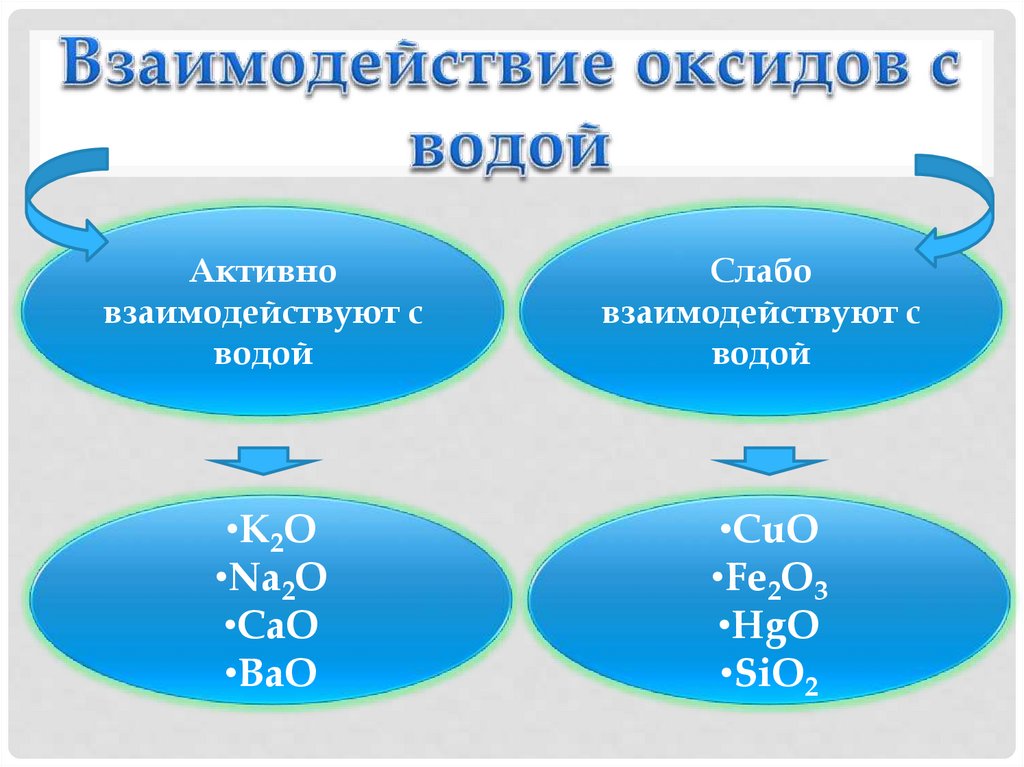
Активновзаимодействуют с
водой
Слабо
взаимодействуют с
водой
•K2O
•Na2O
•CaO
•BaO
•CuO
•Fe2O3
•HgO
•SiO2
17.
Na2O + H2O =2 NaOHCaO + H2O = Ca(OH)2
18.
MgO + H2SO4 = MgSO4+ H2OBaO +2HCL = BaCL2 + H2O
19.
CaO + CO2 = CaCO3BaO + SiO2 = BaSiO3
20.
SO3 + H2O = H2SO4P2O5 +3 H2O =2H3PO4
21.
2 NaOH + SO2 = Na2SO3 + H2OCa(OH)2 + CO2 = CaCO3 + H2O
22.
SiO2 + CaO = CaSiO323.
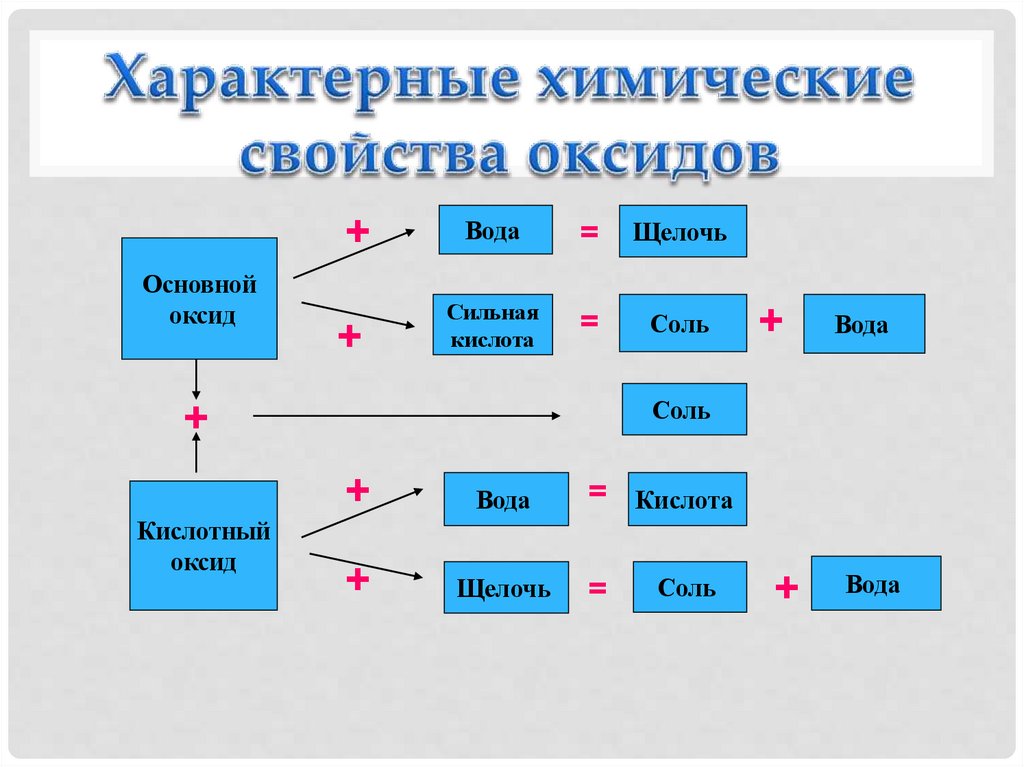
Основнойоксид
+
Вода
=
Щелочь
+
Сильная
кислота
=
Соль
+
Кислотный
оксид
+
Вода
+
Вода
Соль
+
Вода
=
Кислота
+
Щелочь
=
Соль
24.
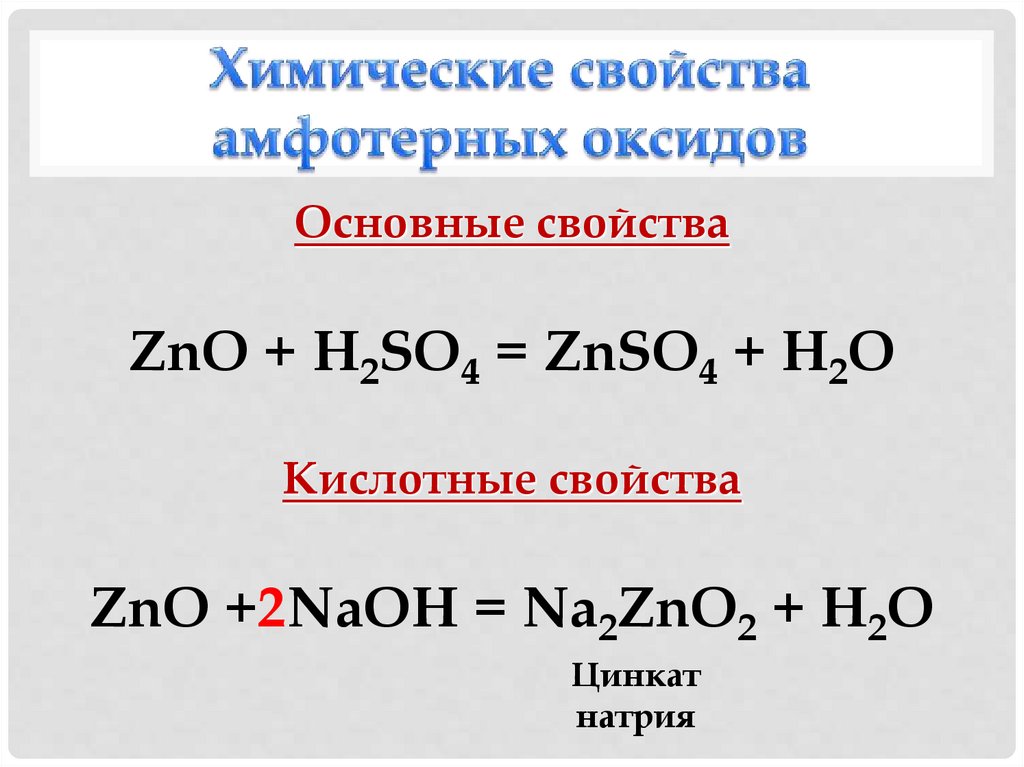
Основные свойстваZnO + H2SO4 = ZnSO4 + H2O
Кислотные свойства
ZnO +2NaOH = Na2ZnO2 + H2O
Цинкат
натрия
25.
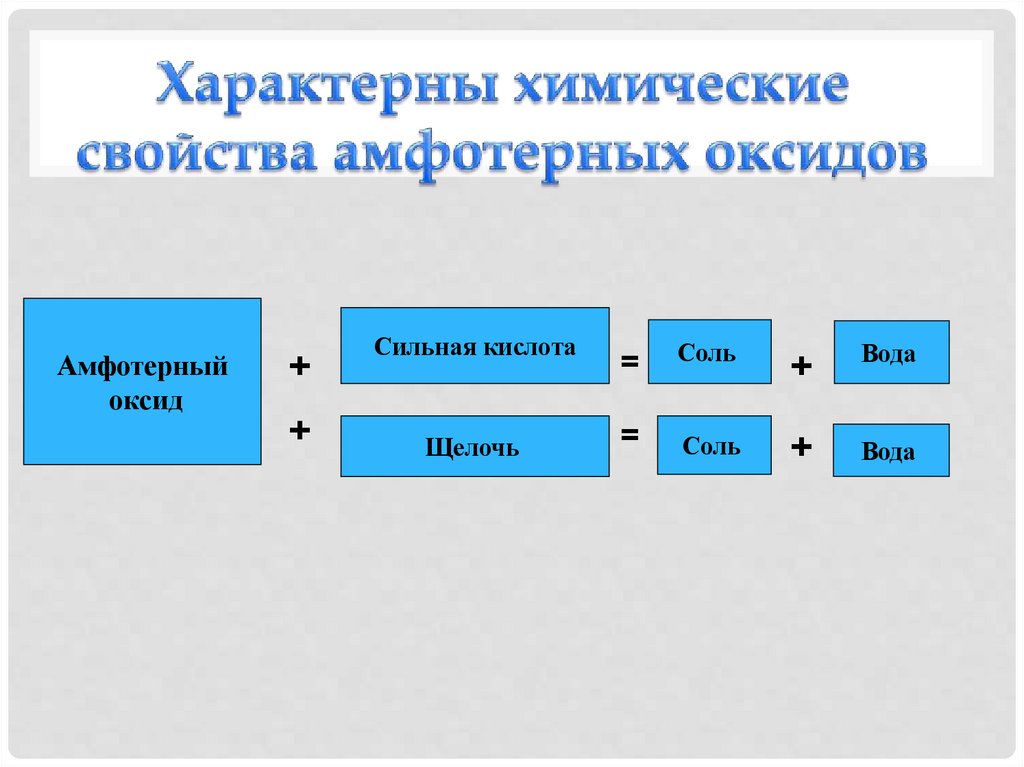
Амфотерныйоксид
+
+
Сильная кислота
Щелочь
=
=
Соль
+
Вода
Соль
+
Вода
26.
ВЫПОЛНИТЕ УПРАЖНЕНИЕ:№1.Составьте формулы оксидов элементов:
Магния, калия, алюминия, фосфора(v), хлора(VII),железа
( III), углерода (IV),серы ( VI). Выпишите в два
столбика: оксиды металлов и неметаллов.
№2.С каким из веществ:KOH, N2O5 , H2SO4 , H2O, HCL
реагирует CuO. Запишите уравнение реакции.
№3. Напишите уравнения реакций получения оксидов
кальция, алюминия, углерода (IV), серы(IV) ,
фосфора (V).
27.
Выполните задания:1.Распределите оксиды на две группы: основные,
кислотные
SO2, CaO, CuO, CO2, Al2O3, N2O5, FeO, Fe2O3
2. Запишите уравнения реакций взаимодействия
между:
•оксидом углерода (IV) и гидроксидом калия,
водой, оксидом бария;
•оксидом лития и водой, серной кислотой,
оксидом фосфора (V).
28.
29.
•§ 44, 45 прочитать;•Стр. 116 № 5-10




















 Химия
Химия