Похожие презентации:
Основания. Определение. Номенклатура
1. Основания
Учитель: Анисимова Е.С.Химия 8 класс
2. Определение. Номенклатура.
Основания – это сложные вещества,состоящие из атомов металлов и одной или
нескольких гидроксильных групп.
Mе (OH) n
где n = число групп OH = валентность металла
Например: NaOH, Ca(OH)2, Fe(OH)3
Название: «гидроксид» + «металла»
(валентность металла, если она переменная)
Cu(OH)2 – гидроксид меди (II)
3. Классификация. Физические свойства.
ОснованияРастворимые в воде
(щёлочи)
I А II А группы,
кроме Mg и Ве
LiOH, Ca(OH)2
Физические свойства:
Т, Ц: белый, хорошо
растворимы в воде,
едкие.
Амфотерные
Al(OH)3 Zn(OH)2
Нерасторимые в
воде
Cu(OH)2, Mg(OH)2
4. Дайте названия гидроксидам:
Fe(OH)2Гидроксид лития
Гидроксид железа (II)
Ca(OH)2
Гидроксид кальция
Al(OH)3
Fe(OH)3
Гидроксид алюминия
LiOH
Гидроксид железа (III)
К каким гидроксидам они относятся?
5. Дайте названия гидроксидам:
Fe(OH)2Гидроксид лития
Щ
Гидроксид железа (II)
Ca(OH)2
Гидроксид кальция
LiOH
Н/Р
Al(OH)3
Fe(OH)3
А
Гидроксид алюминия
Гидроксид железа (III)
К каким гидроксидам они относятся?
6. Действие индикаторов индикатор - от латинского «indication» - указатели
Фенолфталеиновыйв щелочах малиновый !
Индикатор
Нейтральная среда
Щелочная среда
Лакмус
фиолетовый
синий
Метиловый оранжевый
оранжевый
жёлтый
Фенолфталеин
бесцветный
малиновый
Помни! Нерастворимые основания не
меняют окраску индикаторов !!!
7.
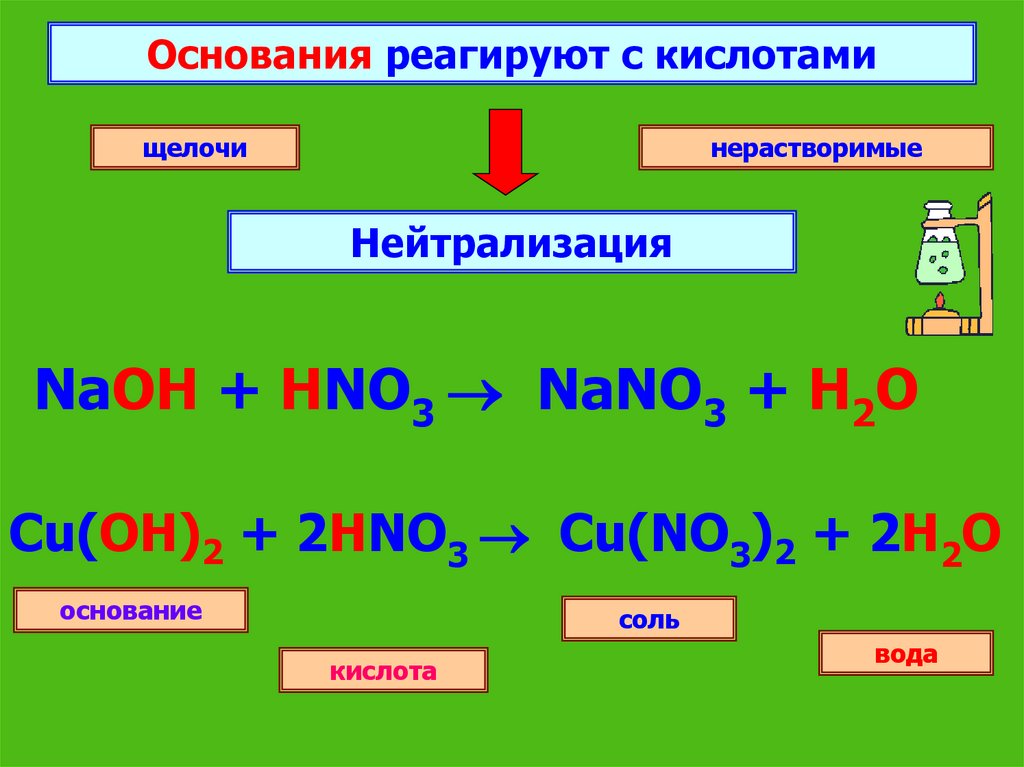
Основания реагируют с кислотамищелочи
нерастворимые
Нейтрализация
NaOH + HNO3 NaNO3 + H2O
Cu(OH)2 + 2HNO3 Cu(NO3)2 + 2H2O
основание
соль
кислота
вода
8.
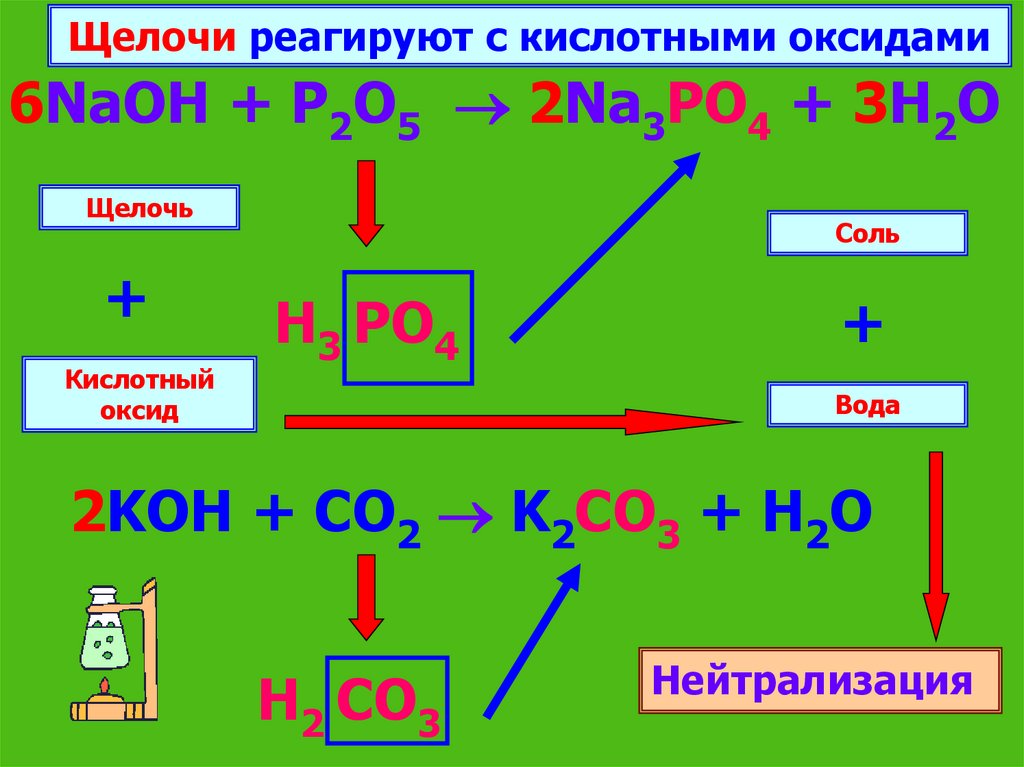
Щелочи реагируют с кислотными оксидами6NaOH + P2O5 2Na3PO4 + 3H2O
Щелочь
+
Кислотный
оксид
Соль
Н3 PO4
+
Вода
2KOH + CO2 K2CO3 + H2O
Н2 CO3
Нейтрализация
9.
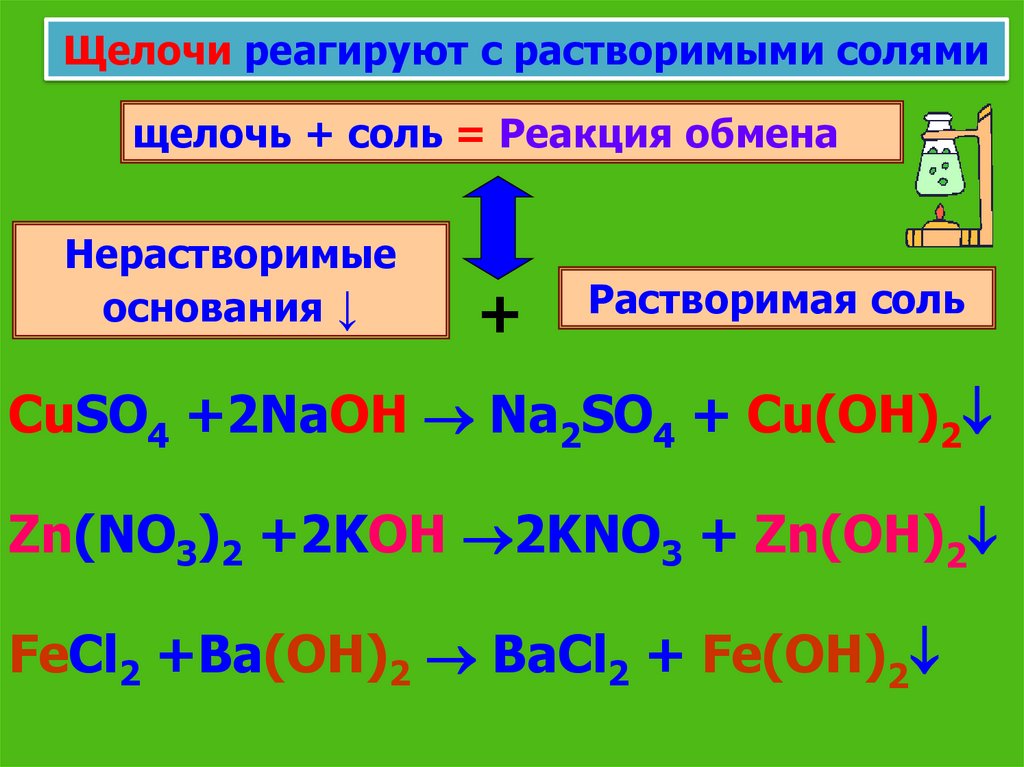
Щелочи реагируют с растворимыми солямищелочь + соль = Реакция обмена
Нерастворимые
основания ↓
+
Растворимая соль
CuSO4 +2NaOH Na2SO4 + Cu(OH)2
Zn(NO3)2 +2KOH 2KNO3 + Zn(OH)2
FeCl2 +Ba(OH)2 BaCl2 + Fe(OH)2
10. Проверьте ваши знания
Закончите молекулярные уравнениявозможных реакций:
KOH + P2O5
Cu(OH)2 + H2SO4
Mg(OH)2 + FeO
KOH + AlCl3
11. Проверьте ваши знания
Закончите молекулярные уравнениявозможных реакций:
6 KOH + P2O5
2K3PO4 + 3H2O
Cu(OH)2 + H2SO4
Mg(OH)2 + FeO
3 KOH + AlCl3
CuSO4 + 2H2O
Реакция не будет протекать, т.к. основной
оксид не может реагировать с основанием
Al(OH)3 + 3KCl
12.
Получение основанийВ лаборатории:
• Щелочей:
1. Взаимодействием активного металла с водой
2К + 2Н2О → 2КОН + Н2↑
2. Взаимодействием основных оксидов с водой
К2О + Н2О → 2КОН
• Нерастворимых оснований:
1. Получают действием щелочей на растворысоли:
CuCl2 + NaOH → Cu(OH)2↓ + 2NaCl
В промышленности:
1. Электролиз солей.









 Химия
Химия








