Похожие презентации:
Периодический закон Д.И. Менделеева
1. ЗАНЯТИЕ №3. Периодический закон Д. И. Менделеева.
2.
3.
Всеэлементы
распределены
по
горизонтальным
рядам,
называемым
периодами (7 периодов), и вертикальным
колонкам, называемым группами (8 групп).
! Таким образом, изменение свойств химических
элементов происходит по мере возрастания
атомной массы не непрерывно в одном и том же
направлении, а имеет периодический характер.
4. Современная формулировка Периодического Закона
Свойства элементов, а также свойстваих соединений находятся в
периодической зависимости от
величины заряда их атомных ядер.
5.
Периоды – это горизонтальные ряды, в которыхэлементы расположены в порядке возрастания их
атомных номеров и последовательного изменения
свойств.
Периодическая система состоит из 7 периодов:
1, 2, 3 – малые или типические;
4, 5 ,6 – большие;
7 – незаконченный
Каждый период всегда начинается щелочным
металлом, заканчивается инертным газом.
6.
Группы - вертикальные ряды, в которыхэлементы обладают сходными химическими
свойствами.
Периодическая система состоит из 8 групп.
Каждая группа делится на главную и
побочную.
Номер группы – максимальная валентность
элемента
7.
Главныеподгруппы–
типические
элементы 1 – 3 периодов и сходные с
ними по свойствам элементы 4 – 7
периодов (s- и р- элементы).
Побочные подгруппы включают только
металлы (d- элементы).
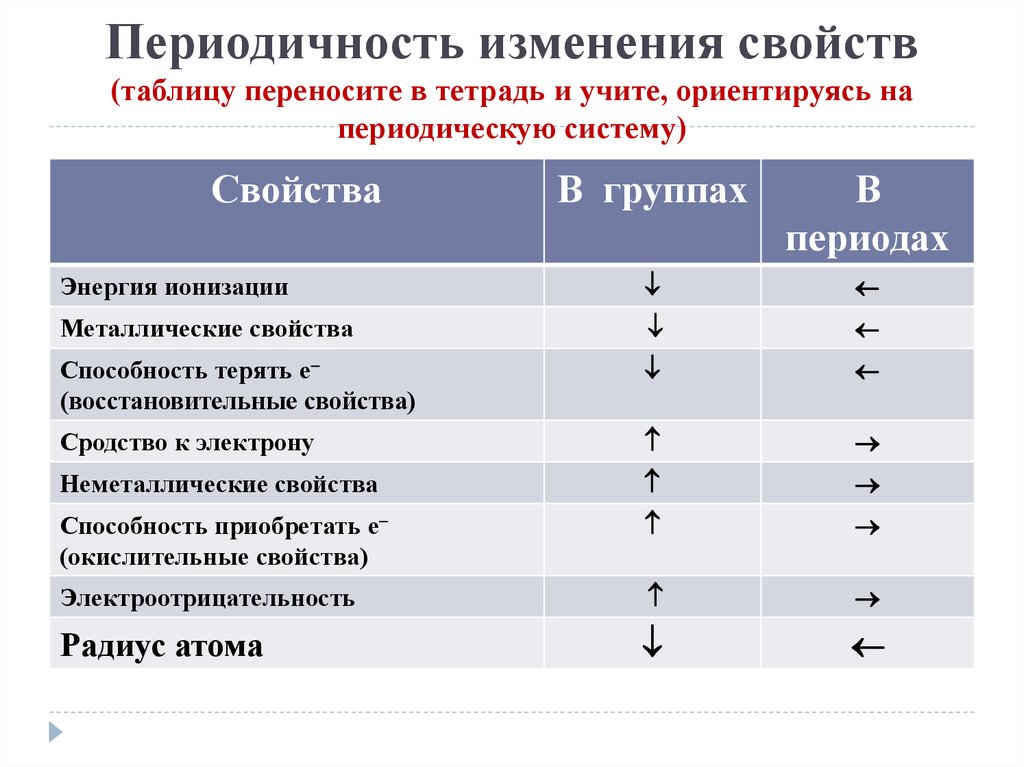
8. Периодичность изменения свойств (таблицу переносите в тетрадь и учите, ориентируясь на периодическую систему)
СвойстваВ группах
В
периодах
Энергия ионизации
Металлические свойства
Способность терять е
(восстановительные свойства)
Сродство к электрону
Неметаллические свойства
Способность приобретать е
(окислительные свойства)
Электроотрицательность
Радиус атома







 Химия
Химия








