Похожие презентации:
Биологическое окисление. Общий путь катаболизма. ОДПВК и ЦТК (лекция № 5)
1.
ПЯТИГОРСКИЙ МЕДИКО-ФАРМАЦЕВТИЧЕСКИЙ ИНСТИТУТ филиал федерального государственного бюджетного образовательного учреждения высшего образования«ВОЛГОГРАДСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ»
Министерства здравоохранения Российской Федерации
Лекция №5
Биологическое окисление. Общий
путь катаболизма. ОДПВК и ЦТК.
Пятигорск, 2020
2. ИСТОРИЯ УЧЕНИЯ О БИОЛОГИЧЕСКОМ ОКИСЛЕНИИ
А.Н. Бах (1898 г) – теория активации кислородаили теория перекисных соединений.
Основные положения:
в окислении обязательно участвует О2,
при его активации разрывается только 1 связь;
О2 передается на субстрат через промежуточные вещества;
участвуют ферменты - оксигеназы.
Схема:
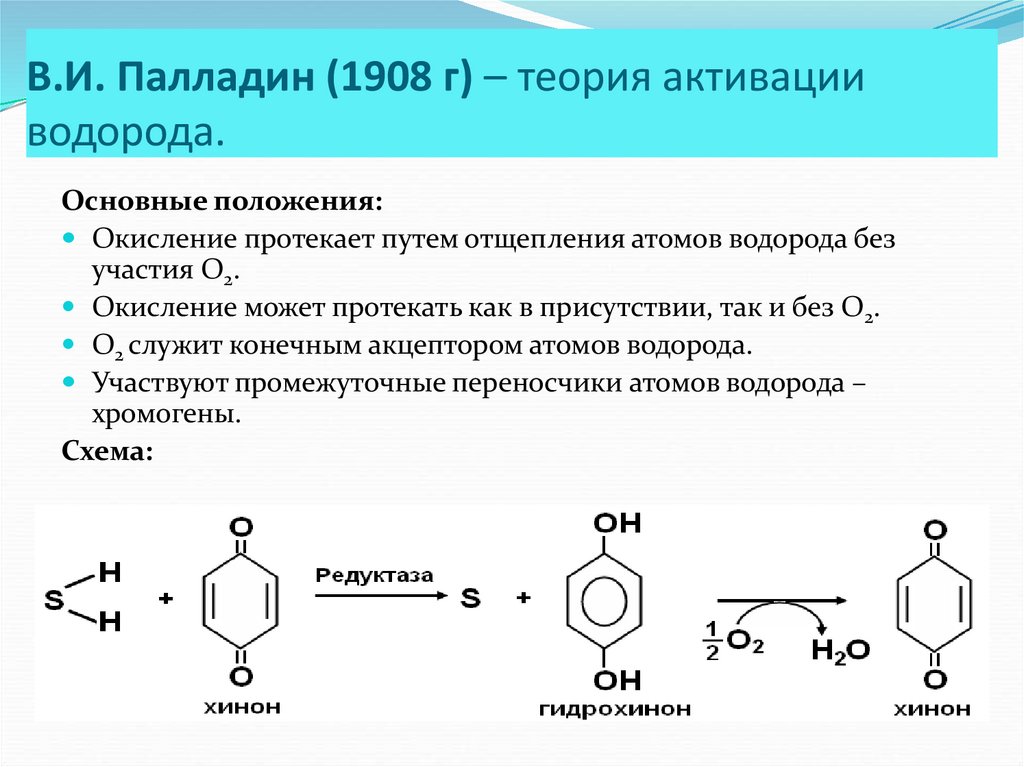
3. В.И. Палладин (1908 г) – теория активации водорода.
Основные положения:Окисление протекает путем отщепления атомов водорода без
участия О2.
Окисление может протекать как в присутствии, так и без О2.
О2 служит конечным акцептором атомов водорода.
Участвуют промежуточные переносчики атомов водорода –
хромогены.
Схема:
4. СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О БИОЛОГИЧЕСКОМ ОКИСЛЕНИИ И ТКАНЕВОМ ДЫХАНИИ.
БИОЛОГИЧЕСКОЕ ОКИСЛЕНИЕ – совокупность всех ОВР в живых системах,протекающие в аэробных и анаэробных условиях.
Метаболизм включает в себя два противоположны процесса катаболизм и
анаболизм
Катаболизм – это прежде всего ферментативное расщепление крупных молекул
(белков, нуклеиновых кислот, жиров, углеводов), осуществляемое
преимущественно за счет реакций гидролиза и окисления
Анаболизм – это ферментативный синтез сравнительно крупных молекул и
надмолекулярных комплексов из простых предшественников, что связано с
потреблением энергии, главным образом в форме энергии фосфатных связей АТФ
Катаболизм и анаболизм связаны общей стадией – лимоннокислым циклом
(циклом трикарбоновых кислот, циклом Кребса), сопряженным с тканевым
дыханием, которая обозначается как центральные, амфиболические, пути
метаболизма.
Тканевое дыхание - комплекс аэробных окислительно-восстановительных
реакций распада субстратов, сопровождающийся передачей протонов и
электронов через дыхательную цепь ферментов на кислород и выделением
энергии
5. Фазы освобождения энергии из питательных веществ
Энергетические потребности клетки удовлетворяются за счёт энергии,освобождаемой при катаболизме питательных веществ (белков, жиров и
углеводов), поступающих с пищей или находящихся в самом организме.
Однако, данные соединения не могут являться непосредственными
донорами протонов и электронов для дыхательной цепи…
Необходимы предварительные этапы, подготавливающие субстраты для
использования по пути синтеза АТФ.
I этап –
превращение полимеров, поступивших с пищей или находящихся
внутри клеток, в мономеры (аминокислоты, жирные кислоты,
моносахариды и др).
II этап –
специфические пути катаболизма всосавшихся мономеров.
III этап –
общий путь катаболизма.
6.
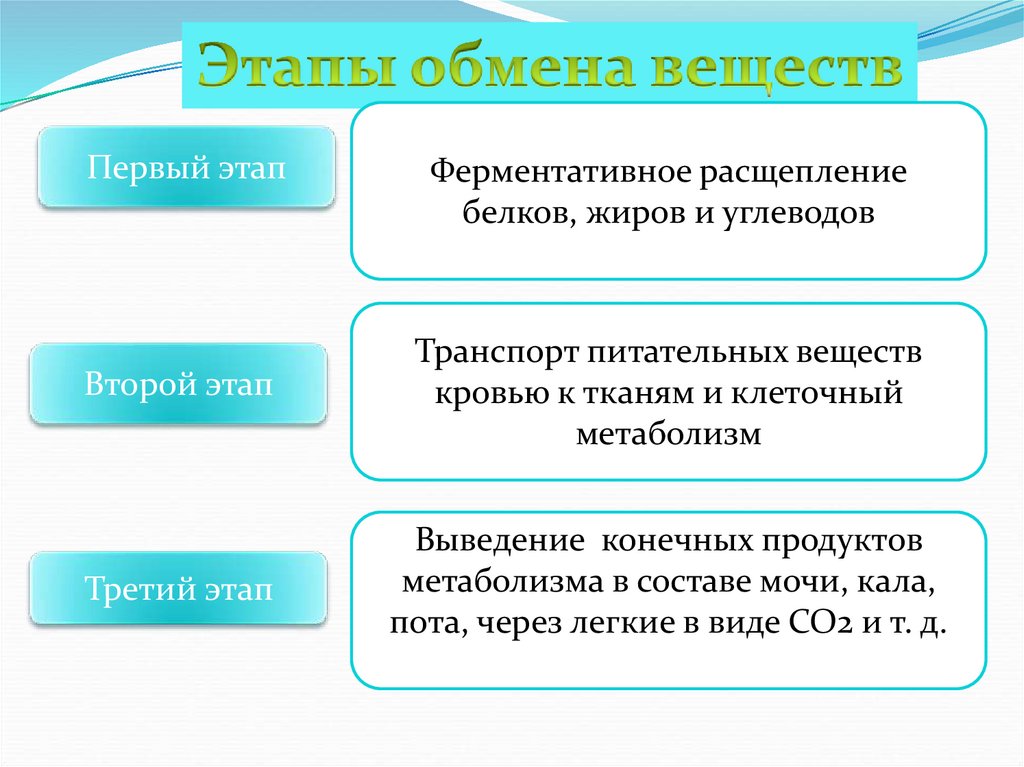
Первый этапФерментативное расщепление
белков, жиров и углеводов
Второй этап
Транспорт питательных веществ
кровью к тканям и клеточный
метаболизм
Третий этап
Выведение конечных продуктов
метаболизма в составе мочи, кала,
пота, через легкие в виде CO2 и т. д.
7.
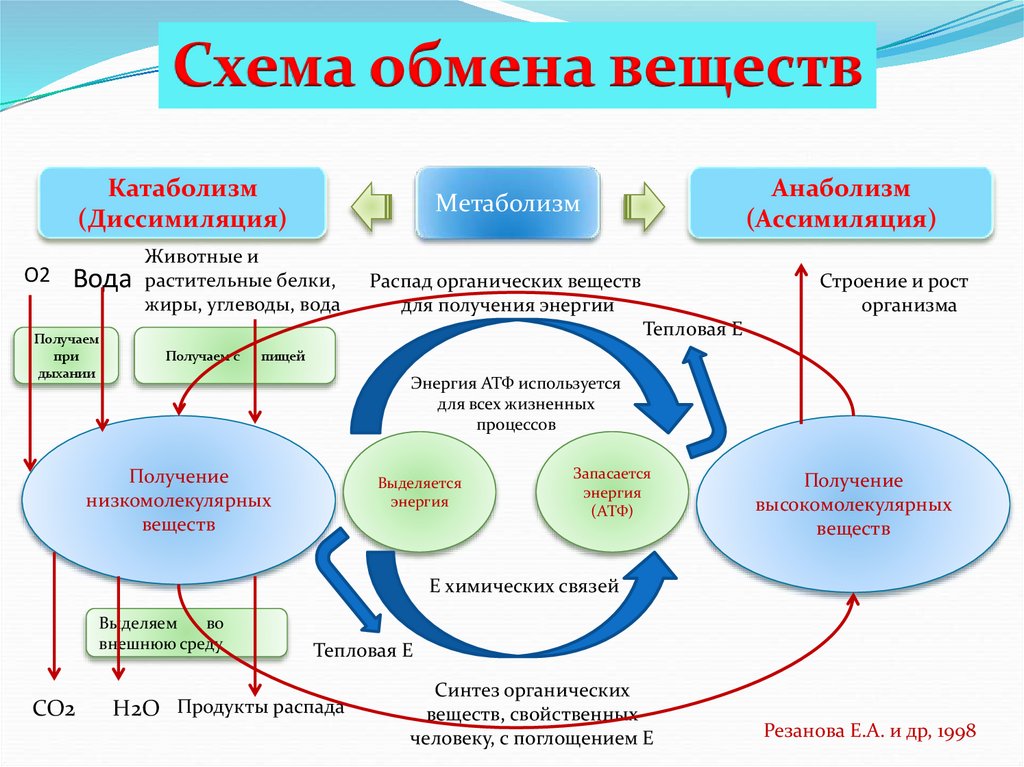
Схема обмена веществКатаболизм
(Диссимиляция)
О2
Животные и
Вода растительные белки,
жиры, углеводы, вода
Получаем
при
дыхании
Анаболизм
(Ассимиляция)
Метаболизм
Распад органических веществ
для получения энергии
Строение и рост
организма
Тепловая Е
Получаем с
пищей
Энергия АТФ используется
для всех жизненных
процессов
Получение
низкомолекулярных
веществ
Выделяется
энергия
Запасается
энергия
(АТФ)
Получение
высокомолекулярных
веществ
Е химических связей
Выделяем
во
внешнюю среду
СО2
Тепловая Е
Н2О Продукты распада
Синтез органических
веществ, свойственных
человеку, с поглощением Е
Резанова Е.А. и др, 1998
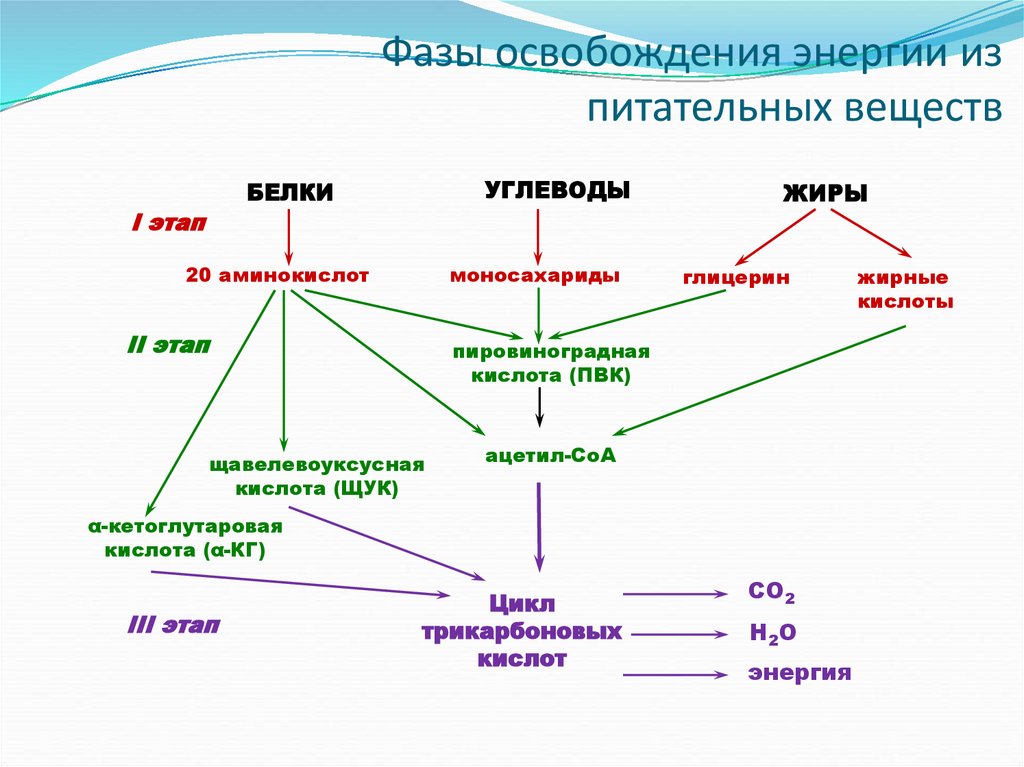
8. Фазы освобождения энергии из питательных веществ
УГЛЕВОДЫБЕЛКИ
I этап
20 аминокислот
моносахариды
II этап
ЖИРЫ
глицерин
пировиноградная
кислота (ПВК)
щавелевоуксусная
кислота (ЩУК)
ацетил-СоА
α-кетоглутаровая
кислота (α-КГ)
III этап
Цикл
трикарбоновых
кислот
СО2
Н2О
энергия
жирные
кислоты
9.
Фазы освобождения энергии изпитательных веществ
БЕЛКИ УГЛЕВОДЫ
ЖИРЫ
пировиноградная
кислота
(ПВК)
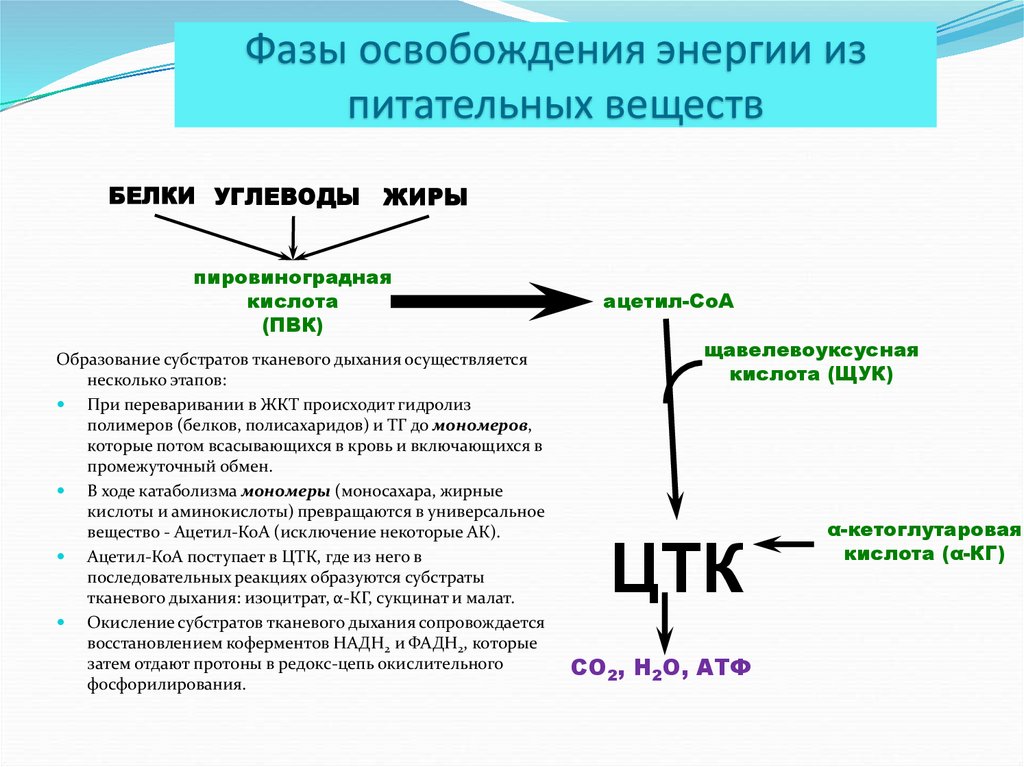
Образование субстратов тканевого дыхания осуществляется
несколько этапов:
При переваривании в ЖКТ происходит гидролиз
полимеров (белков, полисахаридов) и ТГ до мономеров,
которые потом всасывающихся в кровь и включающихся в
промежуточный обмен.
В ходе катаболизма мономеры (моносахара, жирные
кислоты и аминокислоты) превращаются в универсальное
вещество - Ацетил-КоА (исключение некоторые АК).
Ацетил-КоА поступает в ЦТК, где из него в
последовательных реакциях образуются субстраты
тканевого дыхания: изоцитрат, α-КГ, сукцинат и малат.
Окисление субстратов тканевого дыхания сопровождается
восстановлением коферментов НАДН2 и ФАДН2, которые
затем отдают протоны в редокс-цепь окислительного
фосфорилирования.
ацетил-СоА
щавелевоуксусная
кислота (ЩУК)
ЦТК
СО2, Н2О, АТФ
α-кетоглутаровая
кислота (α-КГ)
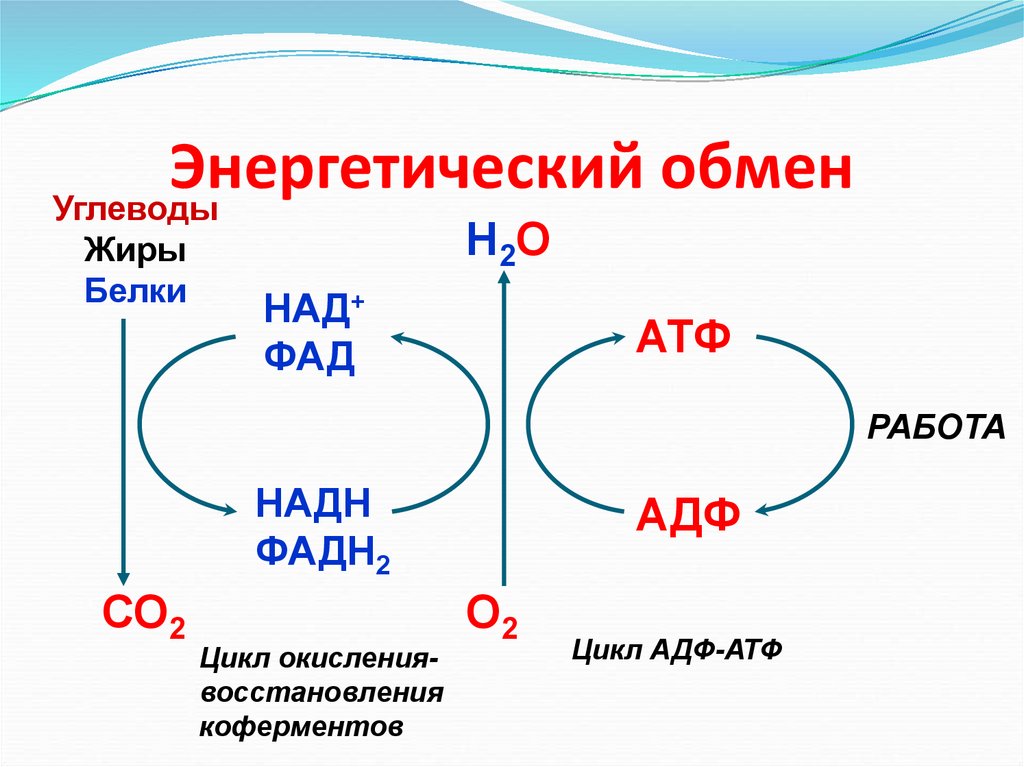
10. Энергетический обмен
УглеводыЖиры
Белки
Н 2О
НАД+
ФАД
АТФ
РАБОТА
НАДН
ФАДН2
СО2
Цикл окислениявосстановления
коферментов
АДФ
О2
Цикл АДФ-АТФ
11.
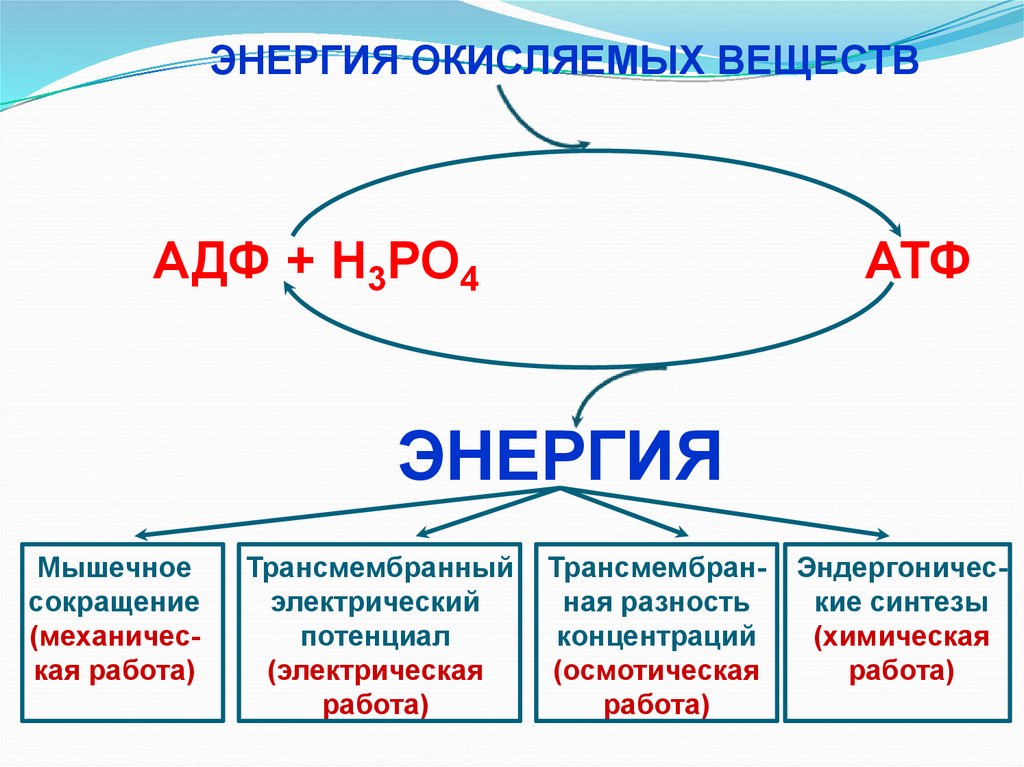
ЭНЕРГИЯ ОКИСЛЯЕМЫХ ВЕЩЕСТВАДФ + Н3РО4
АТФ
ЭНЕРГИЯ
Мышечное
сокращение
(механическая работа)
Трансмембранный
электрический
потенциал
(электрическая
работа)
Трансмембранная разность
концентраций
(осмотическая
работа)
Эндергонические синтезы
(химическая
работа)
12. Макроэргическая связь
Богатая энергией связь (> 5 ккал или 21 кДж/моль);Энергия макроэргической связи превращается в работу, минуя
стадию тепла.
Макроэргические соединения
Производные фосфорной кислоты
OH
O
R
С
O
~P
O
Карбоксилфосфатные
OH
OH
R
С
O
CH2
~P
OH
O
Енолфосфатные
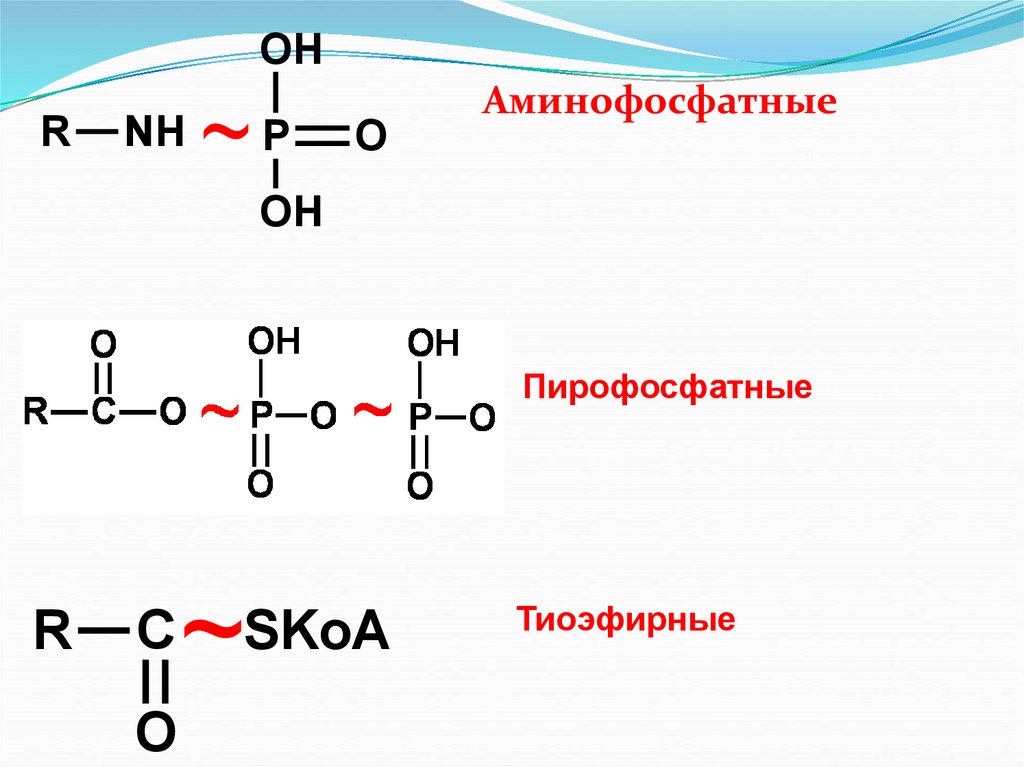
13.
OHR
NH
~P
O
Аминофосфатные
OH
Пирофосфатные
R
С
O
~SKoA
Тиоэфирные
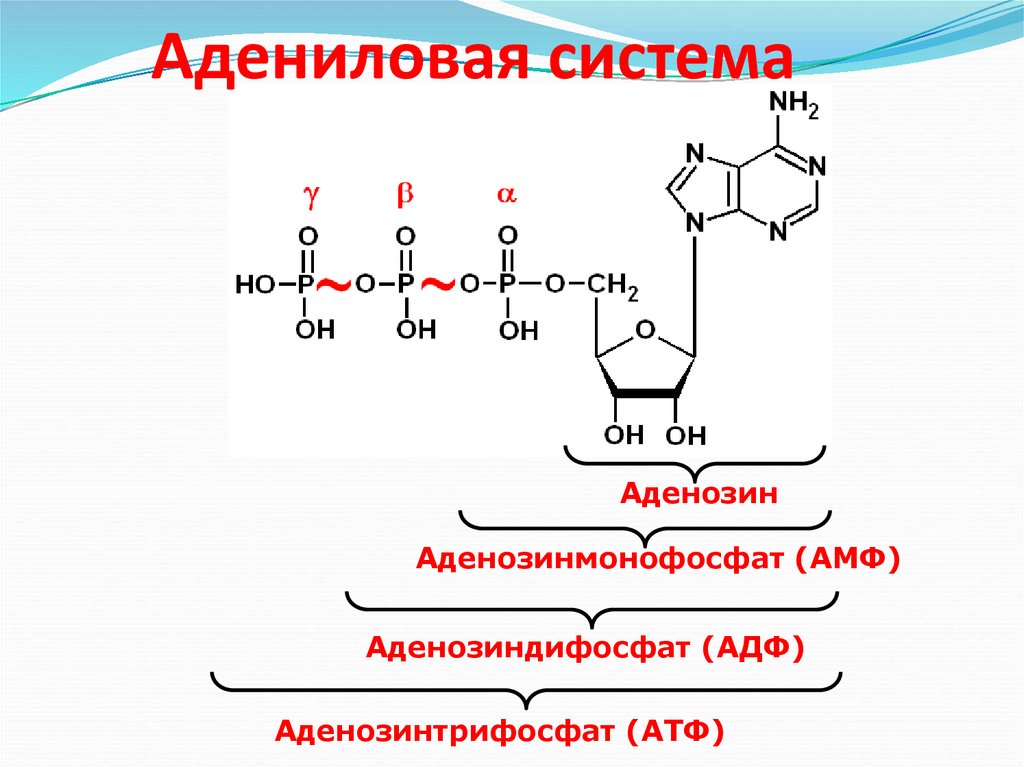
14. Адениловая система
АденозинАденозинмонофосфат (АМФ)
Аденозиндифосфат (АДФ)
Аденозинтрифосфат (АТФ)
15. Пути использования кислорода в клетке
В настоящее время выделено 4 основные пути использования кислорода в организме:Оксидазный путь - окислительное фосфорилирование. Протекает в митохондриях,
является основным источником АТФ в аэробных тканях. Потребляет 90% кислорода.
Монооксигеназный путь. Обеспечивает включение 1 атома кислорода в молекулу
субстрата. Используется для синтеза новых веществ (стероидные гормоны),
обезвреживания ксенобиотиков и токсических продуктов обмена в митохондриях и ЭПР.
Диоксигеназный путь. Обеспечивает включение молекулы кислорода в молекулу
субстрата. Используется для деградации АК и синтеза новых веществ.
Пероксидазный и радикальный пути. Кислород участвует в образовании перекисей и
активных радикалов, которые необходимы в пероксисомах для внутриклеточного
пищеварения, разрушения макрофагами бактерий, вирусов, регуляции метаболизма и т.д.
Перекиси и активные кислородные радикалы оказывают также повреждающее
воздействие на структуры клеток и тканей, активируя ПОЛ. Разрушение перекисей и
инактивация свободных радикалов осуществляется с помощью ферментативной и
неферментативной антиокидантной системы.
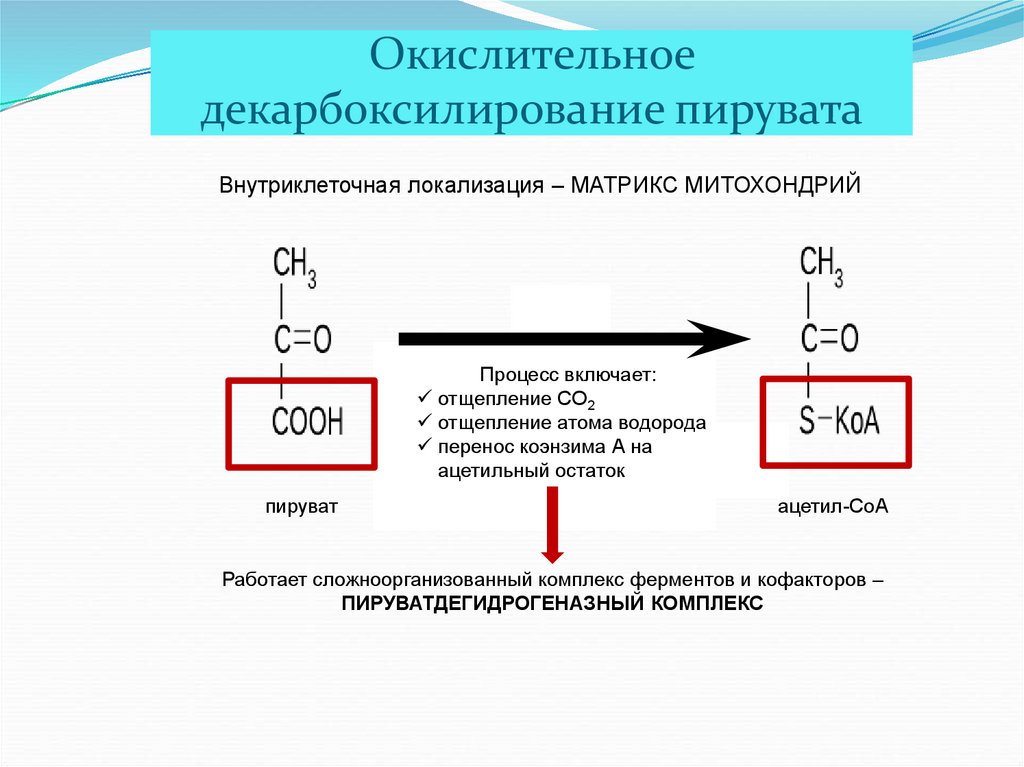
16. Окислительное декарбоксилирование пирувата
Внутриклеточная локализация – МАТРИКС МИТОХОНДРИЙПроцесс включает:
отщепление CO2
отщепление атома водорода
перенос коэнзима А на
ацетильный остаток
пируват
ацетил-CoA
Работает сложноорганизованный комплекс ферментов и кофакторов –
ПИРУВАТДЕГИДРОГЕНАЗНЫЙ КОМПЛЕКС
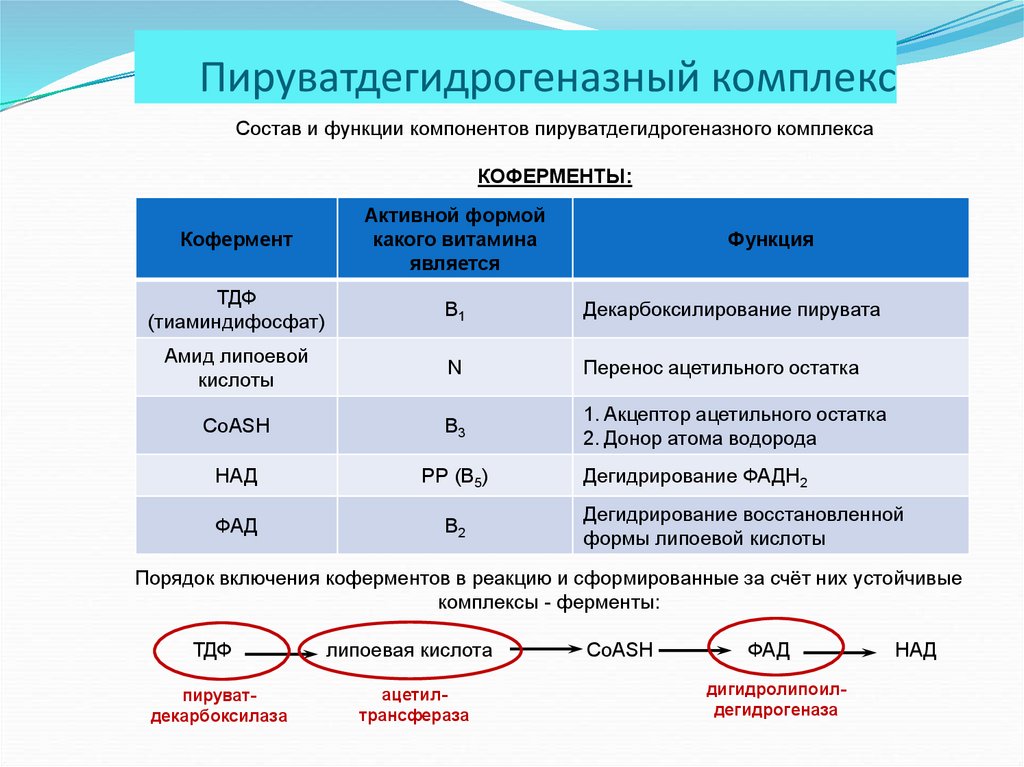
17. Пируватдегидрогеназный комплекс
Состав и функции компонентов пируватдегидрогеназного комплексаКОФЕРМЕНТЫ:
Кофермент
Активной формой
какого витамина
является
ТДФ
(тиаминдифосфат)
В1
Декарбоксилирование пирувата
Амид липоевой
кислоты
N
Перенос ацетильного остатка
CoASH
В3
1. Акцептор ацетильного остатка
2. Донор атома водорода
НАД
РР (В5)
ФАД
В2
Функция
Дегидрирование ФАДН2
Дегидрирование восстановленной
формы липоевой кислоты
Порядок включения коферментов в реакцию и сформированные за счёт них устойчивые
комплексы - ферменты:
ТДФ
липоевая кислота
пируватдекарбоксилаза
ацетилтрансфераза
CoASH
ФАД
дигидролипоилдегидрогеназа
НАД
18. Пируватдегидрогеназный комплекс
12 димерных молекул пируватдекарбоксилазы6 димерных молекул дигидролипоилдегидрогеназы
24 молекулы липоатацетилтрансферазы
Пируватдегидрогеназный комплекс – крупная молекула с молекулярной массой
7-10 млн.
Центральное положение в комплексе занимают полипептидные цепи
субъединиц ацетилтрансферазы, вокруг которых располагаются молекулы
дигидролипоилдегидрогеназы и пируватдегидрогеназы.
Отдельные ферменты соединены друг с другом таким образом, что
серусодержащая часть липоевой кислоты, связанная с ацетилтрансферазой
длинной и гибкой углеводородной цепью, может забирать и переносить
промежуточные продукты реакций последовательно к активным центрам каждого из
трех ферментов.
Поэтому весь комплекс функционирует по принципу конвейера, в котором
образующиеся продукты передаются от одной машины к другой.
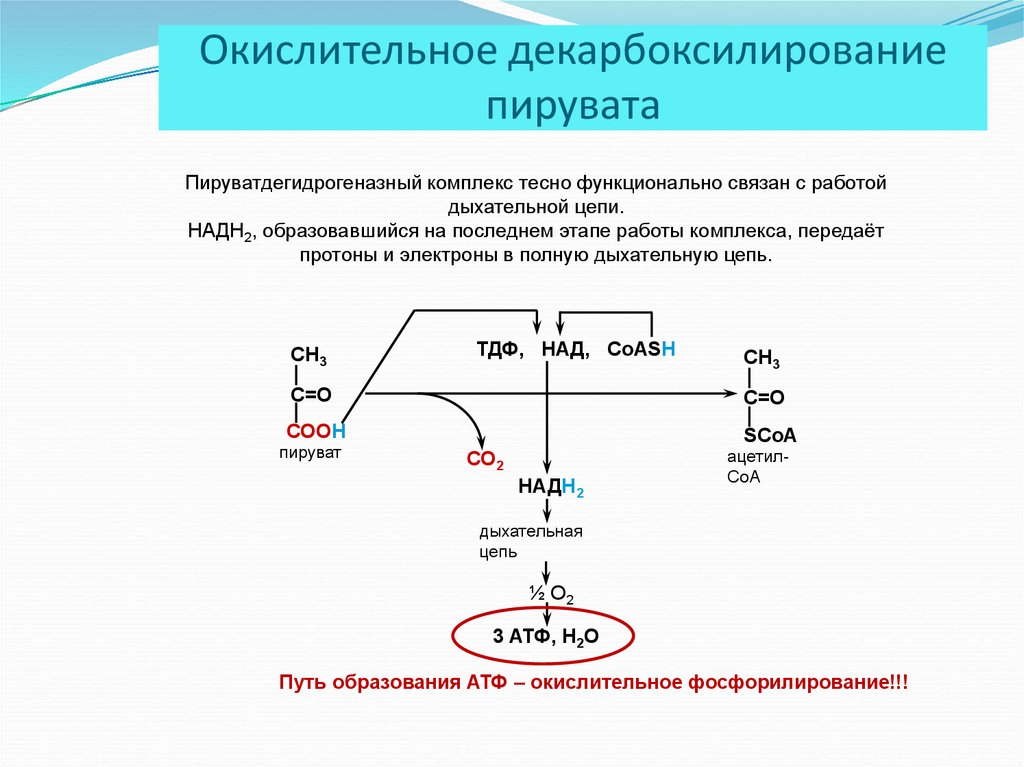
19. Окислительное декарбоксилирование пирувата
Пируватдегидрогеназный комплекс тесно функционально связан с работойдыхательной цепи.
НАДН2, образовавшийся на последнем этапе работы комплекса, передаёт
протоны и электроны в полную дыхательную цепь.
СН3
ТДФ, НАД, CoASH
СН3
С=О
С=О
СООН
SCoA
пируват
СО2
НАДН2
ацетилCoA
дыхательная
цепь
½ О2
3 АТФ, Н2О
Путь образования АТФ – окислительное фосфорилирование!!!
20. Окислительное декарбоксилирование пирувата
Регуляция активности пируватдегидрогеназного комплексаАктивираторы ПВДГК:
высокое содержание пирувата,
инсулин,
АДФ,
НАД,
CoASH
Ингибиторы ПВДГК:
ацетилСоА,
АТФ,
НАДН2
Необходимые условия
для протекания пируватдегидрогеназной реакции:
наличие кислорода!!!!,
витаминов РР, В1, В2, В3, липоевой кислоты и их активных форм,
наличие ионов меди и железа.
Образовавшийся ацетил-СоА
вступает в цикл трикарбоновых кислот
21. Цикл трикарбоновых кислот (цикл Кребса)
Цикл трикарбоновых кислот (ЦТК)был впервые описан Гансом Кребсом
в 1937 году.
КРЕБС (Krebs), Ханс
25 августа 1900 г. – 22 ноября 1981 г.
Нобелевская премия по физиологии и медицине, 1953 г.
(совместно с Фрицем Липманом)
ЦТК является процессом окисления АцетилКоА - универсального продукта катаболизма
углеводов, жиров и белков. ЦТК протекает в митохондриях с участием 8 ферментов,
которые локализованы в матриксе в свободном состоянии, или на внутренней
поверхности внутренней мембраны. В ЦТК участвуют 5 витаминов В1, В2, РР,
пантотеновая кислота и липоевая кислота в виде коферментов тиаминпирофосфата,
ФАД, НАД+, КоА и липоата.
Основной функции ЦТК является образование водородных эквивалентов, которые в
цепи окислительного фосфорилирования обеспечивают синтез макроэргических
соединений.
Кроме того, ЦТК выполняет ведущую роль в процессах глюконеогенеза,
переаминирования, дезаминирования АК, липогенеза и синтеза гема. Интегрирует все
виды обмена веществ.
22. Значение цикла Кребса
1) ЦТК является конечным этапом окисления всех веществ, поступивших вклетку. Его можно сравнить со своеобразным “метаболическим котлом”, в котором
в организме полностью сгорают все питательные вещества до своих конечных
продуктов.
2) ЦТК является основным источником энергии в организме, т.к. в ходе реакций
освобождается 60% энергии, заключенной в питательных веществах.
3) В ЦТК образуются вещества, являющиеся донорами водорода для дыхательной
цепи. Все ферменты ЦТК локализованы в матриксе митохондрий, откуда протоны
и электроны поступают в дыхательную цепь, локализованную на внутренней
мембране.
4) Промежуточные метаболиты ЦТК могут быть использованы для синтеза ряда
биологически важных соединений – аминокислот, углеводов, гемоглобина и др.
Функции ЦТК:
1. Катаболическая
2. Энергетическая
3. Водорододонорная
4. Анаболическая
5. Интегративная
23. Цикл трикарбоновых кислот (цикл Кребса)
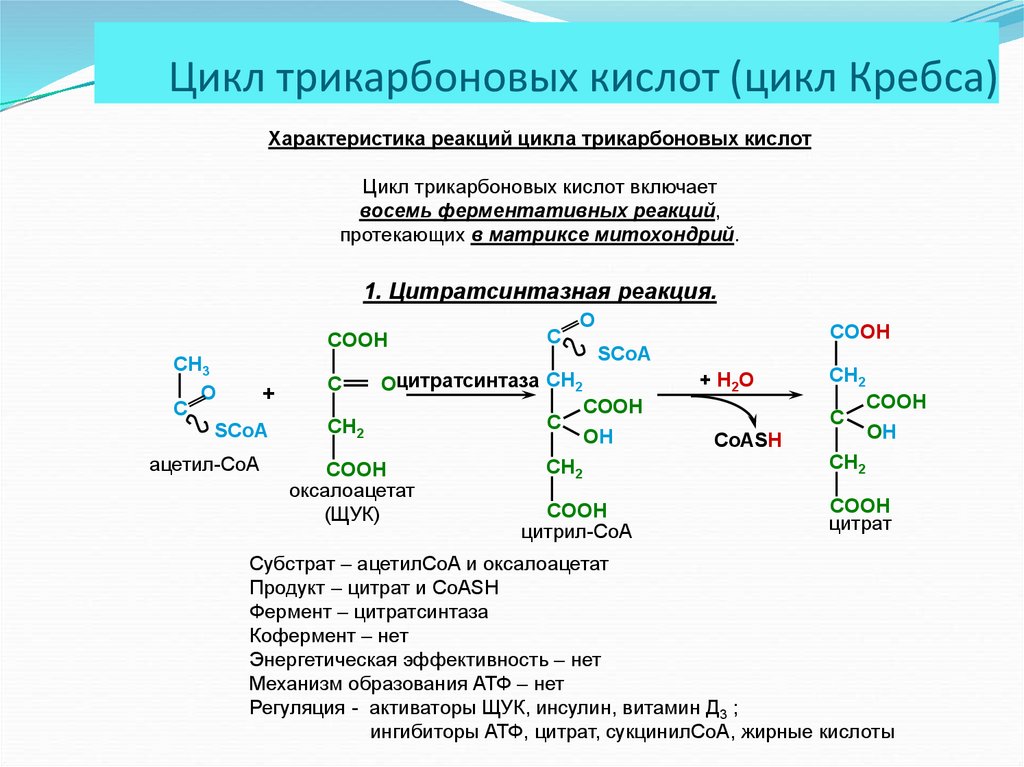
Характеристика реакций цикла трикарбоновых кислотЦикл трикарбоновых кислот включает
восемь ферментативных реакций,
протекающих в матриксе митохондрий.
1. Цитратсинтазная реакция.
CООH
CH3
О
+
C
SCoA
ацетил-СоА
C
C
О
CООН
SCoA
+ Н2О
Оцитратсинтаза CH2
CООH
ОH
CH2
C
CООH
ОH
CH2
C
CООH
оксалоацетат
(ЩУК)
CH2
CH2
CООH
цитрил-СоА
CООH
цитрат
CoASH
Субстрат – ацетилСоА и оксалоацетат
Продукт – цитрат и CoASH
Фермент – цитратсинтаза
Кофермент – нет
Энергетическая эффективность – нет
Механизм образования АТФ – нет
Регуляция - активаторы ЩУК, инсулин, витамин Д3 ;
ингибиторы АТФ, цитрат, сукцинилСоА, жирные кислоты
24. Цикл трикарбоновых кислот (цикл Кребса)
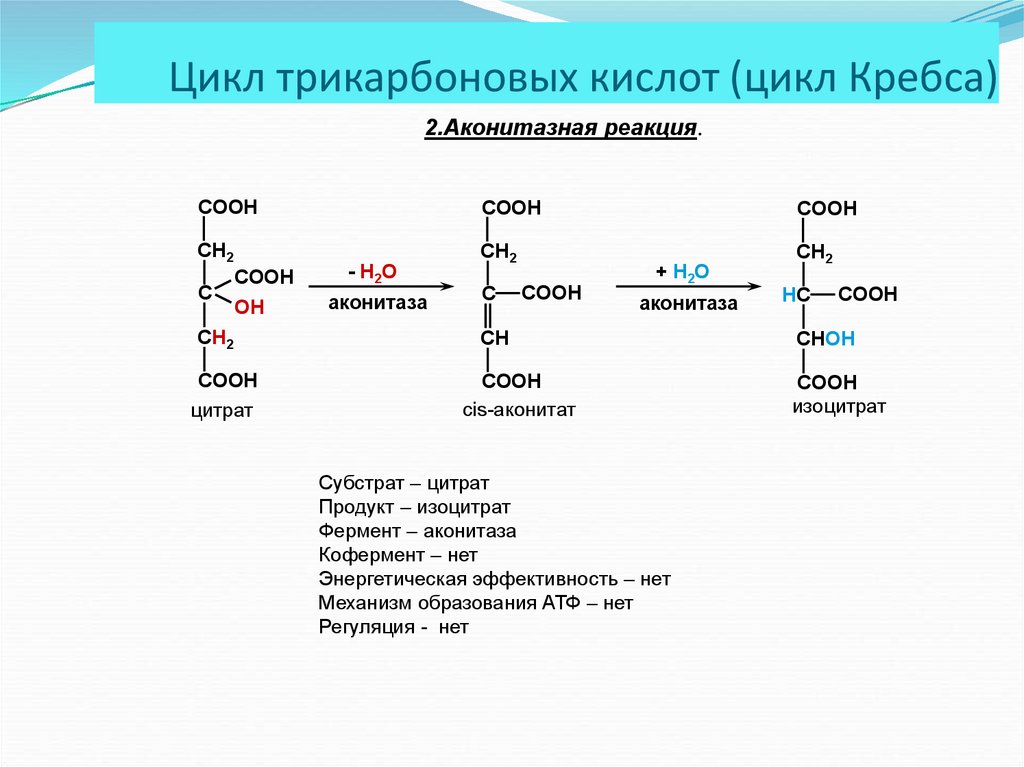
2.Аконитазная реакция.CООН
CООН
CООН
CH2
CH2
CH2
C
CООH
ОH
CH2
CООH
цитрат
- Н2О
аконитаза
C
CООH
+ Н2О
аконитаза
CH
CООH
сis-аконитат
Субстрат – цитрат
Продукт – изоцитрат
Фермент – аконитаза
Кофермент – нет
Энергетическая эффективность – нет
Механизм образования АТФ – нет
Регуляция - нет
НC
CООH
CHOH
CООH
изоцитрат
25. Цикл трикарбоновых кислот (цикл Кребса)
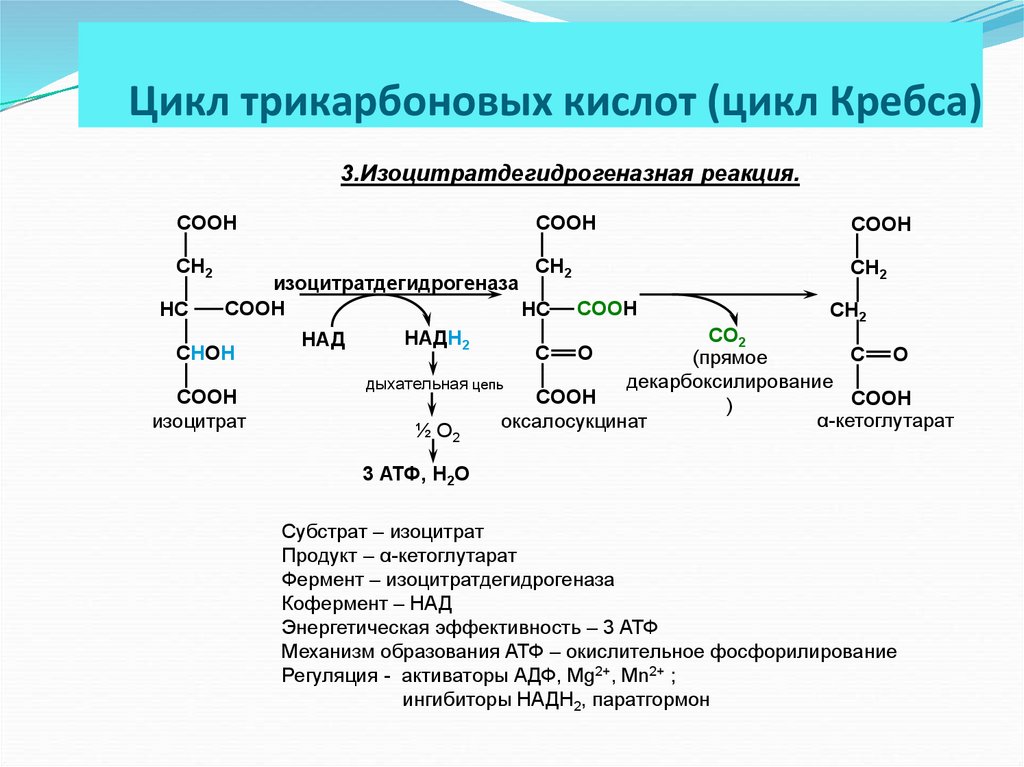
3.Изоцитратдегидрогеназная реакция.CООН
CООН
CООН
CH2
CH2
CH2
изоцитратдегидрогеназа
CООH
НC
НC CООH
CН2
СО2
НАДН2
НАД
CHOH
C O
C O
(прямое
декарбоксилирование
дыхательная цепь
CООH
CООH
CООH
)
α-кетоглутарат
изоцитрат
оксалосукцинат
½ О2
3 АТФ, Н2О
Субстрат – изоцитрат
Продукт – α-кетоглутарат
Фермент – изоцитратдегидрогеназа
Кофермент – НАД
Энергетическая эффективность – 3 АТФ
Механизм образования АТФ – окислительное фосфорилирование
Регуляция - активаторы АДФ, Mg2+, Mn2+ ;
ингибиторы НАДН2, паратгормон
26. Цикл трикарбоновых кислот (цикл Кребса)
4. α-кетоглутаратдегидрогеназная реакция.CООН
ТДФ, НАД, CoASH
CH2
CH2
CН2
C
CООН
CН2
O
CООH
α-кетоглутарат
СО2
C
(окислительное
декарбоксилирование)
НАДН2
О
SCoA
сукцинил-СоА
дыхательная
цепь
½ О2
3 АТФ, Н2О
Реакция протекает с участием α-кетоглутаратдегидрогеназного комплекса,
аналогичного пируватдегидрогеназному!!!
Субстрат – α-кетоглутарат
Продукт – сукцинилСоА, CO2
Фермент – α-кетоглутаратдекарбоксилаза, сукцинилтрансфераза,
дигидролипоилдегидрогеназа
Кофермент – НАД, ФАД, ТДФ, CoASH, амид липоевой кислоты
Энергетическая эффективность – 3 АТФ
Механизм образования АТФ – окислительное фосфорилирование
27. Цикл трикарбоновых кислот (цикл Кребса)
5. Сукцинаттиокиназная реакция.CООН
CООН
CH2
+ ГДФ + Н3РО4
CН2
C
О
SCoA
сукцинил-СоА
сукцинаттиокиназа
CH2
+ ГТФ + CoASH
CН2
CООН
сукцинат
ГТФ + АДФнуклеозиддифосфаткиназа ГДФ + АТФ
Субстрат – сукцинилСоА, Н3РО4 , ГДФ
Продукт – сукцинат, ГТФ, CoASH
Фермент – сукцинаттиокиназа
Кофермент – нет
Энергетическая эффективность – 1 АТФ
Механизм образования АТФ – субстратное фосфорилирование
Регуляция - нет
28. Цикл трикарбоновых кислот (цикл Кребса)
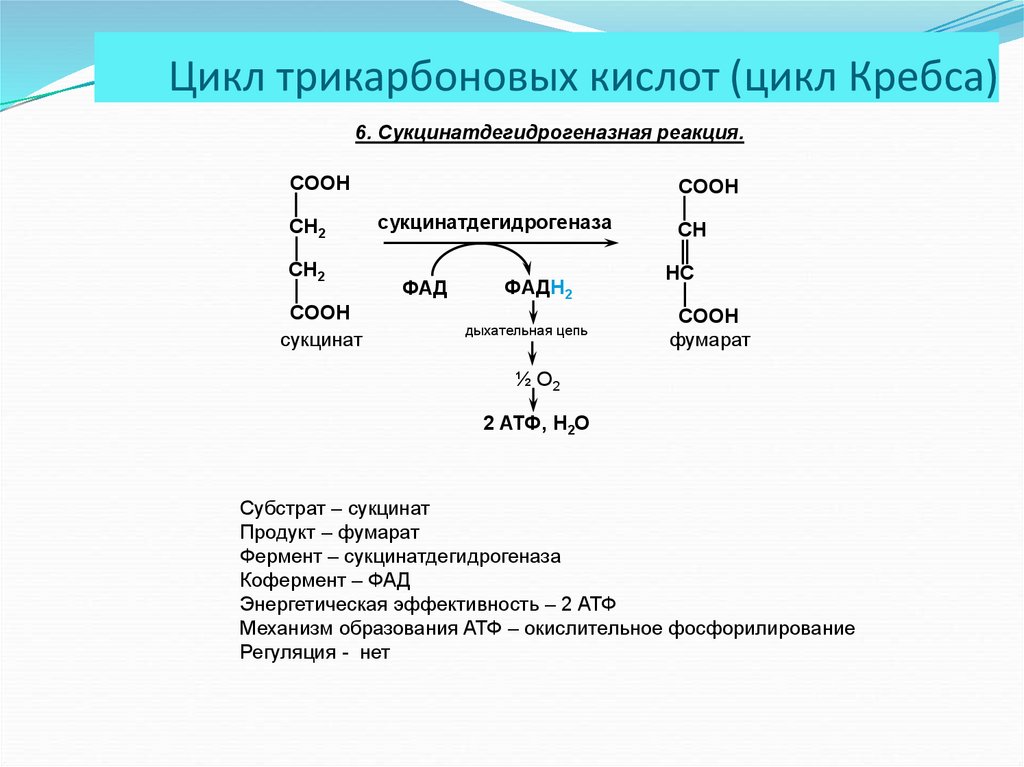
6. Сукцинатдегидрогеназная реакция.CООН
CH2
CН2
CООН
сукцинат
CООН
сукцинатдегидрогеназа
ФАД
ФАДН2
дыхательная цепь
CH
НC
CООН
фумарат
½ О2
2 АТФ, Н2О
Субстрат – сукцинат
Продукт – фумарат
Фермент – сукцинатдегидрогеназа
Кофермент – ФАД
Энергетическая эффективность – 2 АТФ
Механизм образования АТФ – окислительное фосфорилирование
Регуляция - нет
29. Цикл трикарбоновых кислот (цикл Кребса)
7. Фумаразная реакция.CООН
CH
НC
+ Н2О
фумараза
CООН
фумарат
Субстрат – фумарат, вода
Продукт – малат
Фермент –фумараза
Кофермент – нет
Энергетическая эффективность – нет
Механизм образования АТФ – нет
Регуляция - нет
CООН
CHОН
CН2
CООН
малат
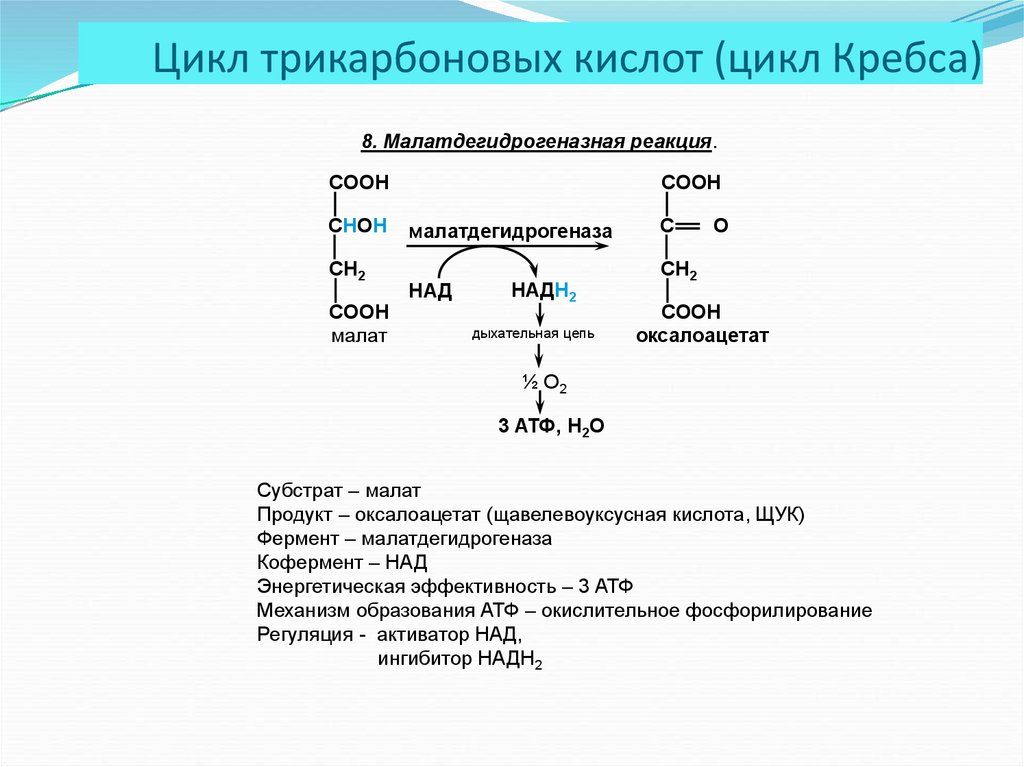
30. Цикл трикарбоновых кислот (цикл Кребса)
8. Малатдегидрогеназная реакция.CООН
CHОН
CН2
CООН
малат
CООН
малатдегидрогеназа
НАД
НАДН2
дыхательная цепь
C
О
CН2
CООН
оксалоацетат
½ О2
3 АТФ, Н2О
Субстрат – малат
Продукт – оксалоацетат (щавелевоуксусная кислота, ЩУК)
Фермент – малатдегидрогеназа
Кофермент – НАД
Энергетическая эффективность – 3 АТФ
Механизм образования АТФ – окислительное фосфорилирование
Регуляция - активатор НАД,
ингибитор НАДН2
31. Цикл трикарбоновых кислот (цикл Кребса)
Хотя цикл Кребса изображают в виде замкнутого ферментативногопроцесса,
на участке от сукцината до оксалоацетата реакции являются
обратимыми.
Поэтому эта ветвь может функционировать в обратном направлении,
то есть оксалоацетат может превращаться в метаболиты цикла Кребса вплоть
до сукцината.
Такая возможность реализуется в тех случаях, когда оксалоацетат интенсивно
синтезируется из других субстратов.
Причины нарушений цикла трикарбоновых кислот
Недостаточное поступление кислорода в клетку (гипоксия)
Недостаток отдельных компонентов цикла, вследствие их утилизации по другим
метаболическим путям или недостаточного восполнения в ходе реакций цикла
Недостаток витаминов, необходимых для нормального функционирования цикла
Кребса.
32. Цикл трикарбоновых кислот (цикл Кребса)
Анаболические реакции цикла КребсаЦикл трикарбоновых кислот поставляет промежуточные продукты для
биосинтетических процессов:
сукцинил-СоА - биосинтез порфиринов, гема и гемоглобина
оксалоацетат – глюконеогенез, образование аспарагиновой кислоты
α-кетоглутарат – образование глутаминовой кислоты
Поэтому утилизация промежуточных метаболитов цикла на цели биосинтеза
должна обязательно сопровождаться их дополнительным образованием за счет других
источников – анаплеротическими реакциями (от греч. – “пополнять”).
Одной из основных анаплеротических реакций является образование
оксалоацетата путем карбоксилирования пирувата при участии пируваткарбоксилазы.
Пируваткарбоксилаза локализована в митохондриях, состоит из 4 субъединиц,
каждая из которых содержит связанный ион Мn2+ и витамин Н (биотин), выполняющий
коферментную функцию.
CООH
АТФ
АДФ + Н3РО4
CООH
C
О
C
О+ СО2
пируваткарбоксилаза
CH2
CH3
CООH
пируват
оксалоацетат
33. Вопросы для письменного ответа
1.2.
3.
4.
5.
Дайте определение терминам «биологическое окисление», «катаболизм»,
«метаболизм», «анаболизм», «макроэргическая связь», «эндергоническая и
экзергоническая реакция», «тканевое дыхание», «амфиболический путь
метаболизма». Какой этап метаболизма протекает анаэробно, а какой не может
быть реализован в отсутствии кислорода?
ОДПВК – что это за процесс, дл чего он нужен, какой продукт образуется в
результате и что с этим продуктом происходит дальше. Без каких коферментов
данный процесс невозможен?
Пируватдегидрогеназный комплекс (система) – почему он так называется, в чем
особенность его функционирования?
ЦТК – биохимический смысл процесса, особенности протекания, 8 реакций с
указанием ферментов и их коферментов
Укажите обратимые и необратимые реакции цикла Кребса. Как осуществляется
регуляция ЦТК?
















 Биология
Биология








