Похожие презентации:
Липиды. Классификация, строение, свойства и биологическая роль липидов
1.
СЗГМУ им. И. И. МЕЧНИКОВАКАФЕДРА КЛИНИЧЕСКОЙ ЛАБОРАТОРНОЙ ДИАГНОСТИКИ,
БИОЛОГИЧЕСКОЙ И ОБЩЕЙ ХИМИИ ИМ. В.В. СОКОЛОВСКОГО
БИОЛОГИЧЕСКАЯ ХИМИЯ-БИОХИМИЯ ПОЛОСТИ РТА
Раздел IX
ЛЕКЦИЯ
ЛИПИДЫ: СТРОЕНИЕ, СВОЙСТВА,
БИОЛОГИЧЕСКАЯ РОЛЬ. ОБМЕН ЛИПИДОВ ТКАНЯХ.
Доцент Антонова Ж.В.
2024/2025
2.
План лекции1. Классификация, строение, свойства и биологическая роль липидов.
1.1. ТАГ: строение, свойства, роль;1.2. ГФЛ: строение, свойства, роль.
2. Жирные кислоты. Примеры важнейших жирных кислот.
3. Анаболизм жирных кислот. Биологическая роль.
4. Энергетическое использование липидов:
4.1. Липолиз жировой ткани. 4.2. Регуляция липолиза жировой ткани
5. Катаболизм жирных кислот. 5.1. Процесс β-окисления.
5.1.1. Активация ЖК. 5.1.2. Транспорт ВЖК в митохондрию
5.1.3. Реакции β-окисления насыщенных ВЖК с четным числом «С».
5.1.4. Энергетический выход β-окисления пальмитиновой кислоты.
5.1.5. β-Окисление ненасыщенных ЖК. 5.1.6. β-окисление ВЖК с нечетным числом «С».
5.1.6. Регуляция β-окисления
6. Пластическое использование липидов. 6.1.Синтез ВЖК (пальмитиновой)
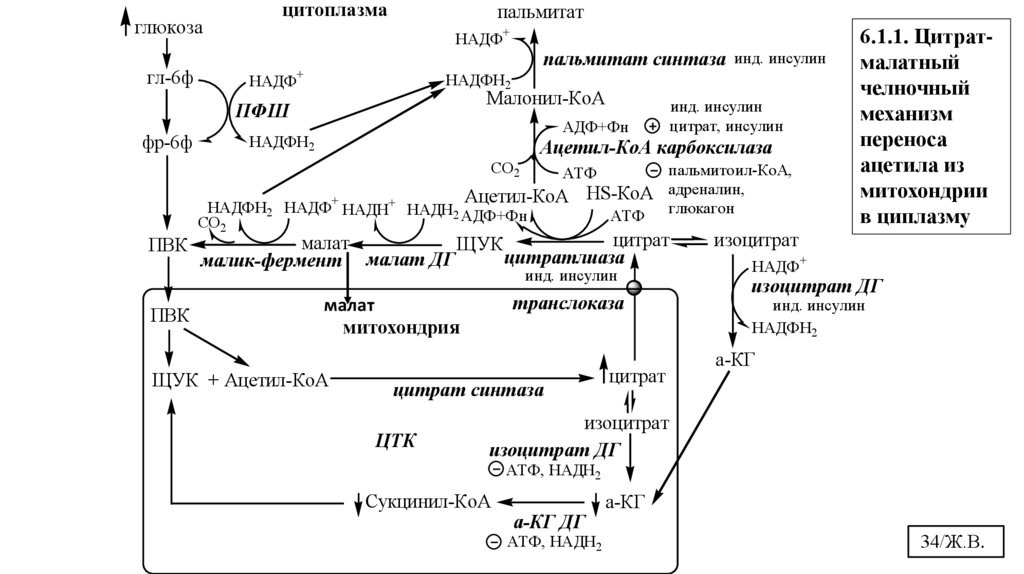
6.1.1. Цитрат-малатный челночный механизм переноса ацетила из митохондрии в циплазму. 6.1.2. Первая
реакция синтеза ВЖК – образование малонила. 6.1.3. Строение синтазного комплекса. 6.1.4.Синтез ВЖК
на синтазном комплексе.
7.Синтез ТАГ и ГФЛ. 7.1. Синтез ТАГ и ФЛ в энтероцитах. 7.2. Глицеролфосфатный путь. 7.3. Синтез
фосфатидилсерина, фосфатидилхолина, фосфатидилэтаноламина. 7.4. Факторы, необходимые для синтеза
ГФЛ.
2/Ж.В.
3.
Условные обозначения.БАВ – биологически активные вещества
ЖК – жирная кислота
ВЖК – высшая жирная кислота
МАГ – моноацилглицеролы
ДАГ- диацилглицеролы
ТАГ -триацилглицеролы
ГФЛ – глицерофосфолипиды
ЛП - липопротеины
ТАФ – тромбоцитактивирующий фактор
ХС – холестерол
ЭХС – эфиры холестерола
D3 - витамин холекальциферол
ЛПЛ - липопротеинлипаза
3/Ж.В.
4.
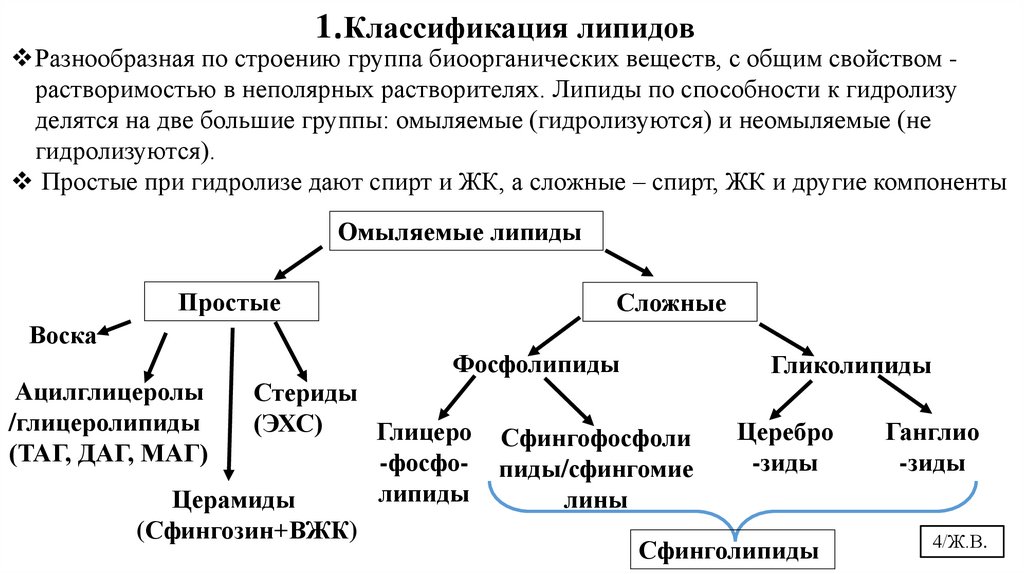
1.Классификация липидовРазнообразная по строению группа биоорганических веществ, с общим свойством растворимостью в неполярных растворителях. Липиды по способности к гидролизу
делятся на две большие группы: омыляемые (гидролизуются) и неомыляемые (не
гидролизуются).
Простые при гидролизе дают спирт и ЖК, а сложные – спирт, ЖК и другие компоненты
Омыляемые липиды
Простые
Сложные
Воска
Ацилглицеролы
/глицеролипиды
(ТАГ, ДАГ, МАГ)
Фосфолипиды
Стериды
(ЭХС)
Глицеро
-фосфолипиды
Церамиды
(Сфингозин+ВЖК)
Гликолипиды
Сфингофосфоли
пиды/сфингомие
лины
Церебро
-зиды
Сфинголипиды
Ганглио
-зиды
4/Ж.В.
5.
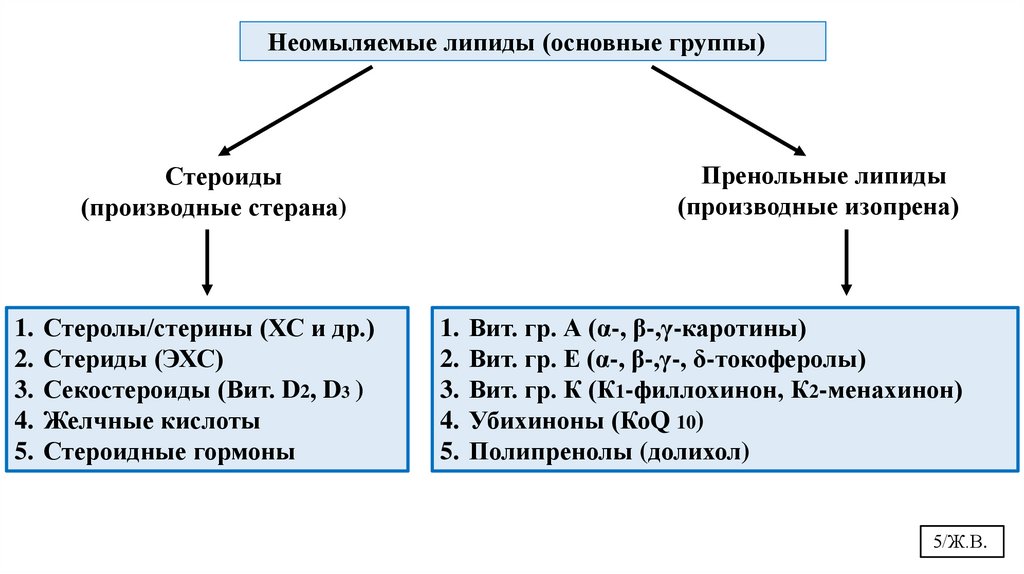
Неомыляемые липиды (основные группы)Стероиды
(производные стерана)
1. Стеролы/стерины (ХС и др.)
2. Стериды (ЭХС)
3. Секостероиды (Вит. D2, D3 )
4. Желчные кислоты
5. Стероидные гормоны
Пренольные липиды
(производные изопрена)
1. Вит. гр. А (α-, β-,γ-каротины)
2. Вит. гр. Е (α-, β-,γ-, δ-токоферолы)
3. Вит. гр. К (К1-филлохинон, К2-менахинон)
4. Убихиноны (КоQ 10)
5. Полипренолы (долихол)
5/Ж.В.
6.
1.1. ТРИАЦИЛГЛИЦЕРОЛЫ (ТАГ):Сложноэфирная связь
1-Олеоил-2-пальмитоил-3стеароилглицерол
строение, свойства, роль.
ТАГ – сложные эфиры трехатомного спирта
глицерола и жирных кислот.
ТАГ - гидрофобные, неполярные липиды.
Роль ацилглицеролов (МАГ, ДАГ, ТАГ в организме:
• ТАГ - основные липиды пищи (жиры – твердые ТАГ
и жидкие ТАГ - масла); ТАГ - основные липиды
жировой ткани (резервная роль). В состав мембран
не входят (гидрофобны)
• Механическая
• Терморегуляторная
• МАГ – амфифильные вещества (Промежуточные
вещества в обмене ацилглицеридов)
• ДАГ – вторичные мессенджеры (посредники) 6/Ж.В.
7.
1.2.Глицерофосфолипиды (ГФЛ): строение, свойства, роль.1,2-диацилглицерол + остаток фосфорной к-ты + аминоспирт или Сер, инозитол.
В 1-м положении – насыщенный ацил, во 2-м- ненасыщенный/полиненасыщенный.
+
Фосфатидилинозитол
-
Фосфатидилсерин
-
3
+
Фосфатидилхолин
-
3
Фосфатидилэтаноламин
7/Ж.В.
8.
У плазмалогенов: в 1-м положении – высший алифатический спирт связан простойэфирной связью
Простая эфирная связь
+
NН3
Плазмалогены входят в
большом количестве в
мембраны митохондрий
и миелиновые оболочки
нервных клеток.
8/Ж.В.
9.
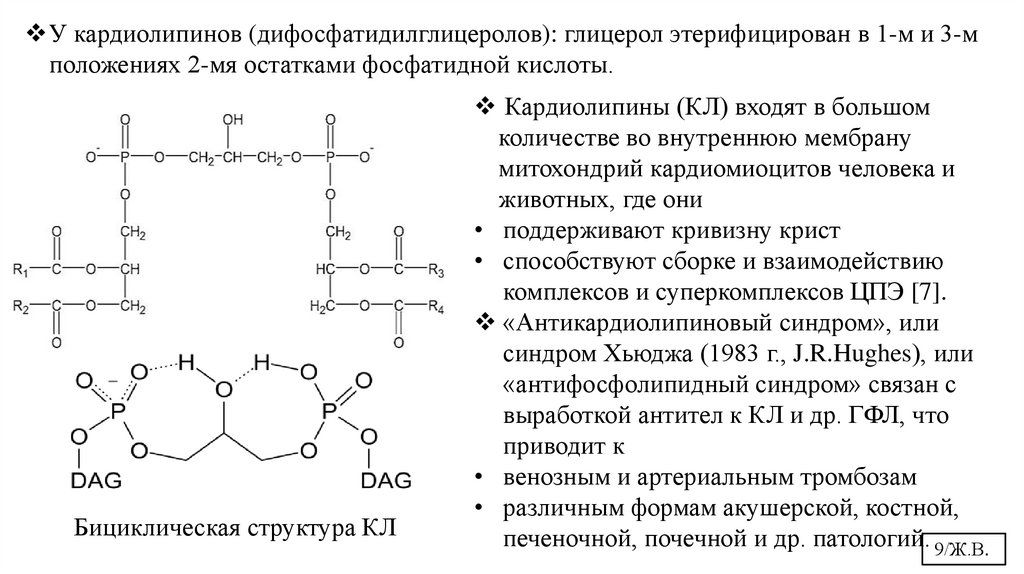
У кардиолипинов (дифосфатидилглицеролов): глицерол этерифицирован в 1-м и 3-мположениях 2-мя остатками фосфатидной кислоты.
Бициклическая структура КЛ
Кардиолипины (КЛ) входят в большом
количестве во внутреннюю мембрану
митохондрий кардиомиоцитов человека и
животных, где они
• поддерживают кривизну крист
• способствуют сборке и взаимодействию
комплексов и суперкомплексов ЦПЭ [7].
«Антикардиолипиновый синдром», или
синдром Хьюджа (1983 г., J.R.Hughes), или
«антифосфолипидный синдром» связан с
выработкой антител к КЛ и др. ГФЛ, что
приводит к
• венозным и артериальным тромбозам
• различным формам акушерской, костной,
печеночной, почечной и др. патологий. 9/Ж.В.
10.
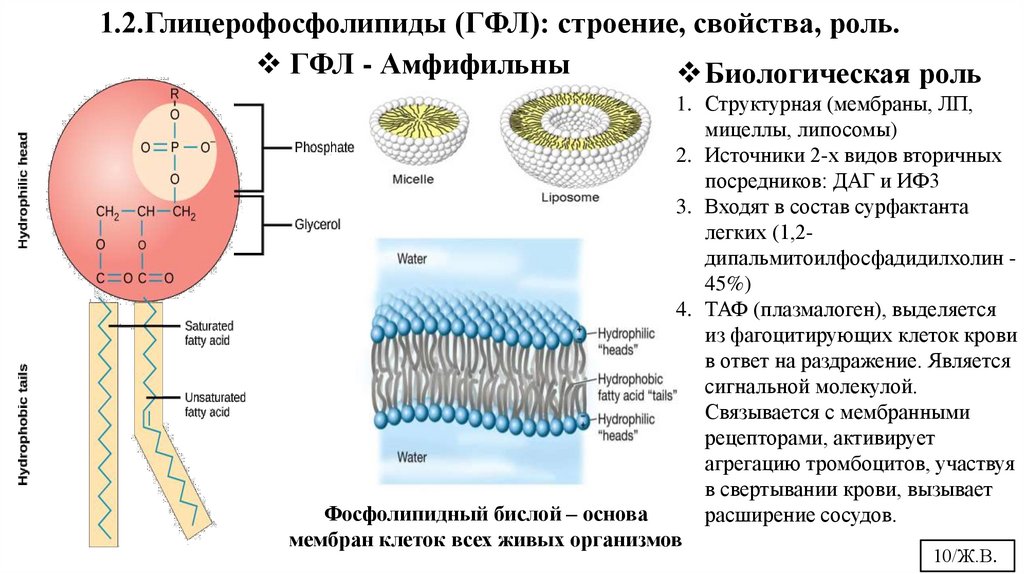
1.2.Глицерофосфолипиды (ГФЛ): строение, свойства, роль.ГФЛ - Амфифильны
Биологическая роль
1. Структурная (мембраны, ЛП,
мицеллы, липосомы)
2. Источники 2-х видов вторичных
посредников: ДАГ и ИФ3
3. Входят в состав сурфактанта
легких (1,2дипальмитоилфосфадидилхолин 45%)
4. ТАФ (плазмалоген), выделяется
из фагоцитирующих клеток крови
в ответ на раздражение. Является
сигнальной молекулой.
Связывается с мембранными
рецепторами, активирует
агрегацию тромбоцитов, участвуя
в свертывании крови, вызывает
Фосфолипидный бислой – основа
расширение сосудов.
мембран клеток всех живых организмов
10/Ж.В.
11.
2. Жирные кислоты• Жирными кислотами (ЖК) - называются карбоновые кислоты,
которые образуются при гидролизе омыляемых липидов.
• В основном к жирным кислотам относятся высшие карбоновые
кислоты (содержащие 12 и более атомов «С»).
• Высшие ЖК гидрофобные, они транспортируются в крови с
помощью альбуминов, а в клетках - с помощью Z-белков.
• Примеры важнейших жирных кислот представлены в табл. 1
11/Ж.В.
12.
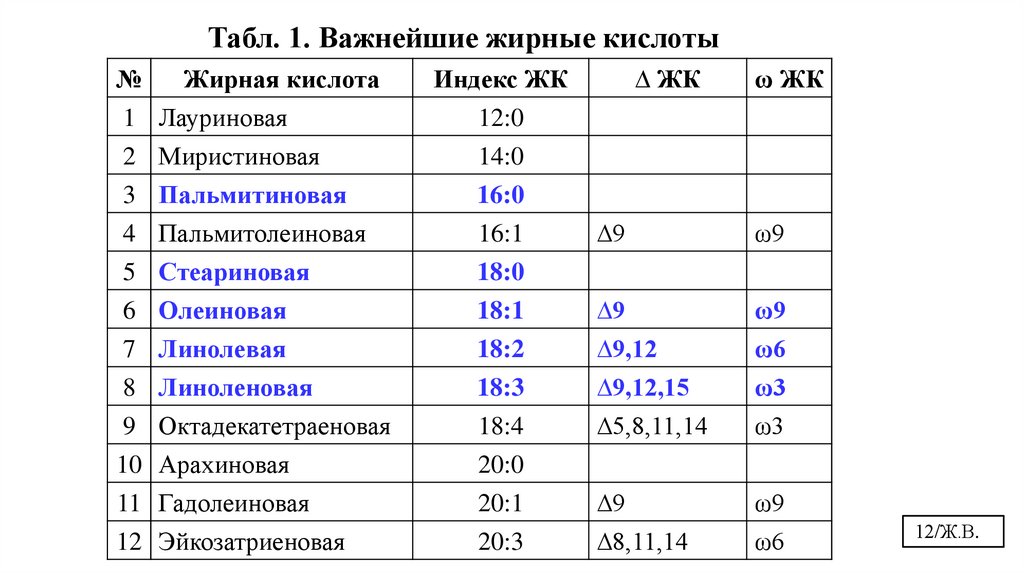
Табл. 1. Важнейшие жирные кислоты№
Жирная кислота
1 Лауриновая
Индекс ЖК
12:0
2 Миристиновая
3 Пальмитиновая
4 Пальмитолеиновая
14:0
16:0
16:1
5 Стеариновая
18:0
6 Олеиновая
7 Линолевая
∆ ЖК
ω ЖК
∆9
ω9
18:1
18:2
∆9
∆9,12
ω9
ω6
8 Линоленовая
9 Октадекатетраеновая
18:3
18:4
∆9,12,15
∆5,8,11,14
ω3
ω3
10 Арахиновая
11 Гадолеиновая
12 Эйкозатриеновая
20:0
20:1
20:3
∆9
∆8,11,14
ω9
ω6
12/Ж.В.
13.
Табл. 1. Важнейшие жирные кислоты (продолжение)№ Жирная кислота
13 Арахидоновая
Индекс ЖК
∆ ЖК
20:4
∆5,8,11,14
ω ЖК
ω6
14 Эйкозапентаеновая
15 Бегеновая
16 Эруковая
20:5
22:0
22:1
∆5,8,11,14,17
ω3
∆13
ω9
17 Андреновая
18 Докозапентаеновая
19 Докозагексаеновая
22:4
22:5
22:6
∆9,12,15,18
ω6
∆4,7,10,13,16
ω6
∆4,7,10,13,16,19 ω3
20 Лигноцериновая
21 Невроновая
22 Цереброновая
24:0
24:1
24:0
∆15
ω9
α-гидрокси ЖК
13/Ж.В.
14.
Ненасыщенные жирные кислотыЦис-конфигурация
двойной связи
Зигзагообразная
Линолевая кислота (С17H31COOH)
конформация
углеродной цепи
ЖК.
СН3
Олеиновая кислота (C18H34O2)
Арахидоновая кислота (C20H32O2)
Леноленовая кислота (C₁₈H₃₀O₂)
14/Ж.В.
15.
3. АНАБОЛИЗМ ЖИРНЫХ КИСЛОТИсточником ЖК в организме являются синтетические
процессы, омыляемые липиды и пища.
ЖК, которые синтезируются в организме, называются
заменимыми. Значительная их часть образуется в печени, в,
меньшей степени — в жировой ткани и лактирующей
молочной железе.
ЖК, которые не синтезируются в организме, но необходимы
для него называются незаменимыми. Единственным
источником незаменимых ЖК является пища. Они образуют
понятие витамин F (линолевая, линоленовая и арахидоновая).
15/Ж.В.
16.
3. Биологическая роль ЖК1. Полиеновые ЖК (арахидоновая, эйкозапентаеновая,
эйкозатриеновая) используются для синтеза БАВ –
эйкозаноидов (простагландинов, простациклинов,
тромбоксанов, лейкотриенов, липоксинов).
2. ЖК окисляются в аэробных условиях с образованием
АТФ;
3. ЖК являются структурным компонентом омыляемых
липидов: восков, глицерофосфолипидов,
сфинголипидов, эфиров холестерола.
16/Ж.В.
17.
4. Энергетическое использование липидов4.1 Липолиз жировой ткани (мобилизация жиров)
• Это ступенчатый гидролиз сложноэфирных связей ТАГ под действием
специфических тканевых липаз с образованием глицерола и ВЖК.
Протекает в постабсорбтивном периоде, при голодании и активной
физической работе.
• Лимитирующим ферментом липолиза является триацилглицероллипаза
(ТАГ-липаза). Она имеет две формы: фосфорилированную (активную)
и нефосфорилированную (неактивную).
• Фермент активируется по аденилатциклазной системе от адреналина,
норадреналина и глюкагона.
• За счет активации протеинфосфатазы от инсулина ТАГ- липаза
дефосфорилируется и инактивируется.
• Глюкокортикоиды индуцируют синтез ТАГ-липазы.
17/Ж.В.
18.
4.1.Реакции липолиза жировой тканиСН2–О–СО–R1
СН2–ОН
ТАГ-липаза |
|
CН–О–СО–R2
|
CН–О–СО–R2
- R1–CООН
СН2–О–СО–R3
ТАГ
ДАГ-липаза
|
- R3–CООН
СН2–О–СО–R3
ДАГ
18/Ж.В.
19.
4.1.Реакции липолиза жировой ткани (продолжение)CН2 – ОН
|
CН – О – СО – R2
|
CН2 – ОН
МАГ
МАГ-липаза
- R2 – CООН
CН2 – ОН
|
CН – ОН
|
CН2 – ОН
Глицерол
19/Ж.В.
20.
4.2.Регуляция липолиза жировой тканиАктивируют липолиз:
• Глюкокортикоиды
• глюкагон
• СТГ, АКТГ
• тироксин
• липотропин гипофиза
• цАМФ
Ингибирует липолиз:
• инсулин
20/Ж.В.
21.
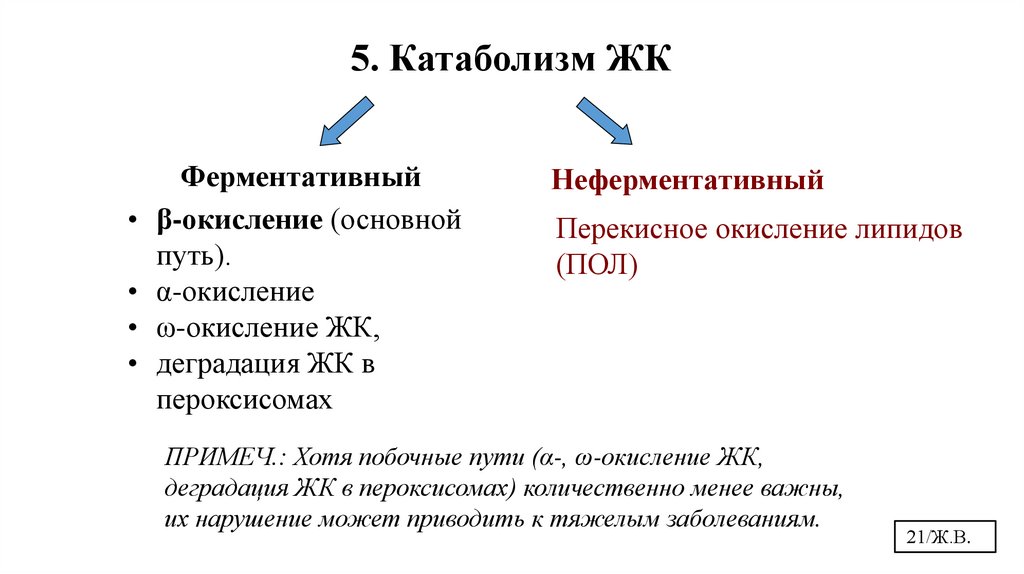
5. Катаболизм ЖКФерментативный
• β-окисление (основной
путь).
• α-окисление
• ω-окисление ЖК,
• деградация ЖК в
пероксисомах
Неферментативный
Перекисное окисление липидов
(ПОЛ)
ПРИМЕЧ.: Хотя побочные пути (α-, ω-окисление ЖК,
деградация ЖК в пероксисомах) количественно менее важны,
их нарушение может приводить к тяжелым заболеваниям.
21/Ж.В.
22.
5.1. Процесс β-окисления• В процессе β-окисления выделяют 3 этапа: активация ЖК в цитоплазме;
транспорт ЖК в составе из цитоплазмы в митохондрию; собственно
процесс окисления до ацетил-КоА и его поступление в ЦТК.
• ЖК с короткой и средней цепью (от 4 до 12 атомов С) могут проникать в
матрикс митохондрий путём диффузии. Активация этих ЖК происходит
ацил-КоА синтетазами в матриксе митохондрий.
• ЖК с длинной цепью, сначала активируются в цитозоле (ацил-КоА
синтетазами на внешней мембране митохондрий), а затем переносятся в
матрикс митохондрий специальной транспортной системой с помощью
карнитина.
•Карнитин* поступает с пищей или синтезируется
из лизина и метионина с участием витамина С.
* Карнитин открыли учёные-биохимики
Владимир Гулевич и Роберт Кримберг.
Они выделили его из мышечных тканей в нач. 20 века.
L-карнитин
22/Ж.В.
23.
5.1.1. Активация жирных кислотНS-КоА
R COOH
АТФ
АМФ + РРi
ацил-КоАсинтетаза
2 R
CO ~ SKoA
ацил-КоА
23
24.
5.1.2.Транспорт ЖК в митохондрию+
N (СН3)3
НS-КоА
СН 2
СН2
R CO ~ SKoA +
ацил-КоА
СН OH
СН2
COOH
цитоплазма
ацилкарнитинтрансфераза
цитоплазматическая
карнитин
НS-КоА
ацил-КоА
СН2
COOH
карнитин
COOH
N (СН3)3
СН2
СН2
СН OH
СН 2
+
+
R CO~ SKoA +
СН О ОС R
ацил-карнитин
матрикс
митохондрии
N (СН3 ) 3
N (СН3 )3
ацилкарнитинтрансфераза
митохондриальная
СН О ОС R
СН2
COOH
ацил-карнитин
24/Ж.В.
25.
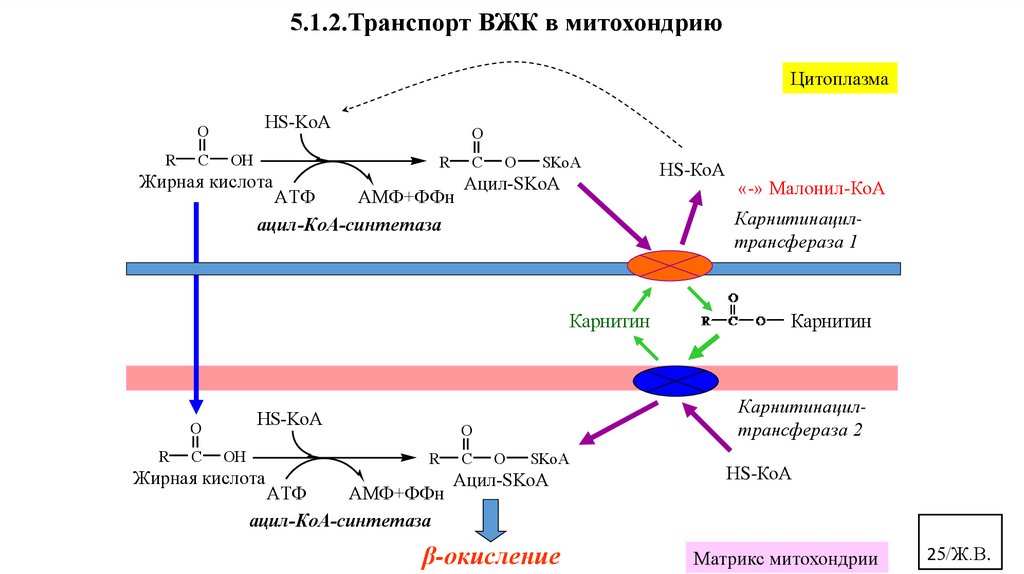
5.1.2.Транспорт ВЖК в митохондриюЦитоплазма
HS-KoA
O
R
C
OH
Жирная кислота
O
R
C
АТФ
АМФ+ФФн
ацил-КоА-синтетаза
O
SKoA
Ацил-SKoA
O
R
C
OH
Жирная кислота
АТФ
АМФ+ФФн
ацил-КоА-синтетаза
C
Карнитин
Карнитинацилтрансфераза 2
O
R
«-» Малонил-КоА
Карнитинацилтрансфераза 1
Карнитин
HS-KoA
НS-КоА
O
SKoA
Ацил-SKoA
β-окисление
НS-КоА
Матрикс митохондрии
25/Ж.В.
26.
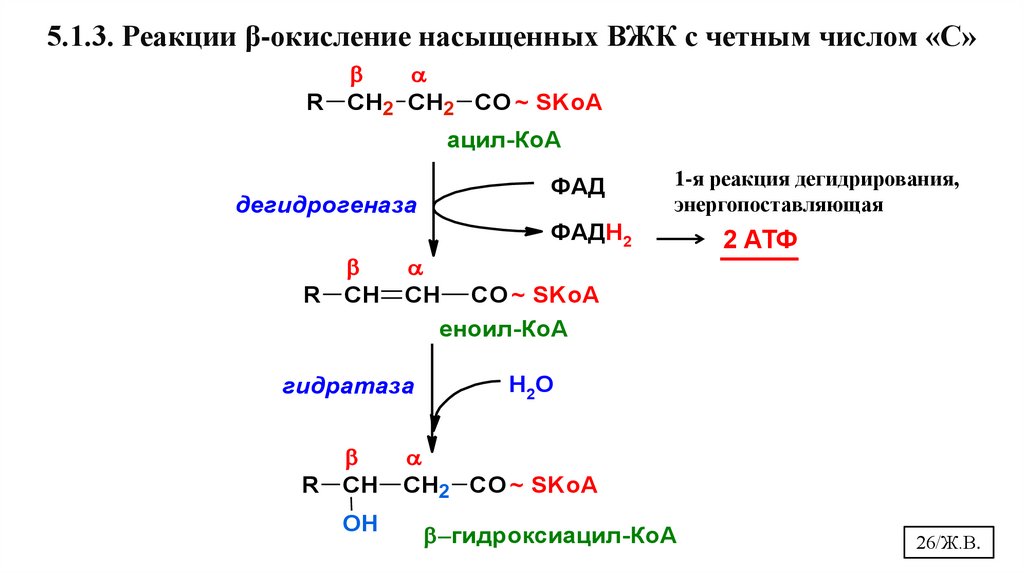
5.1.3. Реакции β-окисление насыщенных ВЖК с четным числом «С»R СН2 СН2 CO ~ SKoA
ацил-КоА
дегидрогеназа
ФАД
1-я реакция дегидрирования,
энергопоставляющая
ФАДН2
R СН СН CO ~ SKoA
еноил-КоА
гидратаза
2 АТФ
Н2О
R СН СН2 CO ~ SKoA
OH
гидроксиацил-КоА
26/Ж.В.
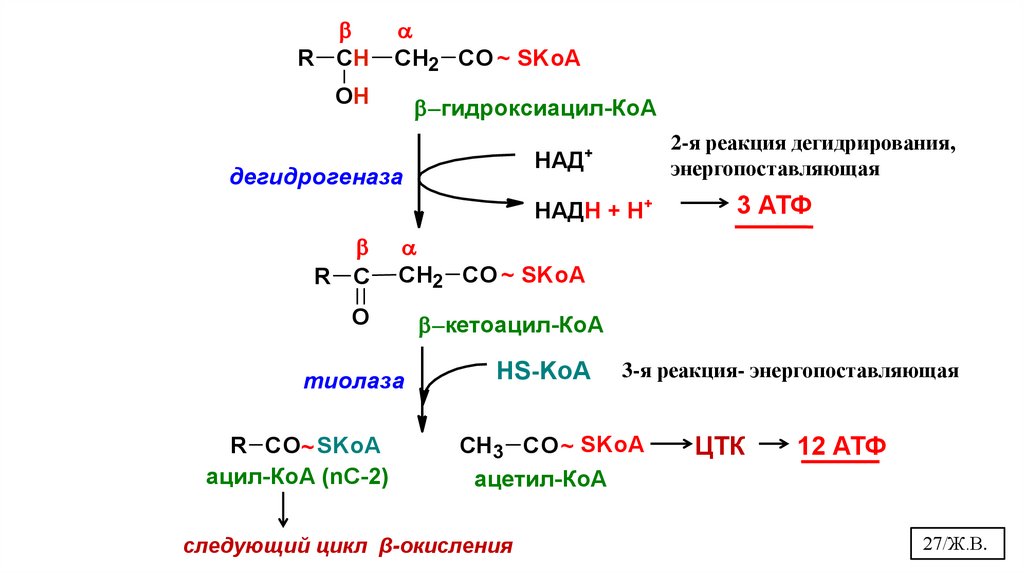
27.
R CH СН2 CO ~ SKoAOH
гидроксиацил-КоА
НАД
дегидрогеназа
2-я реакция дегидрирования,
энергопоставляющая
+
НАДН + Н+
3 АТФ
R С СН2 CO ~ SKoA
O
тиолаза
R CO~ SKoA
ацил-КоА (nС-2)
кетоацил-КоА
НS-KoA
3-я реакция- энергопоставляющая
CH3 CO ~ SKoA
ацетил-КоА
следующий цикл β-окисления
ЦТК
12 АТФ
27/Ж.В.
28.
пальмитил-КоА C=16R
H2
C
O
H2
C C
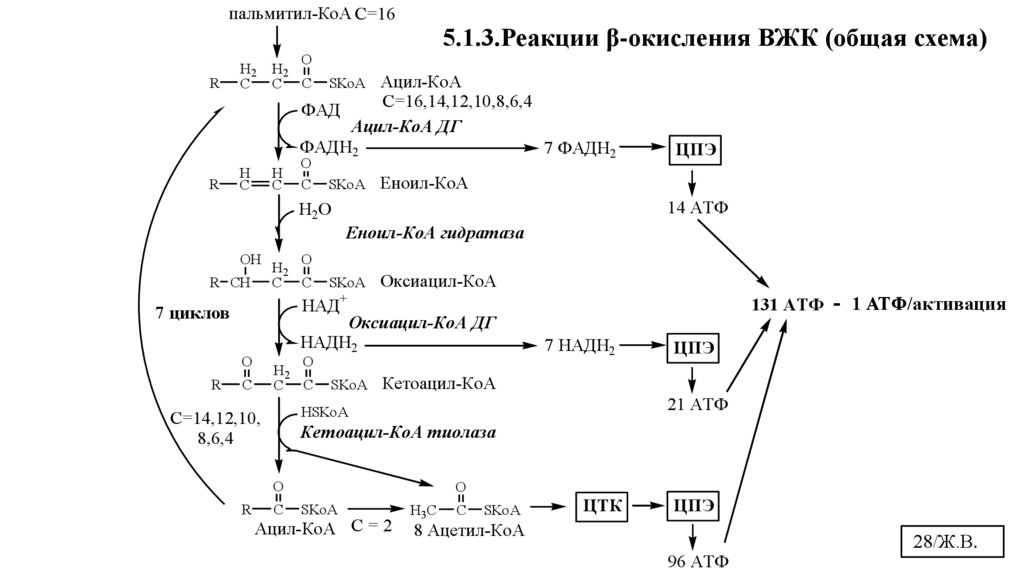
5.1.3.Реакции β-окисления ВЖК (общая схема)
SKoA Ацил-КоА
C=16,14,12,10,8,6,4
Ацил-КоА ДГ
ФАДН2
7 ФАДН2
ФАД
R
H
C
H
C
O
C
ЦПЭ
SKoA Еноил-КоА
14 АТФ
Н2О
Еноил-КоА гидратаза
ОН
R CН
O
H2
C C
НАД+
7 циклов
Оксиацил-КоА ДГ
НАДН2
О
R
SKoA Оксиацил-КоА
O
H2
C C
C
7 НАДН2
ЦПЭ
SKoA Кетоацил-КоА
21 АТФ
НSKoA
C=14,12,10,
8,6,4
Кетоацил-КоА тиолаза
O
R
131 АТФ - 1 АТФ/активация
C
O
SKoA
Ацил-КоА C = 2
H3C
C
SKoA
ЦТК
ЦПЭ
8 Ацетил-КоА
96 АТФ
28/Ж.В.
29.
5.1.4. Энергетический выход β-окисления пальмитиновой кислоты (С16)энергетический выход = n/2 . 12 + (n/2 - 1) . 5
- 1, где
• n – количество С-атомов в жирной кислоте;
• n/2 – количество молекул ацетил-КоА, образованных в
процессе β-окисления;
• 12 – количество АТФ, синтезирующихся при окислении
ацетил-КоА в ЦТК;
• (n/2 – 1) – количество циклов β-окисления;
• 5 – количество молекул АТФ, образованных в каждом цикле за
счёт двух реакций дегидрирования;
• 1 – затрата 1 молекулы АТФ на активацию жирной кислоты
29/Ж.В.
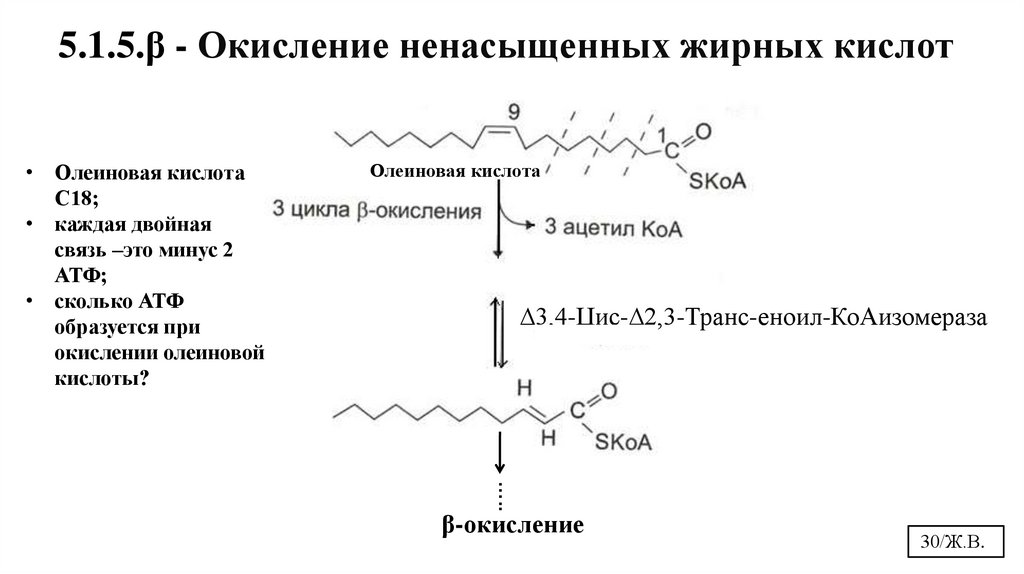
30.
5.1.5.β - Окисление ненасыщенных жирных кислот• Олеиновая кислота
С18;
• каждая двойная
связь –это минус 2
АТФ;
• сколько АТФ
образуется при
окислении олеиновой
кислоты?
Олеиновая кислота
∆3,4-Цис-∆2,3-Транс-еноил-КоАизомераза
…..
β-окисление
30/Ж.В.
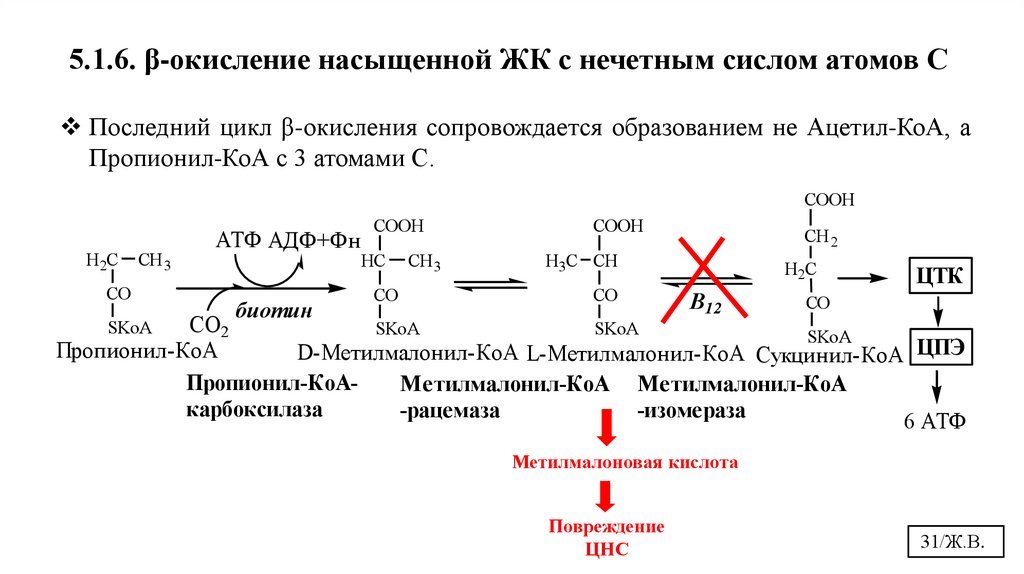
31.
5.1.6. β-окисление насыщенной ЖК с нечетным сислом атомов СПоследний цикл β-окисления сопровождается образованием не Ацетил-КоА, а
Пропионил-КоА с 3 атомами С.
COOH
H2C
CH 3
CO
АТФ АДФ+Фн
биотин
COOH
HC
CO
CH 3
COOH
CH 2
H3C CH
CO
H2C
В12
ЦТК
CO
CO2
SKoA
SKoA
SKoA
Пропионил-КоА
D-Метилмалонил-КоА L-Метилмалонил-КоА Сукцинил-КоА ЦПЭ
Пропионил-КоАМетилмалонил-КоА Метилмалонил-КоА
карбоксилаза
-рацемаза
-изомераза
6 АТФ
SKoA
Метилмалоновая кислота
Повреждение
ЦНС
31/Ж.В.
32.
5.1.6. Регуляция β-окисления ВЖКβ-окисление активируют: глюкагон, адреналин, ЖК, НАД+, АДФ:
Голод, физическая нагрузка → ↑ глюкагон, ↑ адреналин → ↑липолиз ТАГ в
адипоцитах → ↑ ЖК в крови → ↑ β-окисление в аэробных условиях в
мышцах, печени → ↑АТФ;
↑АТФ, ↑НАДH+Н+
↑Ацетил-КоА → ↑ цитрат, ↑ЖК → ↓ гликолиз → ↑ экономию глюкозы для
нервной ткани, эритроцитов и т.д.
β-окисление ингибируют: инсулин, НАДH+Н+ , АТФ.
Пища → ↑ инсулин → ↑ гликолиз → ↑ Ацетил-КоА → ↑ синтез малонил-КоА и
ЖК, ↑ малонил-КоА →↓ активность карнитинацилтрансферазы I в печени
→ ↓ транспорт ЖК в матрикс митохондрий → ↓ ЖК в матриксе → ↓ βокисление ЖК
32/Ж.В.
33.
6. Пластическое использование липидов.Гликолиз
Глюкоза
ПВК
6.1. Общая схема синтеза ВЖК (пальмитата)
НАДФН2
АцетилКоА/Ацил-КоА
Ацетил-КоА
Малонил-КоА
Синтаза ЖК
(Пальмитатсинтазный
Комплекс)
Пальмитиновая
кислота
33/Ж.В.
34.
глюкозагл-6ф
цитоплазма
пальмитат
НАДФ+
НАДФ
пальмитат синтаза инд. инсулин
+
НАДФН2
Малонил-КоА
ПФШ
фр-6ф
АДФ+Фн
НАДФН2
Ацетил-КоА карбоксилаза
СО2
пальмитоил-КоА,
HS-КоА адреналин,
АТФ глюкагон
АТФ
Ацетил-КоА
ПВК
НАДФН2 НАДФ+ НАДН+ НАДН2 АДФ+Фн
СО2
цитрат
малат
ЩУК
цитратлиаза
малик-фермент малат ДГ
инд. инсулин
ПВК
инд. инсулин
цитрат, инсулин
транслоказа
малат
митохондрия
ЩУК + Ацетил-КоА
цитрат синтаза
ЦТК
цитрат
6.1.1. Цитратмалатный
челночный
механизм
переноса
ацетила из
митохондрии
в циплазму
изоцитрат
НАДФ+
изоцитрат ДГ
инд. инсулин
НАДФН2
а-КГ
изоцитрат
изоцитрат ДГ
АТФ, НАДН2
Сукцинил-КоА
а-КГ ДГ
АТФ, НАДН2
а-КГ
34/Ж.В.
35.
6.1.2.Первая реакция синтеза ВЖК –образование малонил-КоААТФ
Ацетил-КоА
СО2
АДФ + Фн
Биотин
Малонил-КоА
Ацетил-КоА карбоксилаза
2 стадии: 1. СО2 + биотин + АТФ → биотин-СООН + АДФ + Фн
2. ацетил-КоА + биотин-СООН → малонил-КоА + биотин
+ Цитрат (положительный аллостерический эффектор)
+ Инсулин (в печени: активация путем дефосфорилирования фермента и индукция его
синтеза; в жировой ткани –активация фермента путем дефосфорилирования)
- Пальмитоил-КоА (отрицательный аллостерический эффектор)
- Адреналин, глюкагон (инактивация фермента путем его фосфорилирования)
35/Ж.В.
36.
Под действием инсулина впечени происходит индукция
синтеза ферментов
пальмитатсинтазного комплекса
36/Ж.В.
37.
6.1.3.Синтаза жирных кислотПолиферментный комплекс, катализирующий синтез жирных кислот
(цитозоль).
• Комплекс представляет собой димер, состоящий из двух идентичных
мономеров (субъединиц) А и Б.
• Мономеры А и Б в синтазном комплексе располагаются по принципу
«голова к хвосту».
• Мономеры А и Б в синтазном комплексе не являются функциональными
единицами.
• Каждый из мономеров включает 7 ферментов (7 активных центров),
катализирующих биосинтез ВЖК, а также ацилпереносящий белок
(АПБ).
37/Ж.В.
38.
Реакционно-способная НS-группа фосфопантетеина АПБ одногомономера находится в непосредственной близости от НS-группы
цистеина 3-кетоацилсинтазы другого мономера.
Поскольку для проявления синтазной активности необходимо участие
обеих HS-групп, то в состав функциональной единицы синтазного
комплекса входят фрагменты обоих мономеров (1 и 2).
При этом половина одного мономера А взаимодействует с
«комплементарной» половиной другого мономера Б.
38/Ж.В.
39.
Синтаза ЖК включает две функциональные единицы, поэтомуодновременно синтезируются две молекулы жирной кислоты.
Весь комплекс функционирует только в виде димера (Рис.1).
Роль: объединение всех ферментов синтеза ЖК в единый
полиферментный комплекс обеспечивает высокую
эффективность его работы и устраняет конкуренцию других
метаболических процессов, в результате чего достигается
эффект компартментализации.
39/Ж.В.
40.
40/Ж.В.41.
41/Ж.В.42.
42/Ж.В.43.
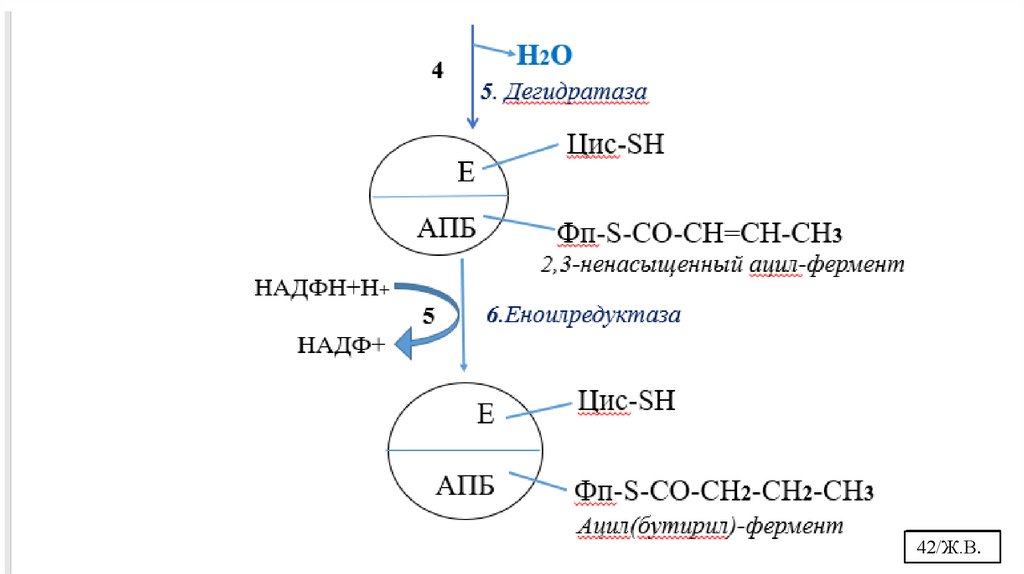
Первый цикл синтеза ВЖК завершается образованием ацила, состоящего изчетырех углеродных атомов (бутирила).
Далее трансацилазы переносят вновь образованный ацил от АПБ на HS-группу
цистеина 3-кетоацилсинтетазы, а новую молекулу малонил-КоА – на HSгруппу фосфопантетеина АПБ (реакция 1).
Затем последовательно осуществляются реакции 2,3,4,5 и образуется следующий
ацил, который длиннее предыдущего на два углеродных атома.
В результате семикратного повторения цикла от реакции 1 до реакции 5
образуется
молекула
пальмитоила
(С=16),
которая
высвобождается
из
синтазного комплекса седьмым ферментом – тиоэстеразой (деацилазой).
43/Ж.В.
44.
Источники, генерирующие НАДФН+Н+ для синтеза ВЖК• Пентозофосфатный цикл (ПФЦ)
• Изоцитратдегидрогеназа (цитозольная)
Малатдегидрогеназа («яблочный фермент»).
44/Ж.В.
45.
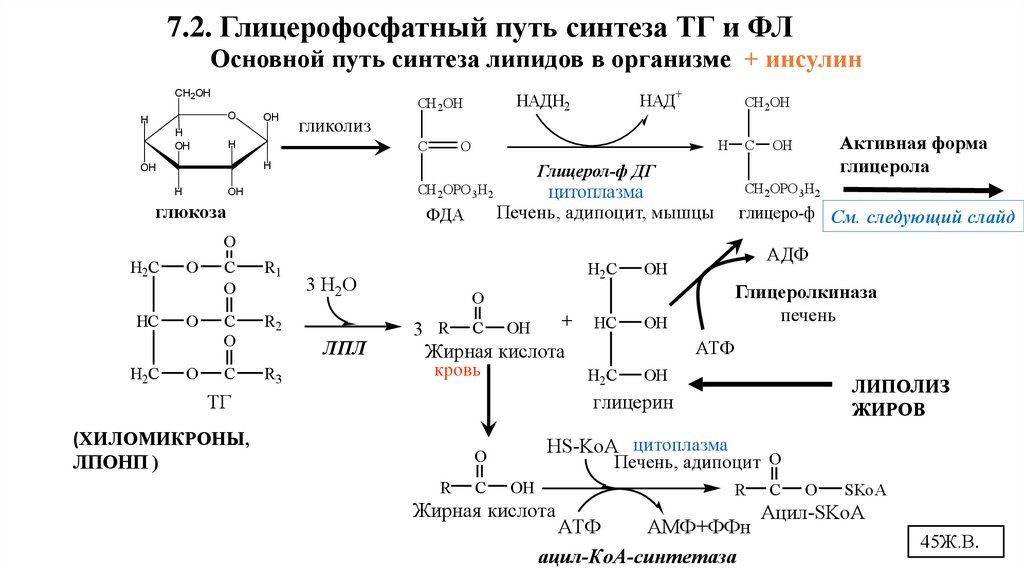
7.2. Глицерофосфатный путь синтеза ТГ и ФЛОсновной путь синтеза липидов в организме + инсулин
CH2OH
O
H
H
OH
OH
С
H
O
H
H
CH 2OH
гликолиз
H
OH
НАД+
НАДН2
CH 2OH
С
Глицерол-ф ДГ
CH 2OPO 3H2
OH
глюкоза
ФДА
CH 2OPO 3H2
цитоплазма
Печень, адипоцит, мышцы
глицеро-ф См. следующий слайд
O
H2C
HC
H2C
O
O
O
С
O
R1
С
O
R2
С
R3
ТГ
H2C
3 Н2О
ЛПЛ
АДФ
OH
Глицеролкиназа
печень
O
+ HC OH
3 R C OH
Жирная кислота
кровь
H2C
OH
глицерин
(ХИЛОМИКРОНЫ,
ЛПОНП )
C
АТФ
ЛИПОЛИЗ
ЖИРОВ
HS-KoA цитоплазма
O
R
Активная форма
глицерола
OH
Печень, адипоцит O
OH
Жирная кислота
R
АТФ
АМФ+ФФн
ацил-КоА-синтетаза
C
O
SKoA
Ацил-SKoA
45Ж.В.
46.
OCH 2OH
R-CO-SKoA
митохондрии
H
С
CH 2O
HS-KoA
OH
H
С
Ацилтрансфераза
CH 2OPO 3H2
C
OH
CH 2OPO 3H2
глицеро-ф
лизофосфатид
Активная форма глицерола
O
O
CH 2O
H
С
C
R
R-CO-SKoA
CH 2O
HS-KoA
OH
H
Ацилтрансфераза
CH 2OPO 3H2
С
С
R
O C
R
фосфатид
O C
R
O
C
O
CH 2OPO 3H2
R
фосфатид
O
H
C
O
CH 2OPO 3H2
лизофосфатид
CH 2O
R
Н2О
CH 2O
Н3РО4
+
фосфотидат
фосфогидролаза
H
С
C
O
R
O C
R
CH 2OH
1,2-ДГ
46/Ж.В.
47.
OCH 2O
H
C
O
C
O
R
O C
R
R-CO-SKoA
CH 2O
HS-KoA
H
Ацилтрансфераза
CH 2OH
ЦМФ
H2C
O
CH
O
C
H2 C
R2 C O CH
O
R1
R
C
R
O
Холинтрансфераза
ЦМФ
O C
O
ТГ
ЦДФ-холин
ЦДФэтаноламин
R
CH 2O
1,2-ДГ
R2 C O
C
C
O
O
O
C
R1
O
H2C O P O CH2CH2N(CH3)3
OH
O
H2C O P O CH2CH2NH2
OH
L –Фосфатидилэтаноламин
L –Фосфатидилхолин
(Лецитин)
47/Ж.В.
48.
7.3.48/Ж.В.
49.
7.4. Факторы, необходимые для синтеза ГФЛ в организме• Наличие незаменимых полиненасыщенных ВЖК.
• Наличие витаминов В12, В6, фолиевой кислоты, витаминоподобного
вещества инозитола.
• Наличие метионина, фосфосерина, фосфоэтаноламина, холина.
Вещества, участвующие в синтезе ГФЛ, называются липотропными
факторами, поскольку они препятствуют жировой инфильтрации
печени.
49/Ж.В.
50.
8. Рекомендованная литератураОсновная
1. Биохимия : учебник / под ред. Е.С. Северина. – М. : ГЭОТАР-Медиа, 2011. – С. 371–399.
2. Биохимия [Электронный ресурс] : учебник / под ред. Е.С. Северина. – 5-е изд., испр. и доп. – М. : ГЭОТАРМедиа, 2015. – http://www.studmedlib.ru / book / ISBN9785970433126.html (разд. 8, п. I–V; с. 371–399).
3. Биологическая химия. Биохимия полости рта : учебник / Т.П. Вавилова, А.Е. Медведев. – М. : ГЭОТАР-Медиа,
2014. – С. 279–307, 314–318.
4. Бологическая химия. Биохимия полости рта [Электронный ресурс]: учебник / Т.П. Вавилова, А.Е. Медведев. –
М. : ГЭОТАР-Медиа, 2014. – http://www.studmedlib.ru/book/ISBN9785970430392.html (ч. V, гл. 14; с. 279–307, 314–
318).
5. Обмен липидов. Биологические мембраны : учебно-методическое пособие к практическим и лабораторным
занятиям по биологической химии – биохимии полости рта для студентов стоматологических факультетов
медицинских вузов / под ред. Ж.В. Антоновой, Р.Н. Павловой, Л.Б. Гайковой. – СПб. : Изд-во СЗГМУ им.
И.И. Мечникова, 2020. – С. 32–42.
Дополнительная
6. Биологическая химия / Т.Т. Березов, Б.Ф. Коровкин. – М. : Медицина, 1998. – С. 363–381, 392–397.
7. Биологическое разнообразие кардиолипина и его ремоделирование при окислительном стрессе и возрастных
патологиях /Г.А. Шиловский, Т.С. Путятина, В.В. Ашапкин и др./ БИОХИМИЯ, 2019, том 84, вып. 12, с. 1815–1831
50/Ж.В.
51.
БЛАГОДАРЮ ЗА ВНИМАНИЕ!Пройдите тестирование
51/Ж.В.




































 Биология
Биология








