Похожие презентации:
Топливо (нефть, уголь и метан). Загрязнение воздуха, способы его предотвращения
1.
Ильина И.В., руководитель ЦДОШ, учитель химии МБОУ «Средняяобщеобразовательная школа №27 имени А.А. Дейнеки» г. Курска
E-mail мой: ilina.irina71@mail.ru
2.
Проверим домашнее заданиеПоставь рядом с высказыванием +, если оно верно, и- ,
если в нём есть ошибка.
1. Оксиды – это сложные вещества, состоящие из двух
химических элементов, один из которых кислород.
2. Валентность кислорода равна двум.
4. Вода на Земле встречается только в двух агрегатных
состояниях: жидкая вода и водяной пар.
5. Кислород не имеет цвета, вкуса и запаха, немного
растворим в воде, тяжелее воздуха.
6. Увеличение количества углекислого газа в атмосфере
ведёт к возникновению парникового эффекта.
7. Углекислый газ поддерживает горение
3.
ОПРЕДЕЛИ ТИП ХИМИЧЕСКИХ РЕАКЦИЙ!НАЙДИ ОШИБКУ!
• 2Cr + Cl2 = 2CrCl3
• NaOH + HCl = NaCl + H2O
• СaO + CO2 = CaCO3
• AgNO3 + NaCl = AgCl + NaNO3
• Мg(OH)2 = MgO + H2O
• CuSO4 + Fe = FeSO4 + Cu
• PbCl4 = PbCl2 + Cl2
• Zn + HCl = ZnCl2 + H2
4.
Топливо (нефть, уголь и метан).Загрязнение воздуха, способы его
предотвращения.
5.
ВИДЫ ТОПЛИВАТвёрдое (Ископаемый уголь, торф,
древесина, горючие сланцы)
Жидкое (Бензин, мазут, керосин)
Газообразное (Природный газ,
промышленные горючие газы)
-А какое топливо использует наша местность?
6.
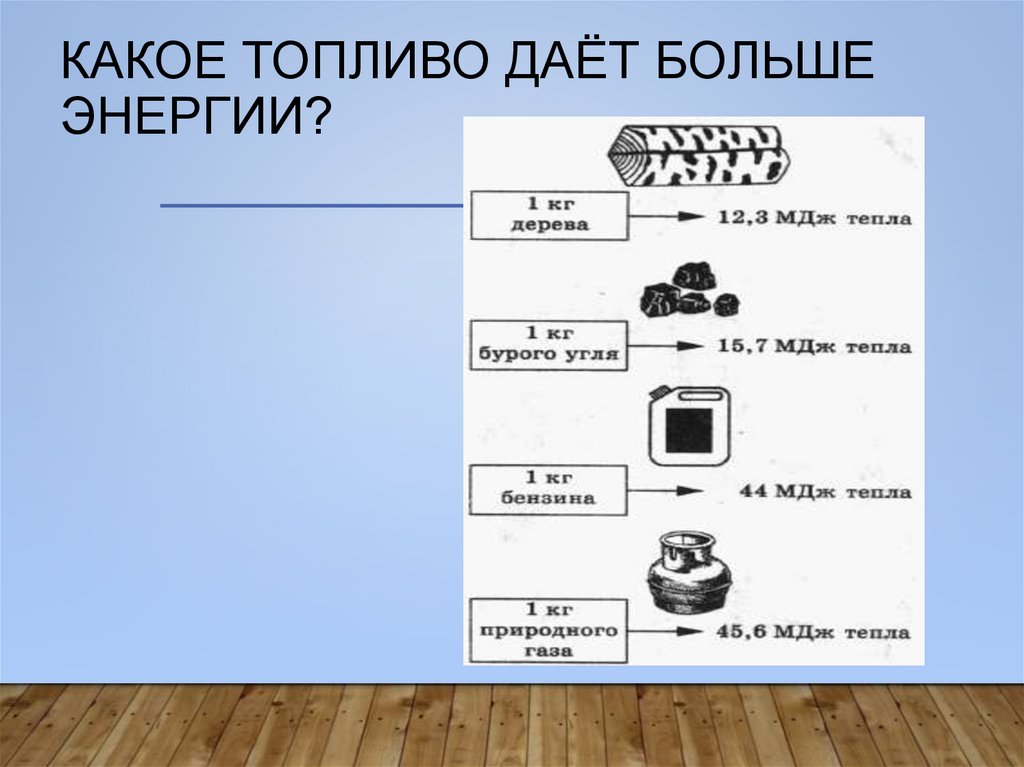
КАКОЕ ТОПЛИВО ДАЁТ БОЛЬШЕЭНЕРГИИ?
7.
ЗАПИШИТЕ РЕАКЦИИ ГОРЕНИЯМЕТАНА
И
ГЕКСАНА
И
РАССТАВЬТЕ КОЭФФИЦИЕНТЫ
СН4 + О2 →
C6H14 + O2 →
8.
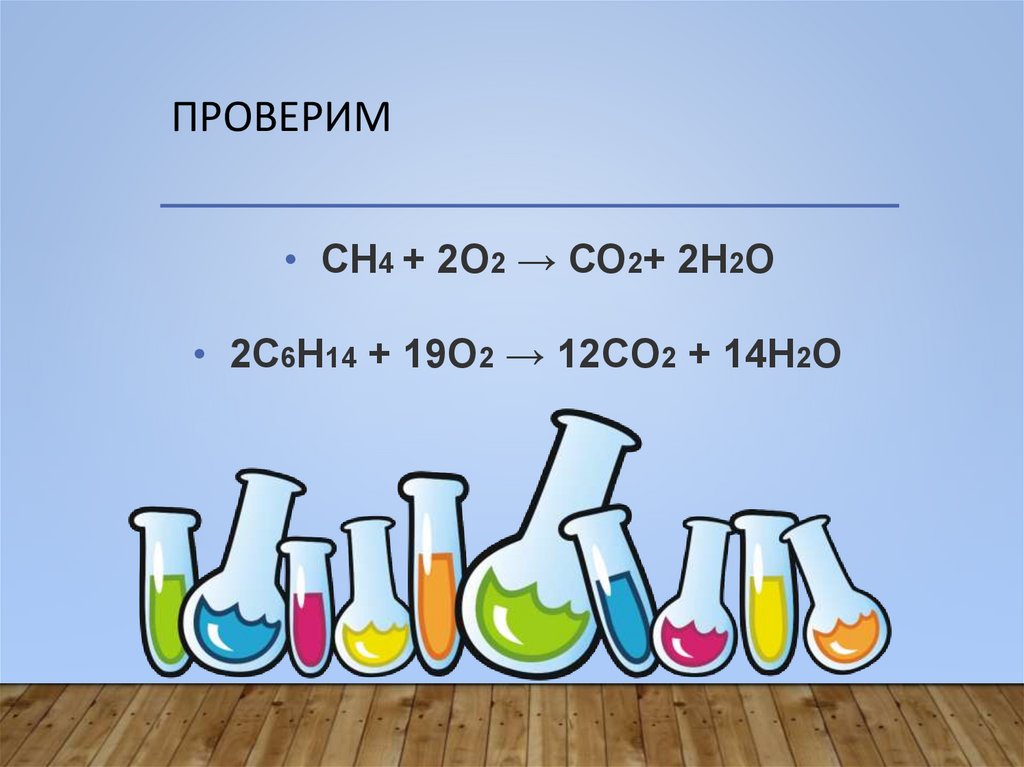
ПРОВЕРИМ• СН4 + 2О2 → СО2+ 2Н2О
• 2C6H14 + 19O2 → 12CO2 + 14H2O
9.
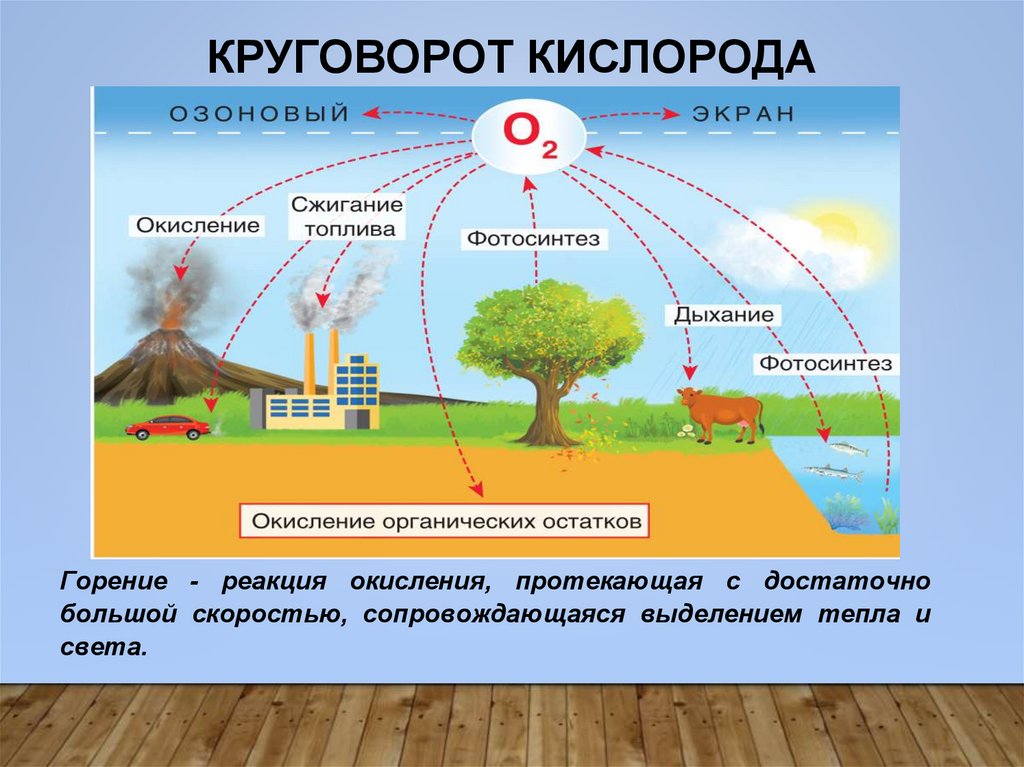
КРУГОВОРОТ КИСЛОРОДАГорение - реакция окисления, протекающая с достаточно
большой скоростью, сопровождающаяся выделением тепла и
света.
10.
11.
12.
13.
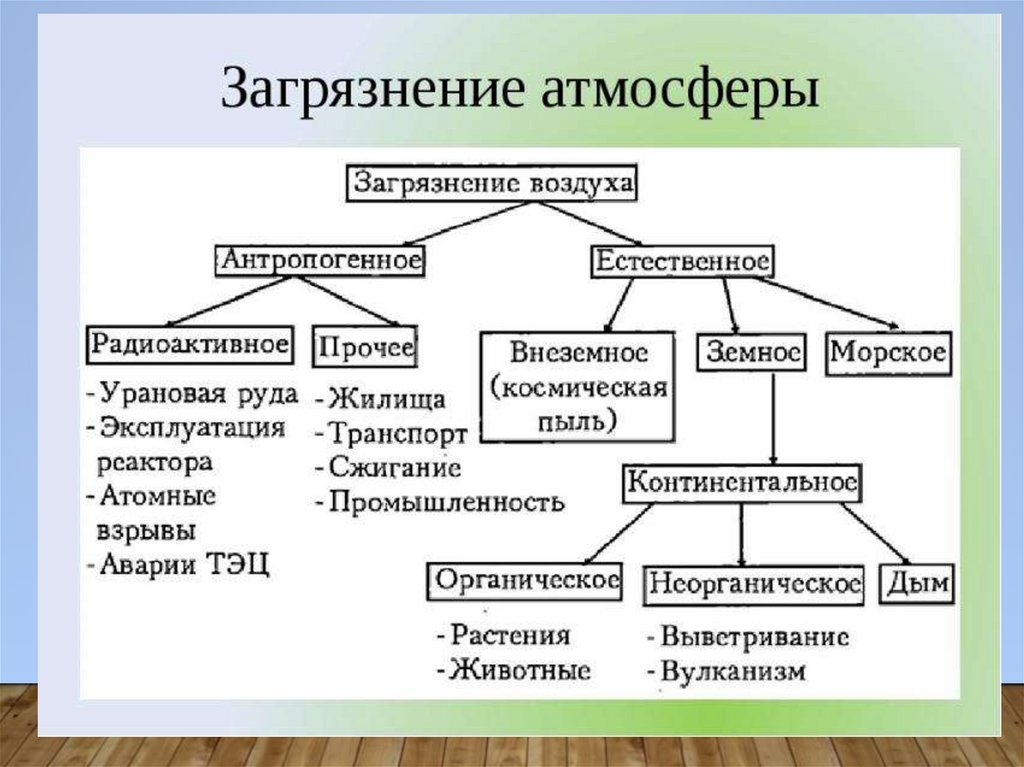
СИТУАЦИОННАЯ ЗАДАЧАК загрязнениям атмосферы относят накопление в
воздухе пыли (твердых частиц). Она образуется при
сжигании
твердого
топлива,
при
переработке
минеральных веществ и в ряде других случаев.
Атмосфера над сушей загрязнена в 15-20 раз больше,
чем над океаном, над небольшим городом в 30-35 раз,
а над большим мегаполисом в 60-70 раз больше.
Пылевое загрязнение атмосферы несет вредные
последствия для здоровья человека.
Почему?
14.
СИТУАЦИОННАЯ ЗАДАЧАВ большую открытую ёмкость поместили свечу и
зажгли её. Свеча горела нормально. Затем вокруг
края сосуда поместили кольцо из ваты и
подожгли её. Вата загорелась, и через несколько
секунд свеча погасла. Объясните, почему погасло
пламя свечи?
Направление поиска. Вспомните условия, при
которых горение прекращается.
15.
ОТВЕТЬТЕ НА ВОПРОСЫ1. Что относится к горючим полезным ископаемым?
2. Что такое уголь? Каких видов он бывает? Как его
используют?
3. Что такое нефть? Какие продукты получают из нефти
и где их применяют?
4. Что такое природный газ? Как он образуется?
5. Опишите круговорот кислорода в природе.
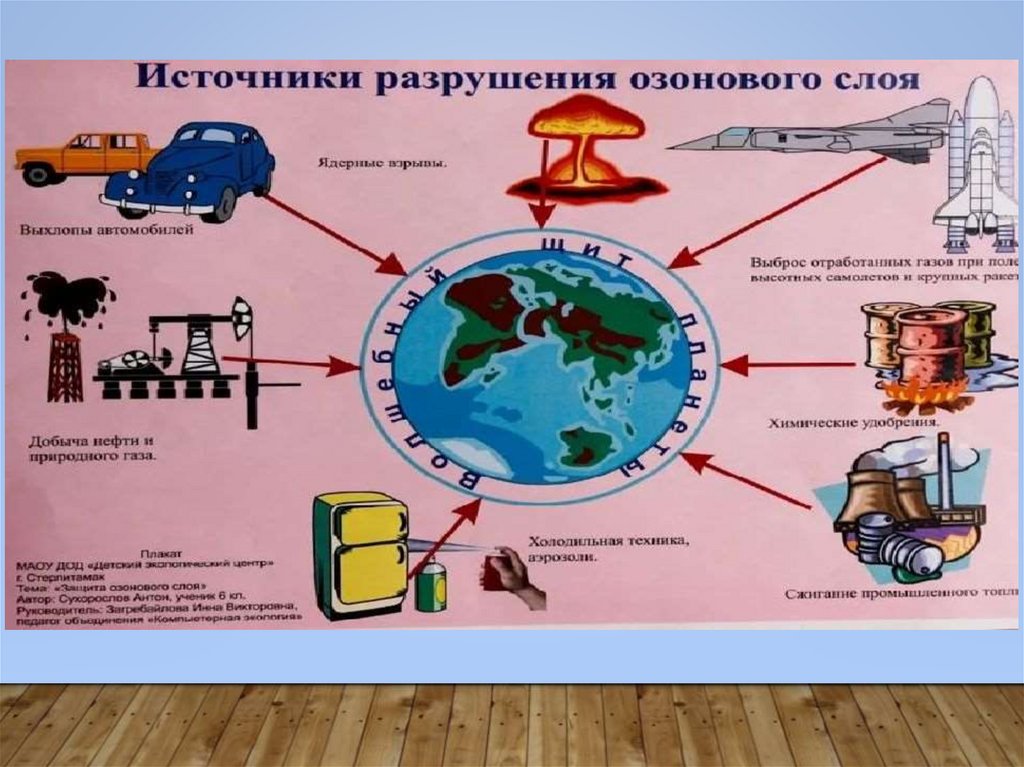
6. Выпишите источники разрушения озонового слоя.
16.
ДОМАШНЕЕ ЗАДАНИЕ1. Повторить параграфы 12 и 13
2. Задача №1 (из презентации)
3. Упражнения 1 и 2 (из презентации)
Пишите в электронный журнал или на мою почту.
E-mail мой: ilina.irina71@mail.ru
17.
ДОМАШНЕЕ ЗАДАНИЕЗадача 1. Напишите термохимическое уравнение
реакции, если сгорело 54 г углерода, а в результате
горения выделилось 2050 кДж теплоты.
Упражнение 1. Из приведенных ниже формул веществ
выпишите только формулы оксидов и дайте им
названия: NaOH, PH3, CuO, HCl, Al2O3, CaBr2, MnO,
SiH4, Mn2O7, N2O, NH3, H2SO4, CaO.
Упражнение 2. Закончите уравнения химических
реакций (сера в уравнении 4 проявляет валентность
IV), расставьте коэффициенты, назовите продукты:
1) P + O2→ ? 2) AI+ O2→ ?
3) C+ O2→ ?
4) S+ O2→ ?
5) Zn + O2→?












 Химия
Химия








