Похожие презентации:
Классификация химических реакций в органической химии
1.
КЛАССИФИКАЦИЯ ХИМИЧЕСКИХРЕАКЦИЙ В ОРГАНИЧЕСКОЙ
ХИМИИ
Подготовили студентки
214 группы
Набиуллина Гулия,
Петрова Злата,
Протасова Варвара
Шарипова Саида
2.
Классификация химических реакций в органической химии сложнее, чем внеорганической, поскольку она учитывает не только типы реагирующих веществ и
продуктов, но и изменения в углеродном скелете молекул и функциональных группах.
• ОРГАНИЧЕСКАЯ ХИМИЯ – ХИМИЯ УГЛЕРОДСОДЕРЖАЩИХ
СОЕДИНЕНИЙ.
• СЛОЖНОСТЬ ОРГАНИЧЕСКИХ МОЛЕКУЛ ТРЕБУЕТ
МНОГООБРАЗНЫХ ПОДХОДОВ К КЛАССИФИКАЦИИ
РЕАКЦИЙ.
• КРИТЕРИИ КЛАССИФИКАЦИИ: ТИП РАЗРЫВА СВЯЗЕЙ, ТИП
РЕАГИРУЮЩИХ ЧАСТИЦ, ИЗМЕНЕНИЯ В УГЛЕРОДНОМ
СКЕЛЕТЕ, ИЗМЕНЕНИЯ ФУНКЦИОНАЛЬНЫХ ГРУПП, УСЛОВИЯ
ПРОВЕДЕНИЯ РЕАКЦИИ.
• МНОГИЕ РЕАКЦИИ МОГУТ ОТНОСИТЬСЯ К НЕСКОЛЬКИМ
КЛАССАМ ОДНОВРЕМЕННО.
3.
ПО ТИПУ РАЗРЫВА И ОБРАЗОВАНИЯСВЯЗЕЙ:
• Гомолитический разрыв:
Ковалентная связь разрывается симметрично,
каждый атом получает по одному электрону,
образуя свободные радикалы. Типичные
реакции: галогенирование алканов,
автоокисление.
Примеры: галогенирование алканов.
• Гетеролитический разрыв:
. Ковалентная связь разрывается асимметрично,
один атом получает оба электрона, образуя
катионы и анионы (или ионы с разделением
заряда). Типичные реакции: нуклеофильное
замещение, электрофильное присоединение
4.
ПО ТИПУ РЕАГИРУЮЩИХ ЧАСТИЦ:• Реакции нуклеофильного замещения (SN): нуклеофил (частица с неподеленной электронной парой)
атакует электрофильный центр (атом с частичным или полным положительным зарядом), замещая уходящую
группу. Разделяются на SN1 (двухстадийный механизм) и SN2 (одностидийный механизм).
Примеры: реакция алкилгалогенида с гидроксид-ионом.
• Реакции электрофильного замещения (SE): электрофил (частица с недостатком электронов) атакует
электронобогатый центр (например, ароматическое кольцо), замещая атом или группу атомов.
Примеры: нитрование бензола.
• Реакции электрофильного присоединения (AE): электрофил атакует кратную связь (двойную или тройную),
приводя к образованию новых σ-связей.
Примеры: галогенирование алкенов.
• Реакции нуклеофильного присоединения: нуклеофил атакует кратную связь, приводя к образованию
новых σ-связей.
Примеры: присоединение цианид-иона к альдегиду.
• Реакции свободнорадикального замещения: свободные радикалы замещают атомы в молекуле.
Примеры: хлорирование метана
• Реакции конденсации: две или более молекулы соединяются с выделением побочного продукта
(часто воды).
Примеры: образование сложных эфиров.
• Реакции присоединения: две или более молекулы соединяются без выделения побочного продукта.
Примеры: гидрирование алкенов.
5.
ПО ИЗМЕНЕНИЮ УГЛЕРОДНОГО СКЕЛЕТА• ЗАМЕЩЕНИЕ: ЗАМЕНА АТОМА ИЛИ ГРУППЫ АТОМОВ. ПРИМЕРЫ:
ГАЛОГЕНИРОВАНИЕ АЛКАНОВ.
• ПРИСОЕДИНЕНИЕ: ДОБАВЛЕНИЕ АТОМОВ ИЛИ ГРУПП К МОЛЕКУЛЕ.
ПРИМЕРЫ: ГИДРИРОВАНИЕ АЛКЕНОВ.
• ОТЩЕПЛЕНИЕ (ЭЛИМИНИРОВАНИЕ): УДАЛЕНИЕ АТОМОВ ИЛИ ГРУПП
АТОМОВ. ПРИМЕРЫ: ДЕГИДРАТАЦИЯ СПИРТОВ.
• ПЕРЕГРУППИРОВКА (ИЗОМЕРИЗАЦИЯ): ИЗМЕНЕНИЕ СТРУКТУРЫ
МОЛЕКУЛЫ БЕЗ ИЗМЕНЕНИЯ СОСТАВА. ПРИМЕРЫ: ПЕРЕГРУППИРОВКА
КЛЯЙЗЕНА.
6.
ПО ИЗМЕНЕНИЮ ФУНКЦИОНАЛЬНЫХГРУПП
• Окисление: Увеличение степени окисления атома углерода.
Примеры: окисление спирта в альдегид.
• Восстановление: Уменьшение степени окисления атома
углерода.
Примеры: восстановление кетона в спирт.
• Гидролиз: Разложение вещества под действием воды.
Примеры: гидролиз сложного эфира.
• Галогенирование: Замена атома водорода на атом галогена.
• Нитрование: Замена атома водорода на нитрогруппу
7.
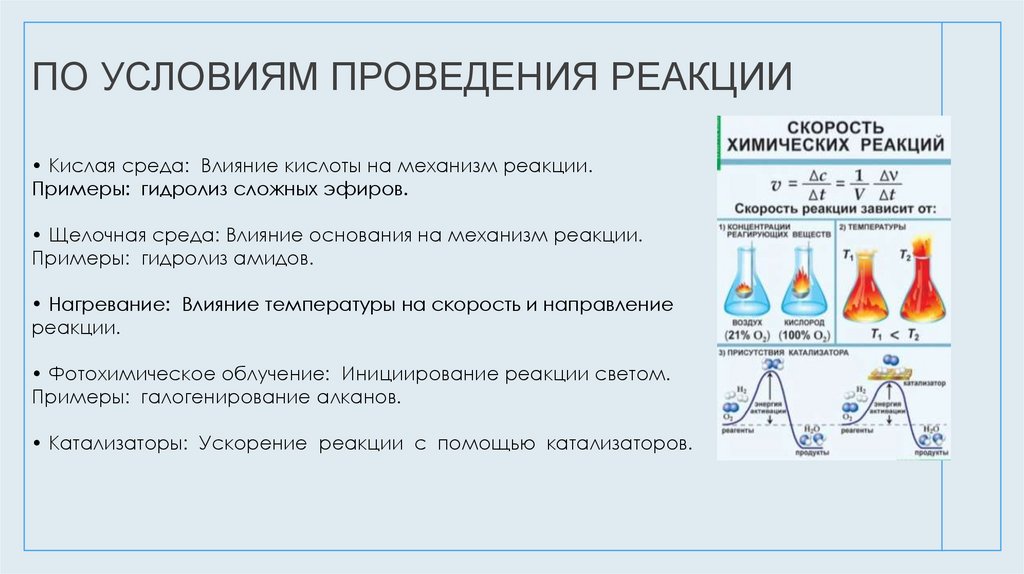
ПО УСЛОВИЯМ ПРОВЕДЕНИЯ РЕАКЦИИ• Кислая среда: Влияние кислоты на механизм реакции.
Примеры: гидролиз сложных эфиров.
• Щелочная среда: Влияние основания на механизм реакции.
Примеры: гидролиз амидов.
• Нагревание: Влияние температуры на скорость и направление
реакции.
• Фотохимическое облучение: Инициирование реакции светом.
Примеры: галогенирование алканов.
• Катализаторы: Ускорение реакции с помощью катализаторов.
8.
ЗАКЛЮЧЕНИЕКЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ В ОРГАНИЧЕСКОЙ ХИМИИ – ЭТО СЛОЖНАЯ, НО НЕОБХОДИМАЯ СИСТЕМА ДЛЯ
СИСТЕМАТИЗАЦИИ ОГРОМНОГО КОЛИЧЕСТВА ПРЕВРАЩЕНИЙ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ. ОТСУТСТВИЕ ЕДИНОЙ,
УНИВЕРСАЛЬНОЙ КЛАССИФИКАЦИИ ОБУСЛОВЛЕНО МНОГООБРАЗИЕМ ОРГАНИЧЕСКИХ МОЛЕКУЛ И МЕХАНИЗМОВ ИХ
ВЗАИМОДЕЙСТВИЙ. РАЗЛИЧНЫЕ ПОДХОДЫ К КЛАССИФИКАЦИИ (ПО ТИПУ РАЗРЫВА СВЯЗЕЙ, РЕАГИРУЮЩИМ ЧАСТИЦАМ,
ИЗМЕНЕНИЯМ В УГЛЕРОДНОМ СКЕЛЕТЕ И ФУНКЦИОНАЛЬНЫХ ГРУППАХ, УСЛОВИЯМ РЕАКЦИИ) ВЗАИМОДОПОЛНЯЮТ
ДРУГ ДРУГА И ПОЗВОЛЯЮТ БОЛЕЕ ГЛУБОКО ПОНЯТЬ СУТЬ ХИМИЧЕСКИХ ПРЕВРАЩЕНИЙ. ВАЖНО ПОМНИТЬ, ЧТО МНОГИЕ
РЕАКЦИИ МОГУТ БЫТЬ ОТНЕСЕНЫ К НЕСКОЛЬКИМ КЛАССАМ ОДНОВРЕМЕННО, И ДЛЯ ПОЛНОГО ПОНИМАНИЯ
НЕОБХОДИМО УЧИТЫВАТЬ МЕХАНИЗМ РЕАКЦИИ.







 Химия
Химия








