Похожие презентации:
Биологическая химия-биохимия полости рта
1.
СЗГМУ им. И. И. МЕЧНИКОВАКафедра клинической лабораторной диагностики,
биологической и общей химии им. В. В. Соколовского
БИОЛОГИЧЕСКАЯ ХИМИЯ-БИОХИМИЯ ПОЛОСТИ РТА
Разделы VI-VII
ЛЕКЦИЯ
АНАЭРОБНОЕ И АЭРОБНОЕ ДИХОТОМИЧЕСКОЕ
ОКИСЛЕНИЕ ГЛЮКОЗЫ. ГЛЮКОНЕОГЕНЕЗ.
Доцент Антонова Ж.В. Доцент Павлова Р.Н.
2024/2025
2.
План лекции1. Пути использования глюкозы.
2. Анаэробное окисление глюкозы. (2.1. Гликогенолиз; 2.2.Гликолиз)
3. Расчет количества АТФ при анаэробном гликолизе / гликогенолизе.
4. Биологическая роль анаэробного окисления глюкозы. 4.1. Регуляция.
5. Этапы аэробного окисление глюкозы.
5.1. Первый этап – гликолитический
5.2. Второй этап – окислительное декарбоксилирование ПВК
5.3. ЦТК
6. Биологическая роль ЦТК
7. Ингибиторы ЦТК
8.Расчет количества АТФ при аэробном окислении глюкозы (баланс)
9. Схема глюконеогенеза. (9.1.Обходные реакции гликолиза)
10. Биологическая роль и регуляция глюконеогенеза.
2/Ж.В.
3.
Условные обозначенияМКМ – межклеточный матрикс
СОПР – слизистая оболочка полости рта
АОС – антиоксидантная система
МОС – монооксигеназная система
ПФЦ – пентозофосфатный цикл
АЦ – активный центр
1,3-ДФГ- 1,3-дифосфоглицерат
ФЕП – фосфоенолпируват
ПВК-пировиноградная кислота
3-ФГА – 3-фосфоглицериновый альдегид
ПДК – пируватдегидрогеназный комплекс
3/Ж.В.
4.
1. Пути использования глюкозы1. Энергетическое (анаэробное и аэробное окисление глюкозы)*
2. Пластическое использование глюкозы: а) моно и олигосахариды - компоненты
мембранных гликолипидов (цереброзидов и ганглиозидов); б ) моносахариды являются
компонентами глюкозаминогликанов (гетерополисахаридов), входящих в состав
протеогликанов синовиальной жидкости, различных видов соединительной ткани, в том
числе хрящевой, костной, зубных тканей (цемент, дентин, пульпа), периодонта, СОПР и
др.; в) моно- и олигосахариды входят в состав гликопротеинов, к которым относятся
многие ферменты, большинство белков слюны (муцины, лактоферрин и др.), белки МКМ
минерализованных тканей, белки-транспортеры, рецепторы, гормоны и т.д.; г)
производные глюкозы – глюкурониды - участвуют в процессах детоксикации
ксенобиотиков и эндогенных метаболитов; в) продукты пентозо-фосфатного цикла –
пентозы- используются для синтеза различных нуклеотидов, а НАДФН+Н+ выполняет
коферментную функцию в реакциях синтеза, работе АОС, МОС.
3. Резервная функция(синтез гликогена в печени и мышцах).
3/Ж.В.
*Примеч.: до 70% нужд человека в энергии обеспечивается за счет окисления глюкозы.
5.
2. Анаэробное окисление глюкозы(гликогенолиз и гликолиз)
Энергетическое использование глюкозы клеткой в процессе ее
окисления происходит в анаэробных и аэробных условиях.
Способ расщепления молекулы глюкозы (С6) на две равные
по количеству углеродов части- две триозы (2С3)- называется
дихотомическое расщепление.*
*Примеч.: по способу расщепления молекулы глюкозы существует еще
апотомическое расщепление (С6 расщепляется на СО2 + С5-пентозу),
имеющее пластическую роль (ПФЦ)
5/Ж.В.
6.
2.1. Гликогенолиз - ферментативное анаэробное окисление долактата, которое начинается с гликогена.
Н3РО4
гликоген → глюкозо-1-фосфат → глюкозофо-6-фосфат
гликогенфосфорилаза
реакции гликолиза
фосфоглюкомутаза
2 пируват
2 лактат
Гликогенфосфорилаза при участии фосфорной кислоты (фосфоролиз)
последовательно расщепляет линейные α – 1,4-гликозидные связи на
невосстанавливающем конце молекулы гликогена с образованием гл-1-фосфата,
который переходит в гл-6-фосфат. В мышцах и клетках мозга нет глюкозо-6фосфатазы, поэтому гл-6-фосфат вступает в реакции окисления глюкозы, т.е. от
глюкозо-6-фосфата гликолиз и гликогенолиз протекают одинаково.
Ферменты этих процессов расположены в цитоплазме.
Гликогенфосфорилаза активируется гормонами адреналином и глюкагоном.
6/Ж.В.
7.
2.2. Гликолиз – это ферментативное анаэробное дихотомическоеокисление глюкозы до лактата с образованием АТФ путем субстратного
фосфорилирования.
В гликолизе выделяют 2 стадии:
1-я стадия – подготовительная (идет до образования 2-х триоз)
в реакциях 1-й стадии используется 2 молекулы АТФ
молекула глюкозы (гексозы) дихотомическ расщепляется на 2 триозы
окислительно-восстановительных реакций в эту стадию нет, идет
подготовка субстрата для них.
2-я стадия - гликолитическая оксидоредукция
в ходе 2-й стадии идут окислительно-восстановительные реакции
образуется АТФ путем субстратного фосфорилирования
7/Ж.В.
8.
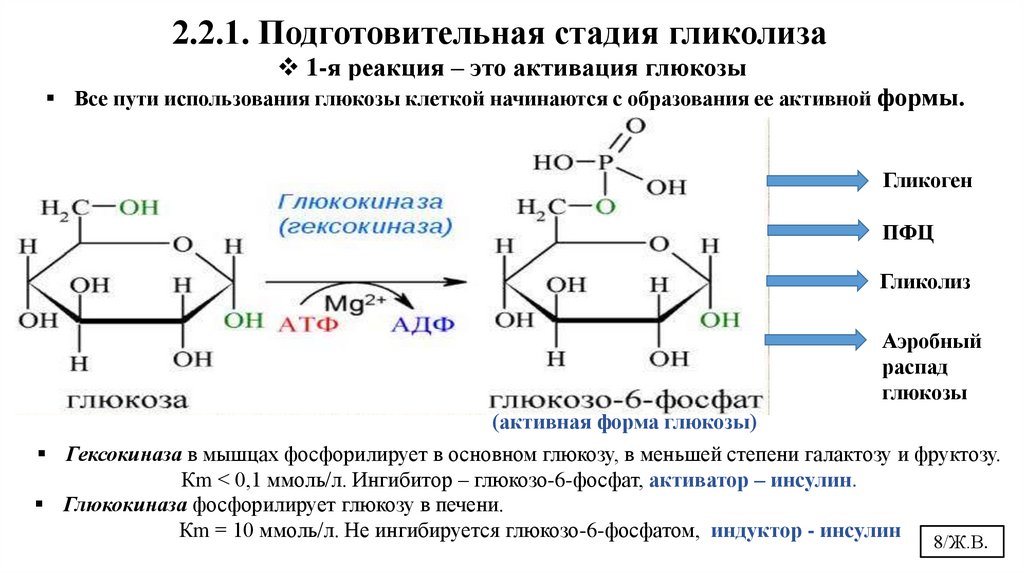
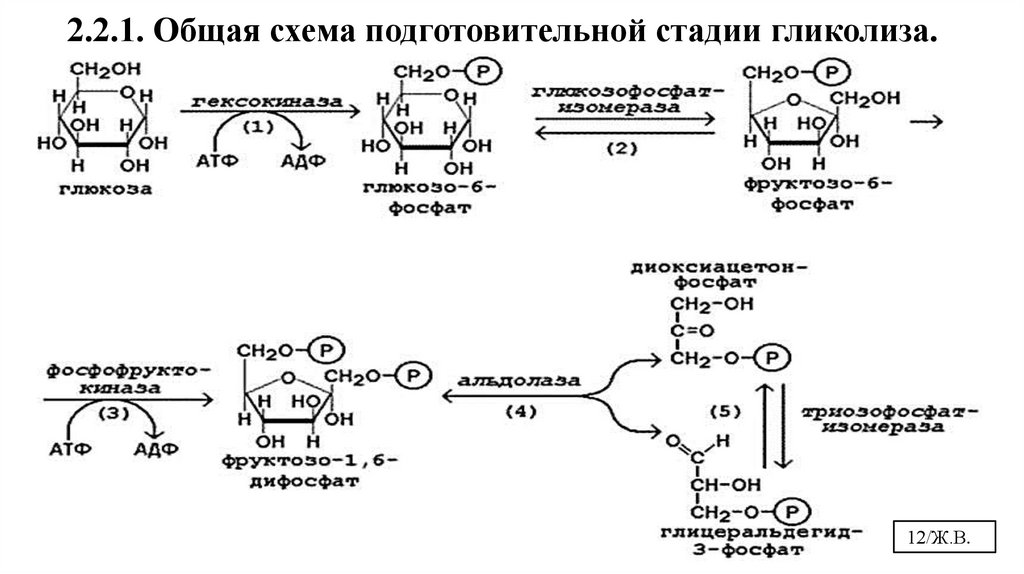
2.2.1. Подготовительная стадия гликолиза1-я реакция – это активация глюкозы
Все пути использования глюкозы клеткой начинаются с образования ее активной формы.
Гликоген
ПФЦ
Гликолиз
Аэробный
распад
глюкозы
(активная форма глюкозы)
Гексокиназа в мышцах фосфорилирует в основном глюкозу, в меньшей степени галактозу и фруктозу.
Кm < 0,1 ммоль/л. Ингибитор – глюкозо-6-фосфат, активатор – инсулин.
Глюкокиназа фосфорилирует глюкозу в печени.
Кm = 10 ммоль/л. Не ингибируется глюкозо-6-фосфатом, индуктор - инсулин
8/Ж.В.
9.
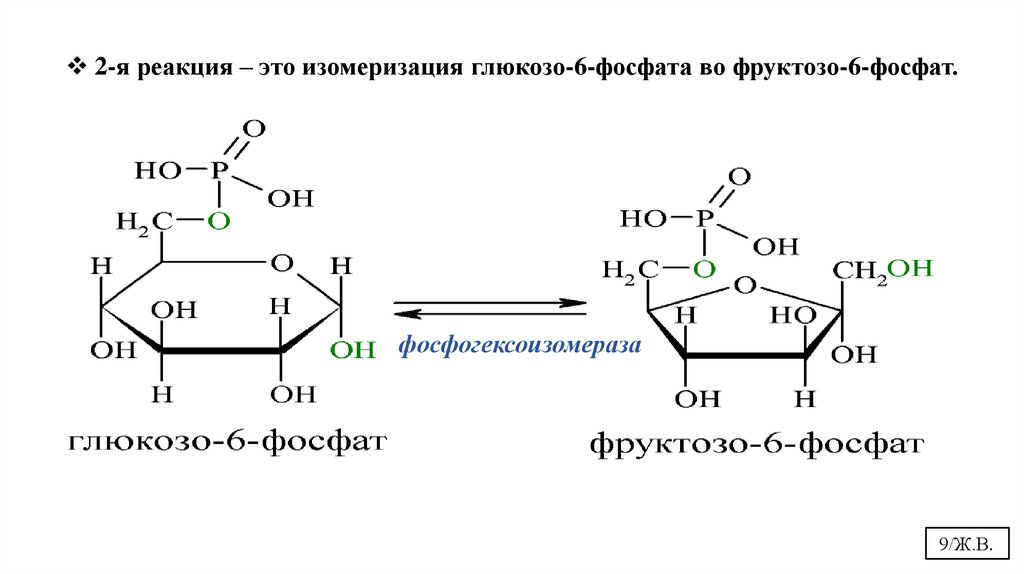
2-я реакция – это изомеризация глюкозо-6-фосфата во фруктозо-6-фосфат.фосфогексоизомераза
9/Ж.В.
10.
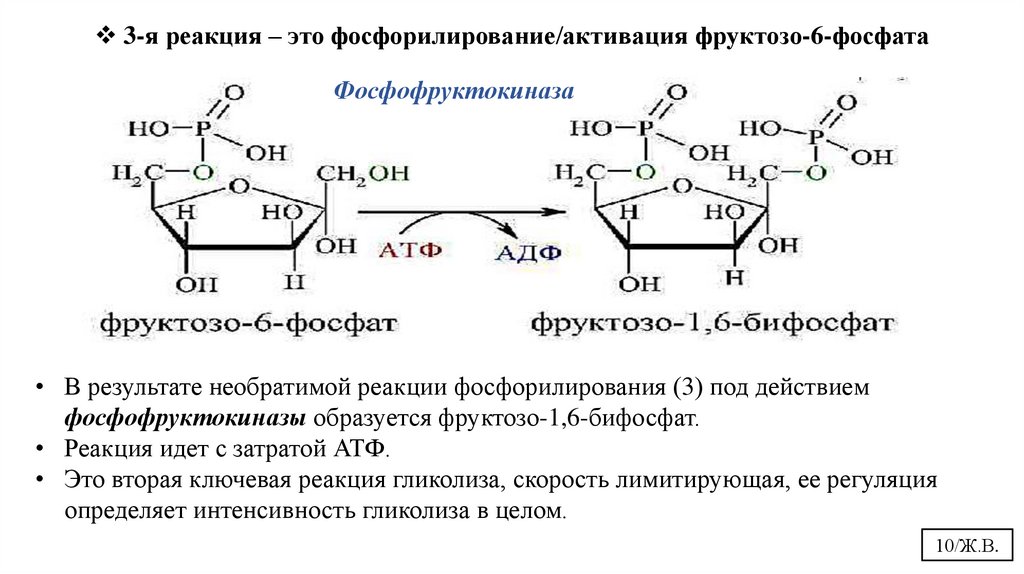
3-я реакция – это фосфорилирование/активация фруктозо-6-фосфатаФосфофруктокиназа
• В результате необратимой реакции фосфорилирования (3) под действием
фосфофруктокиназы образуется фруктозо-1,6-бифосфат.
• Реакция идет с затратой АТФ.
• Это вторая ключевая реакция гликолиза, скорость лимитирующая, ее регуляция
определяет интенсивность гликолиза в целом.
10/Ж.В.
11.
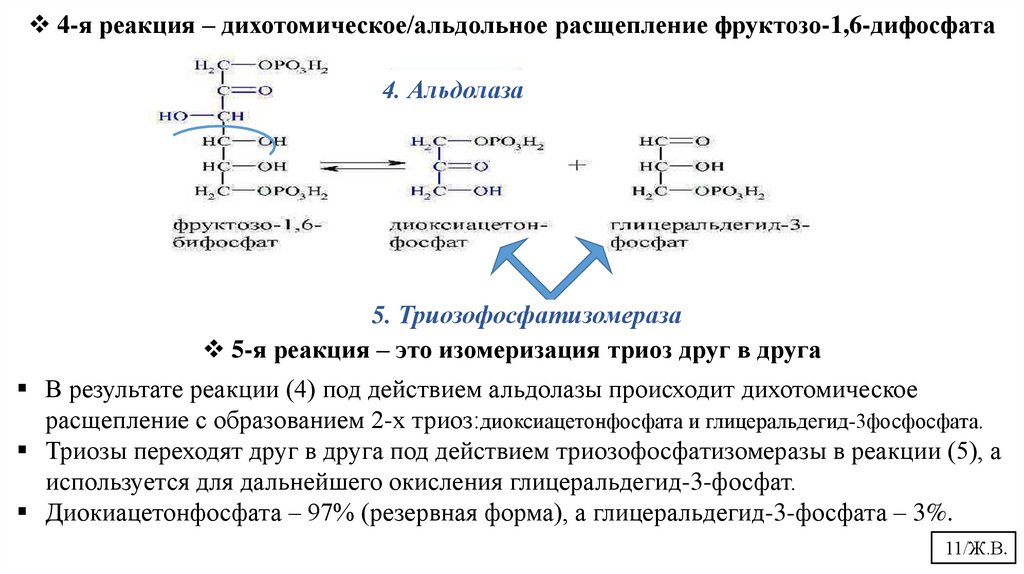
4-я реакция – дихотомическое/альдольное расщепление фруктозо-1,6-дифосфата4. Альдолаза
5. Триозофосфатизомераза
5-я реакция – это изомеризация триоз друг в друга
В результате реакции (4) под действием альдолазы происходит дихотомическое
расщепление с образованием 2-х триоз:диоксиацетонфосфата и глицеральдегид-3фосфосфата.
Триозы переходят друг в друга под действием триозофосфатизомеразы в реакции (5), а
используется для дальнейшего окисления глицеральдегид-3-фосфат.
Диокиацетонфосфата – 97% (резервная форма), а глицеральдегид-3-фосфата – 3%.
11/Ж.В.
12.
2.2.1. Общая схема подготовительной стадии гликолиза.12/Ж.В.
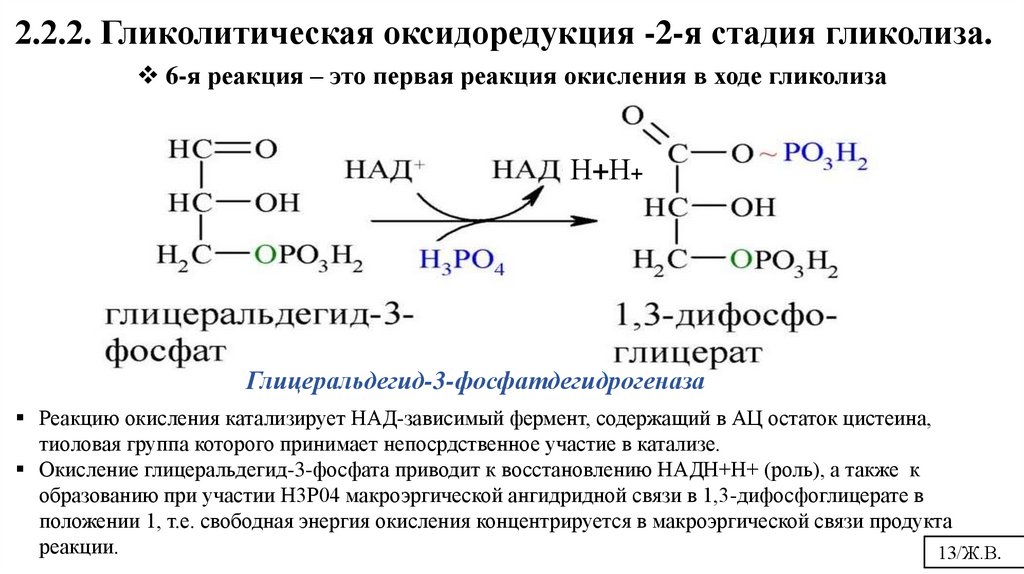
13.
2.2.2. Гликолитическая оксидоредукция -2-я стадия гликолиза.6-я реакция – это первая реакция окисления в ходе гликолиза
Н+Н+
Глицеральдегид-3-фосфатдегидрогеназа
Реакцию окисления катализирует НАД-зависимый фермент, содержащий в АЦ остаток цистеина,
тиоловая группа которого принимает непосрдственное участие в катализе.
Окисление глицеральдегид-3-фосфата приводит к восстановлению НАДН+Н+ (роль), а также к
образованию при участии Н3Р04 макроэргической ангидридной связи в 1,3-дифосфоглицерате в
положении 1, т.е. свободная энергия окисления концентрируется в макроэргической связи продукта
реакции.
13/Ж.В.
14.
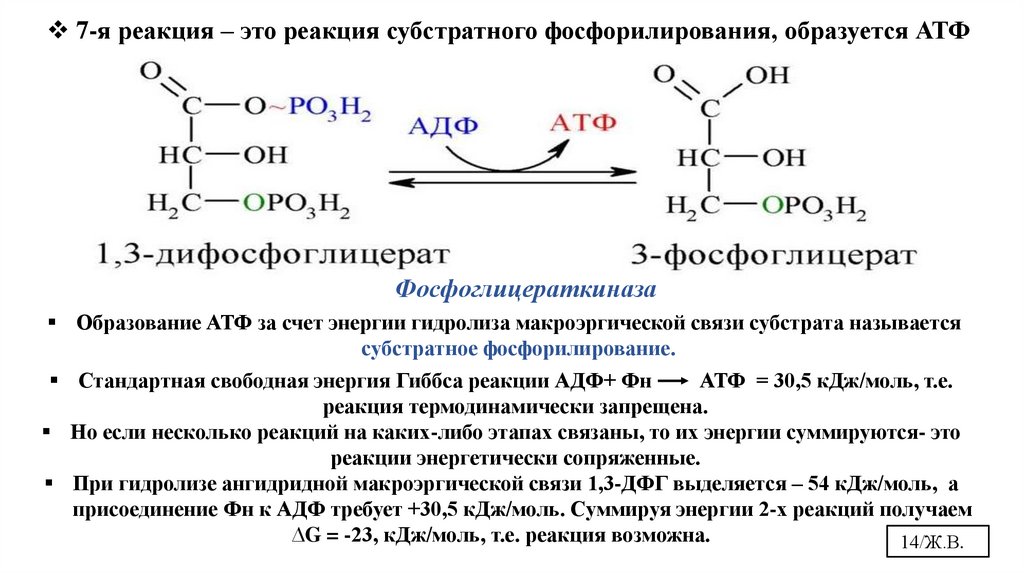
7-я реакция – это реакция субстратного фосфорилирования, образуется АТФФосфоглицераткиназа
Образование АТФ за счет энергии гидролиза макроэргической связи субстрата называется
субстратное фосфорилирование.
Стандартная свободная энергия Гиббса реакции АДФ+ Фн
АТФ = 30,5 кДж/моль, т.е.
реакция термодинамически запрещена.
Но если несколько реакций на каких-либо этапах связаны, то их энергии суммируются- это
реакции энергетически сопряженные.
При гидролизе ангидридной макроэргической связи 1,3-ДФГ выделяется – 54 кДж/моль, а
присоединение Фн к АДФ требует +30,5 кДж/моль. Суммируя энергии 2-х реакций получаем
∆G = -23, кДж/моль, т.е. реакция возможна.
14/Ж.В.
15.
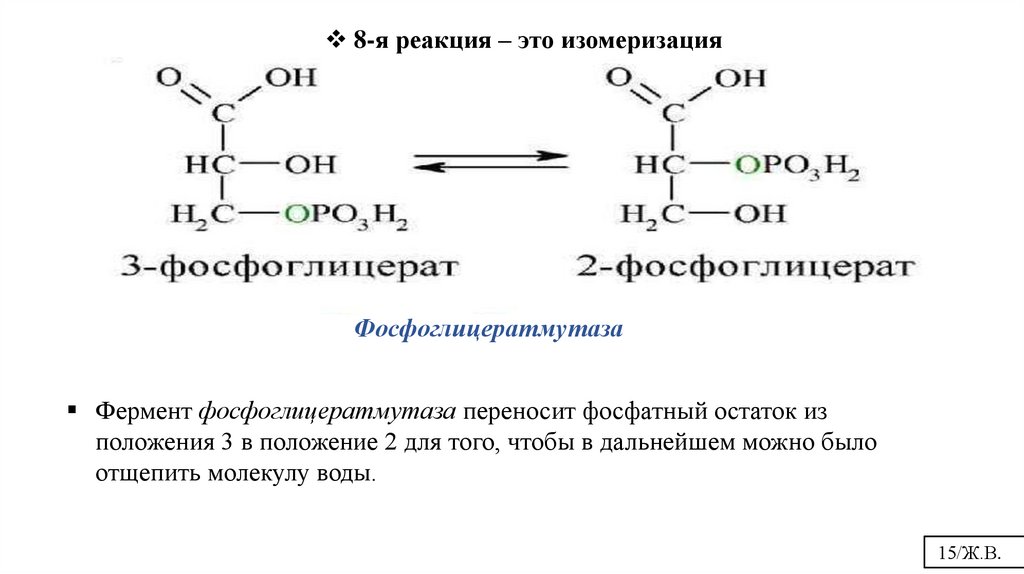
8-я реакция – это изомеризацияФосфоглицератмутаза
Фермент фосфоглицератмутаза переносит фосфатный остаток из
положения 3 в положение 2 для того, чтобы в дальнейшем можно было
отщепить молекулу воды.
15/Ж.В.
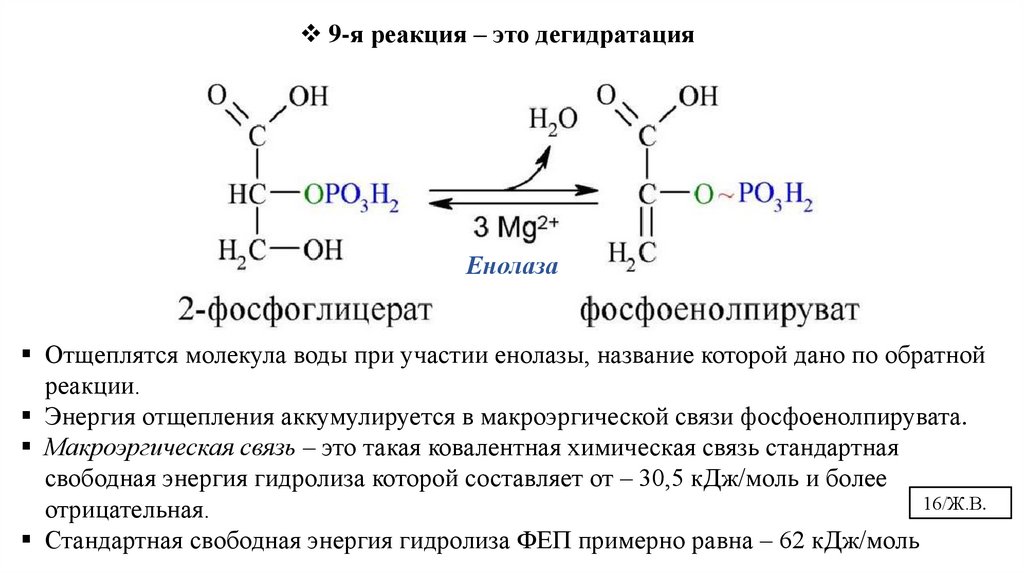
16.
9-я реакция – это дегидратацияЕнолаза
Отщеплятся молекула воды при участии енолазы, название которой дано по обратной
реакции.
Энергия отщепления аккумулируется в макроэргической связи фосфоенолпирувата.
Макроэргическая связь – это такая ковалентная химическая связь стандартная
свободная энергия гидролиза которой составляет от – 30,5 кДж/моль и более
16/Ж.В.
отрицательная.
Стандартная свободная энергия гидролиза ФЕП примерно равна – 62 кДж/моль
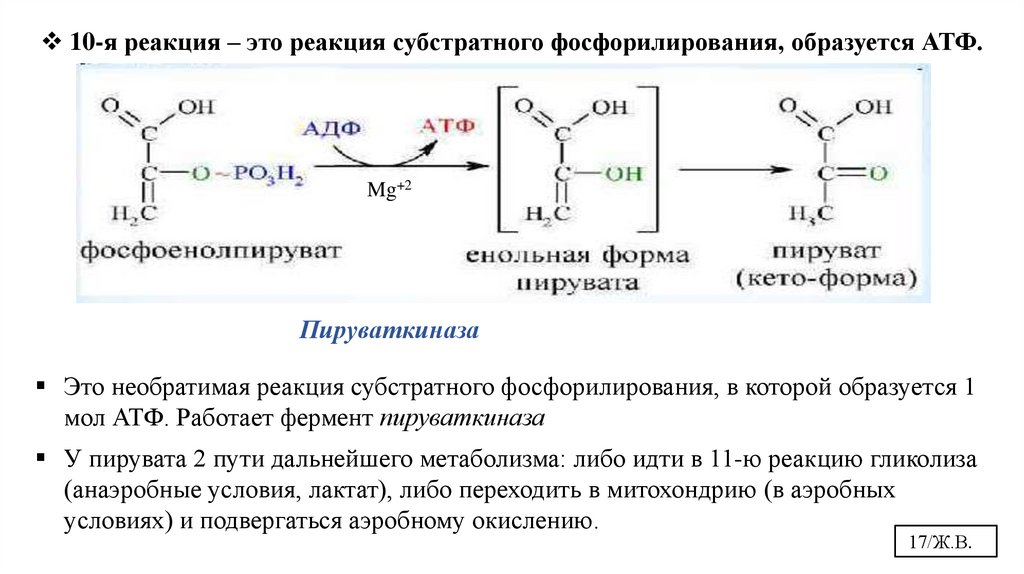
17.
10-я реакция – это реакция субстратного фосфорилирования, образуется АТФ.Mg+2
Пируваткиназа
Это необратимая реакция субстратного фосфорилирования, в которой образуется 1
мол АТФ. Работает фермент пируваткиназа
У пирувата 2 пути дальнейшего метаболизма: либо идти в 11-ю реакцию гликолиза
(анаэробные условия, лактат), либо переходить в митохондрию (в аэробных
условиях) и подвергаться аэробному окислению.
17/Ж.В.
18.
11-я реакция –окисление восстановленного НАДН и регенерация НАД+(Лактат)
В 11-й реакции (анаэробные условия) окисляется восстановленный НАДН из 6-й реакции гликолиза
и образуется окисленная форма НАД+, необходимая для окисления вновь образующихся молекул
глицеральдегид-3-фосфата, т.е. для дальнейшего протекания гликолиза.
Образованный в анаэробных условиях гликолиза лактат проходит через цитоплазматическую
мембрану и, покидая клетку, попадает в плазму крови.
У анаэробных микроорганизмов, осуществляющих молочно-кислое брожение, продукт гликолиза –
лактат.
В скелетной мышце этот процесс, называемый анаэробный гликолиз, служит важным источником
энергии АТФ при напряженной физической работе.
В стадию гликолитической оксидоредукции происходят 2 окислительно-восстановительные реакции:
окисление 3-ФГА и восстановление НАД+, и 11-я реакция –восстановление ПВК до лактата с окислением
НАДН+Н+. В эту стадию идет образование АТФ путем субстратного фосфорилирования
18/Ж.В.
19.
3.Расчет количества молекул АТФ при анаэробном гликолизеи гликогенолизе.
В первую стадию в расчете на гексозу было затрачено 2 молекулы АТФ.
Во вторую стадию в расчете на триозу - образовались 2 молекулы АТФ,
а в расчете на гексозу – 4 АТФ, но за вычетом 2-х мол. АТФ, затраченных
в первую стадию, – суммарный выход гликолиза = 2 мол. АТФ.
Суммарный выход гликогенолиза (в расчете на 1 молекулу глюкозы)
равен 3 мол. АТФ, т.к. в подготовительную стадию затрачена 1 мол. АТФ
В гликогенолизе образование глюкозофо-6-фосфата происходило путем
переноса остатка фосфорной кислоты из 1-го положения в 6-е без затраты
АТФ.
19/Ж.В.
20.
4. Биологическая роль анаэробного окисления глюкозы.Гликолиз и гликогенолиз- энергетически невыгодный процесс, но единственный
путь получения энергии в клетке при гипоксии.
Только гликолиз используется для получения энергии в эритроцитах, т.к. эти клетки
не имеют митохондрий.
В эмбриональный период организм получает энергию посредством гликолиза, т.к. к
плоду притекает смешанная, бедная кислородом кровь.
Раковые клетки переходят на гликолиз.
Гликолиз - основной энергетический процесс в остеоцитах, клетках
минерализованного межклеточного матрикса костной ткани.
При усиленной микробной колонизации в полости рта количество поступающего
кислорода в зубном налете (бляшке) по мере его роста-уменьшается, а
анаэробные сообщества микроорганизмов – увеличиваются. Метаболизм
глюкозы в зубном налете идет до лактата. А также в реакциях брожения из
глюкозы образуются и другие органические кислоты. Накопление кислот
приводит к деструкции минерализованных тканей зубов (эмали, дентина).
20/Ж.В.
21.
4.1. Регуляция гликолизаРегуляторные ферменты гликолиза: гексокиназа, фосфофруктокиназа,
пируваткиназа.
Гексокиназа ингибируется продуктом реакции – глюкозо-6-фосфатом
Глюкокиназа активируется глюкозой, а глюкозо-6-фосфатом не ингибируется.
Фосфофруктокиназа активируется АМФ и фруктозо-2,6-бифосфатом, а
ингибируется избытком АТФ и цитратом. АТФ – субстрат фермента, а при его
избытке – ингибитор.
Пируваткиназа активируется фруктозо-1,6-бифосфатом, ингибируется АТФ и
ацетил-КоА
Исулин стимулирует гликолиз через повышение активности гексокиназы,
фосфофруктокиназы, пируваткиназы. Также он индуцирует синтез глюкокиназы и
пируваткиназы
21/Ж.В.
22.
5. Аэробное окисление глюкозыПроцесс аэробного окисления глюкозы имеет несколько этапов:
5.1. Первый этап -гликолитический
протекает в цитоплазме, имеет точно такие же реакции, как гликолиз, но
есть два отличия:
1. НАДН+Н+ не используется на превращение пирувата в лактат, а
переносится челночными механизмами в митохондрии –
глицерофосфатным в мышечной и мозговой ткани (акцептором
водорода в митохондриях в этом пути является ФАД); и малатаспартатным челночным механизмом, при котором акцептором
водорода в митохондриях является НАД+.
2. Второе отличие состоит в том, что пируват переходит в митохондрии
(Рис.1)
21/Ж.В.
23.
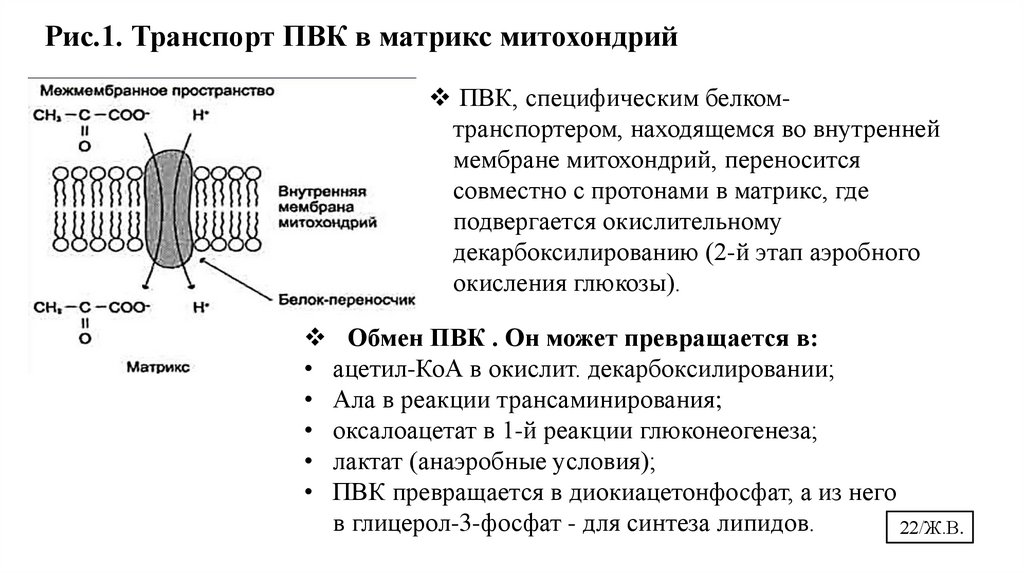
Рис.1. Транспорт ПВК в матрикс митохондрийПВК, специфическим белкомтранспортером, находящемся во внутренней
мембране митохондрий, переносится
совместно с протонами в матрикс, где
подвергается окислительному
декарбоксилированию (2-й этап аэробного
окисления глюкозы).
Обмен ПВК . Он может превращается в:
• ацетил-КоА в окислит. декарбоксилировании;
• Ала в реакции трансаминирования;
• оксалоацетат в 1-й реакции глюконеогенеза;
• лактат (анаэробные условия);
• ПВК превращается в диокиацетонфосфат, а из него
в глицерол-3-фосфат - для синтеза липидов.
22/Ж.В.
24.
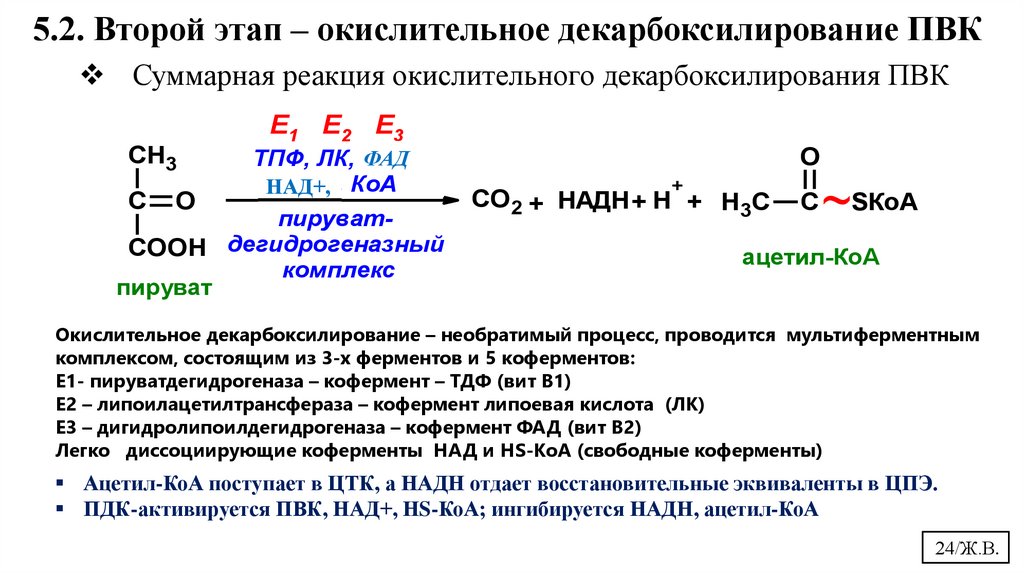
5.2. Второй этап – окислительное декарбоксилирование ПВКСуммарная реакция окислительного декарбоксилирования ПВК
Е1 Е2 Е3
CH3
С
O
ФАД
ТПФ, ЛК, НАД,
ФАД, КоА
НАД+,
пируватCOOH дегидрогеназный
комплекс
пируват
O
+
СО2 + НАДН + Н + H3C
С
~SКоА
ацетил-КоА
Окислительное декарбоксилирование – необратимый процесс, проводится мультиферментным
комплексом, состоящим из 3-х ферментов и 5 коферментов:
Е1- пируватдегидрогеназа – кофермент – ТДФ (вит В1)
Е2 – липоилацетилтрансфераза – кофермент липоевая кислота (ЛК)
Е3 – дигидролипоилдегидрогеназа – кофермент ФАД (вит В2)
Легко диссоциирующие коферменты НАД и HS-КоА (свободные коферменты)
Ацетил-КоА поступает в ЦТК, а НАДН отдает восстановительные эквиваленты в ЦПЭ.
ПДК-активируется ПВК, НАД+, НS-КоА; ингибируется НАДН, ацетил-КоА
24/Ж.В.
25.
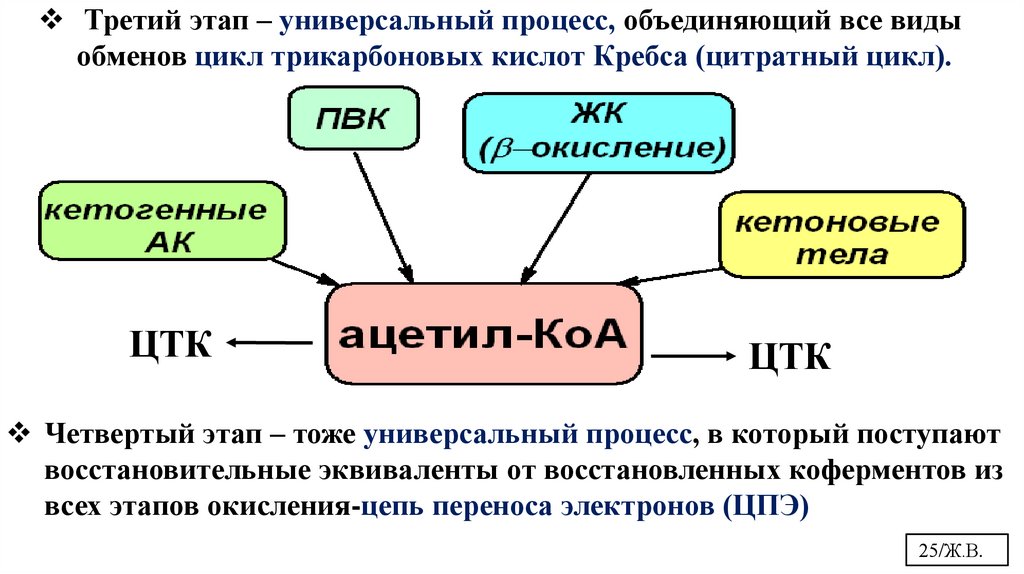
Третий этап – универсальный процесс, объединяющий все видыобменов цикл трикарбоновых кислот Кребса (цитратный цикл).
ЦТК
ЦТК
Четвертый этап – тоже универсальный процесс, в который поступают
восстановительные эквиваленты от восстановленных коферментов из
всех этапов окисления-цепь переноса электронов (ЦПЭ)
25/Ж.В.
26.
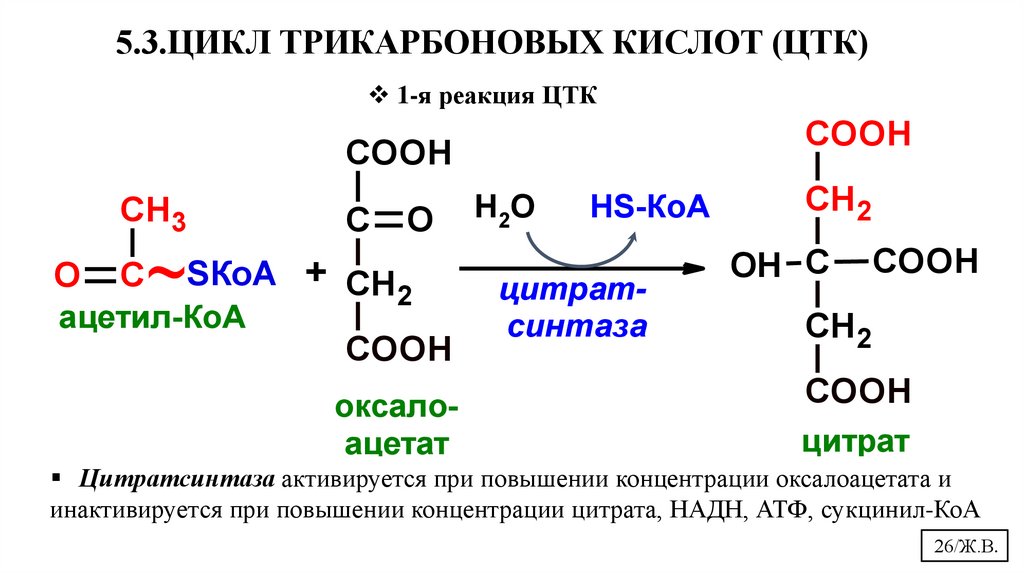
5.3.ЦИКЛ ТРИКАРБОНОВЫХ КИСЛОТ (ЦТК)1-я реакция ЦТК
COOH
COOH
CH3
С
O
~
ацетил-КоА
O
С
SКоА + СН
2
COOH
оксалоацетат
Н2О
НS-КоА
цитратсинтаза
СН 2
OH С
COOH
СН 2
COOH
цитрат
Цитратсинтаза активируется при повышении концентрации оксалоацетата и
инактивируется при повышении концентрации цитрата, НАДН, АТФ, сукцинил-КоА
26/Ж.В.
27.
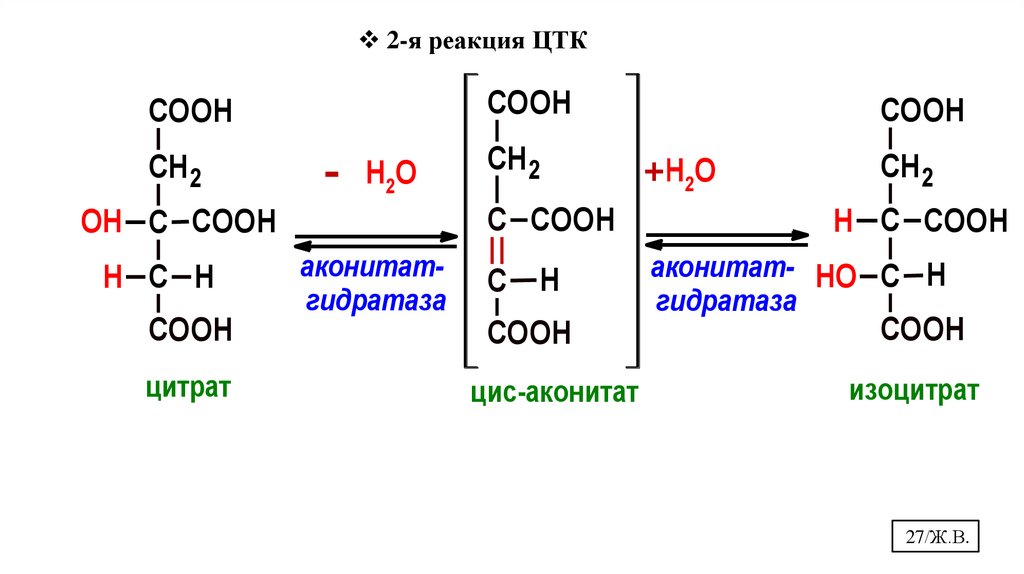
2-я реакция ЦТКCOOH
COOH
СН2
-
Н2О
С COOH
OH С COOH
H С H
СН2
аконитатгидратаза
С
H
COOH
COOH
цитрат
цис-аконитат
COOH
+Н2О
СН 2
H С COOH
аконитат- HO С H
гидратаза
COOH
изоцитрат
27/Ж.В.
28.
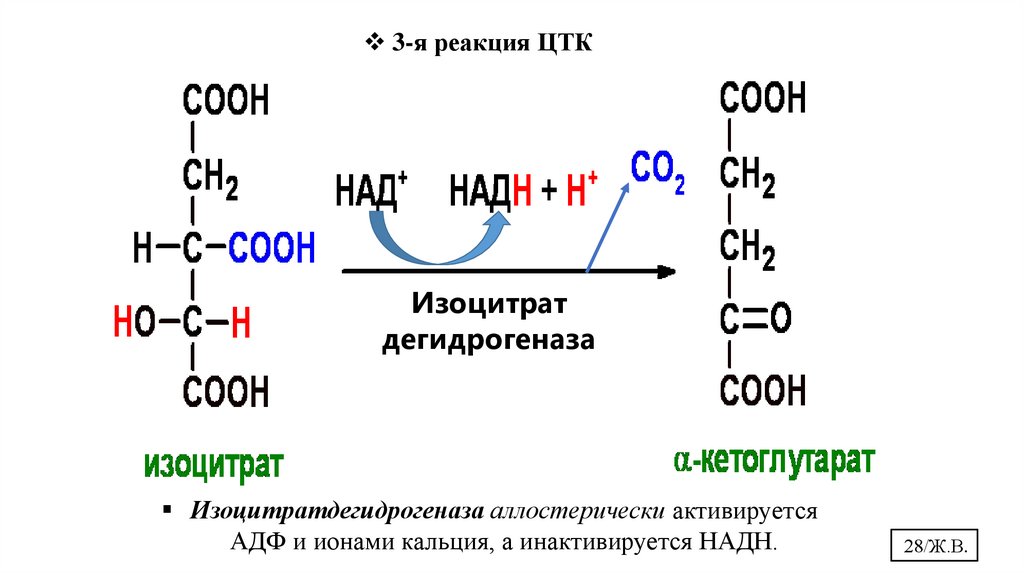
3-я реакция ЦТКИзоцитрат
дегидрогеназа
Изоцитратдегидрогеназа аллостерически активируется
АДФ и ионами кальция, а инактивируется НАДН.
28/Ж.В.
29.
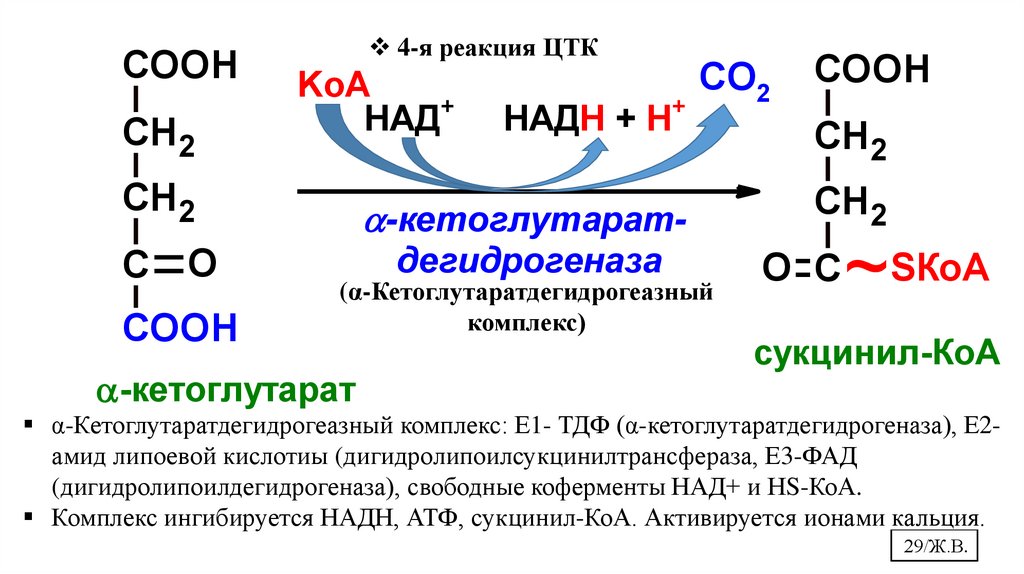
COOHСН 2
4-я реакция ЦТК
KоА
НАД+
НАДН + Н+
СН 2
-кетоглутарат-
С O
дегидрогеназа
COOH
СО2
(α-Кетоглутаратдегидрогеазный
комплекс)
-кетоглутарат
COOH
СН 2
СН 2
O С
~SКоА
сукцинил-КоА
α-Кетоглутаратдегидрогеазный комплекс: Е1- ТДФ (α-кетоглутаратдегидрогеназа), Е2амид липоевой кислотиы (дигидролипоилсукцинилтрансфераза, Е3-ФАД
(дигидролипоилдегидрогеназа), свободные коферменты НАД+ и НS-КоА.
Комплекс ингибируется НАДН, АТФ, сукцинил-КоА. Активируется ионами кальция.
29/Ж.В.
30.
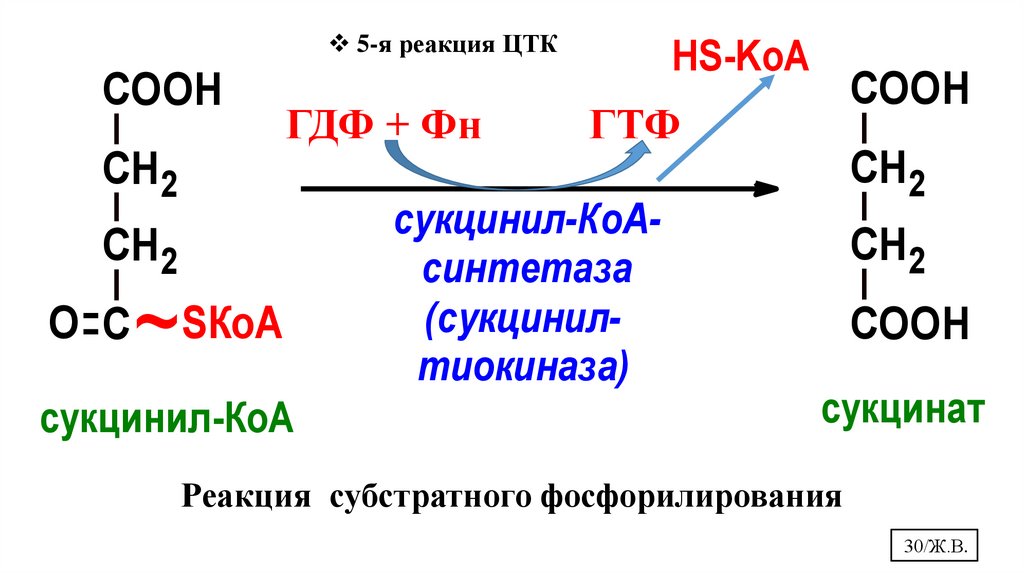
5-я реакция ЦТКCOOH
СН2
АДФ
+
НР
ГДФ + Фн
СН2
O С
~
SКоА
сукцинил-КоА
НS-KоА
COOH
АТФ
ГТФ
сукцинил-КоАсинтетаза
(сукцинилтиокиназа)
СН 2
СН 2
COOH
сукцинат
Реакция субстратного фосфорилирования
30/Ж.В.
31.
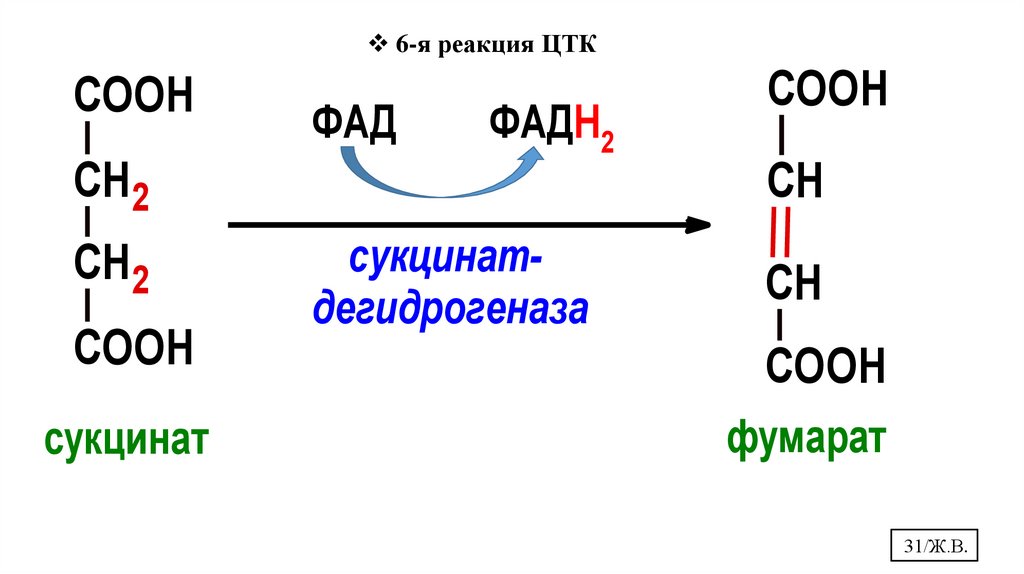
6-я реакция ЦТКCOOH
СН2
СН2
COOH
сукцинат
ФАД
ФАДН2
сукцинатдегидрогеназа
COOH
СН
СН
COOH
фумарат
31/Ж.В.
32.
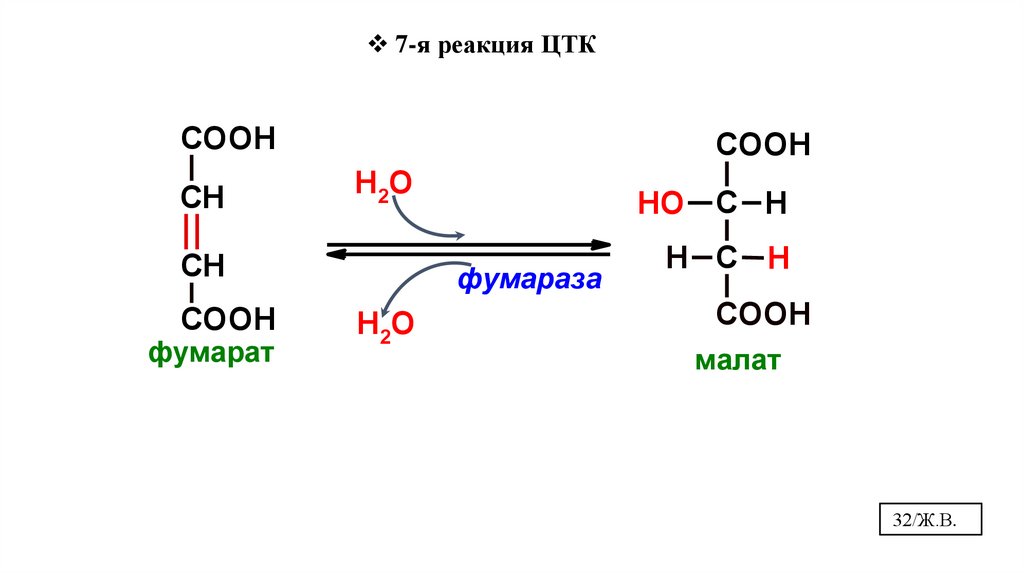
7-я реакция ЦТКCOOH
СН
COOH
Н2О
СН
COOH
фумарат
HO С H
фумараза
Н2О
H С H
COOH
малат
32/Ж.В.
33.
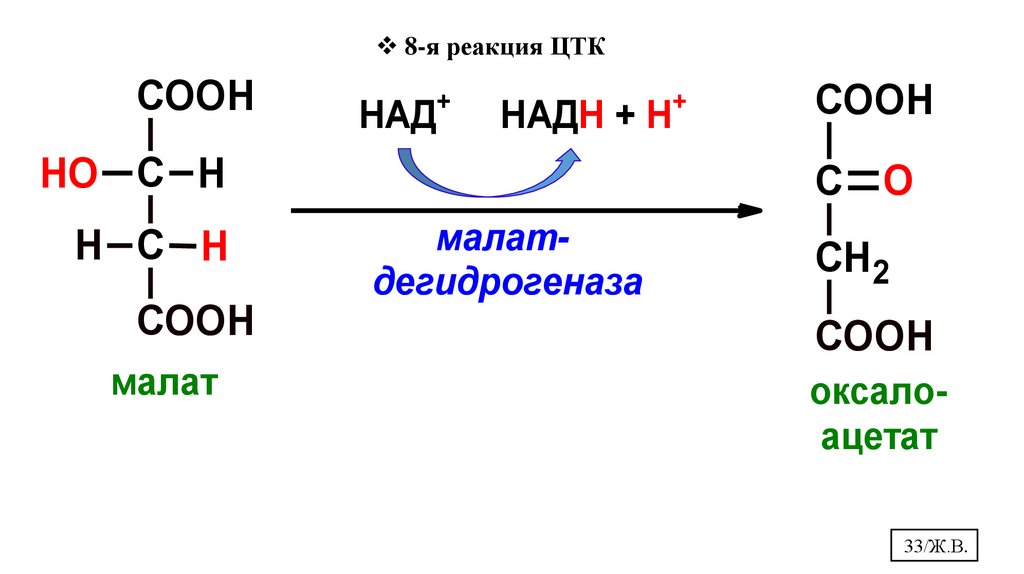
8-я реакция ЦТКCOOH
+
НАД
НАДН + Н
HO С H
H С H
+
COOH
С O
малатдегидрогеназа
СН2
COOH
COOH
малат
оксалоацетат
33/Ж.В.
34.
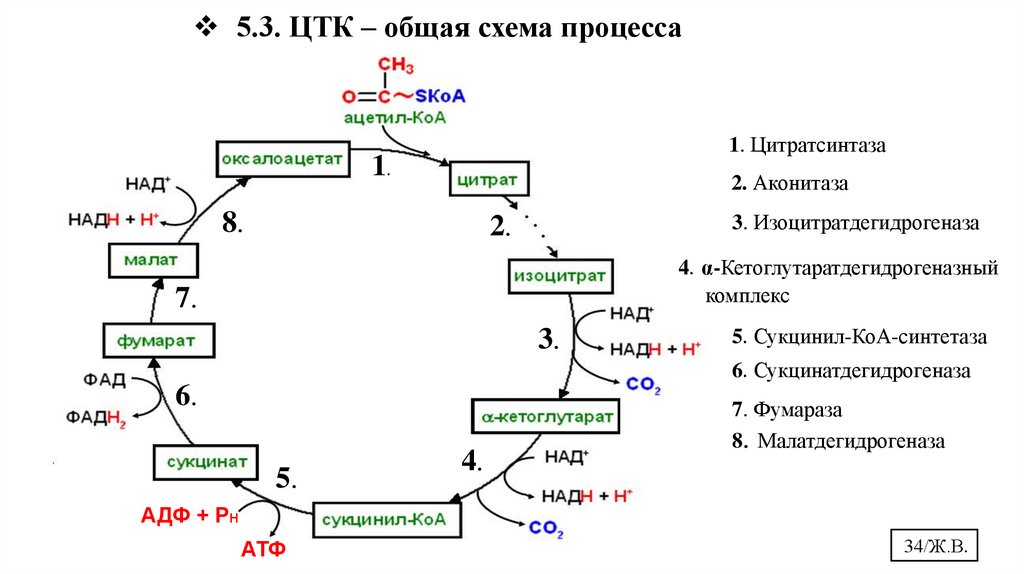
5.3. ЦТК – общая схема процесса1. Цитратсинтаза
1.
2. Аконитаза
8.
3. Изоцитратдегидрогеназа
2.
4. α-Кетоглутаратдегидрогеназный
комплекс
7.
3.
5. Сукцинил-КоА-синтетаза
6. Сукцинатдегидрогеназа
6.
5.
4.
7. Фумараза
8. Малатдегидрогеназа
АДФ + РН
АТФ
34/Ж.В.
35.
6. Биологическая роль ЦТКЭнергетическая – в пяти энергопоставляющих реакциях ЦТК образуются
восстановленные коферменты (3 НАДН+Н и 1 ФАД2Н), а также 1 молекула АТФ
за счет субстратного фосфорилирования. Восстановленные коферменты
поставляют свои восстановительные эквиваленты в ЦПЭ, где образуется основное
количество АТФ посредством окислительного фосфорилирования.
Объединяет все виды обменов за счет наличия общих метаболитов:
ацетил-КоА, оксалоацетата, α-кетоглутарата, фумарата.
Пластическая – метаболиты ЦТК могут использоваться для реакций синтеза:
• оксалоацетат – для синтеза аспартата и глюкозы;
• α-кетоглутарат – для синтеза глутамата;
• сукцинил-КоА для синтеза гема;
• ацетил-КоА в составе цитрата переносится в цитоплпзму и используется для
синтеза липидов;
• цитрат может связывать и переносить ионы кальция, участвуя
в процессах минерализации.
35/Ж.В.
36.
7. Ингибиторы ЦТК1. Тиоловые яды – ингибиторы дегидрогеназ, содержащих SH- группы в
активном центре
2. Ингибирование по типу летального синтеза – при попадании в
организм фторацетата из него синтезируется фторцитрат – необратимый
специфический ингибитор аконитатгидратазы
3. Обратимое конкурентное ингибирование сукцинатдегидрогеназы
малонатом
4. Метаболические аллостерические регуляторы со знаком «-» – это
высокие концентрации АТФ, НАДН+Н, подавляющие активность
дегидрогеназ и цитратсинтазы по механизму отрицательной обратной
36/Ж.В.
связи.
37.
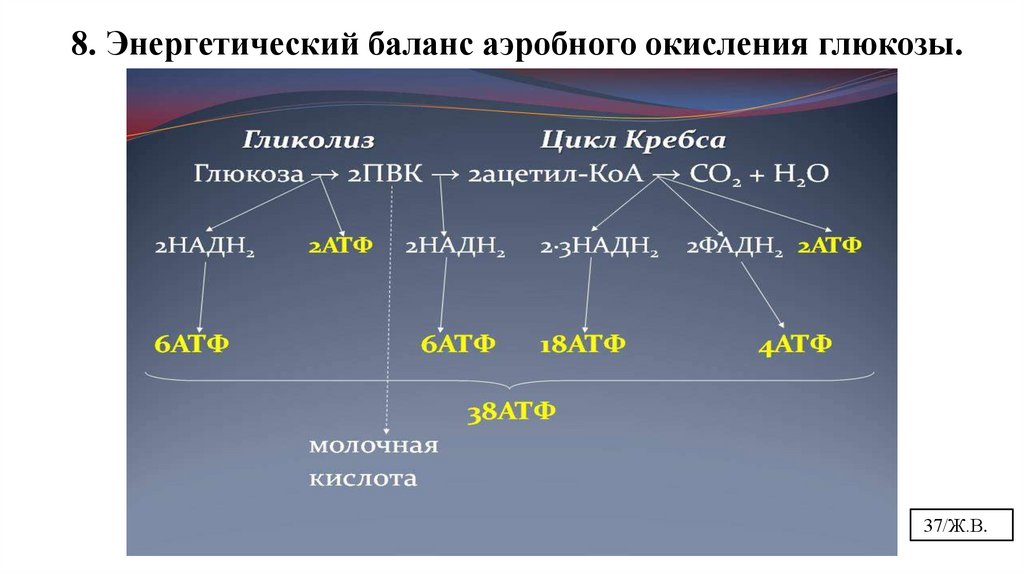
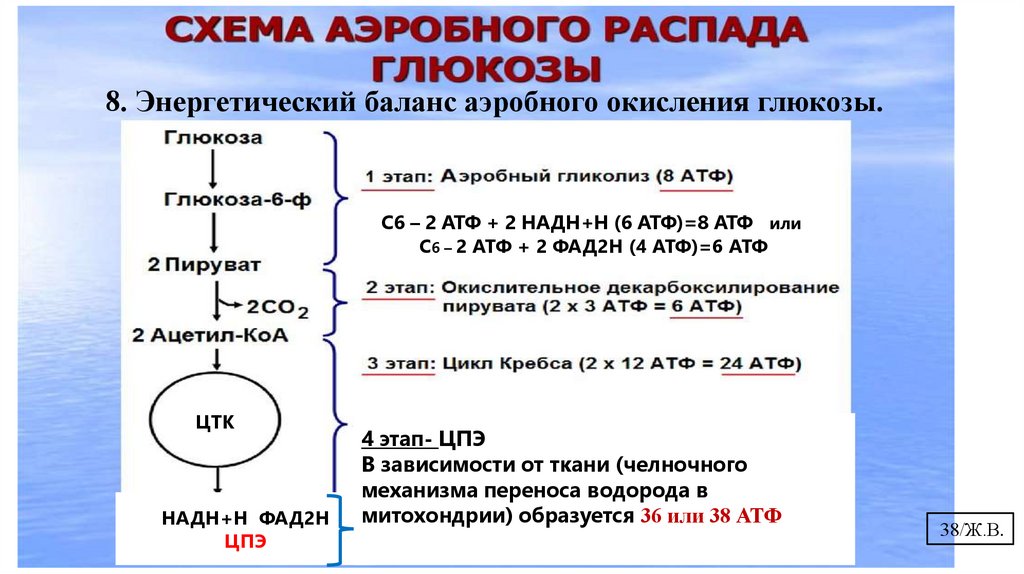
8. Энергетический баланс аэробного окисления глюкозы.37/Ж.В.
38.
8. Энергетический баланс аэробного окисления глюкозы.С6 – 2 АТФ + 2 НАДН+Н (6 АТФ)=8 АТФ или
С6 – 2 АТФ + 2 ФАД2Н (4 АТФ)=6 АТФ
ЦЦТК
НАДН+Н ФАД2Н
ЦПЭ
4 этап- ЦПЭ
В зависимости от ткани (челночного
механизма переноса водорода в
митохондрии) образуется 36 или 38 АТФ
38/Ж.В.
39.
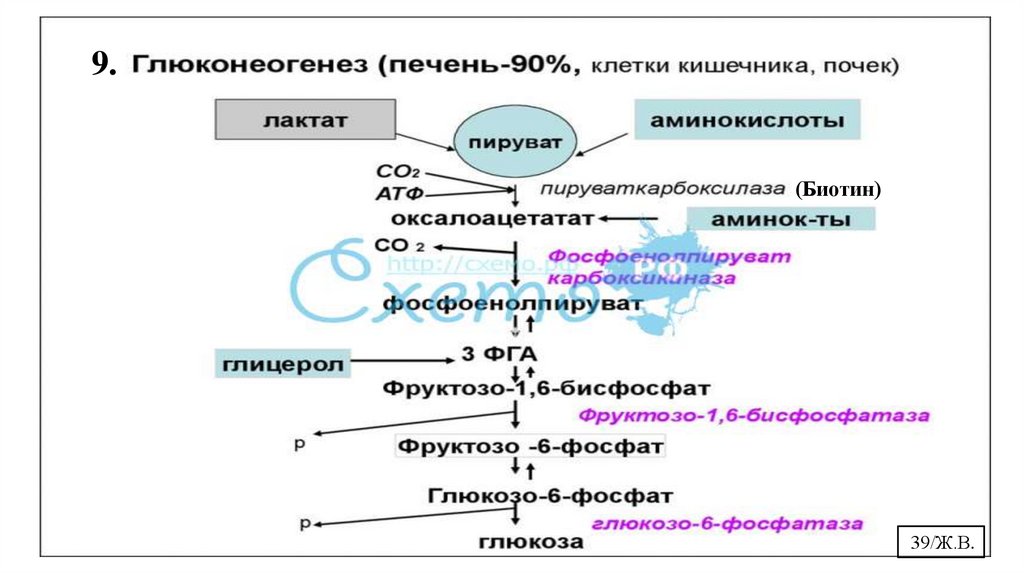
9.(Биотин)
39/Ж.В.
40.
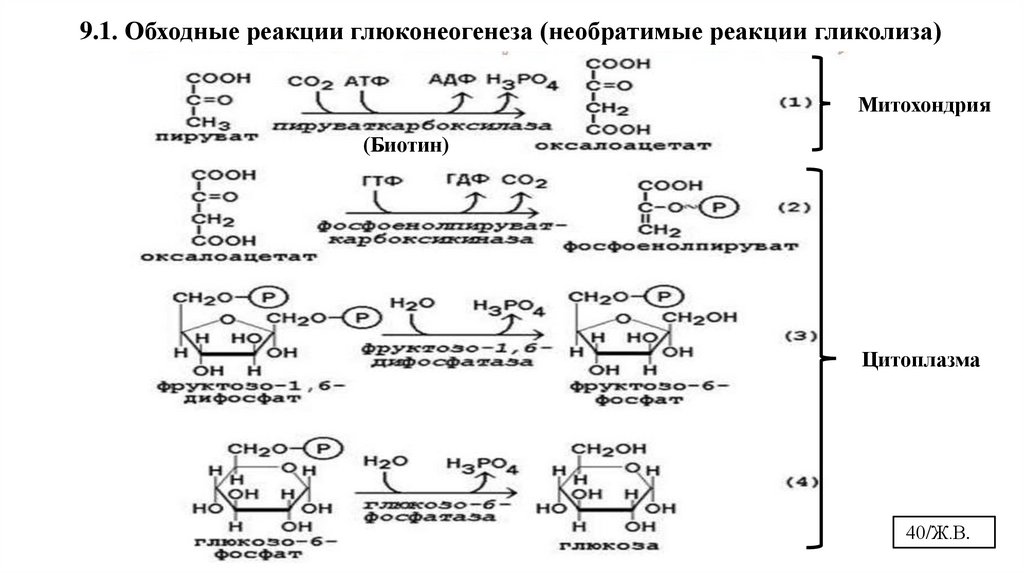
9.1. Обходные реакции глюконеогенеза (необратимые реакции гликолиза)Митохондрия
(Биотин)
Цитоплазма
40/Ж.В.
41.
10. Биологическая роль и регуляция глюконеогенезаГлюконеогенез (от лат neo - новый и genesis - образование) –это процесс
биосинтеза новых молекул глюкозы из неуглеводных предшественников: пирувата,
лактата, глицерола липидов, аминокислот и промежуточных метаболитов ЦТК ,
которые могут превращаться в оксалоацетат.
Основная роль глюконеогенеза – поддержание уровня глюкозы в крови в период
длительного голодания и интенсивных физических нагрузок. Синтезируемая в печени
и почках глюкоза выходит в кровь и используется клетками мозга, сердечной,
скелетных мышц, эритроцитами для метаболических нужд.
Регуляция глюконеогенеза.
Фруктозо-1,6-бифосфатазу инактивируют фруктозо-2,6-бифосфат и АМФ, а
активирует цитрат.
Глюкокортикоиды индуцирут синтез ключевых ферментов глюконеогенеза. Глюкагон
ускоряет глюконеогенез путем индукции синтеза фосфоенолпируваткарбоксикиназы,
фруктозо-1,6-бифосфатазы и глюкозо-6-фосфатазы. Инсулин способствует репрессии
синтеза ключевых ферментов глюконеогенеза.
41/Ж.В.
42.
Рекомендуемая литератураОсновная
Биохимия : учебник / под ред. Е.С. Северина. – М. : ГЭОТАР-Медиа, 2011. – С. 245–247, 279–283, 310–312, 328, 339.
Биохимия [Электронный ресурс] : учебник / под ред. Е. С. Северина. – 5-е изд., испр. и доп. – М. : ГЭОТАР-Медиа,
2015. – http://www.studmedlib.ru / book / ISBN9785970433126.html (разд. 7, п. VIII–X; с. 245–247, 279–283, 310–312,
328, 339).
Биологическая химия. Биохимия полости рта : учебник / Т.П. Вавилова, А.Е. Медведев. – М. : ГЭОТАР-Медиа,
2014. – С. 207–208, 246–264.
Биологическая химия. Биохимия полости рта [Электронный ресурс]: учебник / Т.П. Вавилова, А.Е. Медведев. – М. :
ГЭОТАР-Медиа, 2014. – http://www.studmedlib.ru / book / ISBN9785970430392.html (ч. V, гл. 13; с. 207–208, 246–264).
Обмен углеводов. Энергетический обмен. Гормональная регуляция обмена веществ и функций организма : учебнометодическое пособие к практическим и лабораторным занятиям по биологической химии – биохимии полости рта
для студентов стоматологических факультетов медицинских вузов / под ред. Ж.В. Антоновой, Р.Н. Павловой, Л.Б.
Гайковой. – СПб. : Изд-во СЗГМУ им. И.И. Мечникова, 2019. – С. 34–43.
Сборник тестовых заданий по разделам биологической химии и биохимии полости рта : учебно-методическое
пособие для студентов стоматологического факультета / под ред. В.А. Дадали, Ж.В. Антоновой, Р.Н. Павловой. – СПб.
: Изд-во СЗГМУ им. И.И. Мечникова, 2017. – С. 61–66.
Дополнительная
Биологическая химия / Т.Т. Березов, Б.Ф. Коровкин. – М. : Медицина, 1998. – С. 327–345.
Биологическая химия и биохимия полости рта. Ситуационные задачи и задания : учебное пособие / под ред. С.Е.
Северина. – М. : ГЭОТАР-Медиа, 2017. – С. 64.
42/Ж.В.
43.
БЛАГОДАРЮЗА ВНИМАНИЕ
Пройдите тестирование
43/Ж.В.

















 Биология
Биология








