Похожие презентации:
Состав и строение атома
1.
Тема урокаСостав и
строение атома.
2.
Основные положения атомномолекулярного учения• Вещества состоят из молекул, а молекулы из атомов.
• Молекула-мельчайшая частица вещества,
сохраняющая состав и свойства этого вещества
физически не делимая.
• Атом-мельчайшая частица вещества
химически не делимая.
• Молекулы и атомы находятся в постоянном
хаотическом движении.
• При физических явлениях химический
состав вещества не изменяется а при
химических из одних веществ получаются
другие.
3.
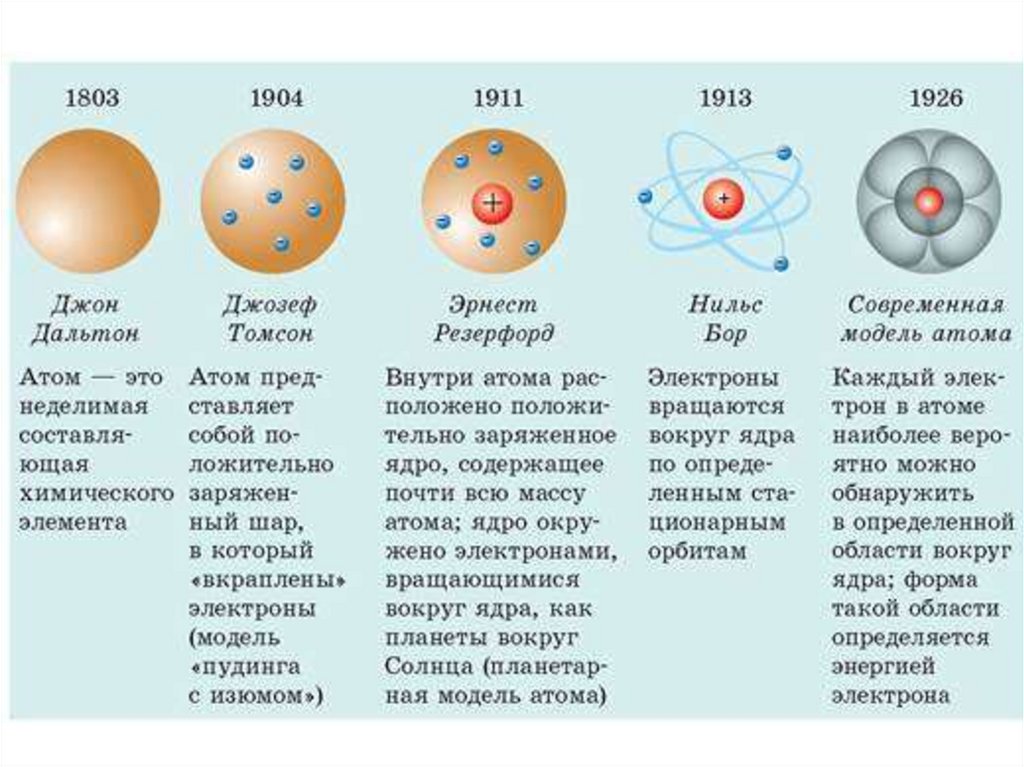
Планетарная модель атомаАтом-микрочастица, которая имеет форму шара
и состоящая из ядра и электронов.
Атом- электронейтральная частица поэтому
число протонов и электронов одинаковое.
Ядро находится в центре атома и имеет оч маленький размер,
но почти вся масса атома сосредоточена в ядре
Ядро имеет положительный заряд,, величина которого
определяется количеством протонов.
Электроны движутся вокруг ядра, имеют ничтожно
малую массу и размеры и обладают отрицательным
зарядом.
Порядковый номер показывает количество электронов и
протонов у элемента.
4.
5.
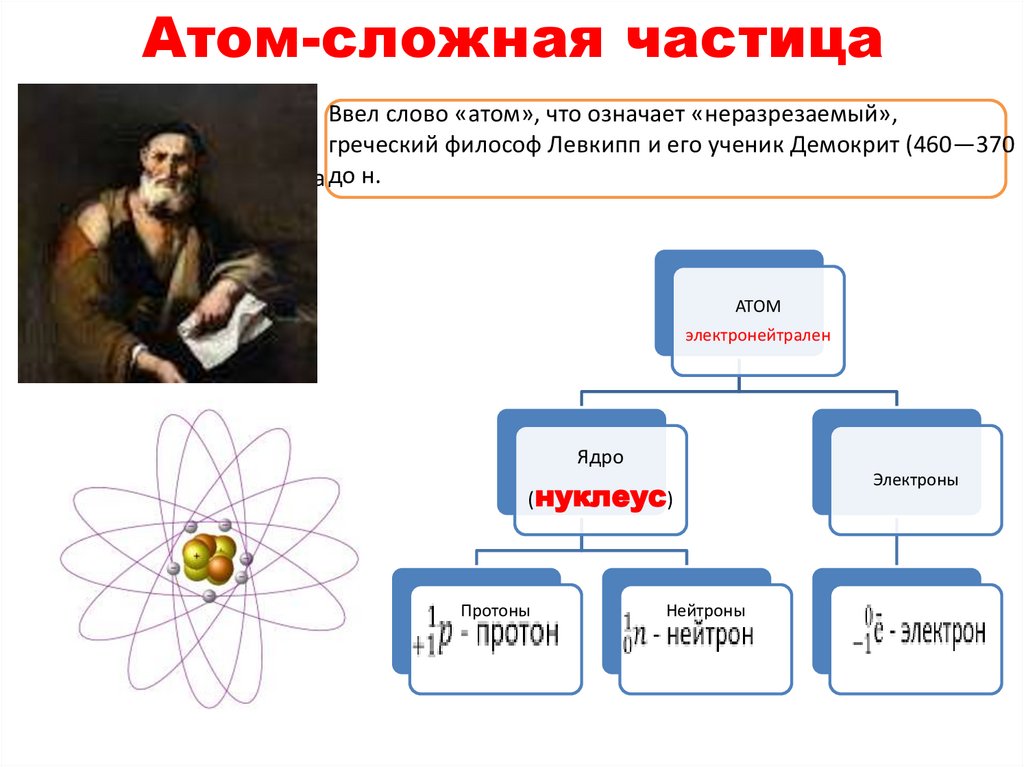
Атом-сложная частицаВвел слово «атом», что означает «неразрезаемый»,
греческий философ Левкипп и его ученик Демокрит (460—370
Открытие электрона до н.
АТОМ
электронейтрален
Ядро
(нуклеус)
Протоны
Нейтроны
Электроны
6.
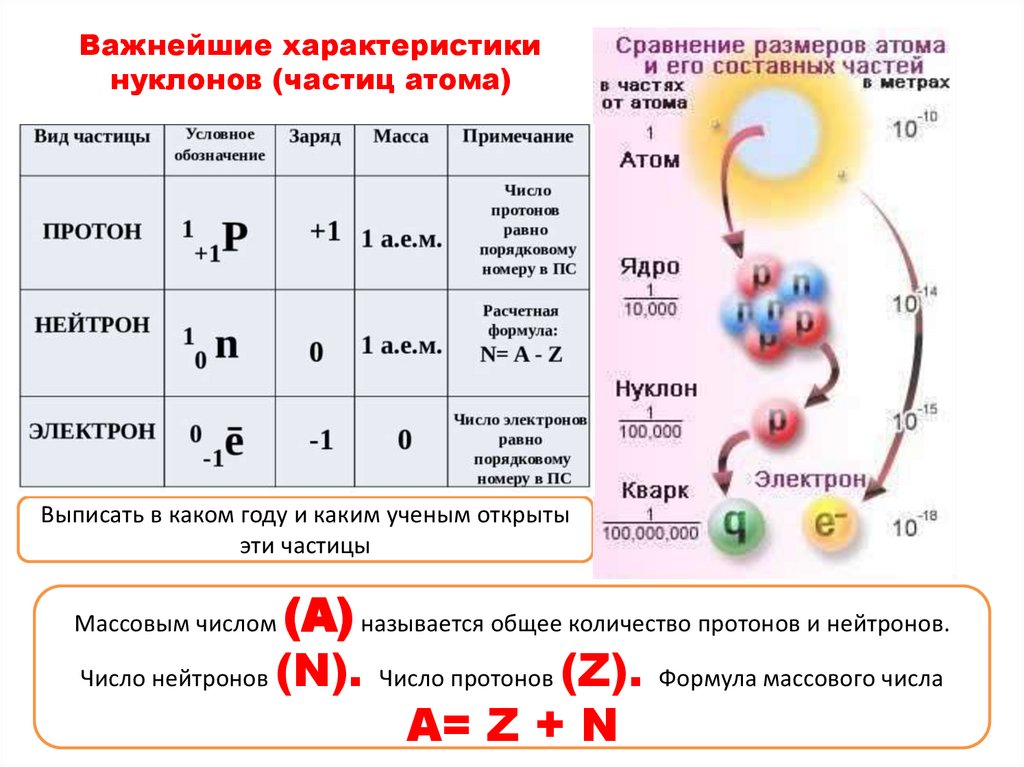
Важнейшие характеристикинуклонов (частиц атома)
Выписать в каком году и каким ученым открыты
эти частицы
(А) называется общее количество протонов и нейтронов.
Число нейтронов (N). Число протонов (Z). Формула массового числа
A= Z + N
Массовым числом
7.
Нуклиды- конкретные виды атомовразличных элементов
• Нуклиды-это совокупность атомов с
определенными значениями заряда ядра Z
(числом протонов) и массового числа А
(сумма протонов и нейтронов)
Тридцать пять нуклонов в
Двести восемь нуклонов в ядре
ядре
8.
Записывают строениеатома так
Задание 1. Записать строение атомов
1 вариант
железа, меди, хлора, кислорода, кальция
2 вариант
кислорода, цинка, магния, серебра, бора
3 вариант
брома, калия, азота, марганца, магния
4 вариант
серы, алюминия, ртути, хрома, кремния
5 вариант
селена, титана, фтора, гелия, скандия.
6 вариант
иода, бериллия, аргона, натрия, фосфора.
9.
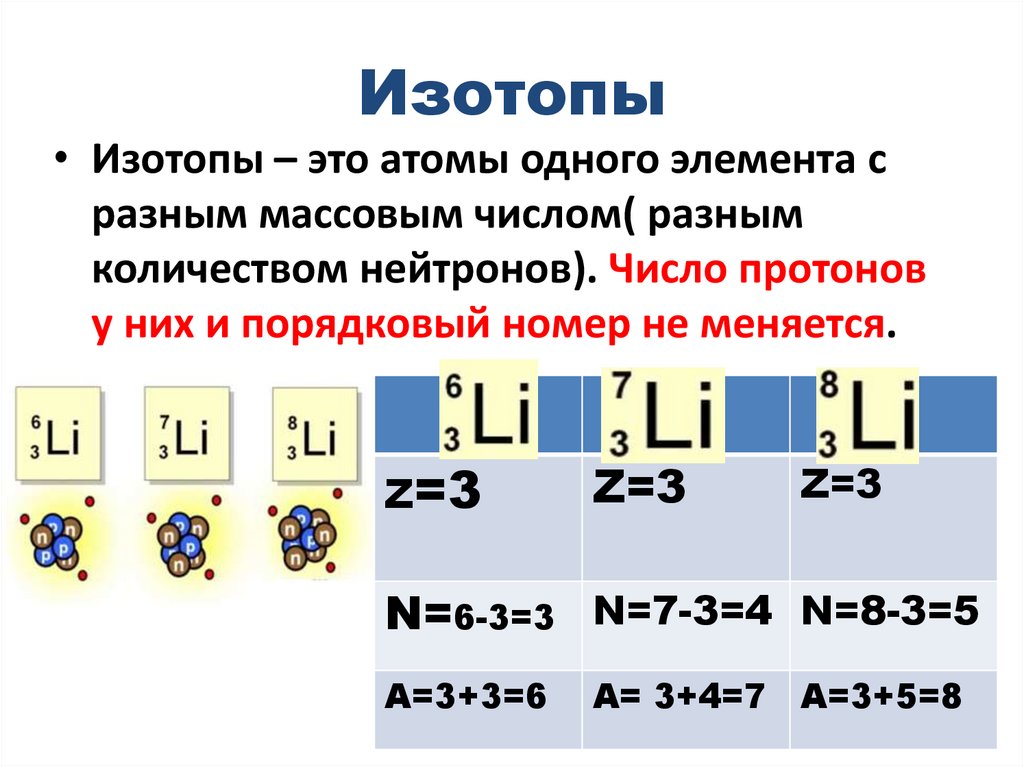
Изотопы• Изотопы – это атомы одного элемента с
разным массовым числом( разным
количеством нейтронов). Число протонов
у них и порядковый номер не меняется.
Z=3
Z=3
Z=3
N=6-3=3 N=7-3=4 N=8-3=5
A=3+3=6
A= 3+4=7 A=3+5=8
10.
Задача1.Вычислить какова процентная доля протонов в
ядрах
W(p+)=общее число протонов(порядк номер) / * 100%
массовое число
W(p+)=3/6 * 100% =50%
W(p+)= 17/35 * 100% =48,57%
Задача 2
Вычислить какова доля протонов в ядрах
W(p+)=общее число протонов(порядк номер) / массовое число
W(p+)=3/6= 0,5
W(p+)= 17/35= 0,4857
11.
Задача 3• Массовое число нуклидов равно
27. Доля протонов в нем 48,2%
Нуклидом какого элемента
является данный нуклид?
Составляем пропорцию
Дано
Пусть 27- 100%
Х- 48,2%
А= 27
Х= 27 * 48,2 / 100%= 13 – число
протонов (т.е. порядковый номер
W(р+)= 48,2%
Э-?
По Периодической таблице
находим что это алюминий
Ответ: это алюминий
12.
В зависимости от значений А, Z, Nразличают
13.
Что произойдет с атомомэлемента если в ядро
например добавить протоны?
Получится ядро другого элемента - серы
14.
Что произойдет с атомомэлемента если изменить
число нейтронов?
15.
16.
Относительная атомнаямасса элемента
Рассчитываетсясуммированием
произведений массовых долей каждого
изотопа на его массовое число
17.
Актуализация знанийВ предложениях вставьте слова «атом» и
«молекула»:
• … водорода образована … водорода
• …углекислого газа образована … кислорода
и … углерода
• ..белого фосфора состоит из четырех ..
Фосфора
Составьте формулы этих веществ
18.
• Выполняем задания рабочего листа.19.
Домашнее задание• Пересказ Атомно-молекулярное учение,
протонная теория,
• Выучить формулу нахождения массовой
доли частиц и определения с примерами
изотопов, изотонов, изобаров.
• В дом тетрадях параграф 1 упр№ 2, №4,№7,
№9















 Физика
Физика








