Похожие презентации:
Отчёт по производственной практике. Покрытия на основе сплавов молибдена и металлов подгруппы железа
1. Отчёт по производственной практике
Выполнил:Кайро П.В. Б1-ХМТН-41
Научный руководитель:
к.х.н. Ченцова Е.В.
Руководитель практики:
к.х.н. Никитюк Т.В.
2. Актуальность
• Покрытия на основе сплавов молибдена и металловподгруппы железа используются как катализаторы в
нефтянной промышленности, в реакции ФишераТропша для получения углеводородов, а также как
катализаторы при электролитическом разложении
воды, также данные сплавы могут использоваться в
качестве
коррозионностойких
покрытий
в
самолётостроении и автомобилестроении.
3. Цели и задачи
• Основные цели и задачи данной практики:• 1.Исследование
отечественной
и
иностранной литературы на данную тему.
• 2.Получение
покрытий
сплавами
молибдена с металлами подгруппы
железа(Fe, Co, Ni.)
• 2.Исследование их физико-химических
свойств.
• 4. Анализ влияния режима осаждения и
состава электролита на полученный сплав и
его свойства.
4. Оборудование
• Весы лабораторные M-ER 122ACFJR- 300.01(Accurate, Корея)
• - Одноканальный потенциостатгальваностат Elins P150I.
• -pH-метр.
• - Портативный анализатор металлов и
сплавов Х-Меt 7500.
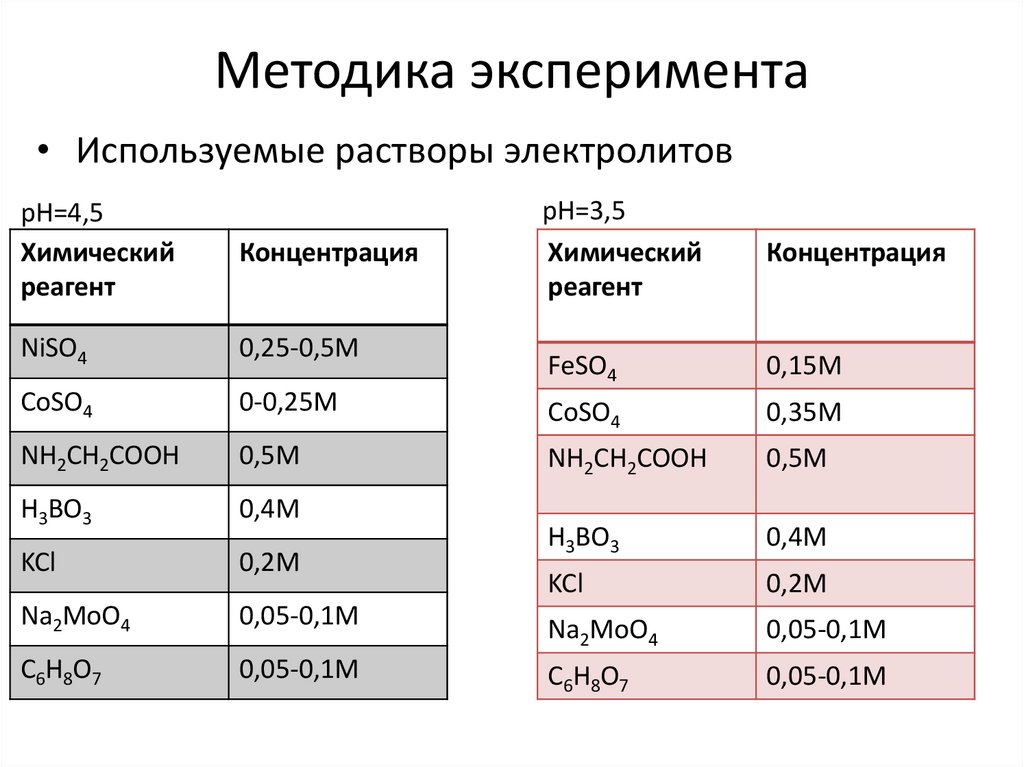
5. Методика эксперимента
• Используемые растворы электролитовpH=3,5
Химический
реагент
Концентрация
FeSO4
0,15М
0-0,25M
CoSO4
0,35M
NH2CH2COOH
0,5M
NH2CH2COOH
0,5M
H3BO3
0,4M
KCl
0,2M
H3BO3
0,4M
KCl
0,2M
Na2MoO4
0,05-0,1M
Na2MoO4
0,05-0,1M
C6H8O7
0,05-0,1M
C6H8O7
0,05-0,1M
pH=4,5
Химический
реагент
Концентрация
NiSO4
0,25-0,5М
CoSO4
6.
Покрытия получаются путёмэлектрохимического осаждения
сплава на поверхность подложки.
В качестве подложки выступают
стальные или медные пластины с
рабочей площадью поверхности в
4 см2. В качестве анода выступают
графитовый электрод, либо
никелевая пластина. Электродом
сравнения является хлорид
серебрянный электрод с
потенциалом E0=220мВ. Режимы
задаются в программе PSpack2
используются 2 основных режима
стационарный и импульсный.
Задаваемые потенциалы -1300мВ-2100 мВ. В случае импульсного
τимп=0,5-20с, τб/т=1-5с.
Рисунок 1- рабочая установка
7. Оборудование
• Весы лабораторные M-ER 122ACFJR- 300.01(Accurate, Корея).
• - Одноканальный потенциостат-гальваностат Elins
P150I.
• -pH-метр.
• Портативный анализатор метала Х-Меt 7500.
8. Результаты
Рисунок 2. NiSO4 0,5 M, Na2MoO4 0,1 M,C6H8O7 0,1 M
Рисунок 3. NiSO4 0,25 M, CoSO4 0,25 M,
Na2MoO4 0,1 M, C6H8O7 0,1 M
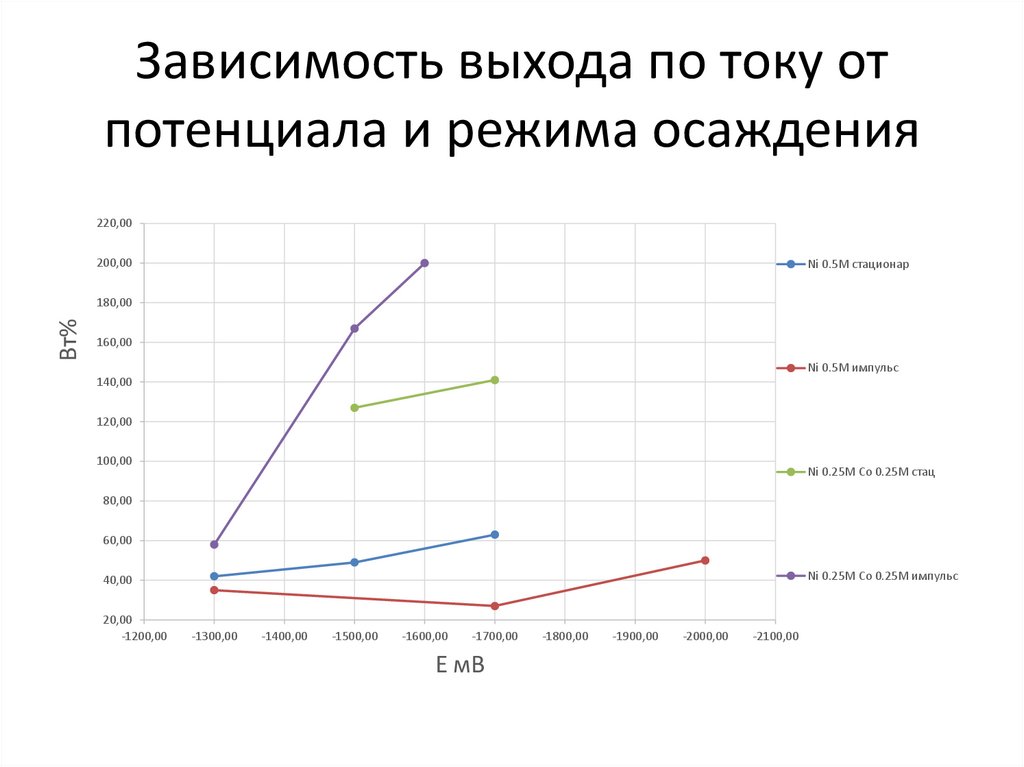
9. Зависимость выхода по току от потенциала и режима осаждения
220,00200,00
Ni 0.5M стационар
Вт%
180,00
160,00
Ni 0.5M импульс
140,00
120,00
100,00
Ni 0.25M Co 0.25M стац
80,00
60,00
Ni 0.25M Co 0.25M импульс
40,00
20,00
-1200,00
-1300,00
-1400,00
-1500,00
-1600,00
-1700,00
E мВ
-1800,00
-1900,00
-2000,00
-2100,00
10. Выводы
По полученным данным и графику зависимости потенциала отосаждения можно сделать вывод, что в электролите содержащем
Ni 0,5M в стационарном режиме выше выход по току чем в
импульсном, но при этом хуже морфология покрытия из-за
внутренних токов и недостатка времени на массообмен. В случае в
импульсном с 0,25M Ni 0,25M Co на -1300мВ наблюдается тёмное
покрытие в результате недостатка плотности тока, в результате же
понижения потенциала до -1500 мВ происходит аномальное
увеличение выхода по току предположительно из-за образования
комплексов с глицином или лимонной кислотой из-за чего можно
заметить необычную окраску покрытий. Если мы рассматривать
стационарный режим то данные процессы также происходят, но в
меньших количествах и из-за крайне низкой адгезии данных
покрытий запечатлеть на фото первоначальное состояние
покрытий не удалось.
11. Дальнейшие цели и задачи
• 1. Исследование систем Fe-Co-Mo• 2. Получение покрытия на медной
подложке.
• 3 Исследование влияния pH раствора
электролита на состав и морфологию
• 4. Проверка каталитических и
коррозионных свойств полученных
сплавов.









 Химия
Химия








