Похожие презентации:
Строение атома. Изотопы
1.
2.
«Отыщи всему начало и тымногое поймешь»
(Козьма Прутков)
3. Строение атома. Изотопы.
4.
ИСТОРИЧЕСКАЯ СПРАВКАВ основе философии
Демокрита лежит
учение:
Атом есть мельчайшее
«неделимое» тело, не
подверженное никаким
изменениям. Неделимость
атома аналогична
неделимости «бытия».
Демокрит
(460 г – 370 г до н.э.)
5.
Как устроен атом?6. Джозеф Джон Томсон (18 декабря 1856- 30 августа 1940) английский физик, лауреат Нобелевской премии по физике 1906 года
Джозеф Джон Томсон(18 декабря 185630 августа 1940)
английский физик,
лауреат Нобелевской
премии по физике
1906 года
7.
Модель атома ТомсонаДжозеф Джон Томсон
«Пудинг с изюмом»
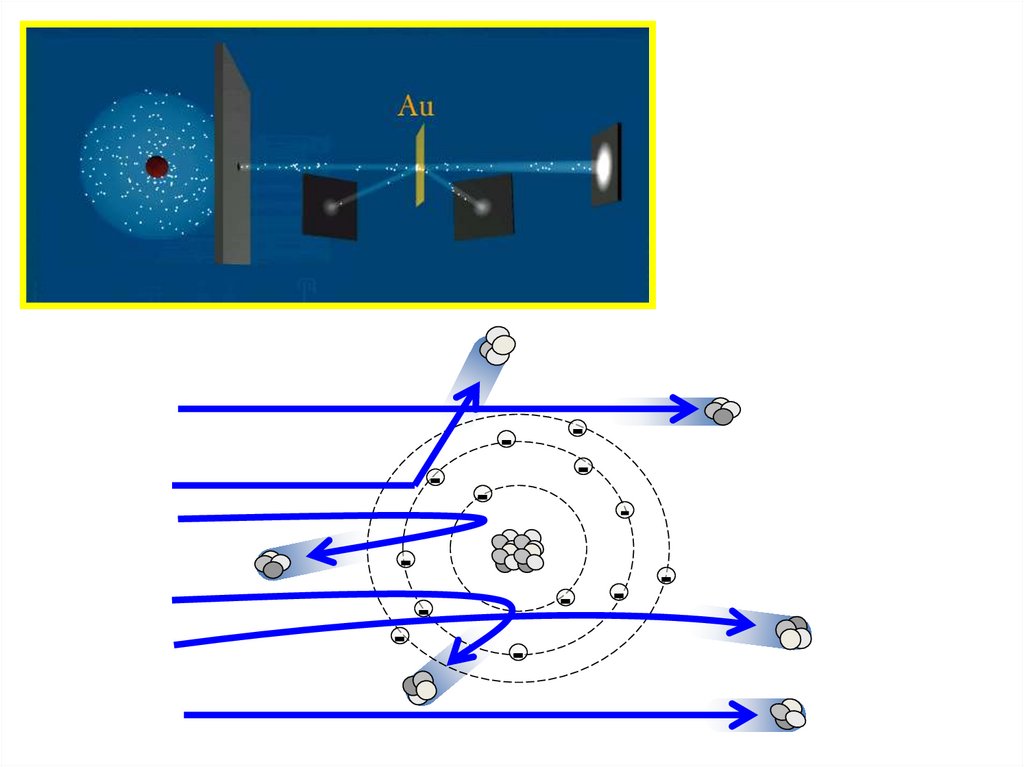
8. Эрнест Резерфорд (30 августа 1871 г. – 19 октября 1937 г.) Нобелевская премия по химии, 1908 год
9.
--
-
-
-
-
-
-
-
10.
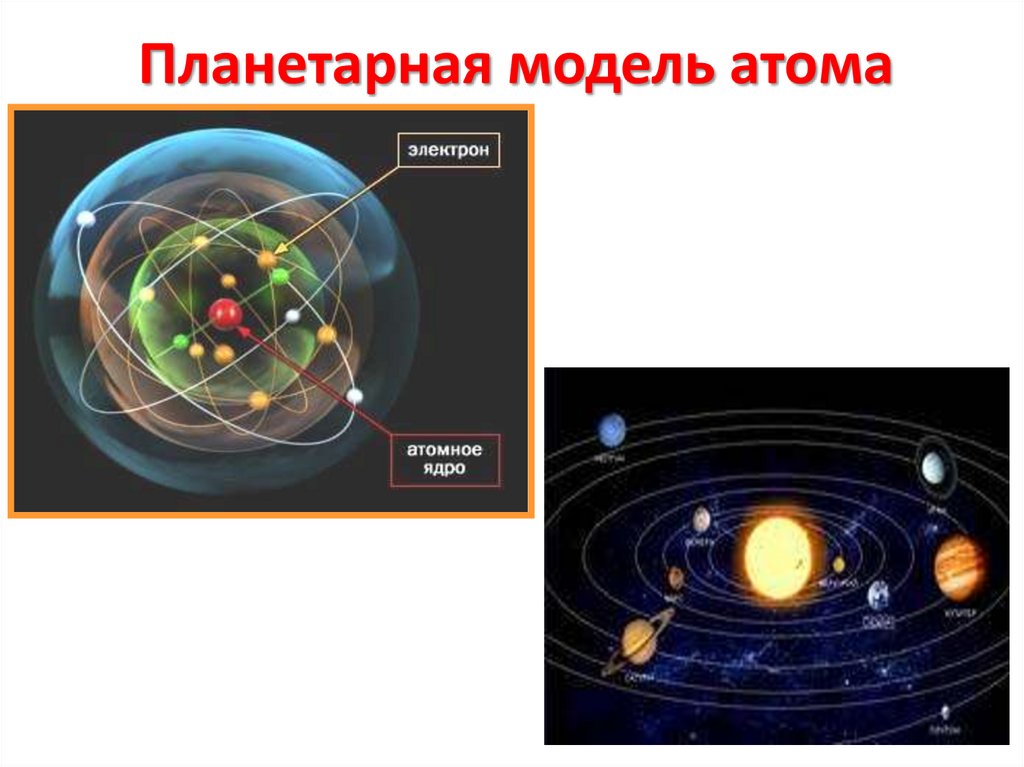
Планетарная модель атома11.
В. Брюсов об атоме (1922 г.)Быть может эти электроны –
Миры, где пять материков,
Искусства, знанья, войны, троны
И память сорока веков!
Еще, быть может, каждый атом –
Вселенная, где сто планет;
Там – все, что здесь, в объеме сжатом,
Но также то, чего здесь нет.
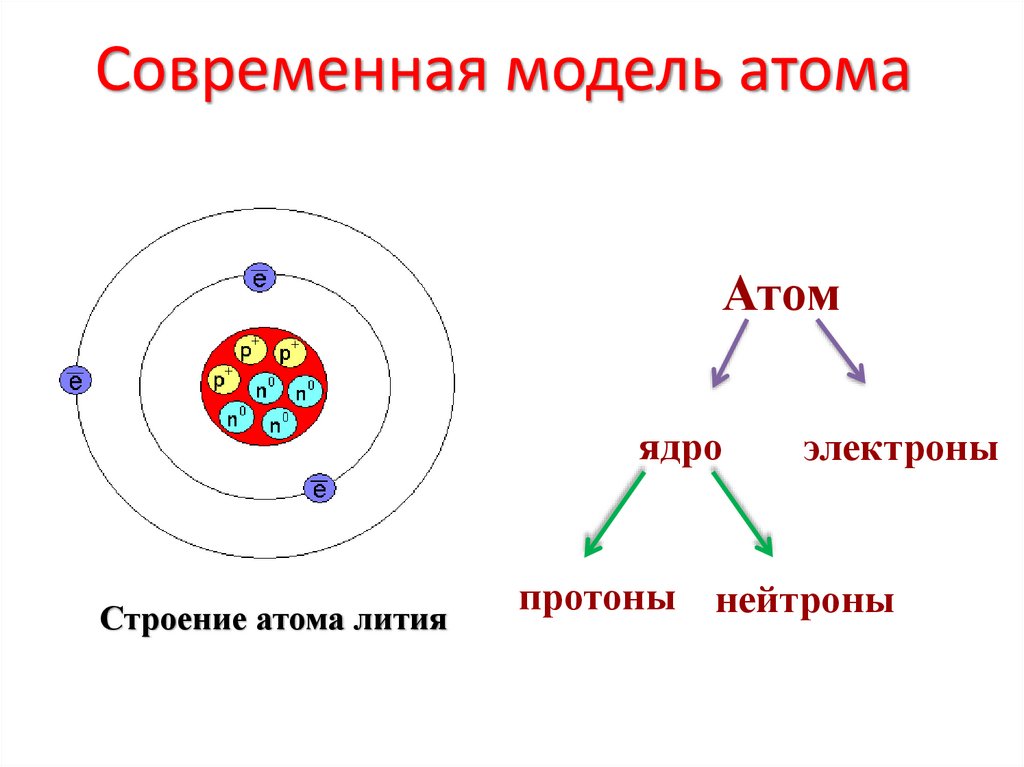
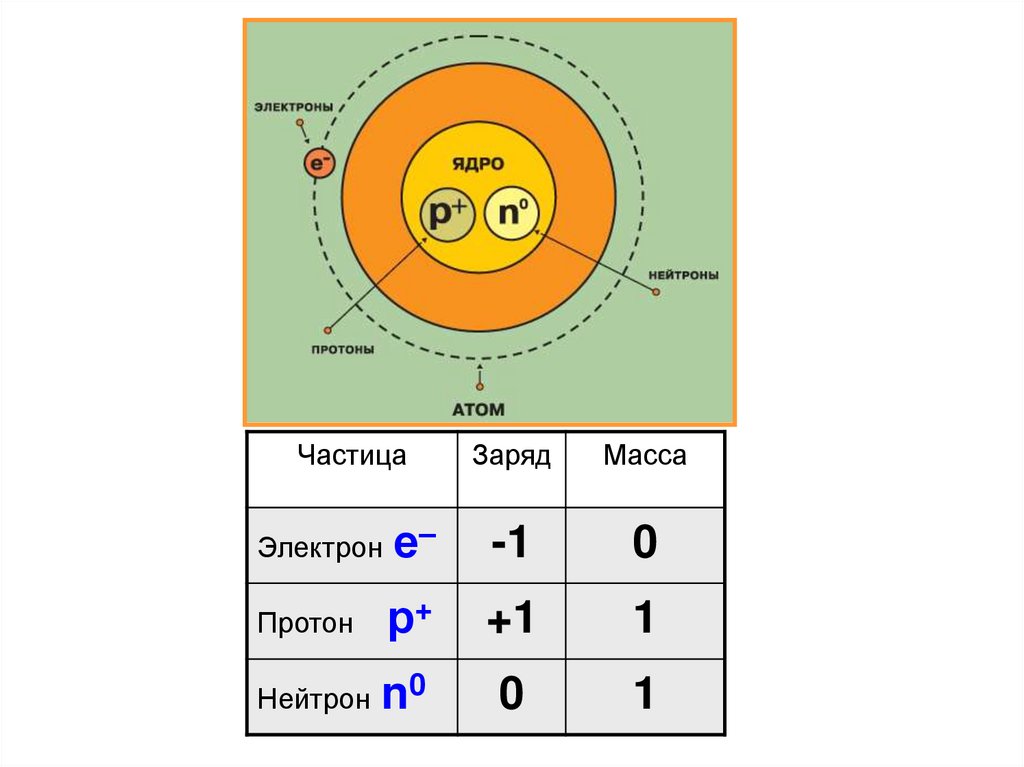
12. Современная модель атома
Атомядро
Строение атома лития
электроны
протоны нейтроны
13.
ЧастицаЗаряд
Масса
Электрон е–
-1
0
р+
+1
1
Нейтрон n0
0
1
Протон
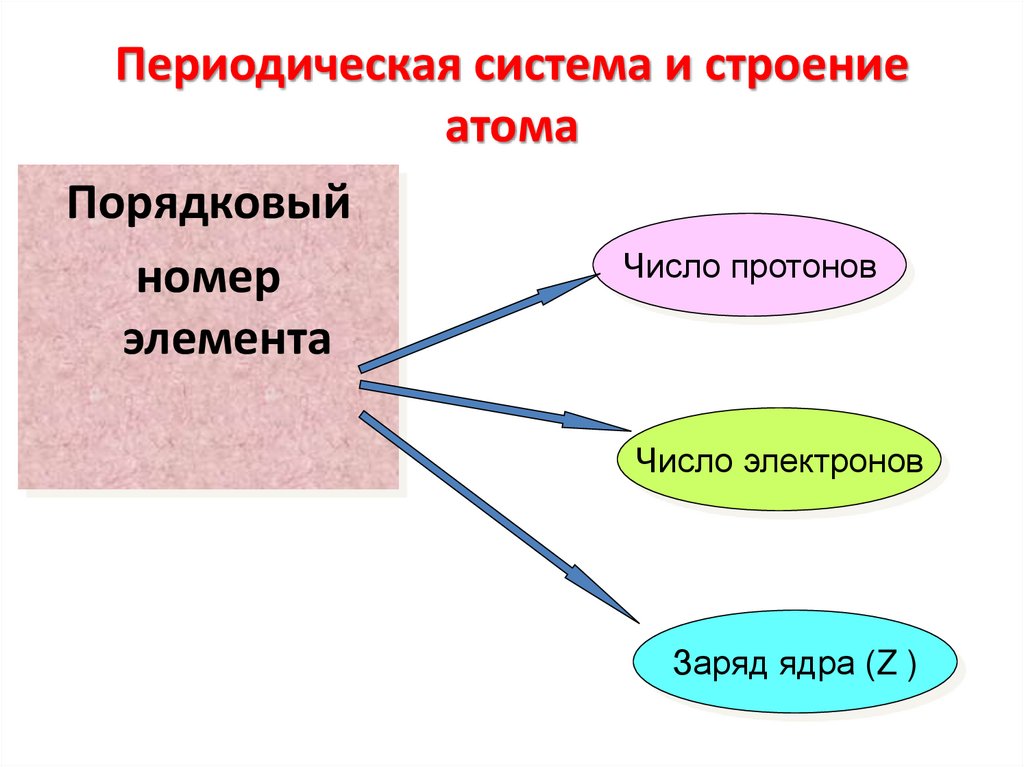
14. Периодическая система и строение атома
ПорядковыйЧисло протонов
номер
элемента
Число электронов
Заряд ядра (Z )
15.
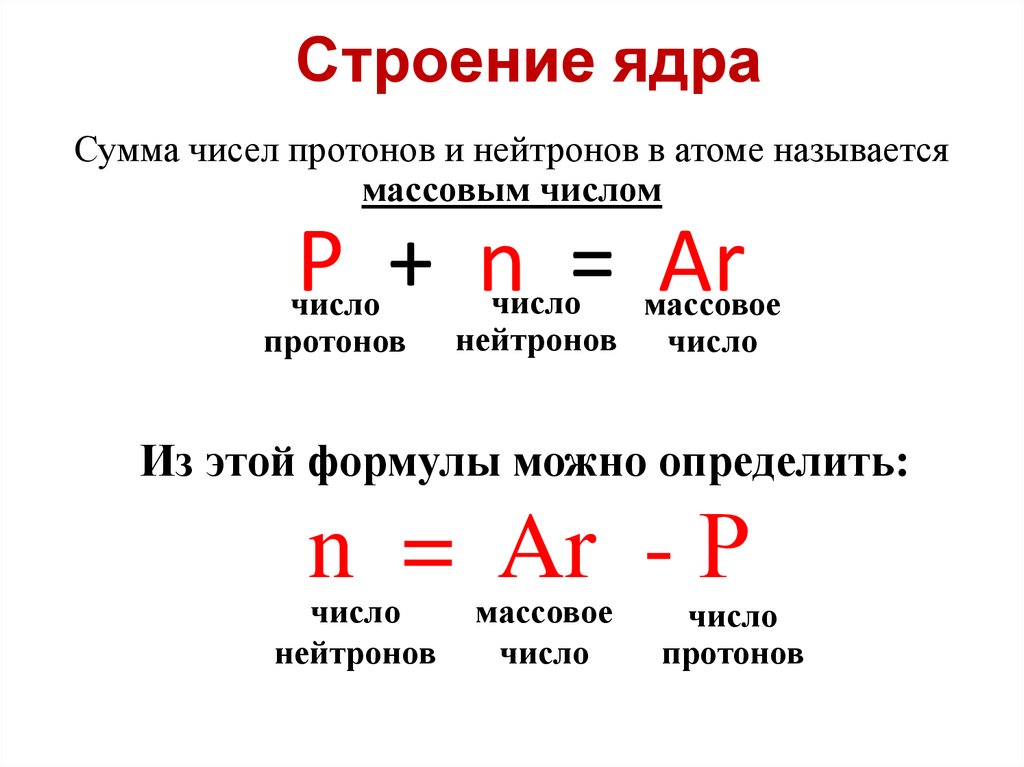
Строение ядраСумма чисел протонов и нейтронов в атоме называется
массовым числом
Р + n = Ar
число
протонов
число
массовое
нейтронов число
Из этой формулы можно определить:
n = Ar - Р
число
нейтронов
массовое
число
число
протонов
16.
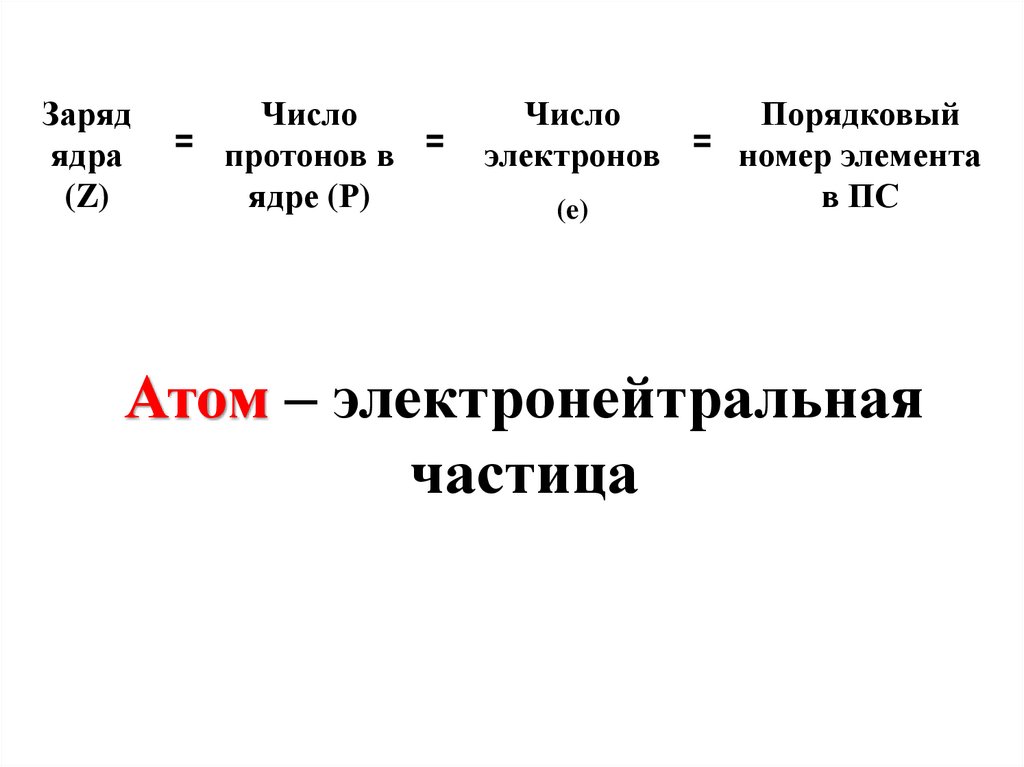
Зарядядра
(Z)
Число
= протонов в =
ядре (Р)
Число
Порядковый
электронов = номер элемента
в ПС
(e)
Атом – электронейтральная
частица
17.
Алгоритм определениясостава атома:
1. По ПСХЭ определить порядковый номер химического
элемента.
Порядковый номер элемента в ПСХЭ = заряду ядра атома
(Z)
2. Заряд ядра атома (Z) = числу протонов (P)
3. Число протонов (Р) = числу электронов (е)
4. Число нейтронов (n) = массовое число (А) – заряд ядра (Z)
18.
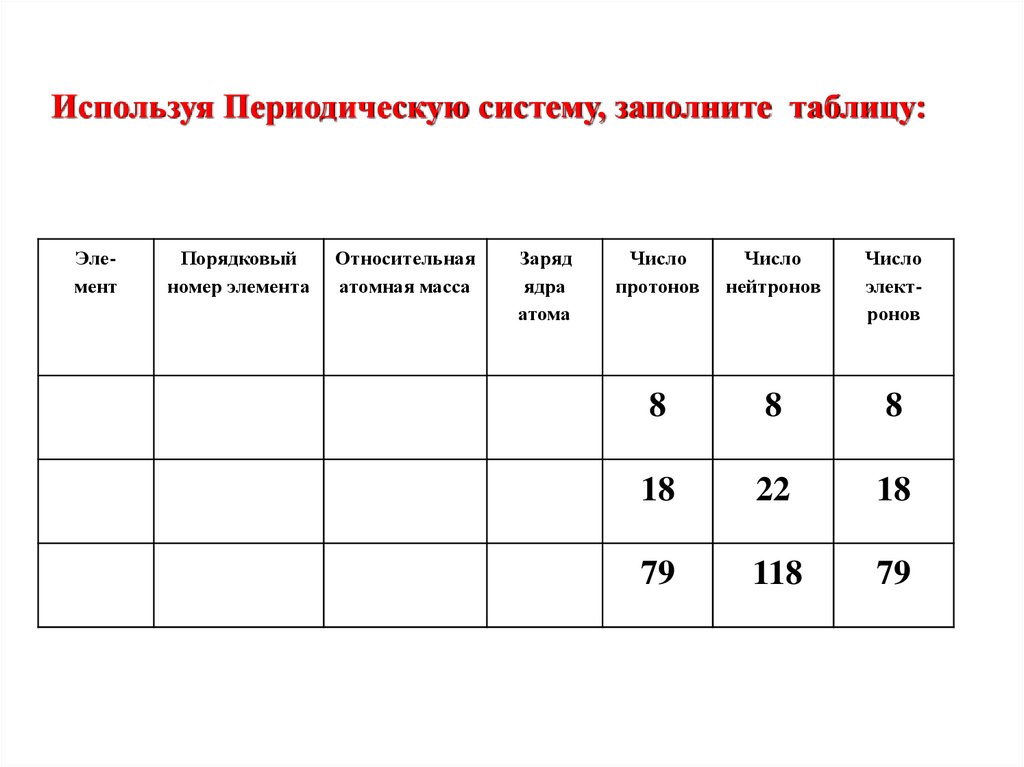
Используя Периодическую систему, заполните таблицу:Элемент
Порядковый
номер элемента
Относительная
атомная масса
Заряд
ядра
атома
Число
протонов
Число
нейтронов
Число
электронов
8
8
8
18
22
18
79
118
79
19.
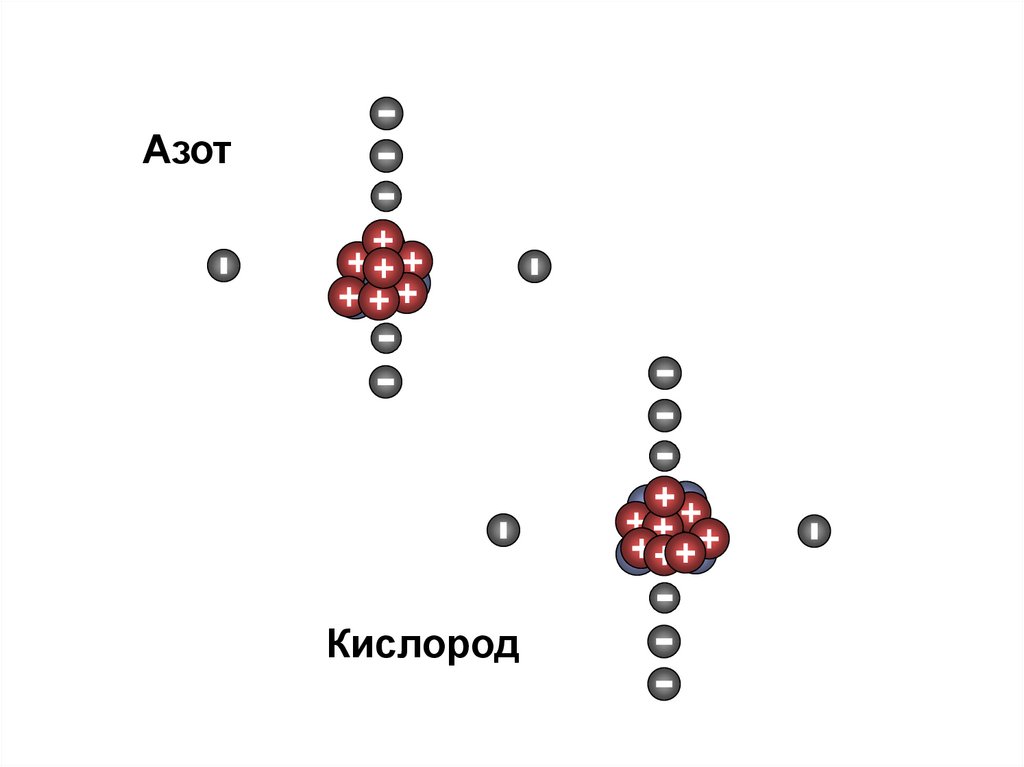
АзотКислород
20.
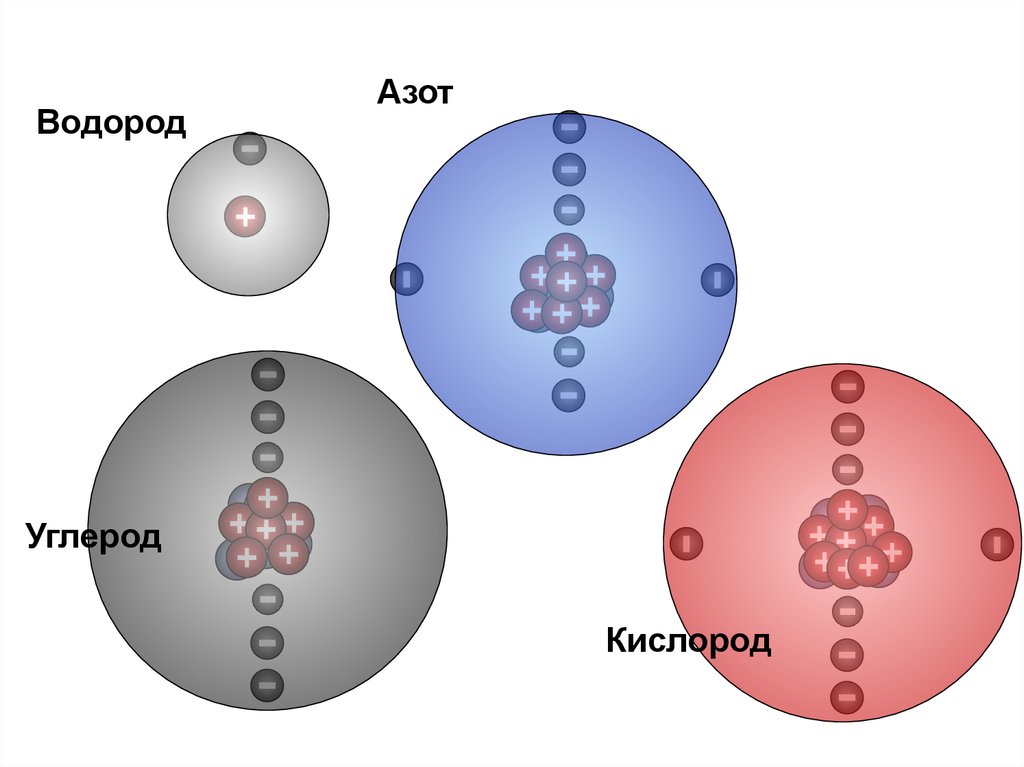
ВодородАзот
Углерод
Кислород
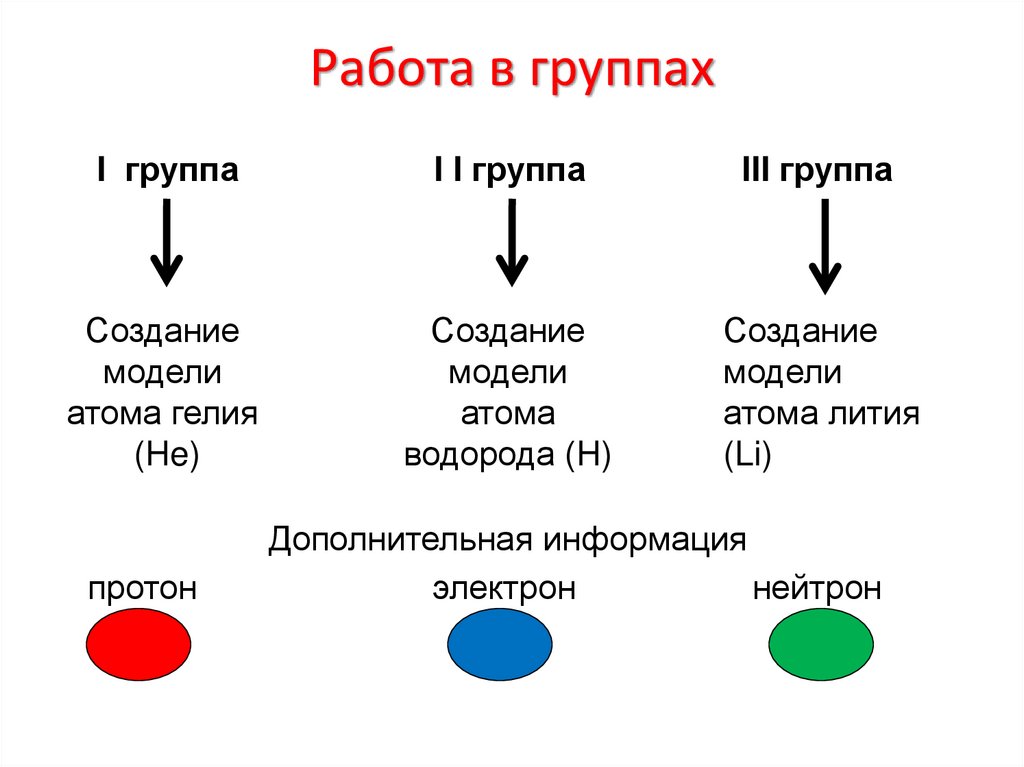
21. Работа в группах
I группаI I группа
III группа
Создание
модели
атома гелия
(He)
Создание
модели
атома
водорода (H)
Создание
модели
атома лития
(Li)
протон
Дополнительная информация
электрон
нейтрон
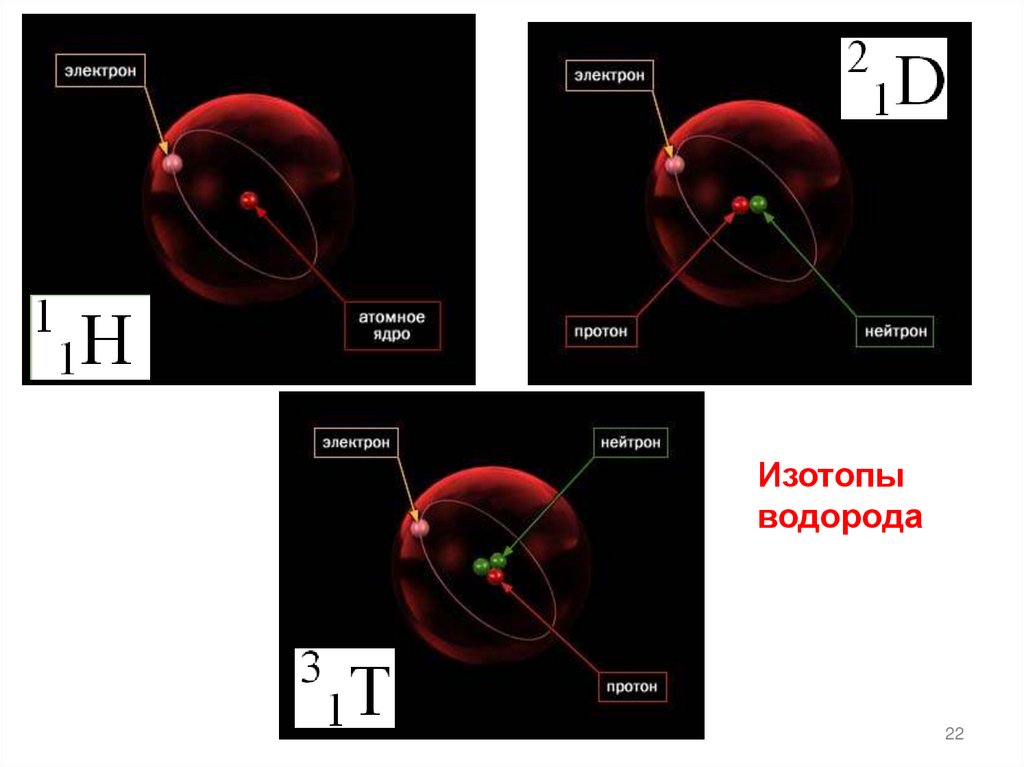
22.
Изотопыводорода
22
23.
е–-
е–
-
е–
р+
n
n
+
р
+
р
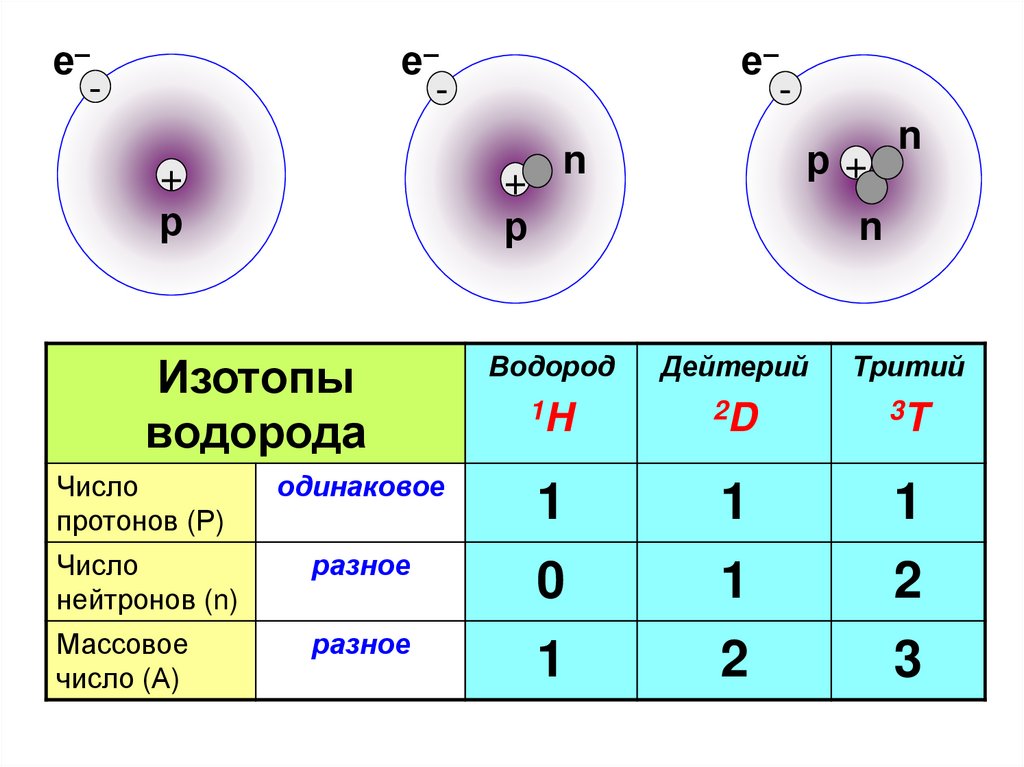
Изотопы
водорода
Водород
Дейтерий
Тритий
1H
2D
3T
n
Число
протонов (Р)
одинаковое
1
1
1
Число
нейтронов (n)
разное
0
1
2
Массовое
число (А)
разное
1
2
3
24.
• Химический элемент – этосовокупность атомов с
одинаковым зарядом ядра.
25. Домашнее задание: Ответить на вопросы тестов
1) Заряд ядра атома азота равен :а) 7 б) 13 в) 4 г) 29 д) 11
2) Число протонов в ядре атома криптона :
а ) 36 б) 17 в) 4 г) 31 д) 6
3) Число нейтронов в ядре атома цинка :
а) 8
б) 35 в) 11 г) 30 д) 4
4) Число электронов в атоме железа :
а) 11 б) 8 в) 56 г) 26 д) 30
5) Изотопы водорода отличаются друг от друга :
а)числом электронов; б)числом нейтронов;
в) химическим знаком; г) числом протонов; д)массовым
числом
26. Критерии оценки:
5, 6 верных ответов –4 верных ответа –
3 верных ответа –
«5»
«4»
«3»
27. Рефлексия
• «Сегодня я узнал…»• «Я понял, что…»
• «Теперь я могу…»
• «Я приобрел…»
• «Я научился…»














 Химия
Химия








