Похожие презентации:
Кристаллические и аморфные тела
1. Кристаллические и аморфные тела
Физика 8 классУрок №3
2.
Твёрдое тело — одно из четырёхосновных агрегатных состояний вещества,
отличающееся от других агрегатных
состояний (жидкости, газов, плазмы)
стабильностью формы и характером теплового
движения атомов, совершающих
малые колебания около положений
равновесия.
3. Свойства вещества в твёрдом состоянии
Сохраняют объём и форму4.
Раздел физики, изучающий состав и внутреннюю структурутвёрдых тел, называется физикой твёрдого тела.
Все твердые тела обладают следующими общими свойствами:
1.Способностью долгое время сохранять форму и объем
(геометрические размеры);
2.Наличием упругих сил, которые возникают при небольших
изменениях объема от внешнего воздействия (сжатия,
растяжения или сдвига).
5. Твёрдое состояние вещества – одно из агрегатных состояний
Плотность некоторых веществ в твёрдом состоянииСталь 7800 кг/м3
Медь 8900 кг/м3
Свинец 11300 кг/м3
6.
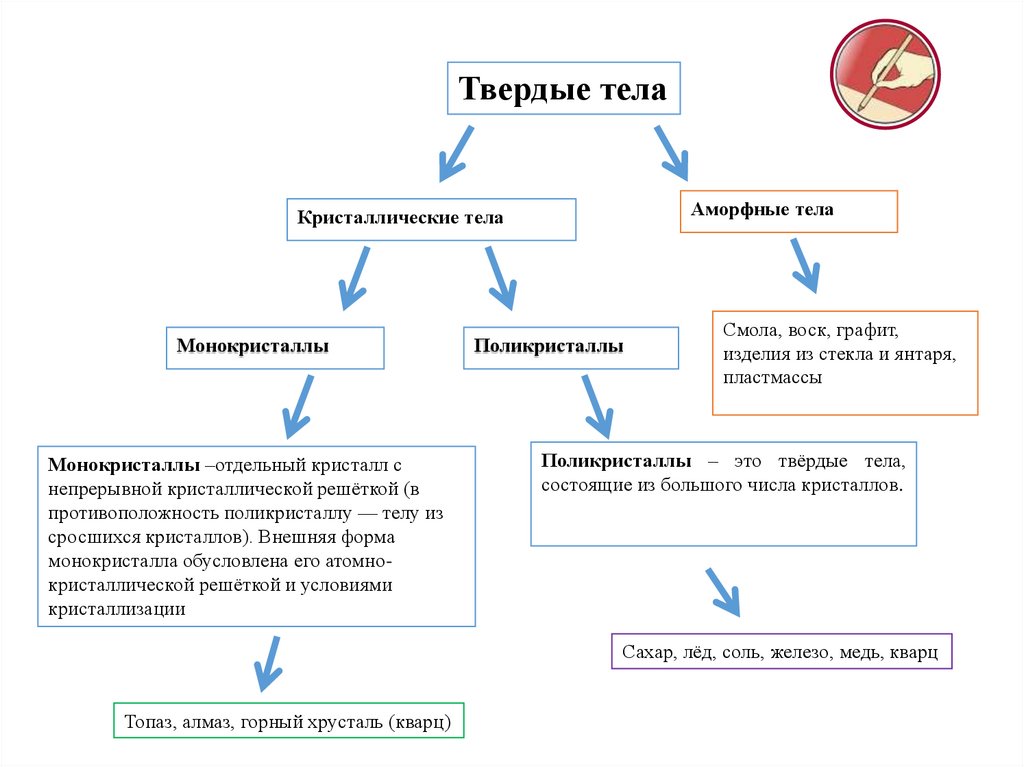
Твердые телаАморфные тела
Кристаллические тела
Монокристаллы
Монокристаллы –отдельный кристалл с
непрерывной кристаллической решёткой (в
противоположность поликристаллу — телу из
сросшихся кристаллов). Внешняя форма
монокристалла обусловлена его атомнокристаллической решёткой и условиями
кристаллизации
Поликристаллы
Смола, воск, графит,
изделия из стекла и янтаря,
пластмассы
Поликристаллы – это твёрдые тела,
состоящие из большого числа кристаллов.
Сахар, лёд, соль, железо, медь, кварц
Топаз, алмаз, горный хрусталь (кварц)
7. Монокристалл – большой одиночный кристалл
малахиткварц
Монокристаллы обладают анизотропией свойств,
т.е. их свойства разные по разным направлениям
8. Поликристаллы – это кристаллы, состоящие из большого числа монокристаллов
Поликристаллыобладают свойством
изотропии,
т.е. свойства
одинаковые
по разным
направлениям
9.
О.В. Кононов у кристалла кварца с г. Неройки (Прип.Урал, Россия), который воспроизведен в
"Занимательной минералогии" А.Е. Ферсмана. Фото:
© А.А. Евсеев.
10.
Уникальная по размеру, качеству и сохранностидруза дальнегорского датолита.
11.
Датолит. Боросиликатное м-ние,Дальнегорск, Приморье, Россия.
Кристалл ~20 см. ".
12.
Изумруды13.
Кристаллические телаКристаллы встречаются нам повсюду. Мы ходим по кристаллам,
строим из кристаллов, обрабатываем кристаллы на заводах,
создаём приборы и изделия из кристаллов; проникаем в тайны
строения кристаллов, любуемся ими.
Песок и гранит, поваренная соль и сахар, алмаз и изумруд, медь
и железо – всё это кристаллические тела.
14. Некоторые твёрдые тела встречаются в природе в виде кристаллов
Кристалл (от греч.κρύσταλλος — лёд,
горный хрусталь) —
твёрдое или жидкое
вещество, состоящее из
регулярно
расположенных атомов,
молекул, ионов или их
групп.
Кристалл кварца
15.
Свойства:1.Геометрическая форма (правильная)
2.Постоянная температура плавления
(известно из практики)
3.Анизотропия
16.
Анизотропия – (от греч. ánisos – неравный и tróроs – направление),зависимость физических свойств вещества от направления. Примеры:
пластинка слюды легко расщепляется на тонкие листочки только вдоль
определённой
плоскости.
особенность монокристаллов.
Анизотропия
–
наиболее
характерная
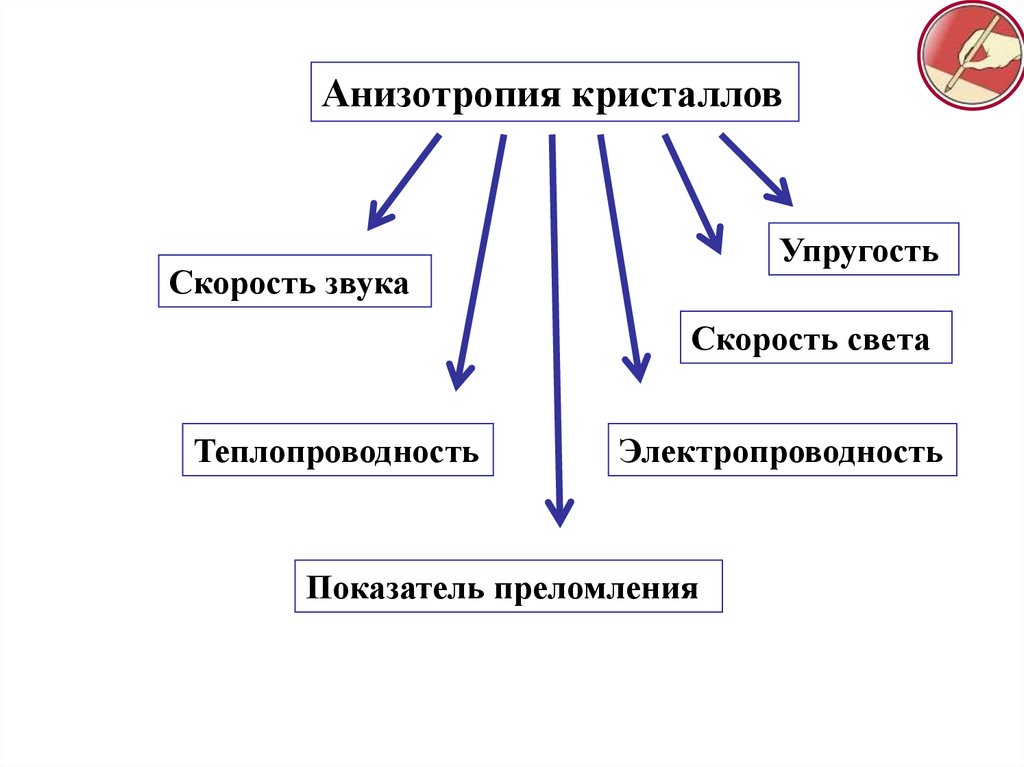
17.
Анизотропия кристалловУпругость
Скорость звука
Скорость света
Теплопроводность
Электропроводность
Показатель преломления
18.
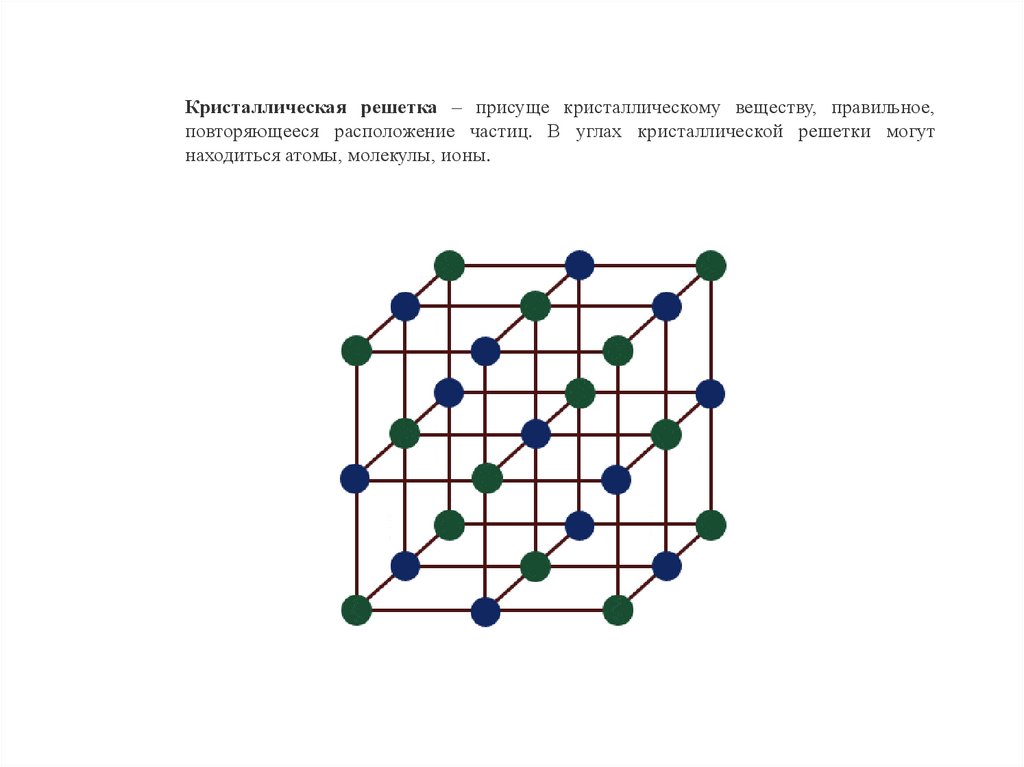
Кристаллическая решетка – присуще кристаллическому веществу, правильное,повторяющееся расположение частиц. В углах кристаллической решетки могут
находиться атомы, молекулы, ионы.
19. Форма кристалла обусловлена его внутренним строением
Кристалл поваренной соли NaClКристалл углерода С
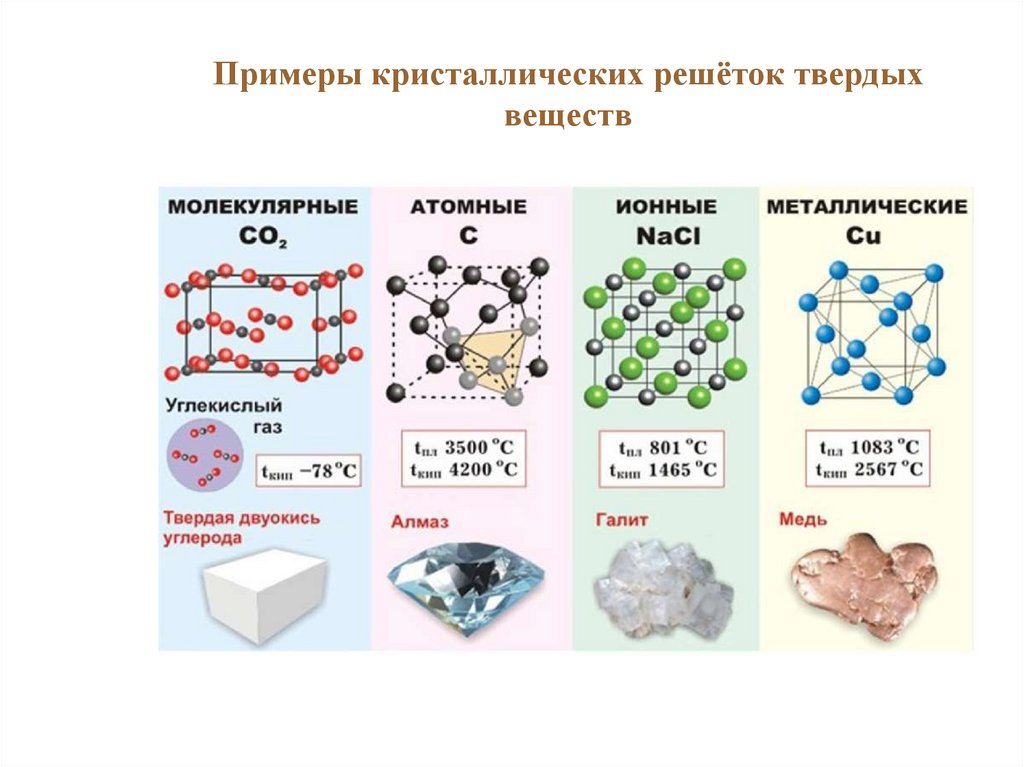
20.
Примеры кристаллических решёток твердыхвеществ
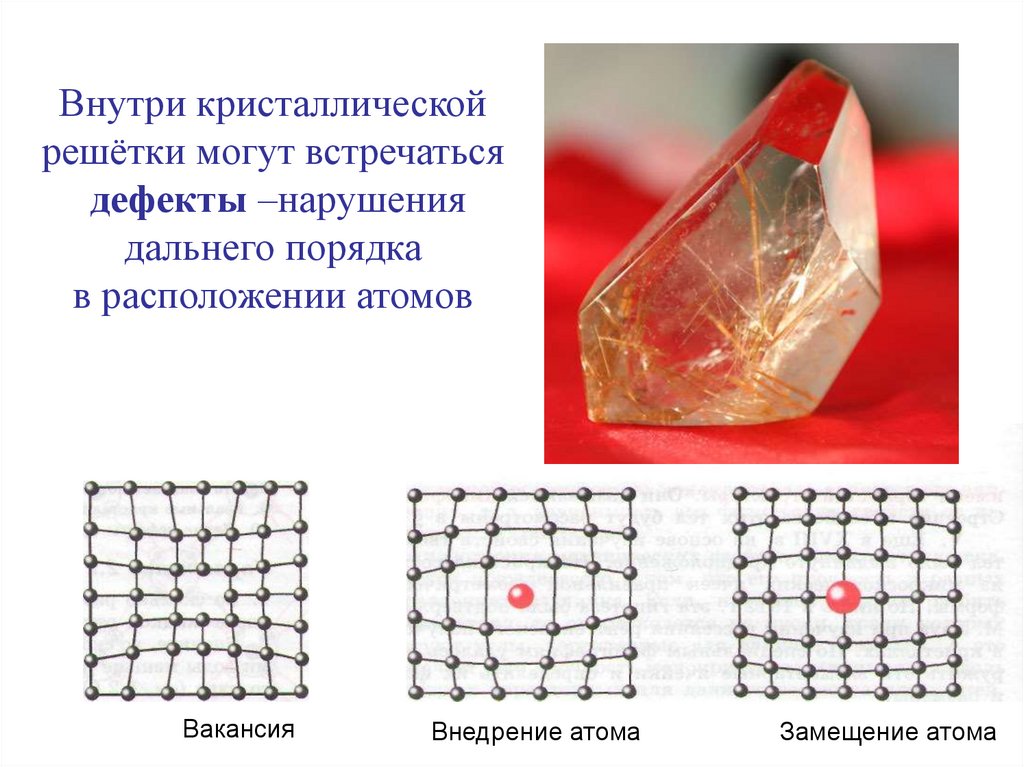
21. Внутри кристаллической решётки могут встречаться дефекты –нарушения дальнего порядка в расположении атомов
ВакансияВнедрение атома
Замещение атома
22.
Часто встречаются кристаллические тела одинаковые по своему химическому составу, нообладающие очень разные физические свойства. Самый известный пример — это углерод,
имеющий две модификации: графит и алмаз. Разное строение кристаллических решеток
является причиной того, что алмаз имеет рекордные показатели твердости, а графит из-за
его мягкости используется в качестве грифелей для карандашей.
23.
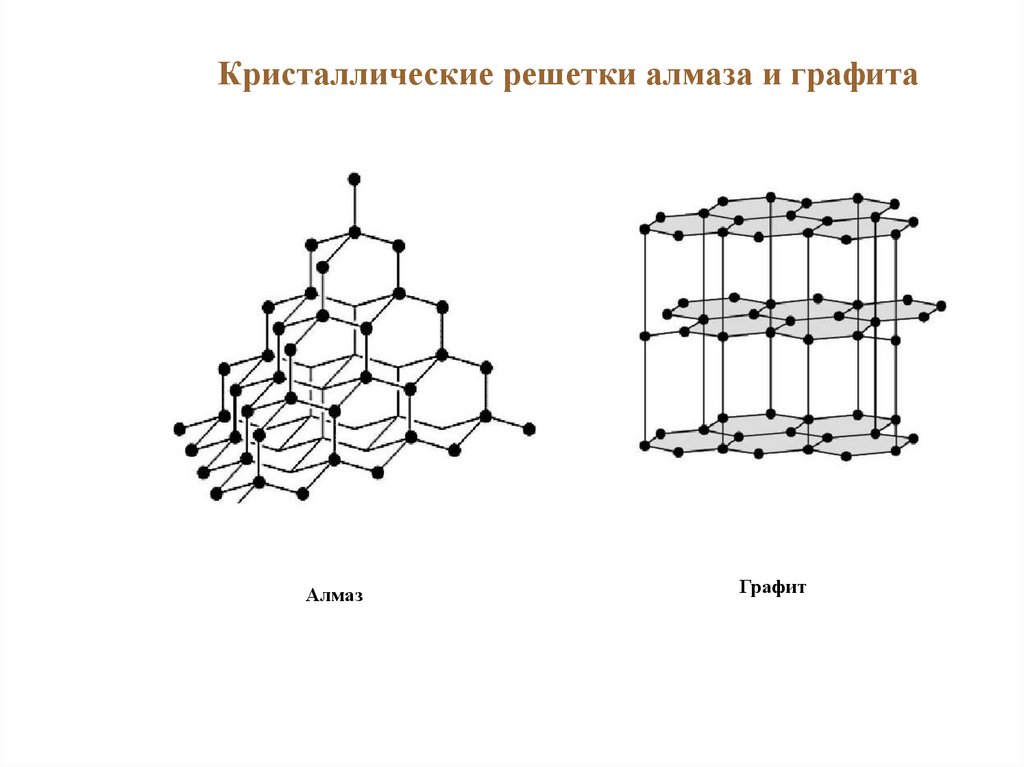
Кристаллические решетки алмаза и графитаАлмаз
Графит
24.
Свойства поликристаллов:1.Геометрическая форма (неправильная)
2.Температура плавления постоянная
3.Изотропия
25.
Изотропия – независимость физических свойств тела от выбранного в нем направления.Слово «изотропия» составлено из двух греческих слов: isos — ровный, tropos —
направление.
Изотропия связана с отсутствием упорядоченного внутреннего строения; присуща газам,
жидкостям (кроме жидких кристаллов) поликристаллам и аморфным телам.
26.
Аморфные телаАморфными называют вещества у которых нет
строгого порядка в расположении частиц.
Смола, воск, графит, изделия из стекла и янтаря, пластмассы —
все это примеры аморфных тел (от греческого слова Amorphous
— бесформенный, некристаллический).
27.
Отсутствие дальнего порядка в расположении частиц вещества уаморфных тел приводит к тому, что их физические свойства
одинаковы во всех направлениях, то есть изотропными.
28.
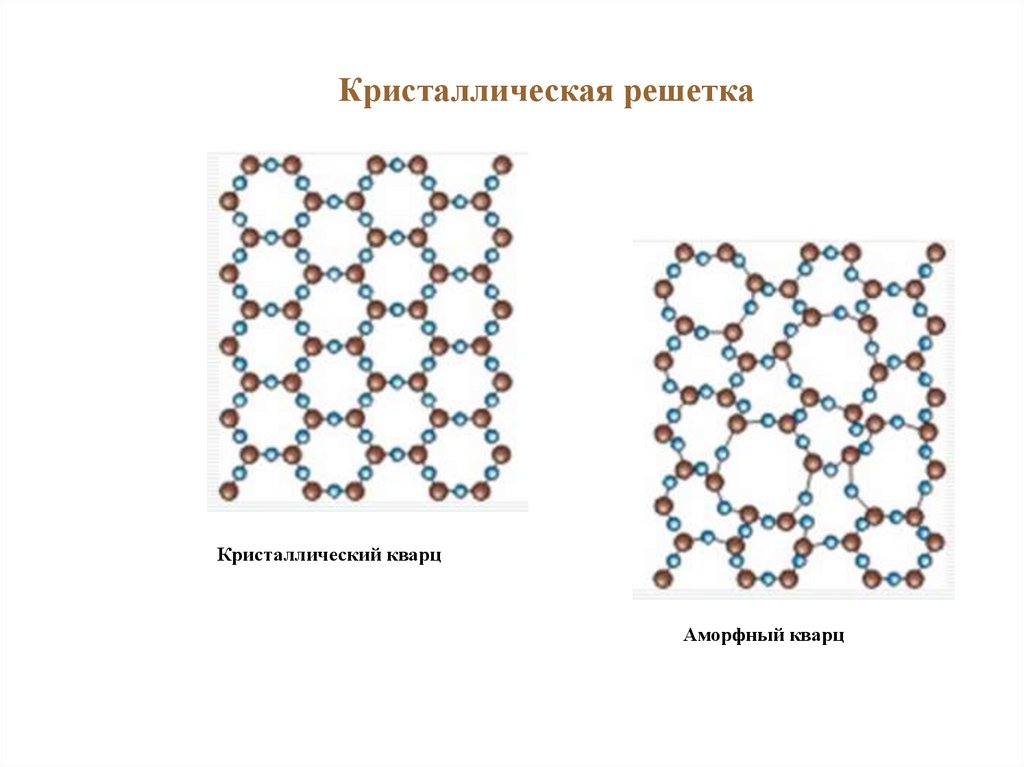
Кристаллическая решеткаКристаллический кварц
Аморфный кварц
29.
Особенности аморфных веществ1. Нет строгого расположения частиц, нет кристаллической
решетки.
2. Изотропность физических свойств. Является следствием
хаотичного расположения составляющих их молекул и
атомов.
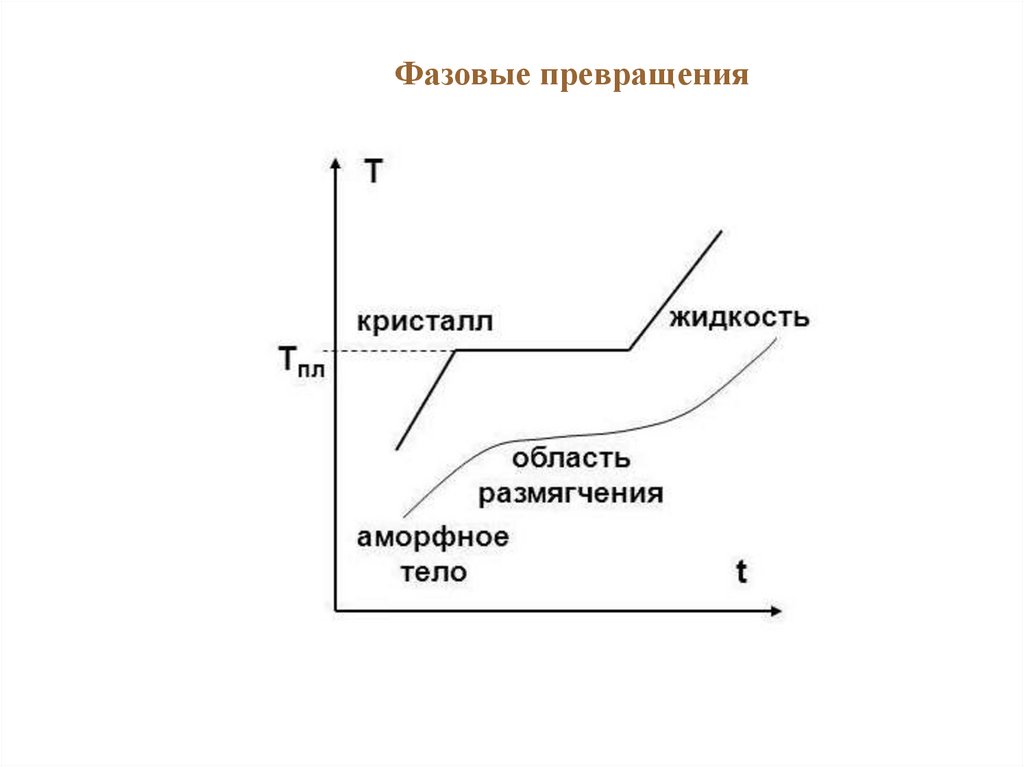
3. Нет строго определенной температуры плавления, то есть
отсутствует четкий переход от твердого состояния к жидкому:
при нагревании аморфное тело становится только более
текучим.
4. Способность аморфных тел становиться вязкими
нагревании позволяет придавать им любую форму.
при
30.
Фазовые превращения31.
Подведём итоги!1. Кристаллические и аморфные тела кроме общих
признаков, которые относят их к твердым телам,
имеют совершенно разные физические свойства.
2. Аморфные
тела
обладают
изотропными
свойствами, а для кристаллов характерна
анизотропия физических параметров.
3. Кристаллические тела делятся на монокристаллы
и поликристаллы.
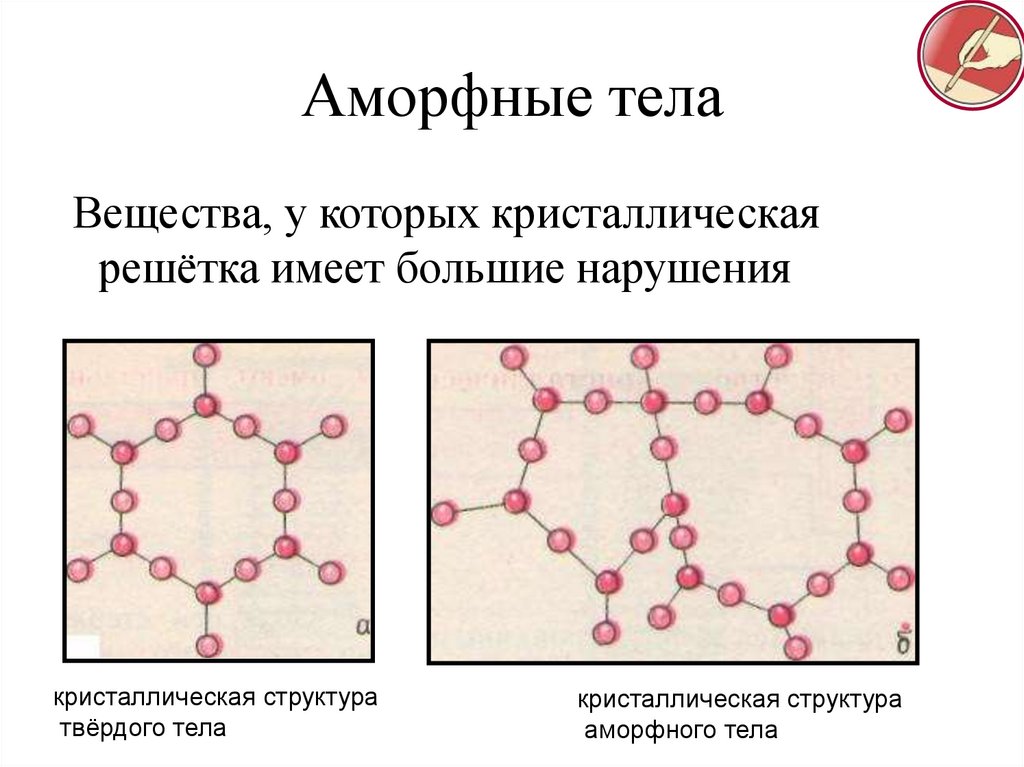
32. Аморфные тела
Вещества, у которых кристаллическаярешётка имеет большие нарушения
кристаллическая структура
твёрдого тела
кристаллическая структура
аморфного тела
33. Примеры веществ, находящихся в аморфном состоянии
• воск,• парафин,
• смола,
• гудрон,
• стекло
• янтарь
34.
Задание: заполните таблицуЛинии сравнения
Кристаллические
Монокристалл
1. Определение
2. Примеры
3. Строение
4. Свойства
5. Где
используются
Поликристалл
Аморфные

























 Физика
Физика








