Похожие презентации:
Алканы. Определение. Общая формула класса углеводородов
1.
Алканы.2. План.
1.2.
3.
4.
5.
6.
7.
8.
Определение. Общая формула
класса углеводородов.
Гомологический ряд.
Виды изомерии.
Номенклатура алканов
Строение алканов.
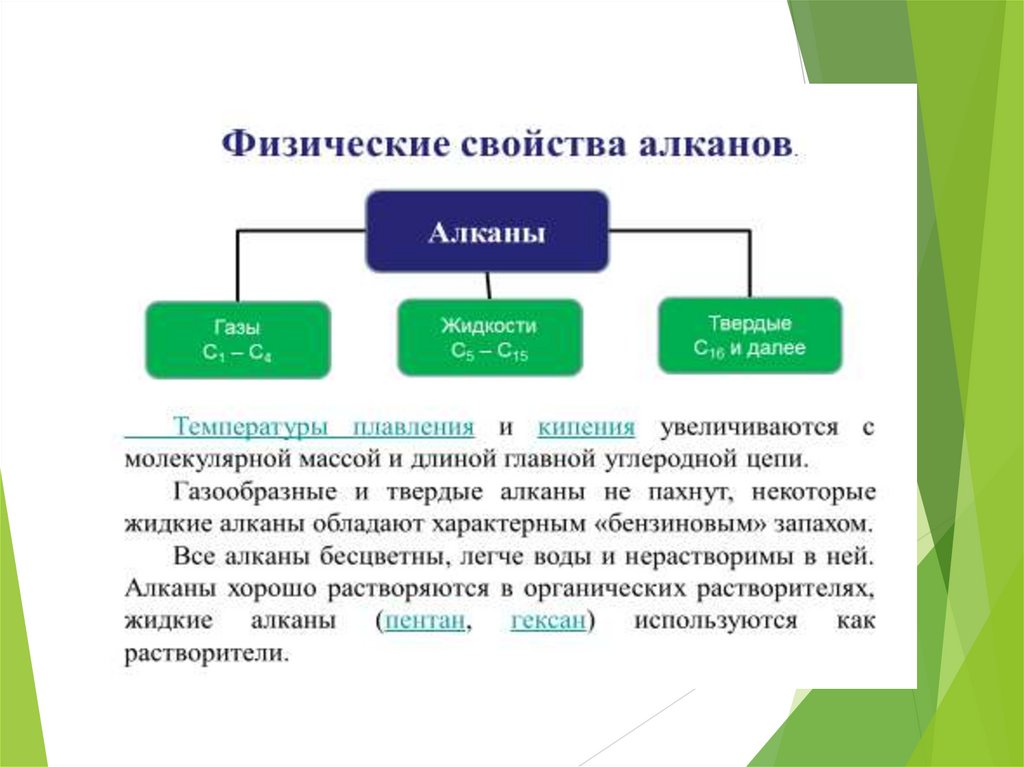
Физические свойства.
Химические свойства.
Применение.
3. Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды.)
Алканы - углеводороды в молекулах которых все атомыуглерода связаны одинарными связями (σ-) и имеют
общую формулу:
CnH2n+2
4. Гомологический ряд метана
Гомологи – это вещества, сходные по строению и свойствами отличающиеся на одну или более групп СH2.
СН4
С2 H 6
C3H8
C4H10
C5H12
метан
этан
пропан
бутан
пентан
C6H14 гексан
C7H16 гептан
C8H18 октан
C9H20 нонан
C10H22 декан
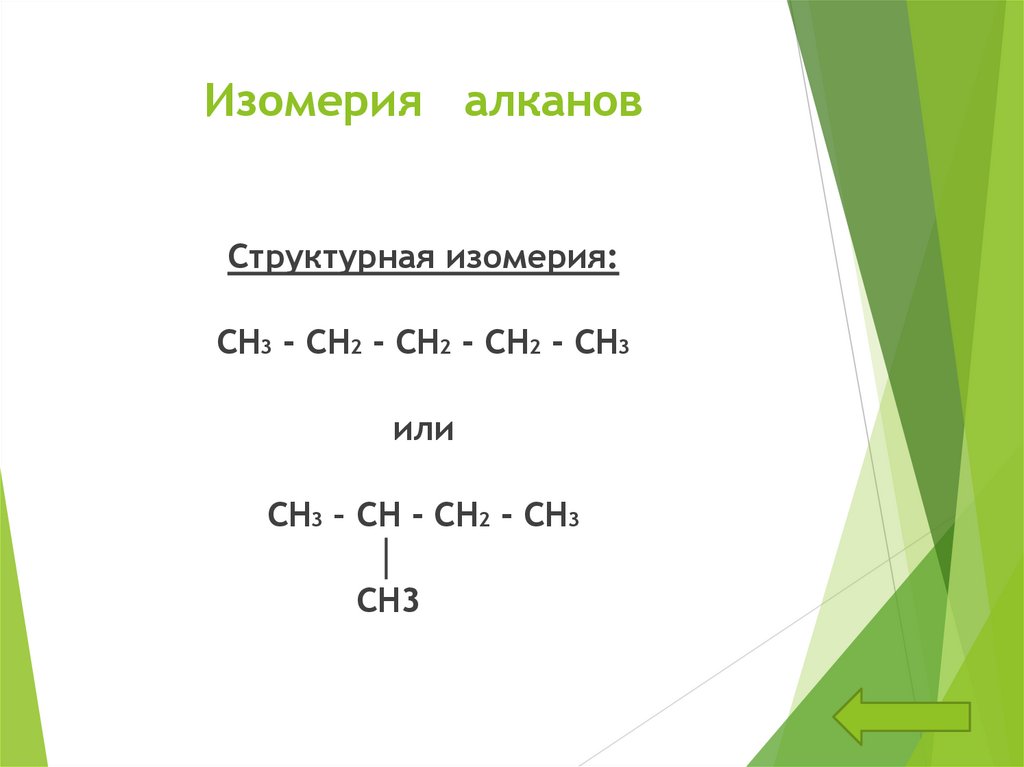
5. Изомерия алканов
Структурная изомерия:CH3 - CH2 - CH2 - CH2 - CH3
или
CH3 – CH - CH2 - CH3
│
CH3
6. номенклатура алканов
Алгоритм называния алканов1.
В структурной формуле выбирают самую
длинную цепь атомов углерода (главную цепь) :
CH3 – CH - CH2 - CH3
│
CH3
7. Номенклатура алканов
2. Атомы углерода главной цепи нумеруют,начиная с того конца, к которому ближе
разветвление :
1
2
3
4
CH3 – CH - CH2 - CH3
│
CH3
8. Номенклатура алканов
3. В начале названия перечисляют радикалы и другие заместители суказанием номеров атомов углерода, с которыми они связаны.
Если в молекуле присутствует несколько одинаковых радикалов
(два, три, четыре и т. д.), то цифрой указывают место каждого из
них в главной цепи и перед их названием ставят соответственно
частицы ди-, три-, тетра- и т. д.:
1
2
3
4
CH3 – CH - CH2 - CH3
│
CH3
2 - метилбутан
9.
4. Основой названия служит наименованиепредельного углеводорода с тем же числом
атомов углерода, что и в главной цепи.
1
2
3
4
CH3 – CH - CH2 - CH3
│
CH3
2 - метилбутан
10. Радикал — это одновалентная частица, которая получается при отщеплении от молекулы алкана атома водорода, т. е. частица,
содержащая неспаренный электрон. Названиерадикала происходит от названия соответствующего алкана
с заменой суффикса -ан, на суффикс –ил
Число
1
Название
числа
Моно-
Формула
радикала
-СН3
Название
радикала
Метил
2
Ди-
-С2Н5
Этил
3
Три-
-С3Н7
Пропил
4
Тетра-
-С4Н9
Бутил
5
Пента-
-С5Н11
Пентил
11.
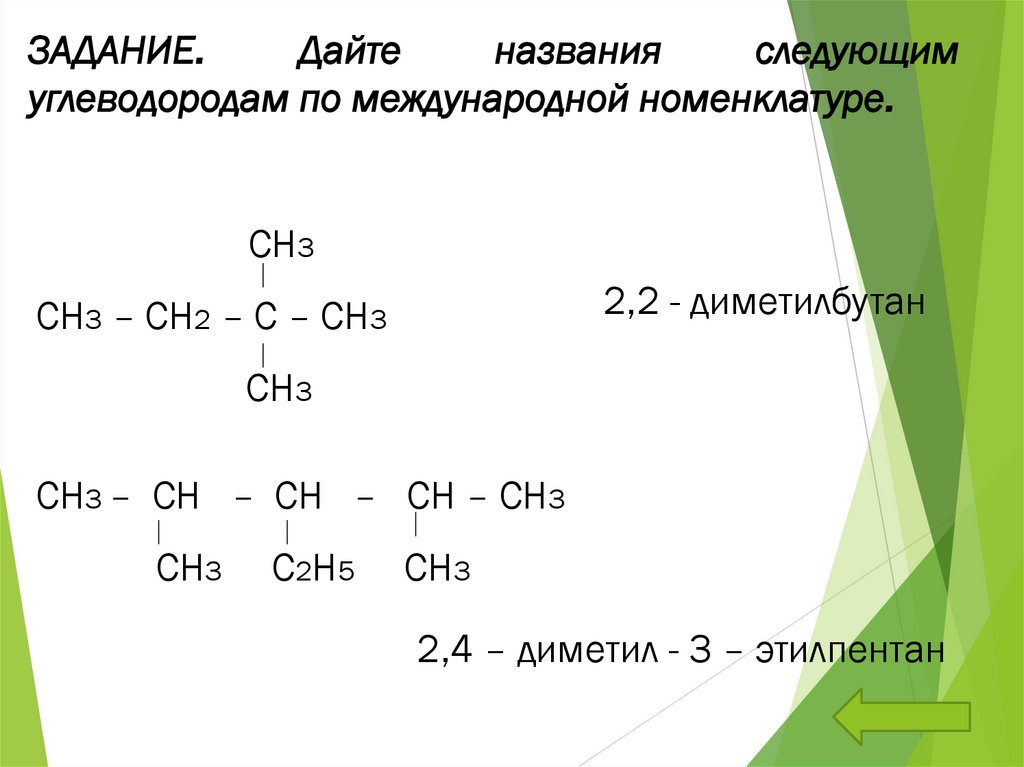
ЗАДАНИЕ.Дайте
названия
следующим
углеводородам по международной номенклатуре.
СН3
2,2 - диметилбутан
СН3 – СН2 – С – СН3
СН3
СН3 – СН – СН – СН – СН3
СН3
С2Н5
СН3
2,4 – диметил - 3 – этилпентан
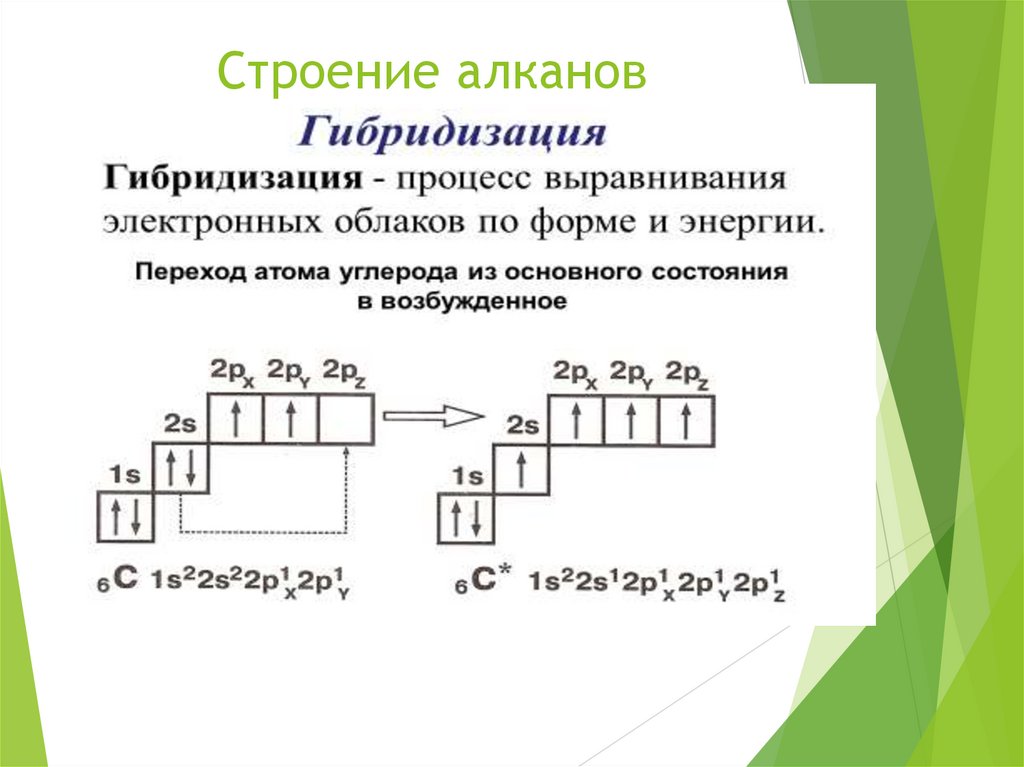
12. Строение алканов
13.
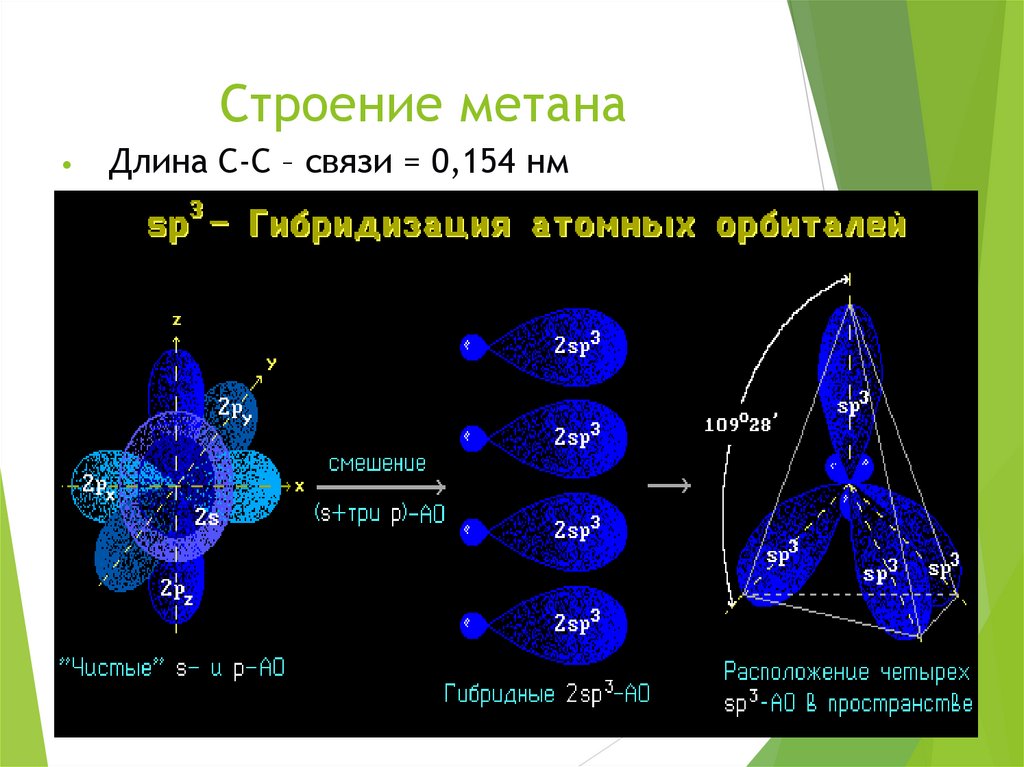
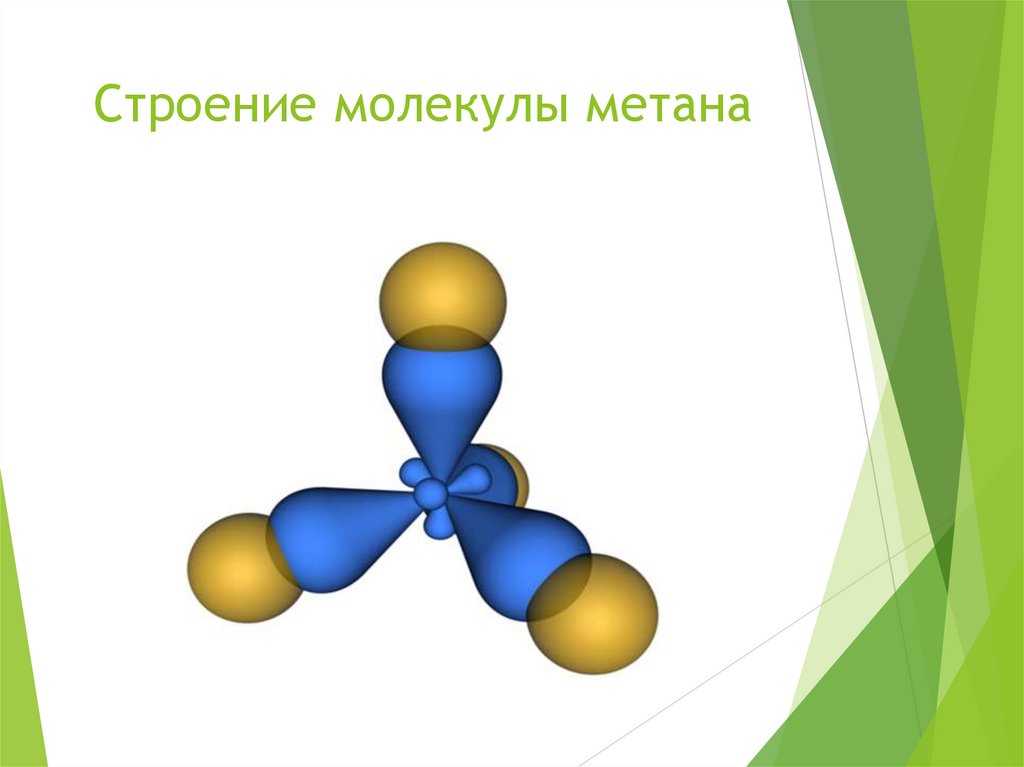
14. Строение метана
Длина С-С – связи = 0,154 нм
15. Строение молекулы метана
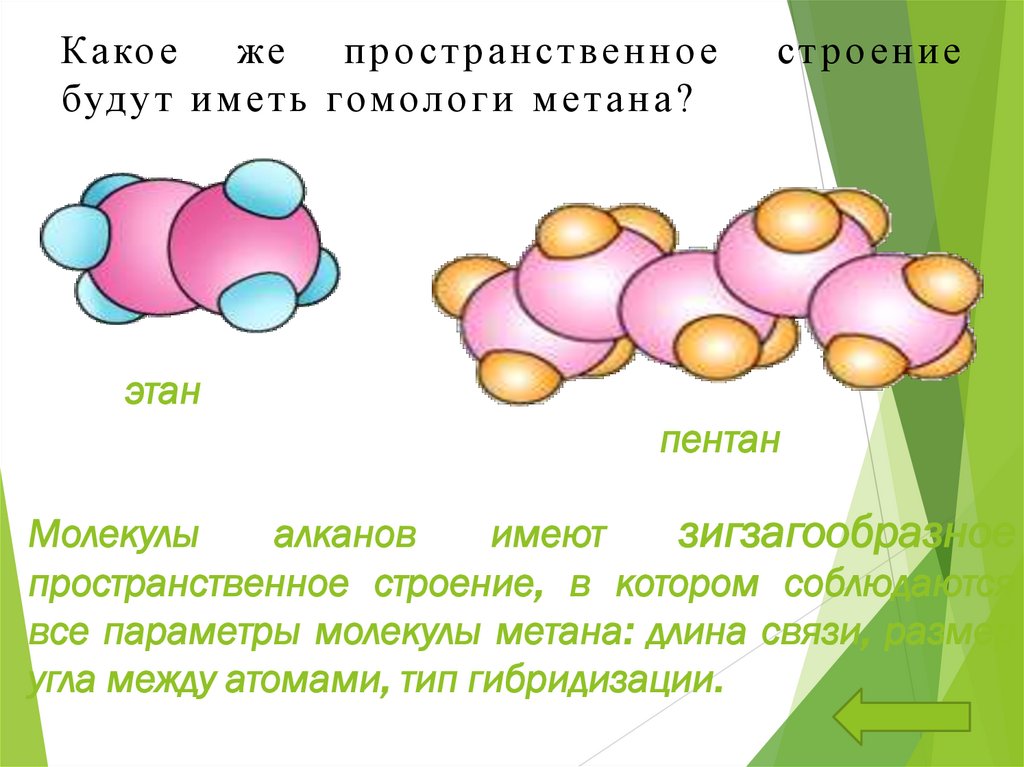
16. Какое же пространственное строение будут иметь гомологи метана?
Ка ко е же п р о с т р а н с т в е н н о ебуд у т и м е т ь гом ол о г и м е т а н а ?
строение
этан
пентан
Молекулы
алканов
имеют
зигзагообразное
пространственное строение, в котором соблюдаются
все параметры молекулы метана: длина связи, размер
угла между атомами, тип гибридизации.
17.
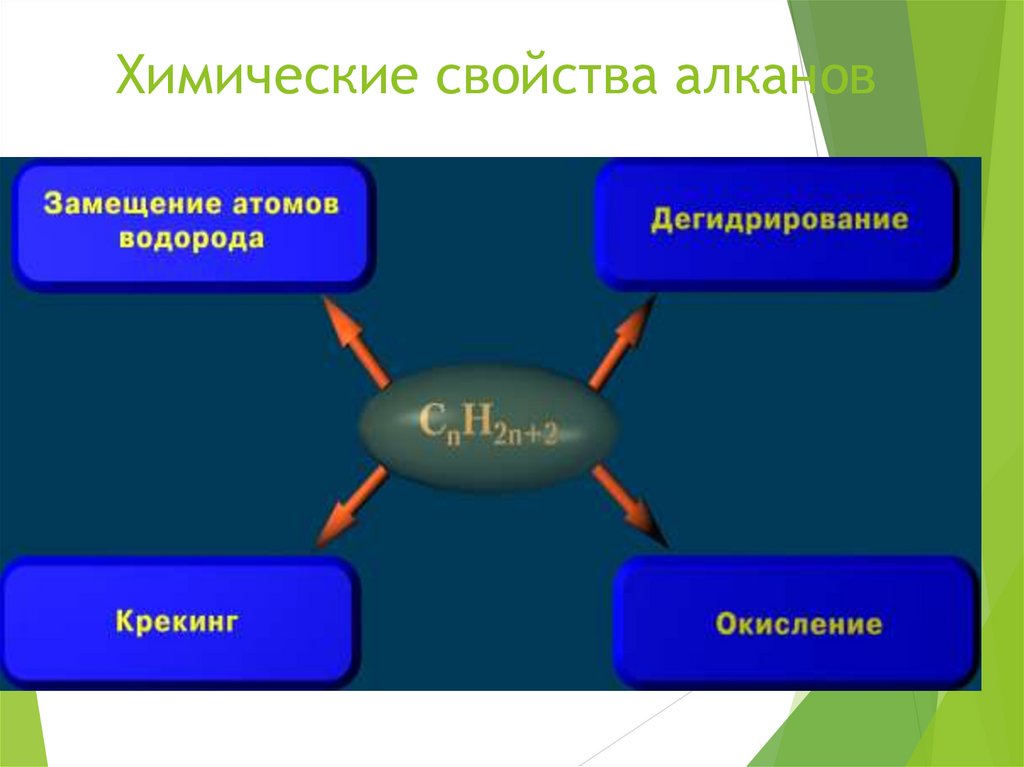
18. Химические свойства алканов
19.
20.
21.
22. 3.Реакции дегидрирования
дегидрированием этана получают этилен— ценный химический продукт:
23. 4. Метан вступает в реакции полного разложения
При температуре 1000 °С происходит полноеразложение метана. При этом образуются сажа
и водород:
24. Метан вступает в реакции неполного разложения
Неполное разложение метана проводят притемпературе 1500 °С и резком охлаждении
продуктов реакции. В результате этого процесса
получают важный углеводород — ацетилен
С2Н2, а также водород:
25.
Получение растворителейПолучение ацетилена
А также сырьё
для синтезов
спиртов,
альдегидов,
кислот.
Горючее для дизельных и
турбореактивных двигателей
В металлургии
26. Применение алканов
1-3 – производствосажи
(1 – картрижи;
2 – резина;
3 – типографическая
краска)
4-7 – получение
органических веществ
(4 – растворителей;
5 – хладогентов,
используемых
в холодильных
установках;
6 – метанол;
7 - ацетилен)
27. Домашнее задание
Учебник О.С. Габриелян(10 класс базовый уровень)
§ 3, упр. 4, 7, 8 (стр. 32)



















 Химия
Химия








