Похожие презентации:
кремний - др9-02-25
1.
Кремний – физика и химия элементаПрезентацию подготовили студентки
1 курса группы ДР9-02-25
Байсарова Иман
Закутняя Милана
Сарымсакова Ясмин
Тохтаева Латифа
Элжанова Шахмина
2.
Физические свойства кремнияВнешний вид
1
Тёмно-серый, хрупкий кристалл с характерным металлическим блеском. В чистом виде выглядит как
полуметаллический материал.
Кристаллическая структура
2
3
Имеет кубическую алмазоподобную кристаллическую решётку. Благодаря прочным ковалентным связям, его твёрдость
составляет 7 по шкале Мооса, что делает его весьма устойчивым к механическим воздействиям.
Термические характеристики
Высокая температура плавления 1415 °C и плотность 2,33 г/см³ при стандартных условиях.
Ключевое свойство: Кремний является полупроводником. Его электропроводность резко возрастает с
повышением температуры и при воздействии света (фотоэффект), что лежит в основе работы всех электронных
устройств.
3.
Химические свойства кремнияКремний относится к IV группе Периодической системы и проявляет различные степени окисления.
Наиболее устойчивая из которых +4.
→ Степени Окисления
−4, 0, +2, +4.
Степень +4 является наиболее устойчивой и типично для
большинства природных соединений (SiO₂).
→ Взаимодействие с кислородом
При нагревании кремний горит на воздухе, образуя
диоксид кремния:
Si + O₂ → SiO₂
→ Образование Силицидов
С активными металлами при высокой температуре
образует силициды — бинарные соединения,
например:
Si + 2Mg → Mg₂Si
Кремний проявляет восстановительные
свойства, особенно при нагревании. Он
может восстанавливать воду, образуя диоксид
кремния и водород: Si + 2H₂O → SiO₂ + 2H₂
4.
Промышленные методы получения кремнияВ природе кремний никогда не встречается в чистом виде, а только в форме соединений, в первую очередь
в виде диоксида кремния (кварца, песка) и силикатов.
Восстановление SiO₂
Подготовка из SiF4
1
Промышленный способ (Металлургический)
Восстановление диоксида кремния
коксом в дуговых электропечах при
температуре ~1800°C
SiO₂ + 2C → Si + 2CO↑
Хлорирование и восстановление
2
Лабораторный метод
Восстановление тетрафторида кремния
щелочными металлами, например
калием: SiF₄ + 4K → Si + 4KF
3
Очистка (Для электроники)
Для полупроводниковых целей кремний
хлорируют до SiCl₄, который затем
очищают ректификацией и
восстанавливают водородом, получая
кремний ультравысокой чистоты.
5.
Ключевые области применения кремнияМикроэлектроника
Основа для производства интегральных схем, транзисторов и микропроцессоров.
Используется монокристаллический кремний высочайшей степени чистоты.
Фотовольтаика (Солнечные Батареи)
Фотовольтаика (Солнечные батареи)
Поликристаллический и монокристаллический кремний являются основными
материалами для создания солнечных элементов, преобразующих свет в
электричество.
Металлургия и медицина
Кремний используется в качестве легирующего элемента для получения
жаропрочных, кислотоустойчивых и прочных сплавов (например, силумина).
Кремний в медицине играет ключевую роль как структурный элемент,
необходимый для здоровья кожи, волос, ногтей, костей, суставов и сосудов,
Строительство и Керамика
Соединения кремния (SiO₂ и силикаты) незаменимы в производстве стекла,
цемента, керамических материалов и высокопрочных абразивов.
Микроэлектроника
6.
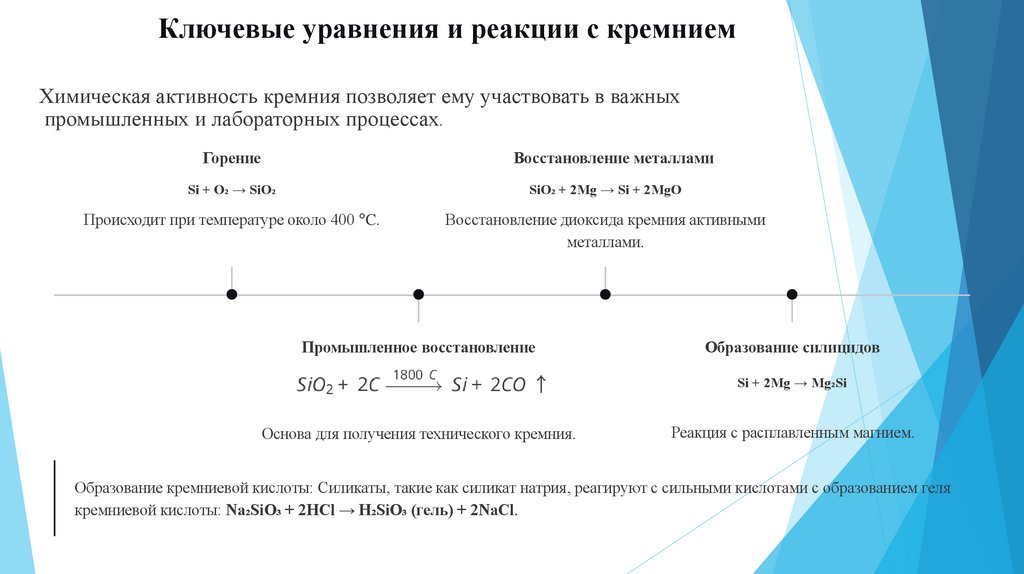
Ключевые уравнения и реакции с кремниемХимическая активность кремния позволяет ему участвовать в важных
промышленных и лабораторных процессах.
Горение
Восстановление металлами
Si + O₂ → SiO₂
SiO₂ + 2Mg → Si + 2MgO
Происходит при температуре около 400 °C.
Восстановление диоксида кремния активными
металлами.
Промышленное восстановление
Образование силицидов
Si + 2Mg → Mg₂Si
Основа для получения технического кремния.
Реакция с расплавленным магнием.
Образование кремниевой кислоты: Силикаты, такие как силикат натрия, реагируют с сильными кислотами с образованием геля
кремниевой кислоты: Na₂SiO₃ + 2HCl → H₂SiO₃ (гель) + 2NaCl.
7.
Интересные факты о кремнииКремний и древние технологии
Распространённость
Соединения кремния использовались человеком с каменного
века. Кремний (разновидность SiO₂) был критически важен
для изготовления орудий труда и добычи огня
Кремний является самым распространённым
неметаллом в земной коре и вторым по
распространённости элементом после
кислорода, составляя около 28% массы коры.
Природные формы
Роль в биологии
Кремний — основной компонент песка, кварца, горного
хрусталя, а также множества минералов, включая полевые
шпаты и слюды
Кремний необходим для многих организмов.
У растений он укрепляет клеточные стенки и
стебли. У человека входит в состав
соединительной ткани, ногтей и волос.
8.
Кремний в электронике и технологияхСпособность кремния принимать примеси (легирование) с образованием зонной структуры лежит в
основе всей современной полупроводниковой индустрии.
Легирование P-типа
Добавление атомов бора или галлия
(акцепторов) создаёт полупроводник с
дырочной проводимостью (P-тип).
Применение
Легирование N-типа
Добавление атомов фосфора или мышьяка
(доноров) создаёт электронную
проводимость (N-тип).
P-N переход
Создание высокопроизводительных
Соединение P- и N-областей формирует
микросхем, сенсоров изображения
ключевой элемент электроники — диод,
(CMOS) и мощных процессоров.
который является основой для транзисторов
и чипов.
Современные кремниевые солнечные панели достигают эффективности преобразования света в электричество более 25% в
лабораторных условиях, оставаясь наиболее распространённым типом фотоэлементов.
9.
Визуализация: от атома до энергииДва способа применения кремния: идеальная кристаллическая структура для микроэлектроники и
способность генерировать чистую энергию.
Кристаллическая решётка кремния
Идеально упорядоченная кубическая алмазоподобная
решётка обеспечивает стабильность и предсказуемость
электрических свойств.
Солнечная Энергия
Кремниевые фотоэлементы — это наиболее
распространённый источник чистой энергии в
мире








 Химия
Химия








