Похожие презентации:
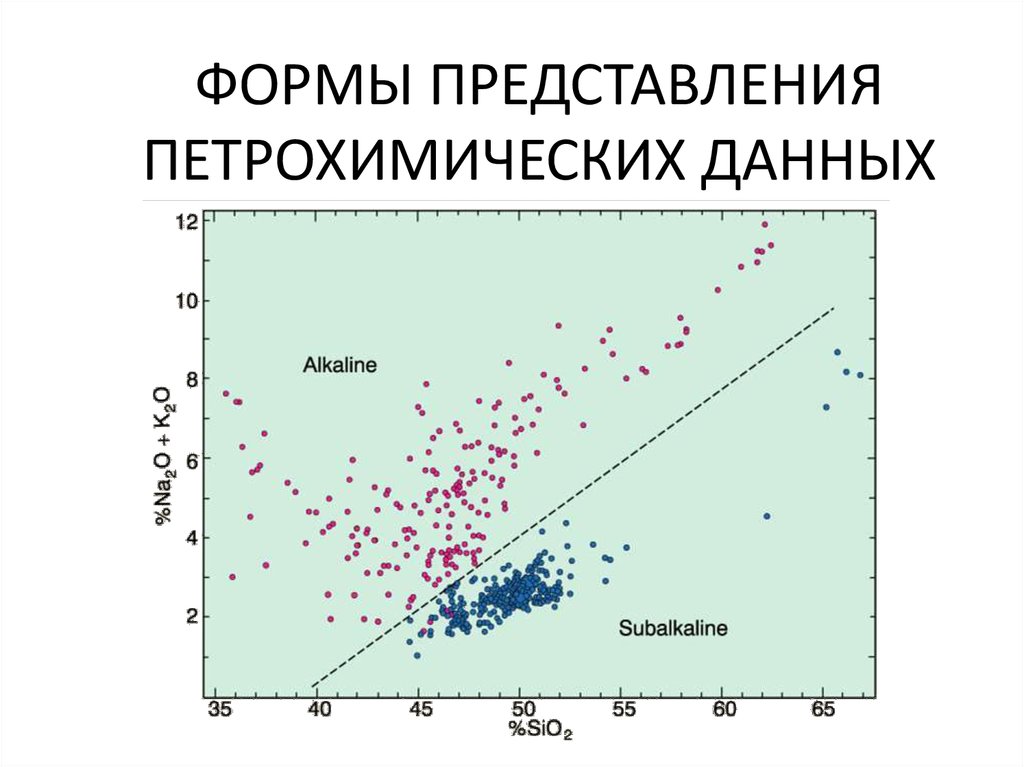
Формы представления петрохимических данных
1. ФОРМЫ ПРЕДСТАВЛЕНИЯ ПЕТРОХИМИЧЕСКИХ ДАННЫХ
2.
• Петрохимические данные представляют ввиде таблиц и графиков.
• Первичный аналитический материал
следует представлять в виде таблиц. Это
дает возможность использовать его в
дальнейших исследованиях.
• Также широко используются
петрохимические коэффициенты.
3. Что должно быть в курсовой работе
• Таблица первичных анализов.• Для каждого анализа вычислены петрохимические
коэффициенты железистости, коэффициент окисления
железа, глиноземистости, агпаитности.
• Построены диаграммы:
Диаграмма Петрокомитета или TAS (для всех типов пород)
Диаграммы Харкера (для всех типов пород),
AFM (для ультраосновных, основных, средних пород),
бинарные диаграммы ОКСИД vs MgO (для ультраосновных,
основных пород),
Диаграмма NaAlK (для высокоглиноземистых или щелочных
пород)
Диаграмма Маниара и Пикколи (для гранитов)
Диаграмма Фроста (для гранитов)
Диаграмма Заварицкого (для всех типов пород, по желанию
руководителя)
4.
№ обр.Участок
1
2
3
4
1880
/406,5
мас.
НюдПоаз
1880
/413,5
1882
/41,3
мас.
НюдПоаз
1882
/533,7
мас. НюдПоаз
5
6
7
8
9
10
11
1525/143
с1612/22,4
В36-09
87
В 89-09
В 35-09
Nu-2
мас. Нюд- Дунитовы Дунитовы Вурэчуай
Поаз
й блок
й блок
венч
Порода
норит
норит
норит
норит
Дунит
Дунит
SiO2
TiO2
Al2O3
Fe2O3
FeO
MnO
MgO
CaO
Na2O
K2O
H2OH2O+
P2O5
CO2
S
V2O5
Cr2O3
NiO
Cl
F
Ni
Co
Cu
сумма
52,77
0,12
7,12
2,07
6,95
0,18
21,44
5,14
0,66
0,19
0,16
50,75
0,07
6,57
2,36
6,92
0,14
21,92
4,66
0,28
0,31
0,48
52,79
0,11
15,46
0,77
4,22
0,12
13,62
8,79
1,11
0,11
0,1
43,72
0,08
4,96
4,31
5,9
0,18
26,46
5,19
0,14
0,085
0,41
0,44
0,18
<0,025
0,34
<0,01
0,66
0,03
<0,025
0,13
н,о,
2,82
0,08
<0,025
0,27
37,47
0,07
1,34
3,34
3,86
0,09
48,17
0,41
0,03
0,01
0,25
1,36
0,01
0,32
0,02
42,16
0,13
2,42
2,90
6,83
0,13
39,09
2,34
0,17
0,08
0,27
1,98
0,03
0,23
0,01
1,04
0,24
0,01
0,02
0,22
<0,01
0,21
99,74
0,014
0,007
0,037
<0,01
<0,005
99,9
2,81
0,37
0,01
0,39
0,2
<0,025
0,39
0,13
<0,01
0,09
99,74
0,12
<0,01
0,013
100,07
99,86
100,08
габброн
орит
50,69
0,06
22,48
0,67
2,44
0,06
5,32
12,54
2,42
0,56
0,08
2,35
≤0,01
0,25
0,02
≤0,025
0,01
0,016
0,008
≤0,01
<0,01
<0,01
99,97
Нюд 2
Норит
оливинсод
ержащий
49,38
0,32
7,89
2,83
7,22
0,22
23,98
3,46
0,96
0,31
0,26
1,5
0,04
0,42
0,07
0,01
0,28
0,008
0,008
0,0016
99,17
Вурэчуайв Вурэчуайв
енч
енч
Габброно
Габбронор
рит
ит лейкокр
53,89
53,23
0,06
0,07
14,41
16,18
0,6
1,03
4,83
3,95
0,11
0,09
10,51
8,82
11,16
11,43
1,47
1,86
0,26
0,22
0,11
0,22
Нюд
Норит
0,02
0,12
0,06
≤0,025
0,05
0,02
0,39
0,02
<0,025
0,01
50,23
0,14
16,86
0,81
4,36
0,1
13,42
9,21
1,48
0,13
0,32
2,48
0,03
<0,1
0,02
<0,025
0,116
0,045
0,01
0,02
≤0,01
<0,01
99,76
0,025
0,007
0,02
≤0,01
<0,01
99,56
0,095
0,023
0,033
≤0,01
<0,01
99,86
5.
• В примечании к таблице указывается, вкаких единицах измерены содержания
компонентов, обозначения (не обн. не
опр.);
• для каждого образца - название породы,
номер, место отбора, автор коллекции, где
выполнен анализ,
6.
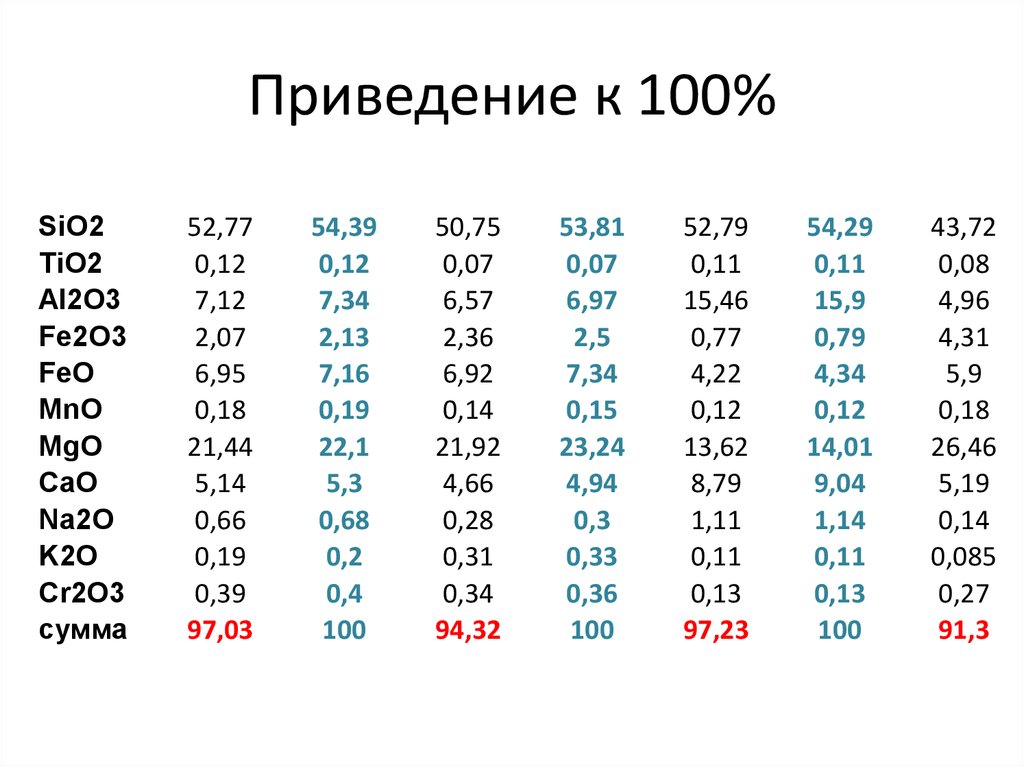
• Для того, чтобы в наибольшей степениприблизить состав породы к первичному,
надо пересчитать химический анализ на
100% сухого вещества, т.е. вычесть
содержания H2O, CO2, SO3, П.П.П. и пр., а
остаток привести к 100%.
7. Только петрогенные компоненты
8. Приведение к 100%
SiO2TiO2
Al2O3
Fe2O3
FeO
MnO
MgO
CaO
Na2O
K2O
Cr2O3
сумма
52,77
0,12
7,12
2,07
6,95
0,18
21,44
5,14
0,66
0,19
0,39
97,03
54,39
0,12
7,34
2,13
7,16
0,19
22,1
5,3
0,68
0,2
0,4
100
50,75
0,07
6,57
2,36
6,92
0,14
21,92
4,66
0,28
0,31
0,34
94,32
53,81
0,07
6,97
2,5
7,34
0,15
23,24
4,94
0,3
0,33
0,36
100
52,79
0,11
15,46
0,77
4,22
0,12
13,62
8,79
1,11
0,11
0,13
97,23
54,29
0,11
15,9
0,79
4,34
0,12
14,01
9,04
1,14
0,11
0,13
100
43,72
0,08
4,96
4,31
5,9
0,18
26,46
5,19
0,14
0,085
0,27
91,3
9. Исходные данные: мас.%
SiO2TiO2
Al2O3
Fe2O3
FeO
MnO
MgO
CaO
Na2O
K2O
Cr2O3
сумма
1
54,39
0,12
7,34
2,13
7,16
0,19
22,1
5,3
0,68
0,2
0,4
100
2
53,81
0,07
6,97
2,5
7,34
0,15
23,24
4,94
0,3
0,33
0,36
100
массовые %
3
4
5
54,29
47,89
38,39
0,11
0,09
0,07
15,9
5,43
1,37
0,79
4,72
3,42
4,34
6,46
3,95
0,12
0,2
0,09
14,01
28,98
49,35
9,04
5,68
0,42
1,14
0,15
0,03
0,11
0,09
0,01
0,13
0,3
2,88
100
99,99
100
6
43,33
0,13
2,49
2,98
7,02
0,13
40,18
2,41
0,17
0,08
1,07
100
7
52,12
0,06
23,12
0,69
2,51
0,06
5,47
12,89
2,49
0,58
0,01
100
8
50,99
0,33
8,15
2,92
7,45
0,23
24,76
3,57
0,99
0,32
0,29
100
9
55,36
0,06
14,8
0,62
4,96
0,11
10,8
11,46
1,51
0,27
0,05
100
10
54,94
0,07
16,7
1,06
4,08
0,09
9,1
11,8
1,92
0,23
0,01
100
11
51,86
0,14
17,41
0,84
4,5
0,1
13,86
9,51
1,53
0,13
0,12
100
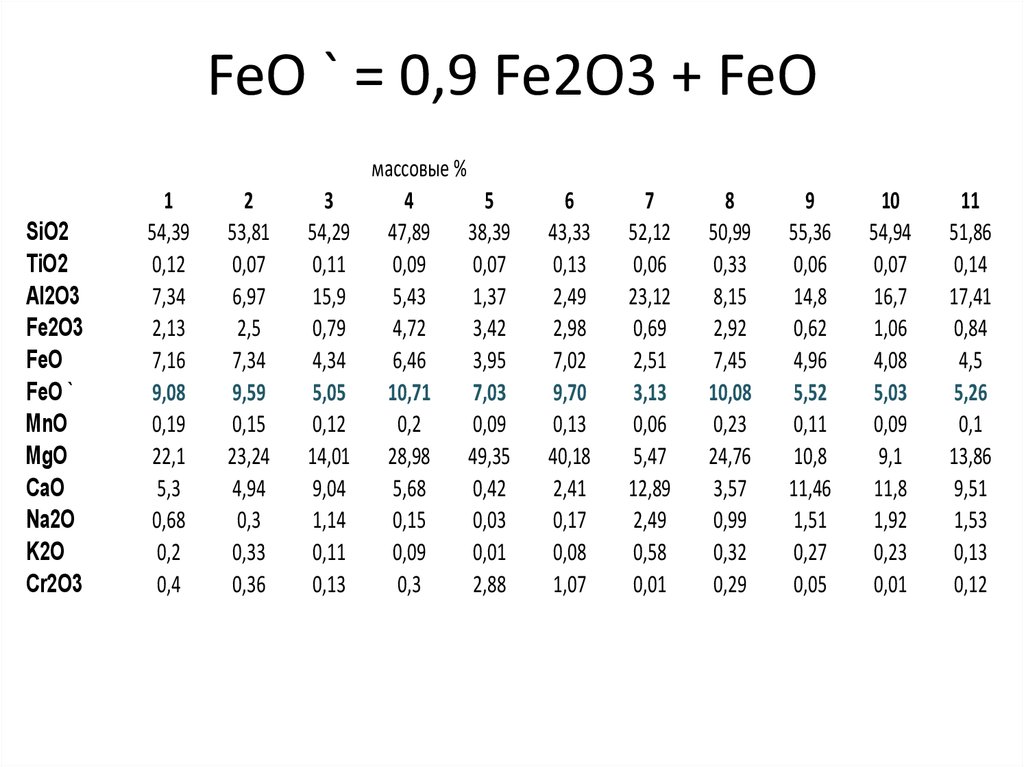
10. FeO ` = 0,9 Fe2O3 + FeO
SiO2TiO2
Al2O3
Fe2O3
FeO
FeO `
MnO
MgO
CaO
Na2O
K2O
Cr2O3
1
54,39
0,12
7,34
2,13
7,16
9,08
0,19
22,1
5,3
0,68
0,2
0,4
2
53,81
0,07
6,97
2,5
7,34
9,59
0,15
23,24
4,94
0,3
0,33
0,36
массовые %
3
4
5
54,29 47,89 38,39
0,11
0,09
0,07
15,9
5,43
1,37
0,79
4,72
3,42
4,34
6,46
3,95
5,05
10,71
7,03
0,12
0,2
0,09
14,01 28,98 49,35
9,04
5,68
0,42
1,14
0,15
0,03
0,11
0,09
0,01
0,13
0,3
2,88
6
43,33
0,13
2,49
2,98
7,02
9,70
0,13
40,18
2,41
0,17
0,08
1,07
7
52,12
0,06
23,12
0,69
2,51
3,13
0,06
5,47
12,89
2,49
0,58
0,01
8
50,99
0,33
8,15
2,92
7,45
10,08
0,23
24,76
3,57
0,99
0,32
0,29
9
55,36
0,06
14,8
0,62
4,96
5,52
0,11
10,8
11,46
1,51
0,27
0,05
10
54,94
0,07
16,7
1,06
4,08
5,03
0,09
9,1
11,8
1,92
0,23
0,01
11
51,86
0,14
17,41
0,84
4,5
5,26
0,1
13,86
9,51
1,53
0,13
0,12
11.
• Простейшими и часто используемымипетрохимическими графиками являются
двойные диаграммы в ортогональной системе
координат:
• 1. ДИАГРАММЫ ХАРКЕРА (Альфред Харкер –
английский петролог начала ХХ века)
• 2. Кроме диаграмм Харкера используют
двойные графики, на которых вдоль одной оси
откладываются MgO или другие величины.
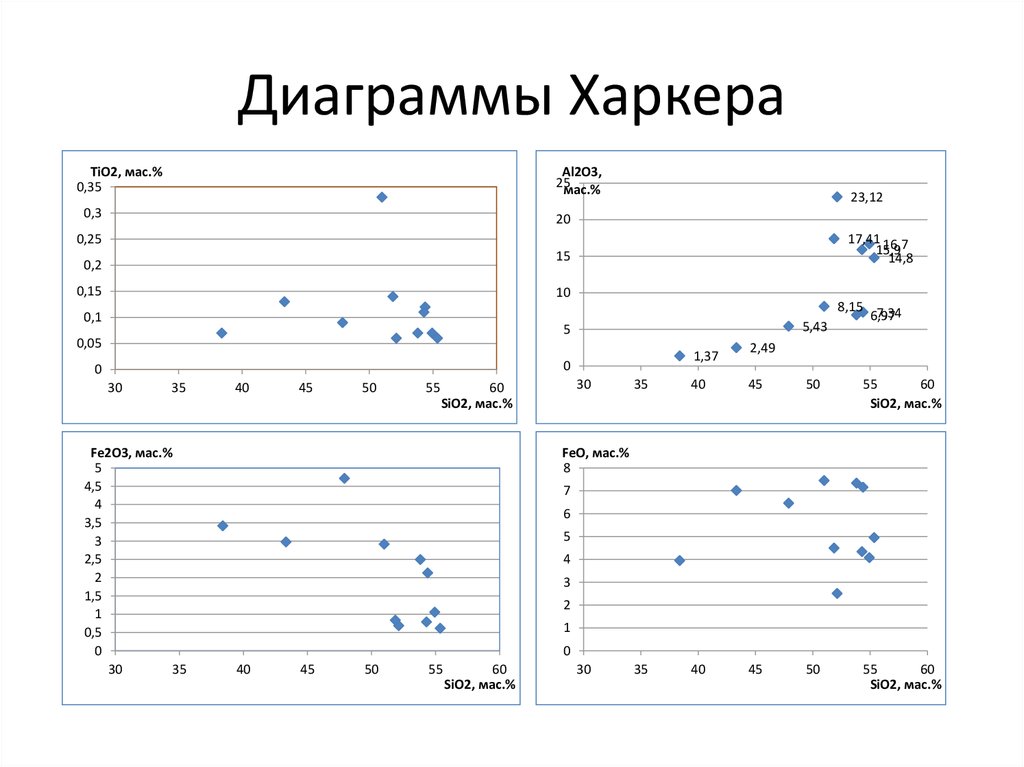
12. Диаграммы Харкера
TiO2, мас.%0,35
Al2O3,
25мас.%
0,3
23,12
20
0,25
17,41 16,7
15,9
14,8
15
0,2
0,15
10
0,1
5,43
5
0,05
1,37
0
0
30
35
Fe2O3, мас.%
5
4,5
4
3,5
3
2,5
2
1,5
1
0,5
0
30
35
40
45
50
55
30
60
SiO2, мас.%
8,15 7,34
6,97
2,49
35
40
45
50
55
60
SiO2, мас.%
35
40
45
50
55
60
SiO2, мас.%
FeO, мас.%
8
7
6
5
4
3
2
1
0
40
45
50
55
60
SiO2, мас.%
30
13. Диаграммы Харкера
FeO сумм,мас.%
12
MnO, мас.%
0,25
10
0,2
8
0,15
6
0,1
4
0,05
2
0
0
30
35
40
45
50
55
60
SiO2, мас.%
30
MgO, мас.%
60
CaO, мас.%
14
50
12
35
40
45
50
55
60
SiO2, мас.%
35
40
45
50
55
60
SiO2, мас.%
10
40
8
30
6
20
4
10
2
0
0
30
35
40
45
50
55
60
SiO2, мас.%
30
14. Диаграммы Харкера
K2O, мас.%0,7
Na2O, мас.%
3
0,6
2,5
0,5
2
0,4
1,5
0,3
1
0,2
0,5
0,1
0
0
30
35
40
45
50
55
30
60
SiO2, мас.%
35
40
Cr2O3, мас.%
3,5
3
2,5
2
1,5
1
0,5
0
30
35
40
45
50
55
60
SiO2, мас.%
45
50
55
60
SiO2, мас.%
15.
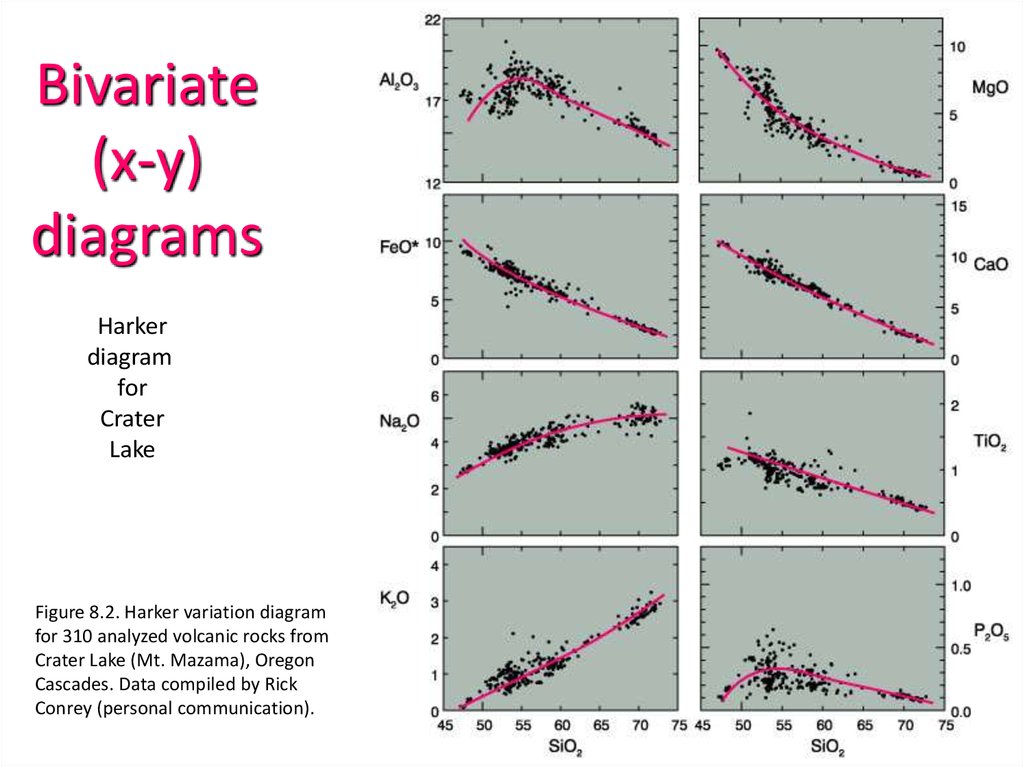
Bivariate(x-y)
diagrams
Harker
diagram
for
Crater
Lake
Figure 8.2. Harker variation diagram
for 310 analyzed volcanic rocks from
Crater Lake (Mt. Mazama), Oregon
Cascades. Data compiled by Rick
Conrey (personal communication).
16.
Bivariate(x-y)
diagrams
Harker
diagram
for
Crater
Lake
Figure 8.2. Harker variation diagram
for 310 analyzed volcanic rocks from
Crater Lake (Mt. Mazama), Oregon
Cascades. Data compiled by Rick
Conrey (personal communication).
17.
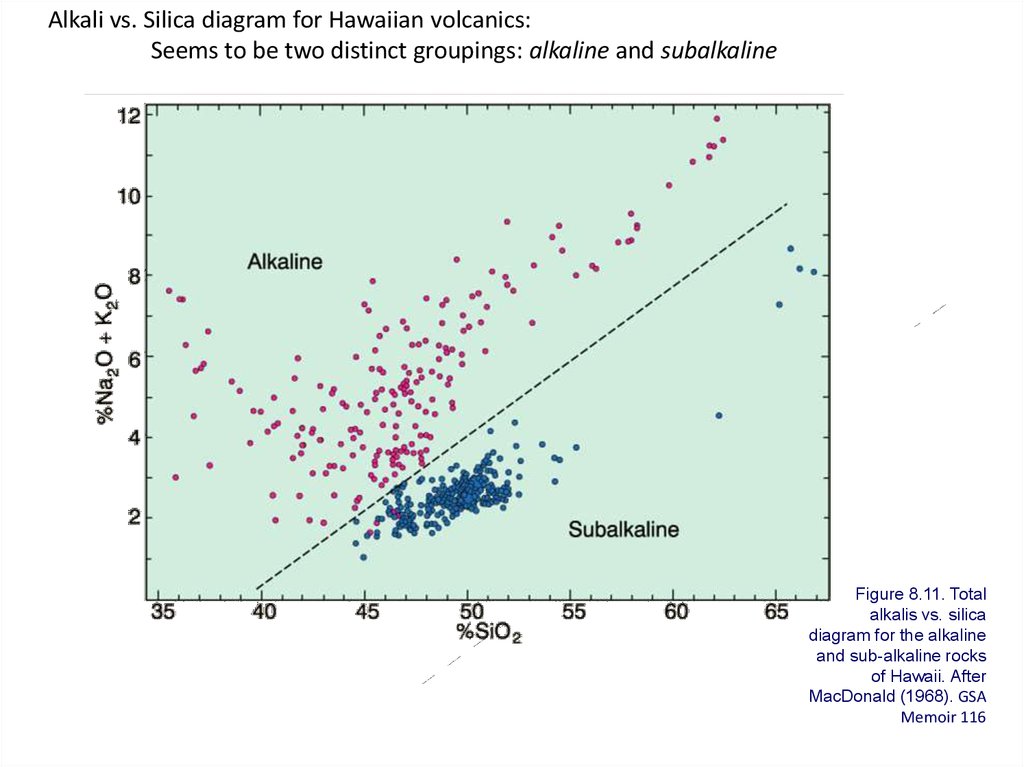
Alkali vs. Silica diagram for Hawaiian volcanics:Seems to be two distinct groupings: alkaline and subalkaline
Figure 8.11. Total
alkalis vs. silica
diagram for the alkaline
and sub-alkaline rocks
of Hawaii. After
MacDonald (1968). GSA
Memoir 116
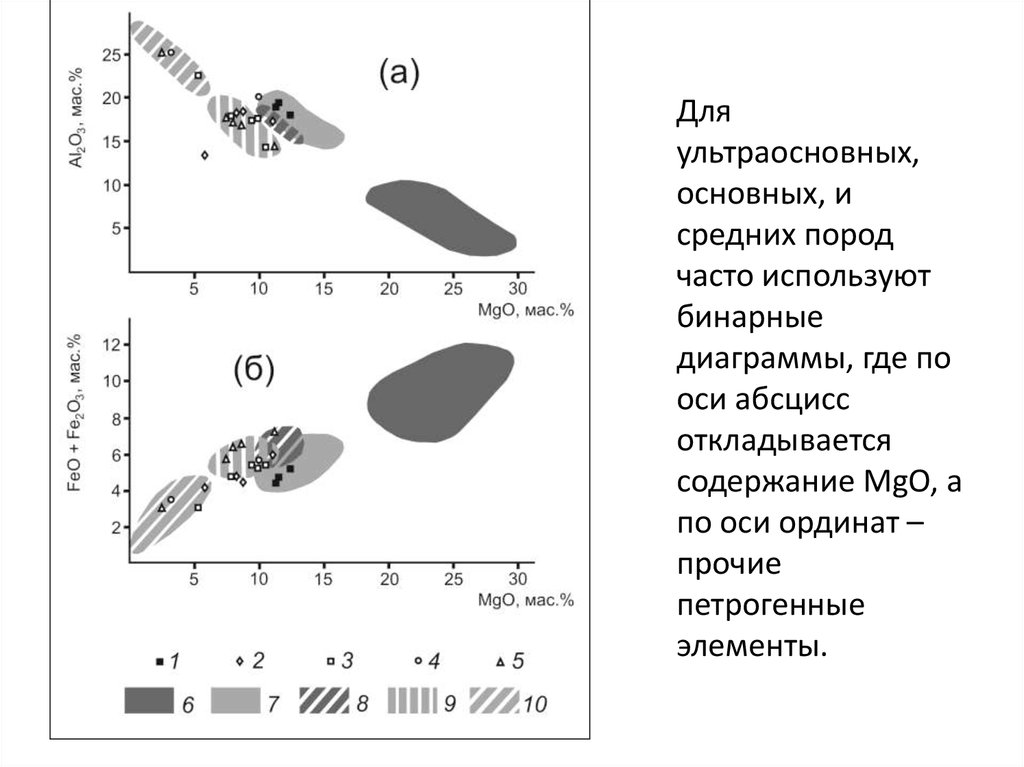
18.
Дляультраосновных,
основных, и
средних пород
часто используют
бинарные
диаграммы, где по
оси абсцисс
откладывается
содержание MgO, а
по оси ординат –
прочие
петрогенные
элементы.
19.
The major elementchemistry of MORBs
“Fenner-type” variation diagrams
for basaltic glasses from the Afar
region of the MAR. Note different
ordinate scales. From Stakes et al.
(1984) J. Geophys. Res., 89, 69957028.
Decrease in MgO and relative
increase in FeO early
differentiation trend of tholeiites
20.
• Классификационная диаграмма SiO2 –(Na2O+K2O) по существу является диаграммой
Харкера, на которую нанесены средние
составы всех магматических пород.
• Строго говоря, сложение Na2O+K2O (мас.%)
некорректно, поскольку молекулярные массы
Na2O (62) и K2O (94) отличаются в полтора
раза. Правильнее представлять эту сумму в
молекулярных количествах или вводить
поправку: 1,5 Na2O+K2O, мас.% или
Na2O+0,7K2O, мас.%.
• То есть, классификационная диаграмма
предполагает упрощение, недопустимое при
строгих пересчетах.
21.
• Во многих случаях используются не мас.%, амолекулярные или атомные количества.
• Во всех случаях, когда суммируются
содержания разных оксидов или хим.
элементов, эти содержания должны быть
выражены в молекулярных или атомных
количествах !!!!!!
22.
• Молекулярное количество (М)– этовеличина, пропорциональная числу
молекул того или иного химического
соединения в единице массы.
Содержание (мас.%) (из таблицы хим.
анализов
М
=
х
Молекулярная масса (из табл.
Менделеева)
1000
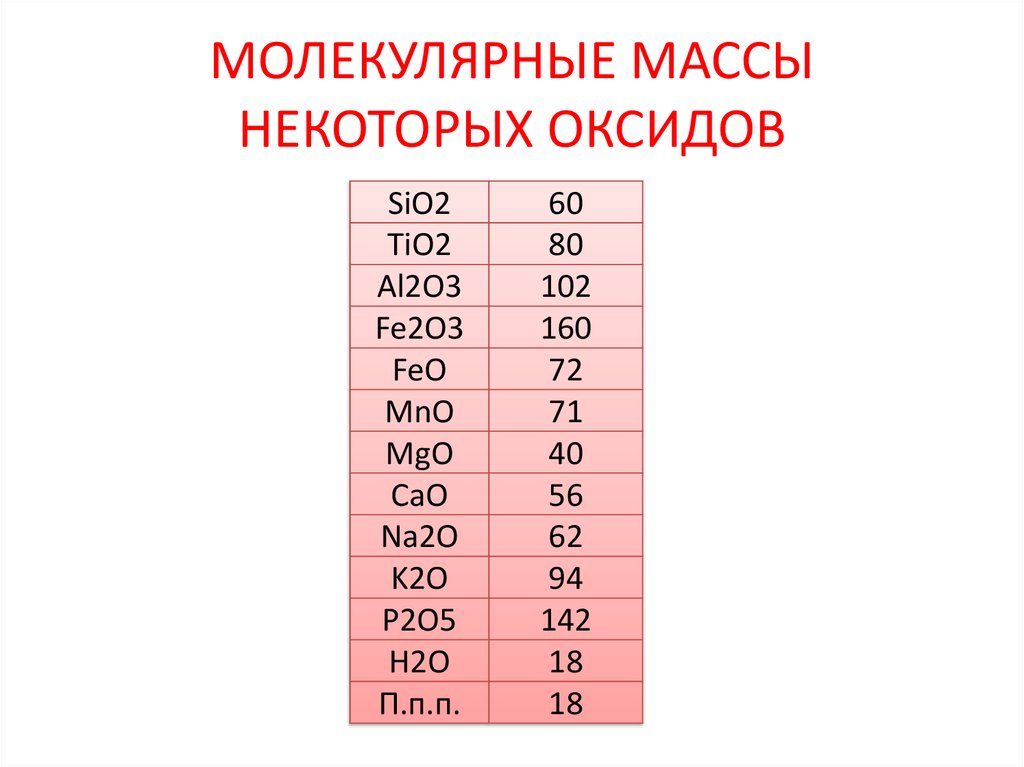
23. МОЛЕКУЛЯРНЫЕ МАССЫ НЕКОТОРЫХ ОКСИДОВ
SiO2TiO2
Al2O3
Fe2O3
FeO
MnO
MgO
CaO
Na2O
K2O
P2O5
H2O
П.п.п.
60
80
102
160
72
71
40
56
62
94
142
18
18
24. Исходные данные: молекулярные количества
SiO2TiO2
Al2O3
Fe2O3
FeO
MnO
MgO
CaO
Na2O
K2O
Cr2O3
1
907
2
72
13
99
3
553
95
11
2
3
2
897
1
68
16
102
2
581
88
5
4
2
3
905
1
156
5
60
2
350
161
18
1
1
4
798
1
53
30
90
3
725
101
2
1
2
5
640
1
13
21
55
1
1234
8
0
0
19
6
722
2
24
19
98
2
1005
43
3
1
7
7
869
1
227
4
35
1
137
230
40
6
0
8
850
4
80
18
103
3
619
64
16
3
2
9
923
1
145
4
69
2
270
205
24
3
0
10
916
1
164
7
57
1
228
211
31
2
0
11
864
2
171
5
63
1
347
170
25
1
1
25. Важные петрохимические параметры
• Петрохимические коэффициенты могут быть представлены в различнойформе (используются молекулярные или атомные количества!!!)
• Коэффициент железистости. Он отражает соотношения Fe и Mg в
силикатах (оливине, пироксенах, амфиболах, биотите и др.), а также
относительное количество оксидов железа (магнетит, ильменит и пр.).
• f1 = FeO`/ (FeO` + MgO) = Fe / (Fe + Mg)
• f2 = FeO` / MgO = Fe / Mg
• Магнезиальное число (М) характеризует долю магния от суммы железа
и магния или отношение Mg/Fe 2+:
• M1 = 1 – f1; M2 = 1/f2
• Коэффициент окисления железа
• φ1 = Fe203 / (Fe2O3 + FeO)
• φ2 = Fe203 / FeO
26. Важные петрохимические параметры
• Коэффициент агпаитности указывает наналичие или отсутствие в породе натриевых
цветных минералов : пироксена (эгирина)
или амфибола (арфведсонита, рибекита и
др.). При наличии этих минералов Ка > 1.
Если всё количество Na и К заключено в
полевых шпатах, то Ка ≤ 1.
• Ка = (Na2O + K2O) / Al2O3 = (Na + K) / Al
27. Важные петрохимические параметры
Коэффициент глиноземистости
al1 = Al / (2Ca + Na + K);
al2 = (2Ca + Na + K - Al) / 2Ca.
Этот параметр отражает степень насыщения пород
алюминием относительно стехиометрии полевых
шпатов (al1 = 1 и al2 = 0).
• В породах с al1 > 1 и al2 < 0, кроме полевых шпатов,
содержатся высокоглиноземистые минералы: слюды,
силлиманит, кордиерит, гранат и др.
• В породах с 0 ≤ al2 ≤ 1, Са, Na и K заключены
преимущественно в полевых шпатах.
• Если al1 < 1 и al2 > 1, то это указывает на наличие в
породе натриевых цветных минералов (при этом Ка > 1).
28. Важные петрохимические параметры
Отношения Na и K:
N1 = Na2O / (Na2O +K2O) = Na / (Na + K)
N2 = Na2O / K2O = Na / K
K1 = K / (Na + K) = 1 - N1
K2 = K / Na = 1 / N2
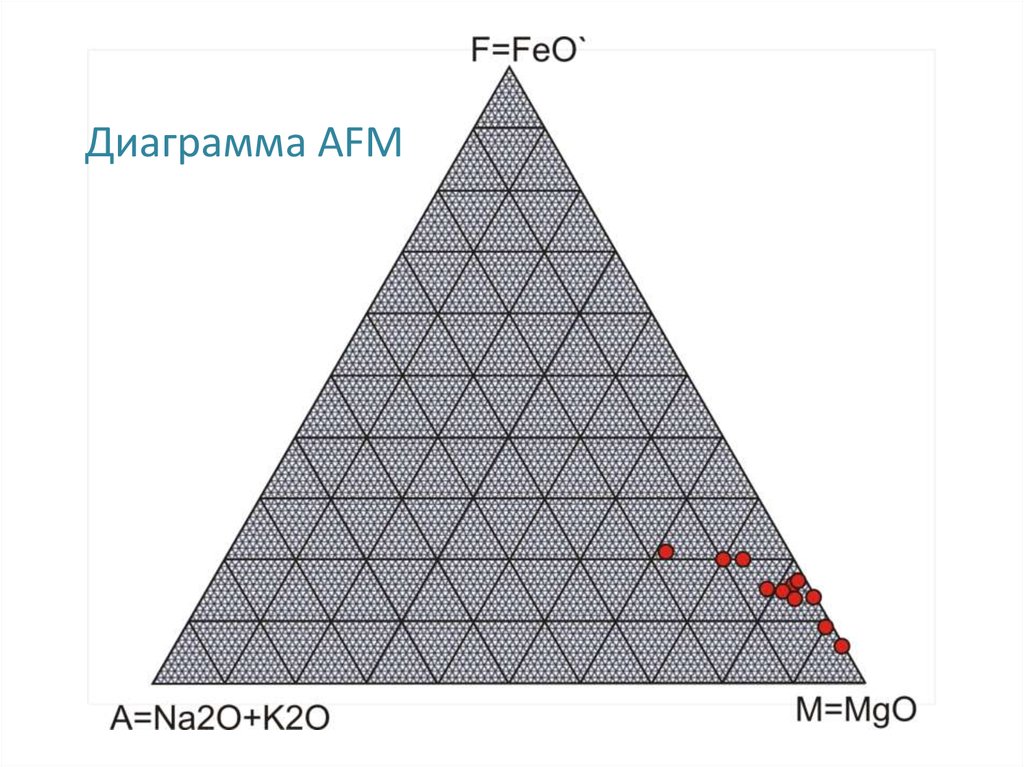
29. Диаграмма AFM
Тройная диаграммаМолекулярные количества
А = Na2O + K2O
F = FeO` = 0,9 Fe2O3 + FeO
M = MgO
Привести к 100%
Внимание! Возможна ложная корреляция!
30.
ДИАГРАММА AFM, Wager, Deer, 1939, — тройная, треугольнаяпетрохим. диаграмма, в которой переменными величинами
являются хим. компоненты в окисной форме (в вес. %): М =
MgO, F = FeO, А = (Na2O + К2О). В дальнейшем разл. авторами Д.
AFM неоднократно модифицировалась в отношении F,
величина которого принималась равной FeO + 0, 9Fe2O3 или FeO
+ Fe2O3 (Kuno, 1959; Shimasu, 1963). На Д. AFM хорошо
различаются серии, в которых преобладает разделение железомагнезиальных, или салических, м-лов на разных стадиях их
образования. Недостатки Д. AFM: 1) трудно различать
известково-щелочные и щелочные п., а также магм. комплексы,
отличающиеся по кислотности; 2) невозможно установить пути
эволюции в сторону натровых или калиевых дифференциатов.
31.
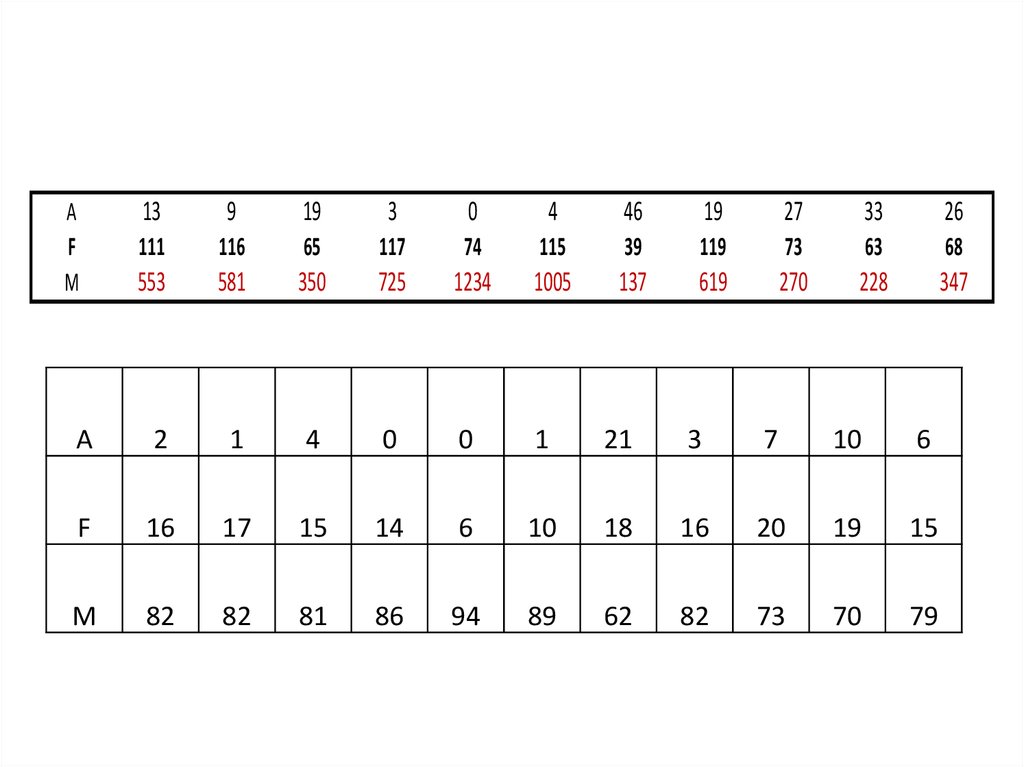
139
19
3
0
4
46
19
27
33
26
111
116
65
117
74
115
39
119
73
63
68
553
581
350
725
1234
1005
137
619
270
228
347
A
2
1
4
0
0
1
21
3
7
10
6
F
16
17
15
14
6
10
18
16
20
19
15
M
82
82
81
86
94
89
62
82
73
70
79
A
F
M
32.
Диаграмма AFM33.
34.
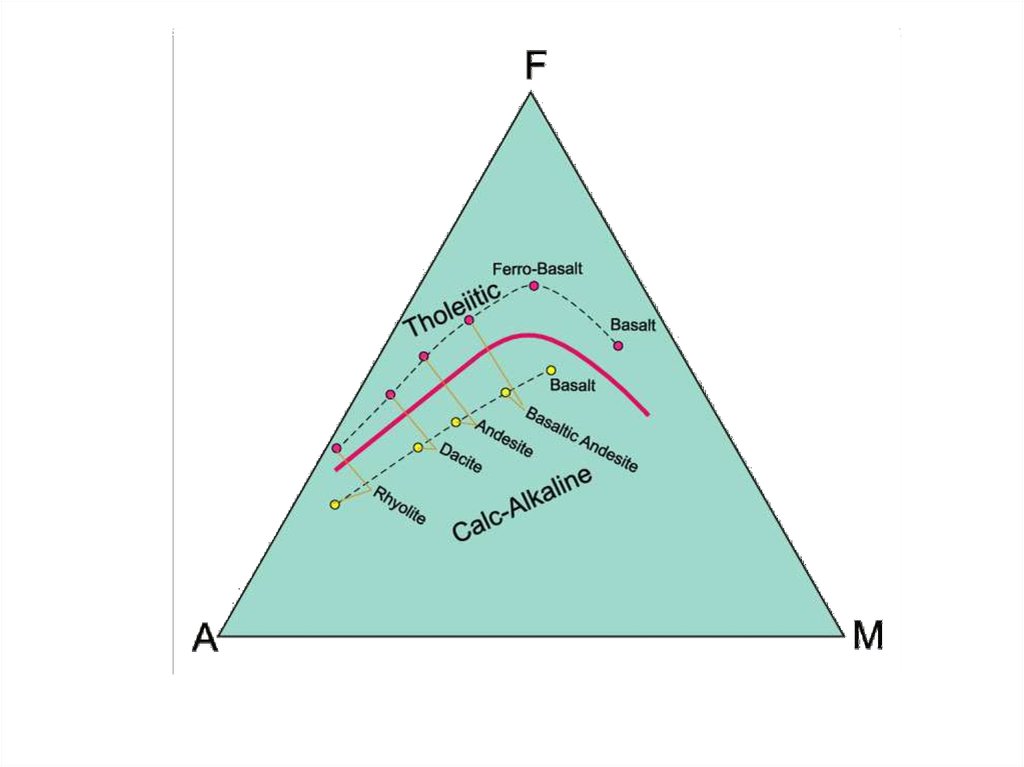
AFM diagram: can further subdivide the subalkalinemagma series into a tholeiitic and a calc-alkaline series
Figure 8.14. AFM diagram showing the distinction between
selected tholeiitic rocks from Iceland, the Mid-Atlantic
Ridge, the Columbia River Basalts, and Hawaii (solid circles)
plus the calc-alkaline rocks of the Cascade volcanics (open
circles). From Irving and Baragar (1971). After Irvine and
Baragar (1971). Can. J. Earth Sci., 8, 523-548.
35.
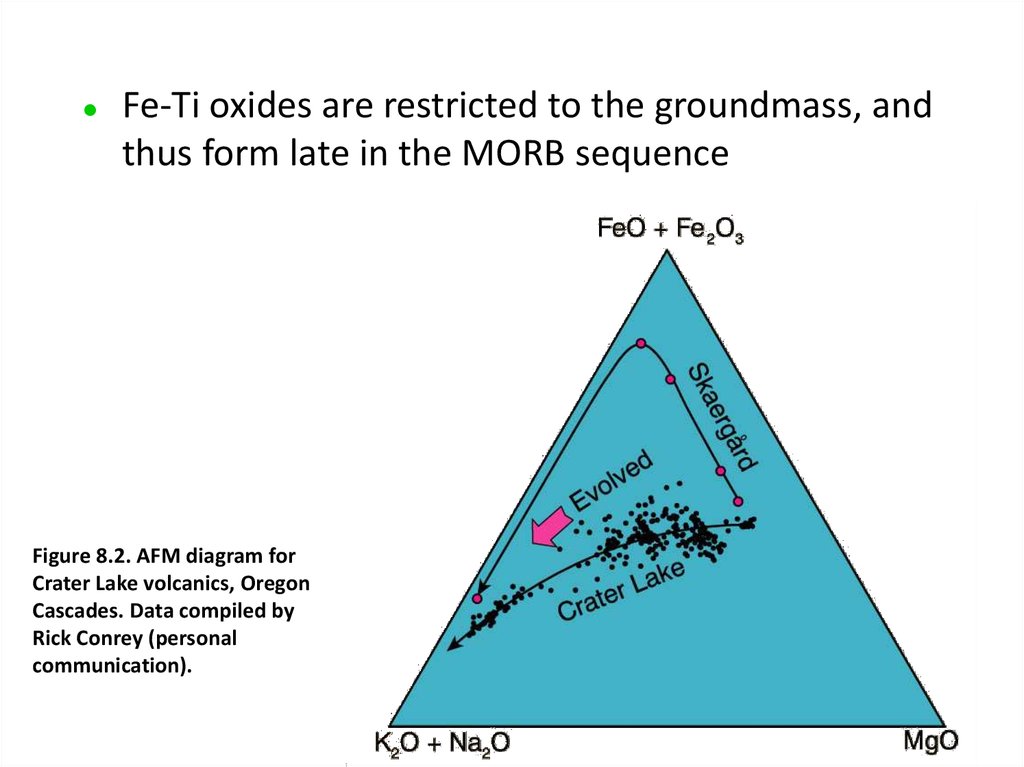
Fe-Ti oxides are restricted to the groundmass, andthus form late in the MORB sequence
Figure 8.2. AFM diagram for
Crater Lake volcanics, Oregon
Cascades. Data compiled by
Rick Conrey (personal
communication).
36.
Диаграмма ДженсенаКлассификационная диаграмма Al2O3 - (FeO* + TiO2) – MgO Дженсена
(Jensen, 1976), скорректированная Риквудом (Rickwood, 1989) с полями
коматиитовых, толеитовых и известково-щелочных вулканитов, в мол.%.
FeO* = FeO + 0.89 Fe2O3.
37.
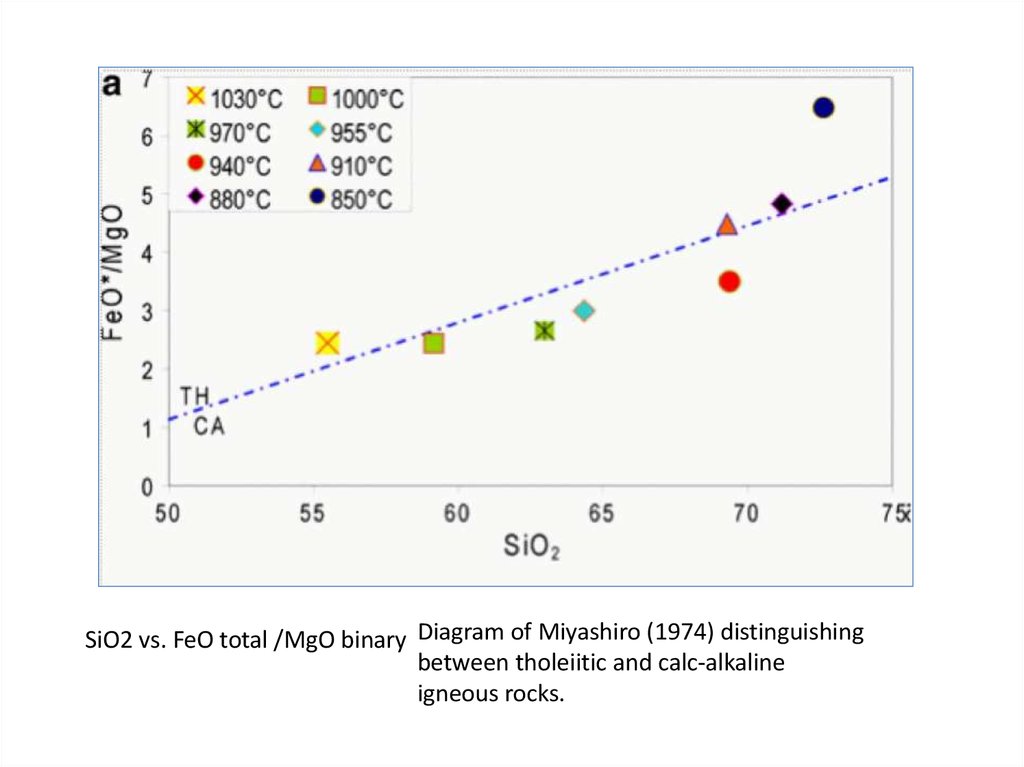
SiO2 vs. FeO total /MgO binary Diagram of Miyashiro (1974) distinguishingbetween tholeiitic and calc-alkaline
igneous rocks.
38.
Диаграмма NaAlKNa2O – Al2O3 – K2O (mol. %)
Na2O – Al2O3 – K2O Тройная диаграмма – позволяет различить
высокоглиноземистые и щелочные породы, а также калийные и натровые
серии.
39.
Диаграмма Пирса и др. (1977)Применяется для базальтоидов и средних вулканитов
40.
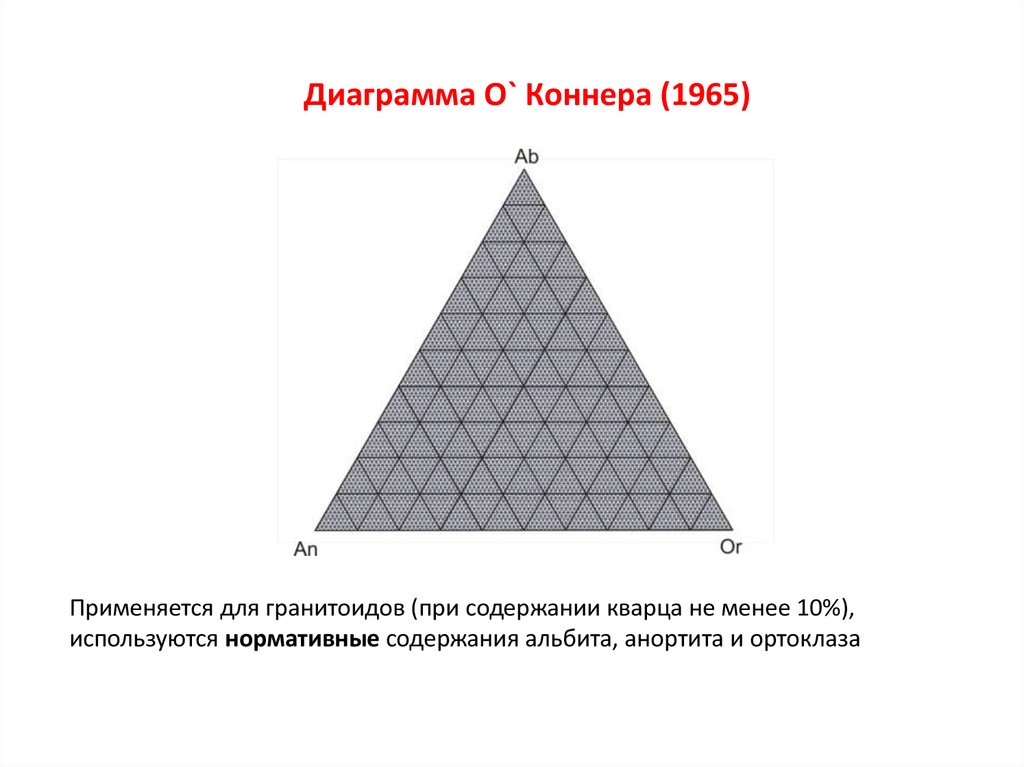
Диаграмма О` Коннера (1965)Применяется для гранитоидов (при содержании кварца не менее 10%),
используются нормативные содержания альбита, анортита и ортоклаза
41.
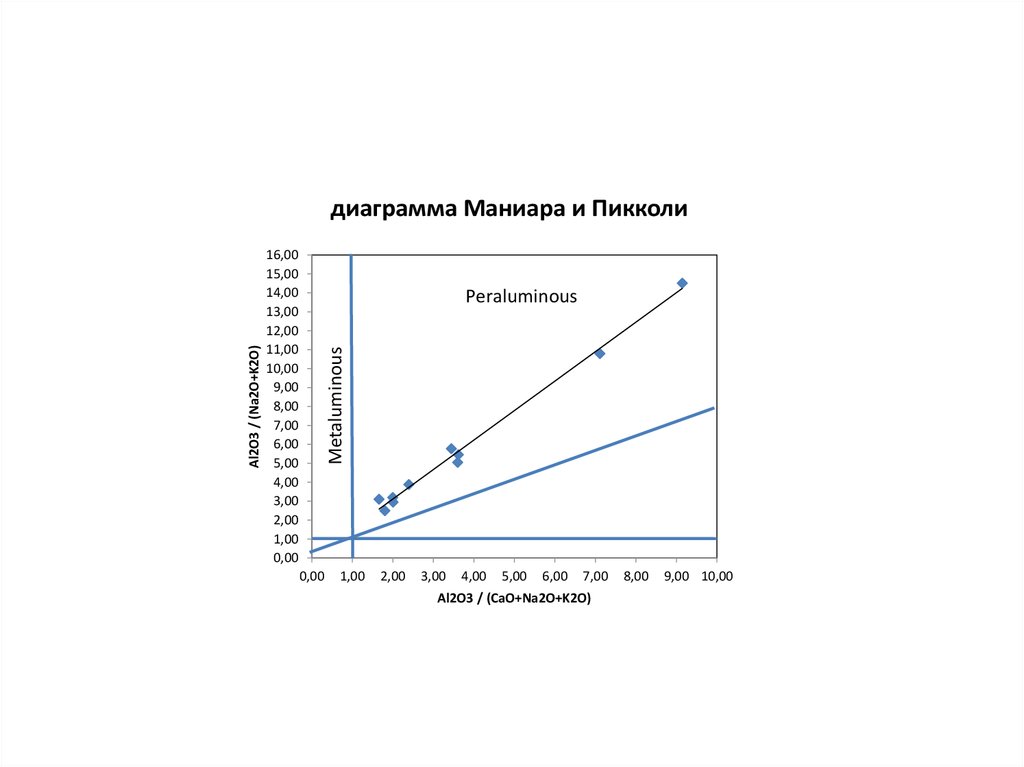
Диаграмма Маниара и Пикколи (1989)Применяется для гранитоидов, позволяет проводить геотектоническую
классификацию гранитоидов
42.
Диаграммы Фроста и др. (2001)1) SiO2 vs FeO` / FeO` + MgO
2) SiO2 vs Na2O + K2O – CaO
Применяются для
гранитоидов,
гранитогнейсов
43.
16,0015,00
14,00
13,00
12,00
11,00
10,00
9,00
8,00
7,00
6,00
5,00
4,00
3,00
2,00
1,00
0,00
Peraluminous
Metaluminous
Al2O3 / (Na2O+K2O)
диаграмма Маниара и Пикколи
0,00
1,00
2,00
3,00
4,00
5,00
6,00
7,00
Al2O3 / (CaO+Na2O+K2O)
8,00
9,00 10,00




























 Химия
Химия