Похожие презентации:
предмет орг.химии
1.
Органическая химиякак наука
1827
год рождения
органической химии
основоположник
шведский
ученый
Берцелиус
2.
Органические вещества.Вещества
Органические
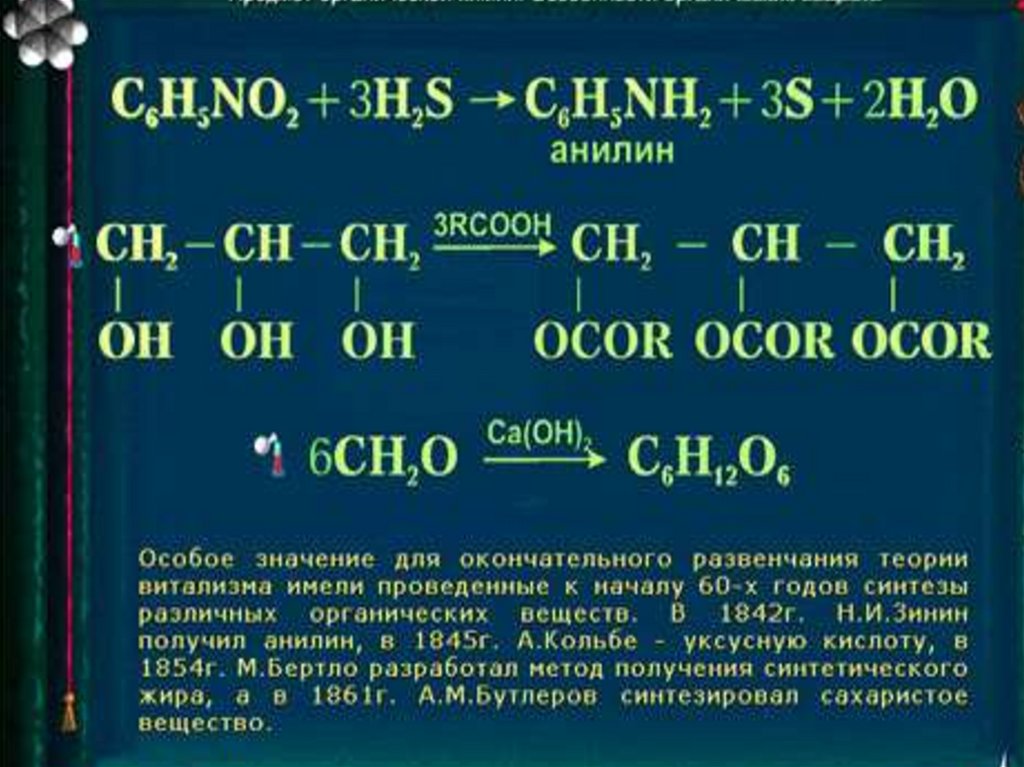
Получены из продуктов
жизнедеятельности растительных и животных
организмов (сахар, жиры, масла, красители и
др.), а также синтетические вещества (полиэтилен, капрон и др.).
Известно около 27млн.
Неорганические
Минеральные
(вещества
неживой природы:
глина, песок,
металлы и др.).
Таких веществ
около 0,5 млн.
3. Органические вещества. Вещества
Раздел химии, который изучаеторганические вещества, стали называть
«органической химией»
Так как в состав каждого органического
вещества входит элемент углерод, то
Органическая химия - это химия
соединений углерода ( кроме
оксидов углерода, угольной кислоты
и её солей).
4. Раздел химии, который изучает органические вещества, стали называть «органической химией»
5.
Фридрих Вёлер6.
7.
8.
Пьер Эжен МарселенБертло
9.
Органические вещества имеют рядособенностей:
их гораздо больше, чем неорганических
веществ;
орг. вещества имеют более сложное строение,
чем неорганические;
многие орг. вещества обладают
огромной молекулярной массой
например,белки углеводы, нуклеиновые кислоты и др.)
при горении органических веществ
обычно образуются углекислый газ и
вода.
ДНК
10. Органические вещества имеют ряд особенностей:
химические реакции протекают медленнее;среди них распространено явление изомерии;
орг. вещества располагаются в ряды, сходные
по строению и свойствам – гомологические
ряды;
связь между атомами ковалентная,
поэтому большинство из них неэлектролиты;
Органические соединения – это материалы, из
которых построены организмы животных и
растений.
11. Органические вещества имеют ряд особенностей:
12.
Алексей МихайловичБутлеров
Алексей Михайлович Бутлеров - профессор
Казанского университета, академик,
создатель теории химического строения
органических соединений.
13.
Понятие «химическое строение» в теорииявляется ключевым. А.М. Бутлеров определял
«химическое строение» как последовательность
соединения атомов в молекуле*.
Бутлеров представил свою теорию на суд
общественности в 1861 году в химической
секции Съезда немецких естествоиспытателей и
врачей в докладе «О химическом строении
вещества».
Другим значимым аспектом теории А.М.
Бутлерова стало утверждение, что химическое
строение веществ можно установить опытным
путём химическими методами и отразить в
формуле.
14.
Основные положения ТХС1. Атомы химических элементов в молекулах
соединены в строгой последовательности в
соответствии с их валентностями.
Порядок соединения атомов химических
элементов в молекуле согласно их валентности
называется химическим строением.
Запомни! Углерод в органических
соединениях всегда четырёхвалентен.
C (IV), H (I), O (II), N (III), S(II), Cl (I).
15. Основные положения ТХС
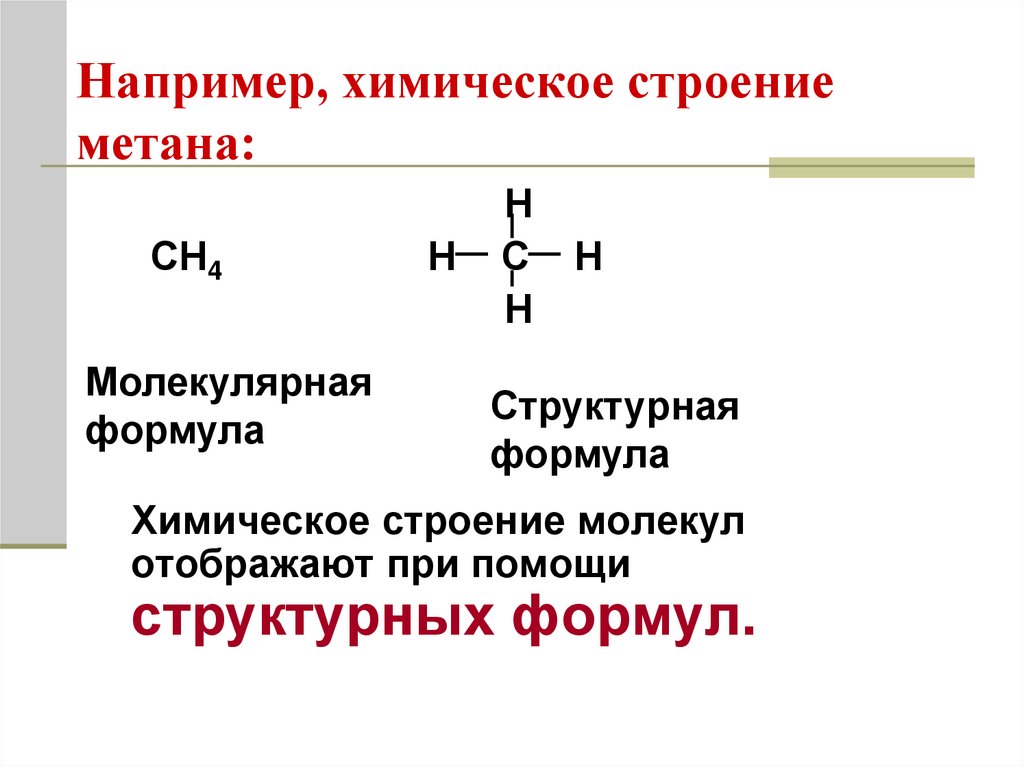
Например, химическое строениеметана:
СН4
Молекулярная
формула
Н
Н
С
Н
Н
Структурная
формула
Химическое строение молекул
отображают при помощи
структурных формул.
16. Например, химическое строение метана:
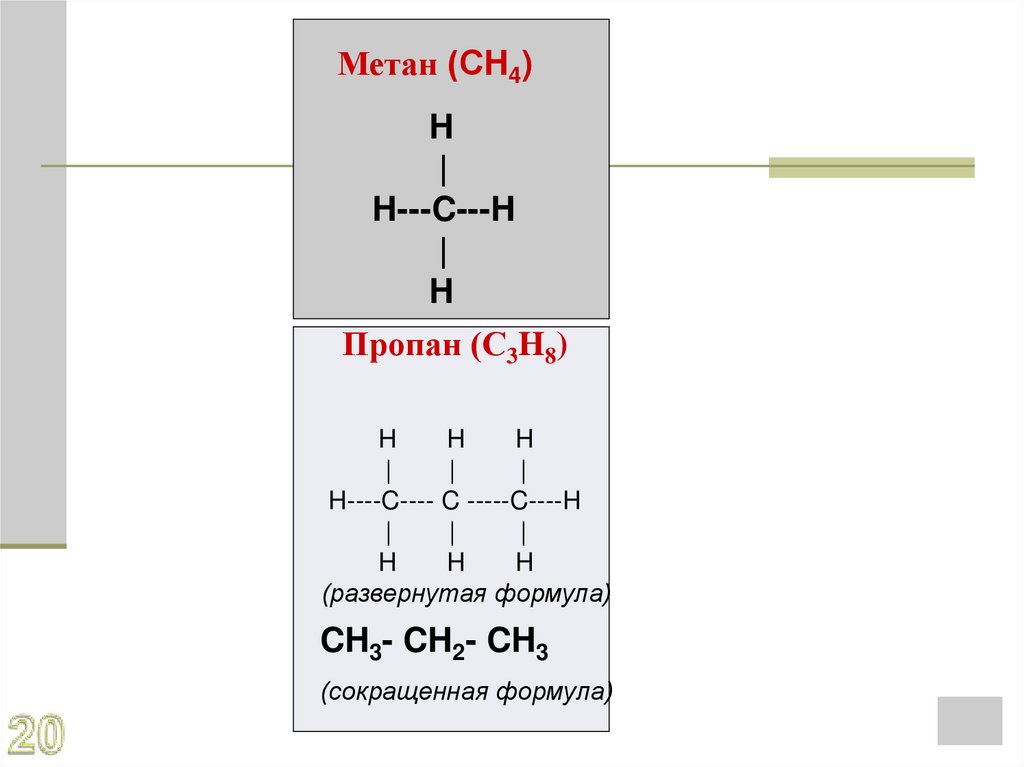
Метан (СH4)H
|
H---C---H
|
H
Пропан (С3H8)
H
H
H
|
|
|
H----C---- C -----C----H
|
|
|
H
H
H
(развернутая формула)
CH3- CH2- CH3
(сокращенная формула)
17. Пропан (С3H8)
Основное положение ТХС:2. Свойства вещества зависят не только от того,
какие атомы и в каком количеств входят в состав
его молекулы, но и от того, в каком порядке они
соеденены. То есть от химического строения.
(следствием является изомерия).
Изомерия – явление существования разных веществ с
одинаковым качественным и количественным
составом, но имеющих разное строение и свойства.
Изомеры – вещества, имеющие одинаковую
молекулярную форму, но разное строение и свойства.
18. Основное положение ТХС:
Изомерия- от греч.isos- равный, meros-часть, доля
СН3-СН2-СН2-СН3
СН3-СН-СН3
бутан
изобутан
СН3
Изомеры -вещества, имеющие одну и ту
же молекулярную формулу, но разное
строение и поэтому обладающие
разными свойствами
19. Изомерия- от греч. isos- равный, meros-часть, доля
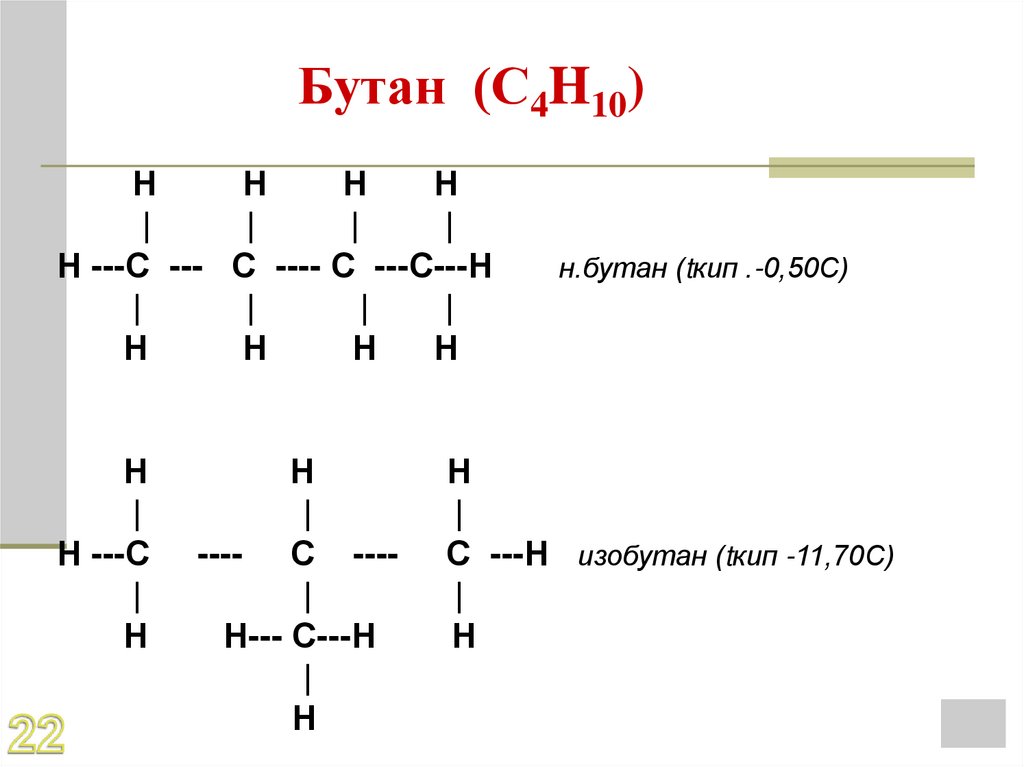
Бутан (С4H10)Н
Н
Н
Н
|
|
|
|
Н ---С --- С ---- С ---С---Н
|
|
|
|
Н
Н
Н
Н
Н
|
Н ---С
|
Н
Н
|
---- С ---|
Н--- С---Н
|
Н
н.бутан (tкип .-0,50С)
Н
|
С ---Н изобутан (tкип -11,70С)
|
Н
20. Бутан (С4H10)
Основное положение ТХС:3. Атомы или группы атомов, образующие
молекулы взаимно влияют друг на друга, от
чего зависят свойства вещества и его
реакционная способность.
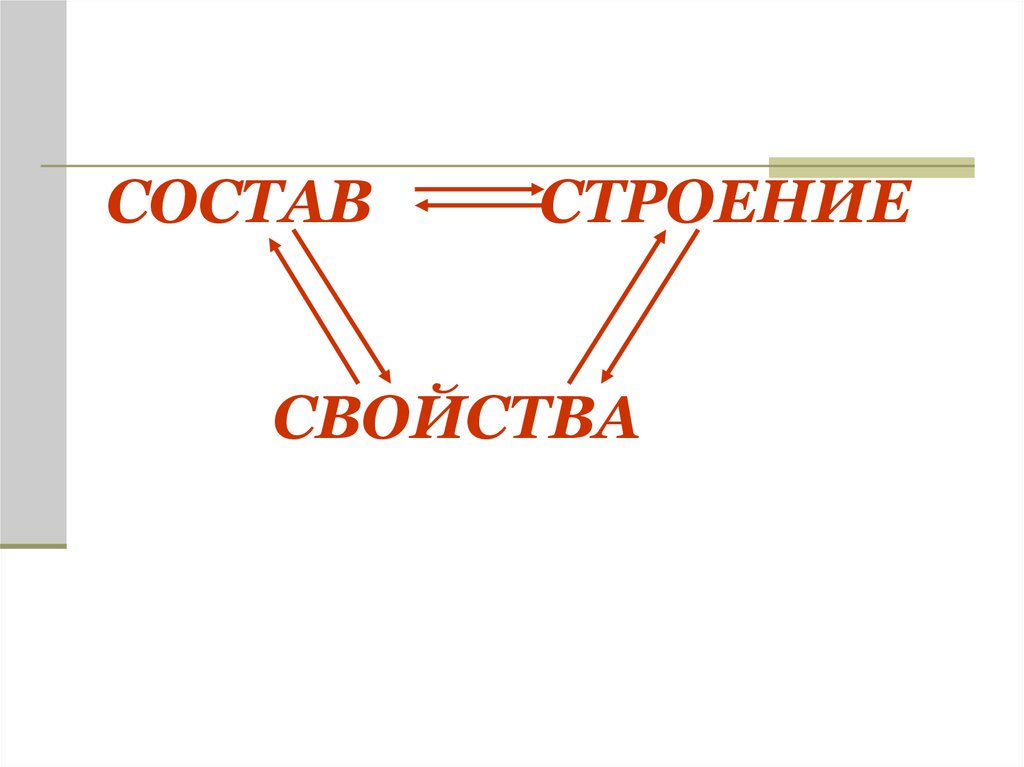
Вывод: свойства вещества определяются
химическим, пространственным и
электрическим строением.
21. Основное положение ТХС:
СОСТАВСТРОЕНИЕ
СВОЙСТВА
22. СОСТАВ СТРОЕНИЕ СВОЙСТВА
Теория химического строения- дала возможность систематизировать
органические вещества;
- ответила на все вопросы, возникшие к
тому времени в органической химии (см.
выше);
- позволила теоретически предвидеть
существование неизвестных веществ,
найти пути их синтеза.
23. Теория химического строения
Значение теории химическогостроения.
ТХС органических соединений А.М. Бутлерова внесла
существенный вклад в создание общенаучной картины
мира, способствовала диалектико – материалистическому
пониманию природы
1. - Закон перехода количественных
изменений в качественные;
(можно проследить на примере алканов) :
С1 – С5 – газы
С6 – С10 – жидкости
С11 – и более – твердые вещества.
Изменяется только количество атомов углерода.
24. Значение теории химического строения.
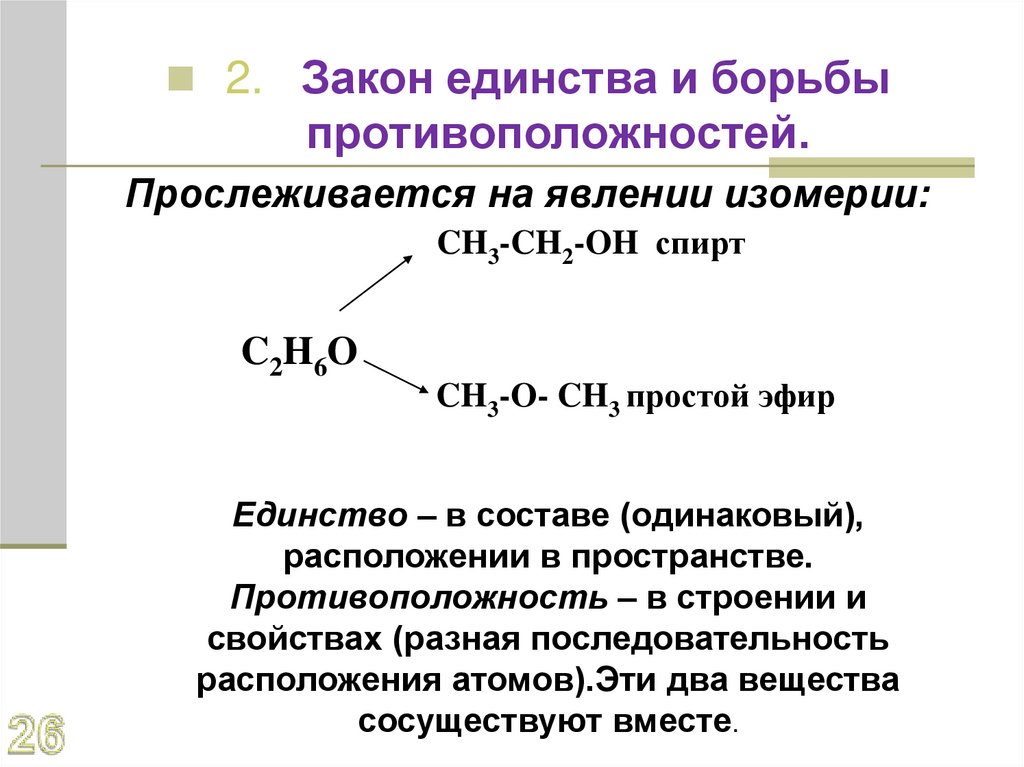
2. Закон единства и борьбыпротивоположностей.
Прослеживается на явлении изомерии:
CH3-CH2-OH спирт
C2H6O
CH3-O- CH3 простой эфир
Единство – в составе (одинаковый),
расположении в пространстве.
Противоположность – в строении и
свойствах (разная последовательность
расположения атомов).Эти два вещества
сосуществуют вместе.
25.
3. Закон отрицания отрицания.Изомеры сосуществуя отрицают друг
друга своим
существованием.



















 Химия
Химия








