Похожие презентации:
14_perv_zakon
1. МОЛЕКУЛЯРНАЯ ФИЗИКА
Сенин В.Г., МАОУ «СОШ №4», г. КорсаковПервый закон термодинамики
Домашнее задание: § 84; ЕГЭ(стр.281)
2. Сделано дома
ЕГЭ (стр. 275)№1. 0,48 кг
№2. 4
№3. 0,042 кг
№4. 400 м/с
3. Задачи нашего урока
• Ввести первый законтермодинамики как закон
сохранения энергии
термодинамической системы,
• Раскрыть его физическое
содержание при рассмотрении
конкретных процессов;
• Продолжить формирование
умения описывать тепловые
процессы с помощью физических
величин и законов.
Первый закон термодинамики —
это частный случай закона
сохранения энергии, главного
закона природы. Он показывает, от
каких причин зависит изменение
внутренней энергии.
4. Физическая разминка
• Вывод формулы работы газа при измененииего объёма,
• Геометрическое истолкование работы на
примере изобарного и изотермического
процессов.
• В каком случае газ совершает работу?
Почему работа не является функцией
состояния системы?
• Как теоретически доказать, что работа газа
при изотермическом и изобарном процессах
неодинакова?
• При каких условиях это справедливо?
• При каком условии работа не изменяет
внутренней энергии системы?
5. Первый закон термодинамики
Энергия в природе не возникает из ничего и не исчезает: количествоэнергии неизменно, она только переходит из одной формы в другую.
История открытия первого закона термодинамики…
Суть (статус) закона…
• как определяется полная механическая энергия любой системы?
• Как формулируется закон сохранения полной механической энергии?
• Когда происходит изменение кинетической (или потенциальной)
энергии тела?
• Приведите примеры превращения одного вида энергии в другой.
• В каких случаях не выполняется закон сохранения механической
энергии?
Изменение внутренней энергии системы при переходе её из одного
состояния в другое равно сумме работы внешних сил и количества
теплоты, переданной системе: ∆U= А + Q.
Первый закон термодинамики устанавливает общее свойство
взаимодействия термодинамических систем — сохранение полной
энергии.
6. Первый закон термодинамики
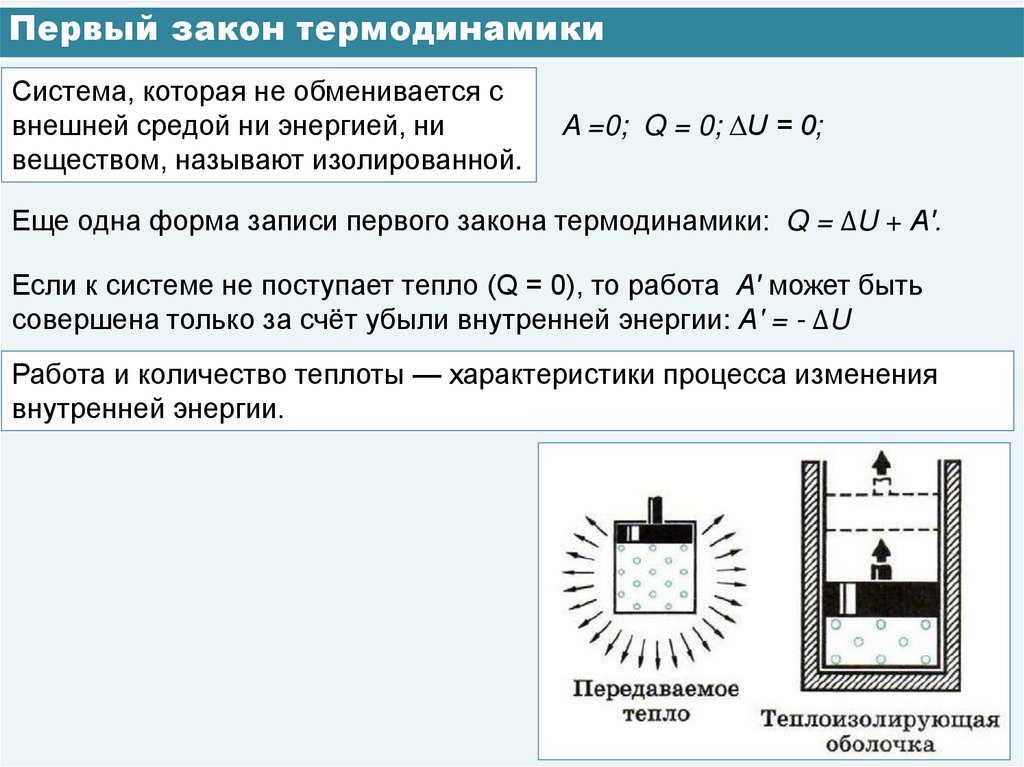
Система, которая не обменивается свнешней средой ни энергией, ни
веществом, называют изолированной.
A =0; Q = 0; ∆U = 0;
Еще одна форма записи первого закона термодинамики: Q = ∆U + А'.
Если к системе не поступает тепло (Q = 0), то работа А' может быть
совершена только за счёт убыли внутренней энергии: А' = - ∆U
Работа и количество теплоты — характеристики процесса изменения
внутренней энергии.
7. Наши задачи
8. Итоги
• Как формулируется первый закон термодинамики?• В каком случае изменение внутренней энергии
отрицательно?
• Почему можно говорить, что система обладает
внутренней энергией, но нельзя сказать, что она
обладает запасом определённого количества теплоты
или работы?
• Можно ли считать систему изолированной, если её
температура остаётся постоянной?
• Известно, что при изотермическом процессе идеальный
газ совершил работу 2000 Дж. Чему равно количество
теплоты, сообщённой системе?







 Физика
Физика








