Похожие презентации:
сор 2 Х8 подготовка (1)
1.
1. Расположите химические элементы в порядке возрастанияэлектроотрицательности: (пользуясь таблицей периодической системы)
С, N, I, Cl , Br, F, O, B, Be, Li
2. Составьте схемы образования связи между атомами:
А) водород и йод
В) литий и хлор
2.
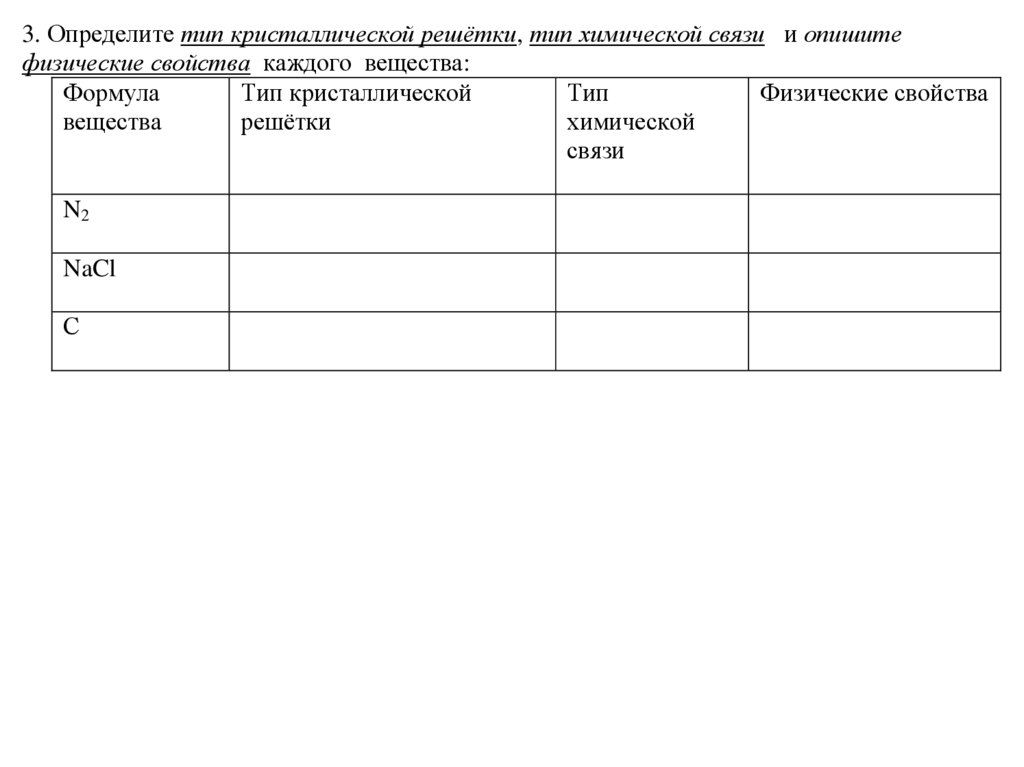
3. Определите тип кристаллической решётки, тип химической связи и опишитефизические свойства каждого вещества:
Формула
Тип кристаллической
Тип
Физические свойства
вещества
решётки
химической
связи
N2
NaCl
С
3.
4. Из данных химических формул веществ HCl, HBr, НFa) Укажите атом наиболее электроотрицательного химического элемента:
_________________________________________________[1]
b) Изобразите схему образования связи для веществ с помощью диаграммы «точек и
крестов» (показывая только внешние электроны).
Br₂
HBr
CaBr₂
4.
5. Сравните электроотрицательность элементова) Поставьте знак «<», « >» или «=»
Na
Cl
H
I
K
b) Определите между какими элементами из задания 5a образуется ковалентная связь
__________________________________________________________
O
5.
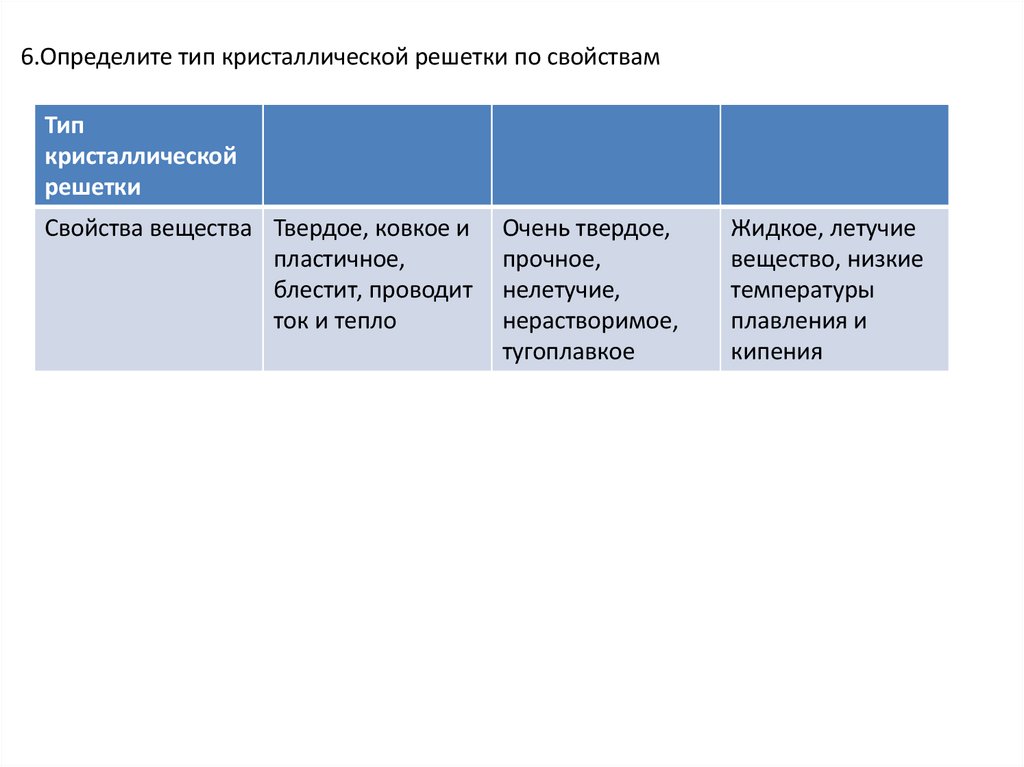
6.Определите тип кристаллической решетки по свойствамТип
кристаллической
решетки
Свойства вещества Твердое, ковкое и
пластичное,
блестит, проводит
ток и тепло
Очень твердое,
прочное,
нелетучие,
нерастворимое,
тугоплавкое
Жидкое, летучие
вещество, низкие
температуры
плавления и
кипения



 Химия
Химия