Похожие презентации:
8b6911c205eb48bcb8ed26c5a4d7ab77
1.
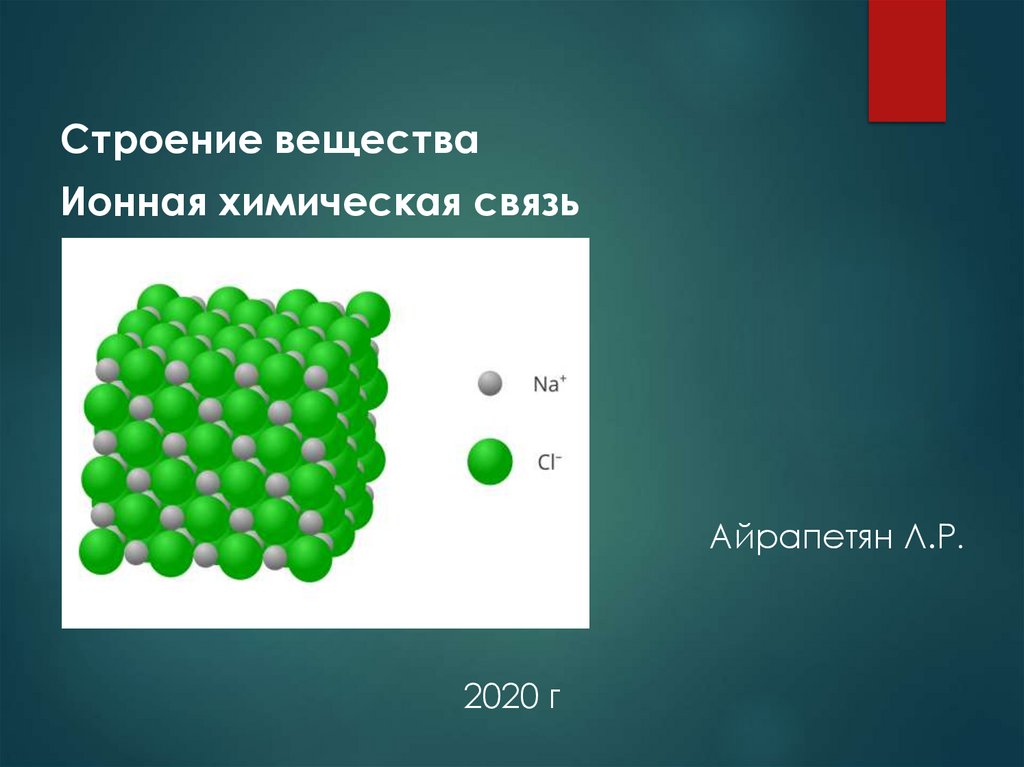
Строение веществаИонная химическая связь
Айрапетян Л.Р.
2020 г
2. Ионная химическая связь
Частицы, которые образуются в результатеперехода электронов от одного атома к другому,
называют ионами. Отрицательно заряженные ионы
называются анионом, положительно заряженные
ионы – катионом.
Химическая связь, которая возникает между
катионами и анионами в результате
электростатического притяжения, называется
ионной.
Электроотрицательность – это способность
атома притягивать электронную плотность от других
атомов.
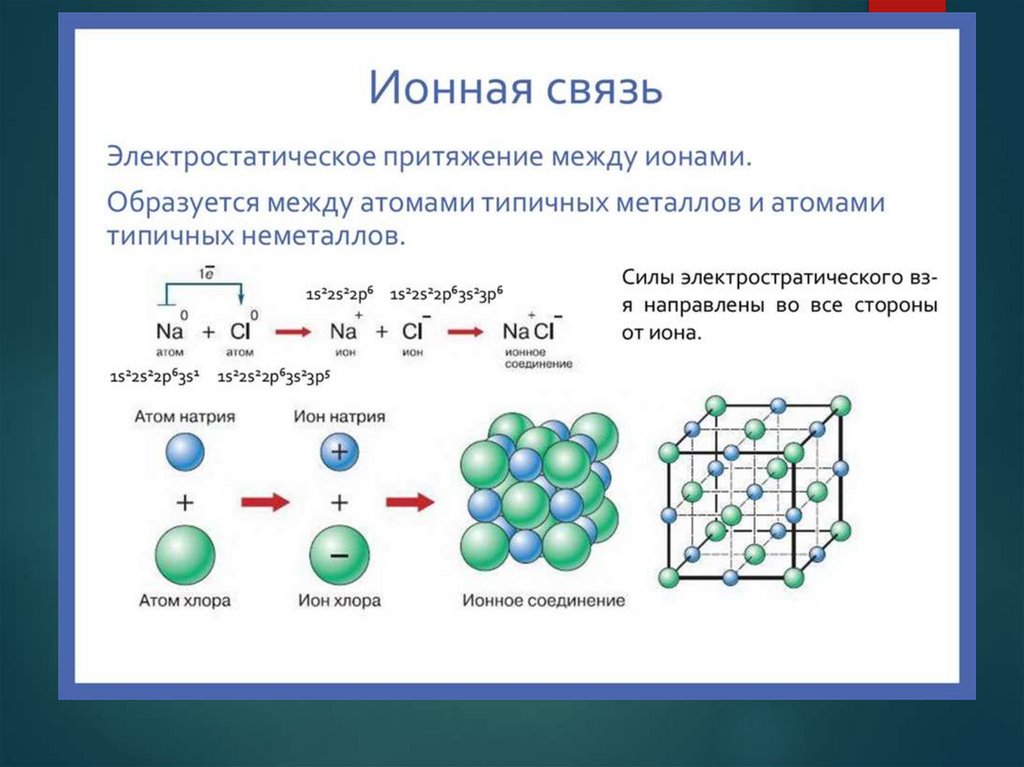
3. Ионная химическая связь
Рассмотрим образование ионной связи на примерехлорида натрия.
Nа + С1 → NаС1.
Атомы натрия и хлора имеют по одному неспаренному
электрону. При сближении этих атомов до определённого
расстояния происходит перекрывание электронных облаков
неспаренных электронов и образуется общее для двух
атомов электронное облако. Но так как
электроотрицательность хлора намного больше, чем
электроотрицательность натрия, то общая электронная пара
практически полностью смещается к атому хлора. В
результате перехода электрона от атома натрия к атому
хлора появляются заряженные частицы — атом хлора
приобретает отрицательный заряд, атом натрия —
положительный заряд.
4. Ионная химическая связь
Схема образования ионной связи между атомаминатрия и хлора :
Na -1e → Na +
Сl + 1е — С1 Ионная связь образуется между атомами
типичных металлов (щелочные и
щёлочноземельные) и типичных неметаллов
(галогены, кислород), электроотрицательность
которых сильно отличается.
5. Ионная химическая связь
Два разноименно заряженных иона, связанныхсилами взаимного притяжения, способны
взаимодействовать и с другими противоположно
заряженными ионами с образованием
кристаллических соединений.
Кристаллические вещества характеризуются
правильным расположением частиц (ионов) в
строго определенных точках пространства,
образуя кристаллическую решетку. Вещества с
ионным типом связи имеют ионные
кристаллические решетки. Эти вещества твердые,
прочные, нелетучие с высокими температурами
плавления, хрупкие.
6. Ионная химическая связь
Примеры веществ с ионной связьюХлорид натрия (NaCl), фторид калия (KF), бромид
меди (CuBr2), сульфат натрия (Na2SO4)
Ионы бывают простые (Na+, Cl-, Ca2+) и сложные
(ОН-, SO42-, NH4-)
7.
8.
9.
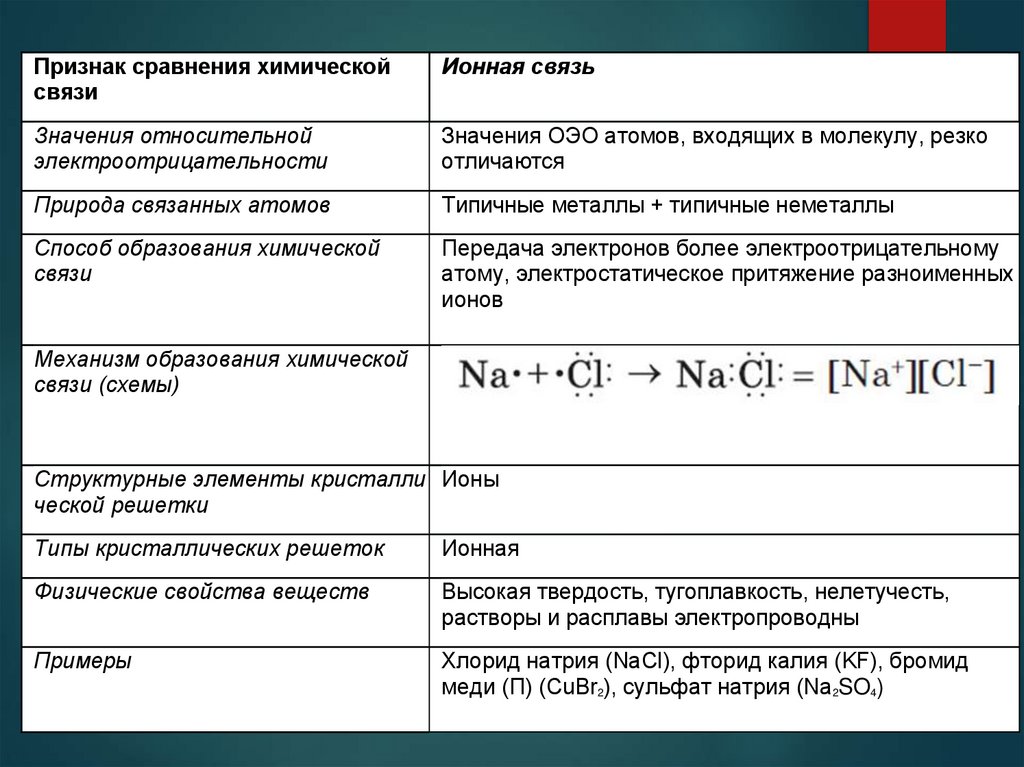
Признак сравнения химическойсвязи
Ионная связь
Значения относительной
электроотрицательности
Значения ОЭО атомов, входящих в молекулу, резко
отличаются
Природа связанных атомов
Типичные металлы + типичные неметаллы
Способ образования химической
связи
Передача электронов более электроотрицательному
атому, электростатическое притяжение разноименных
ионов
Механизм образования химической
связи (схемы)
Структурные элементы кристалли Ионы
ческой решетки
Типы кристаллических решеток
Ионная
Физические свойства веществ
Высокая твердость, тугоплавкость, нелетучесть,
растворы и расплавы электропроводны
Примеры
Хлорид натрия (NaCl), фторид калия (KF), бромид
меди (П) (CuBr2), сульфат натрия (Na2SO4)
10. Домашнее задание
Раздел 3.1 Контрольные вопросы и задания№3-8 стр. 34.








 Химия
Химия








