Похожие презентации:
Волокнистый катализатор для деструкции красителей методом нанесения комплексов полиэтиленполиамина на его поверхность
1. Министерство образования и науки РФ Федеральное государственное бюджетное образовательное учреждение «Санкт – Петербургский государст
Министерство образования и науки РФФедеральное государственное бюджетное образовательное
учреждение
«Санкт – Петербургский государственный университет
промышленных технологий и дизайна»
«Разработка волокнистого катализатора для
деструкции красителей методом нанесения
комплексов полиэтиленполиамина на его
поверхность»
Исполнитель: Кузьмина Дарья Борисовна
Руководитель: доц., к.т.н., Петров Сергей
Викторович
Санкт – Петербург
2017 г
2.
Цель работы – разработка указанного метода для получения катализаторапригодного для окисления антрахиноновых красителей в сточной воде
пероксидом водорода при нормальной температуре.
Задачи:
1. Подобрать количество компонентов таким образом, чтобы получить
тонкую пленку, не меняющую механических свойств волокна, но
обладающую достаточной каталитической активностью в реакции
жидкофазного окисления атрахиноновых красителей пероксидом
водорода
2. Изучить влияние механических и каталитических свойств волокна
технологических параметров.
3. Изучить влияние типа переходного металла на активность катализатора.
4. Изучить кинетику разложения красителя при разных рН, концентрации
пероксида и количества катализатора
5. Изучить активность катализатора на разных типах атрахиноновых
красителей. Атрахиноновые красители выбраны как один из наиболее
химически и физически устойчивых соединений, ярко окрашены, хорошо
сорбируемых тканями, дешевых, часто используемых и в то же самое
время, токсичных и трудно удаляемых из сточных вод.
6. Разработать и рассчитать промышленную установку для очистки сточных
вод этим методом и дать рекомендации для ее применения
2
3.
Фотографияполученного
образца
Микрофотография
волокна при 800
кратном
увеличении
3
4.
Расходные коэффициентыСтадия
обработки
Реагент
Доза на кг
сетки
Обезжиривание
ацетоном
Ацетон
10 л
Пропитка 10
минут при
комнатной
температуре
и сушка на
воздухе 30
мин
Обработка
водным
раствором
ПЭПА
NiSO4
Вода
3л
NiSO4*7H2O
0,1моль Ni2+ = 26,3 г
ПЭПА
28,72 г
Пропитка
в
кювете,
сушка при
105 оС, 30
мин
Стадия
обработки
Реагент
Доза на
сетки
Обработка
ацетоновым
раствором
эпоксидной
смолы
Ацетон
3 л = 2,37 кг
Эпоксидная смола ЭД-20
28,72*5 = 143,6 г
кг
исходной Условия
обработки
исходной Условия
обработки
Пропитка
в
кювете,
сушка, 30
мин,
прогрев при
130 оС, 30
4
мин
5.
Установка очистки сточных вод от красителей7
6
9
1
3
4
2
8
10
5
11
1- Реактор с водяной рубашкой и стеклянным фильтром , 2 - навеска
катализатора, 3 - реакционный раствор, 4 –водяной термостат, 5 – колба, 6 –
аэролифт, 7 - блок автоматического титрования, 8 –фотоэлектроколориметр, 9 –
бюретка, 10- клапан, 11- воздуходувка.
5
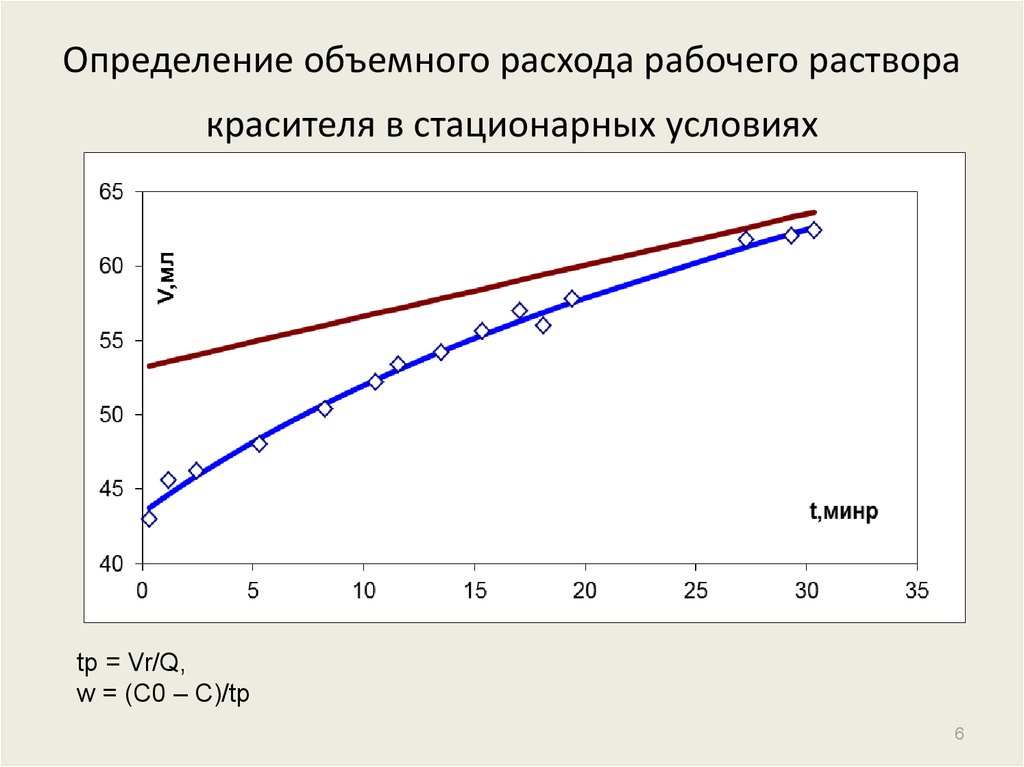
6. Определение объемного расхода рабочего раствора красителя в стационарных условиях
tp = Vr/Q,w = (C0 – C)/tp
6
7. Зависимость скорости разложения красителя от содержания Ni2+ на волокне
w, мг/мин/г1
0,9
0,8
0,7
0,6
0,5
0,4
0,3
0,2
0,1
0
0
0,2
0,4
0,6
0,8
1
1,2
1,4
Сод Ni2+, моль/кг
7
8. Зависимость каталитической активности от отношения ЭД-20:ПЭПА на волокне
10,9
0,8
w, мг/мин/л
0,7
0,6
0,5
0,4
0,3
0,2
0,1
0
0
1
2
3
4
5
6
Отношение ЭД-20 /ПЭПА г/г
8
9. Влияние природы металла на каталитическую активность волокна
Влияние природы металла на каталитическую1,2
1
w, мг/л/мин
активность волокна
0,8
0,6
0,4
0,2
0
Ni2+
Co2+
F3+
Cu2+
Ag+
Mn3+
Cr3+
9
10. Влияние концентрации красителя на скорость окисления
16Скорость разложения, мг/л/мин:
w = K1*C, где: K1 = 0,493 1/мин;
С, мг/л - концентрация
14
10
8
6
w, мг/л/мин
12
4
2
0
0
5
10
15
20
C, мг/л
25
30
35
10
11. Влияние содержания пероксида на скорость реакции
4Скорость разложения, мг/л/мин:
w = K2*C*CH2O2, где: K2 = 0,0329 л/мин/мг;
С, мг/л - концентрация
3,5
w, мг/л/мин
3
2,5
2
1,5
1
0,5
0
0
20
40
60
80
100
120
CH2O2 мг/л
11
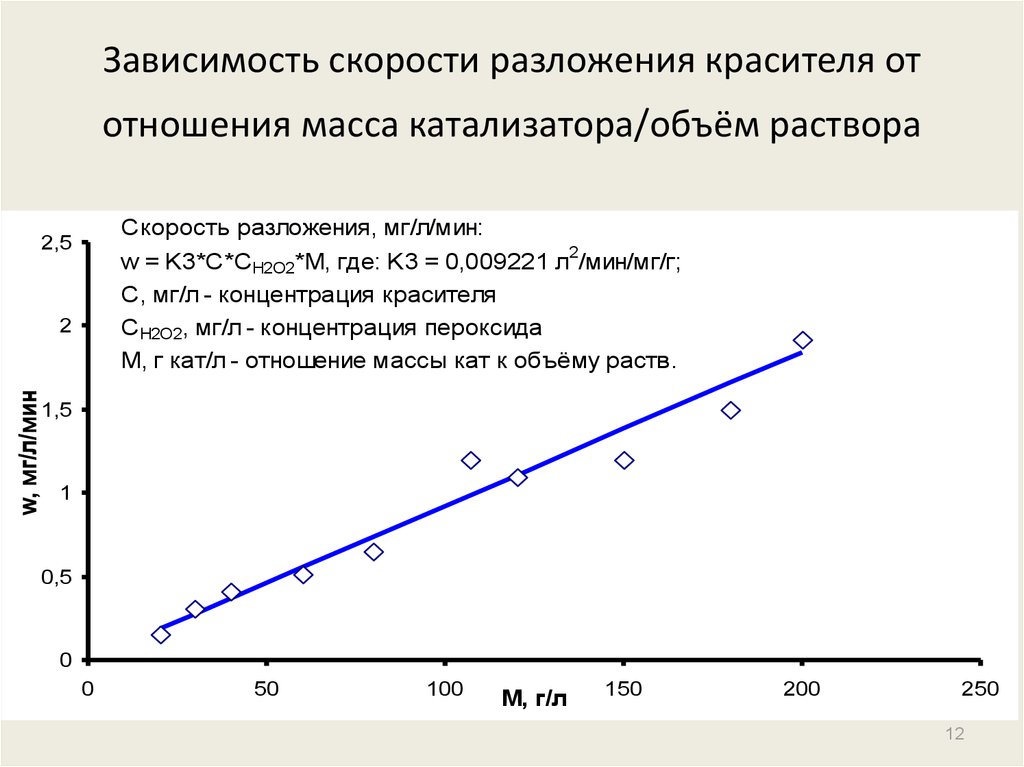
12. Зависимость скорости разложения красителя от отношения масса катализатора/объём раствора
Скорость разложения, мг/л/мин:2,5
2
w = K3*C*C H2O2*M, где: K3 = 0,009221 л /мин/мг/г;
С, мг/л - концентрация красителя
CH2O2, мг/л - концентрация пероксида
M, г кат/л - отношение массы кат к объёму раств.
w, мг/л/мин
2
1,5
1
0,5
0
0
50
100
M, г/л
150
200
250
12
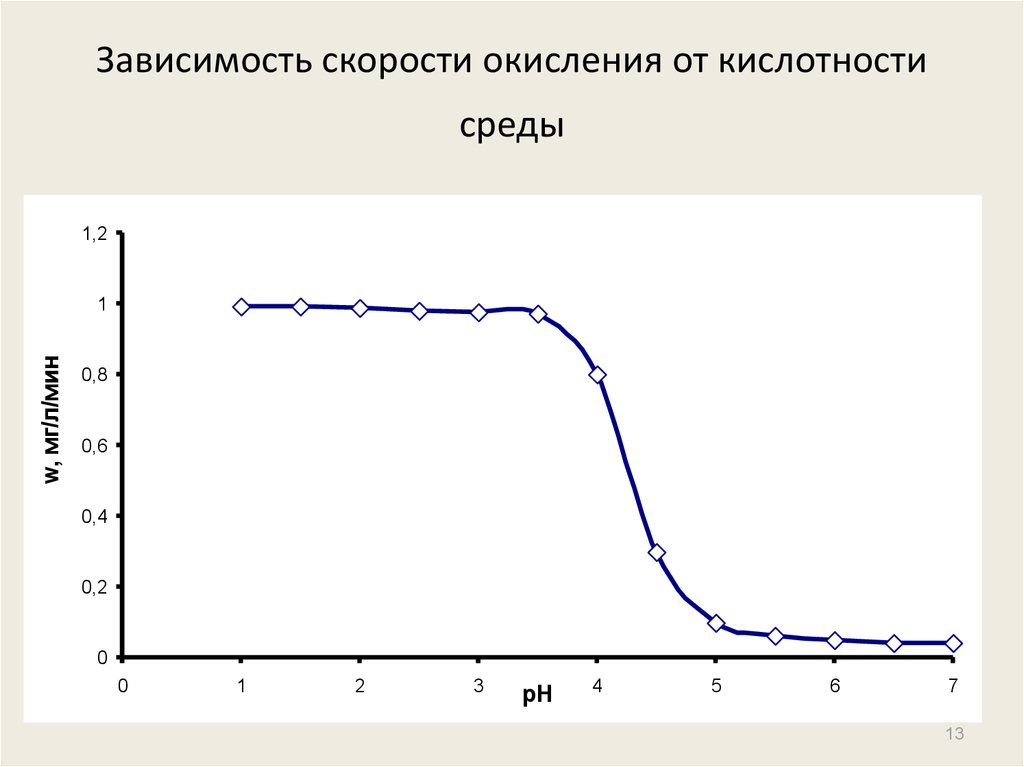
13. Зависимость скорости окисления от кислотности среды
1,2w, мг/л/мин
1
0,8
0,6
0,4
0,2
0
0
1
2
3
рН
4
5
6
7
13
14. Зависимость скорости реакции разложения красителя от концентрации красителя и температуры
30,00Температура , о С
w, мг/л /мин
10
25,00
20,00
15
20
30
40
50
15,00
60
70
10,00
5,00
С , мг/л
0,00
0
5
10
15
20
25
30
14
15. Зависимость константы разложения красителя от температуры в координатах Аррениуса
-8,2K3 = K30*exp(-Ea/RT) - константа реакции ;
K30 = 0,003179, л2/мин/мг/г;
Ea = 7380 Дж/моль - энергия активации;
R = 8.314 Дж/моль/л - газовая постоянная;
Т, К - абсолютная температура
-8,4
-8,5
-8,6
-8,7
-8,8
L n(K 3, л 2/мин/мг/г)
-8,3
-8,9
-9
0,00034
1/R T
0,00036
0,00038
0,0004
0,00042
15
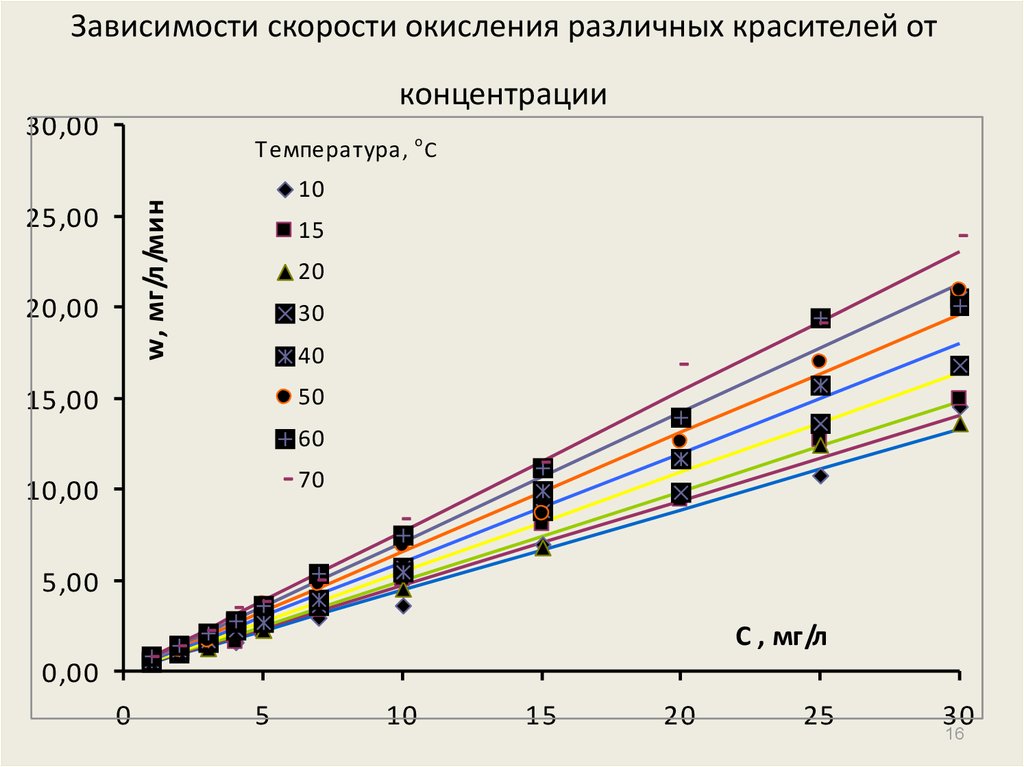
16. Зависимости скорости окисления различных красителей от концентрации
30,00Температура , о С
w, мг/л /мин
10
25,00
20,00
15
20
30
40
50
15,00
60
70
10,00
5,00
С , мг/л
0,00
0
5
10
15
20
25
30
16
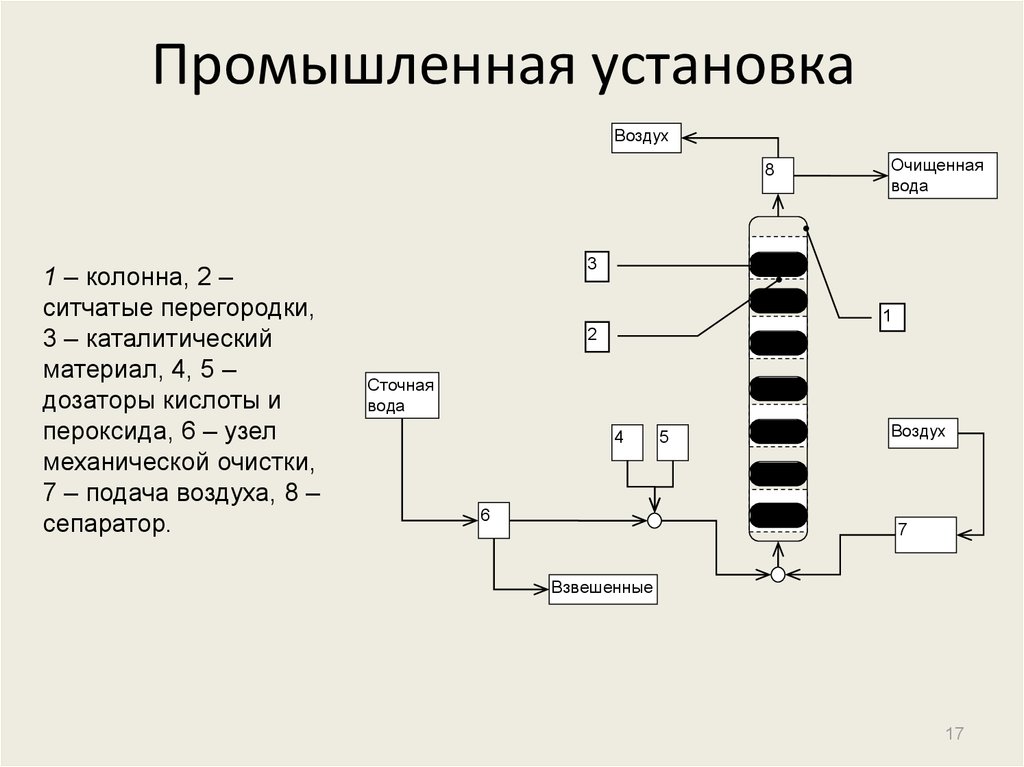
17. Промышленная установка
Воздух8
1 – колонна, 2 –
ситчатые перегородки,
3 – каталитический
материал, 4, 5 –
дозаторы кислоты и
пероксида, 6 – узел
механической очистки,
7 – подача воздуха, 8 –
сепаратор.
Очищенная
вода
3
1
2
Сточная
вода
4
6
5
Воздух
7
Взвешенные
17
18.
Объёмный расход сточной воды Q = 10000 м3/сут, 6944 л/мин, 0.1157 м3/сек.Концентрация красителя на входе, С0 = 15 мг/л, на выходе, С1 = 0.5 мг/л.
Доза пероксида CH2O2 = 15 мг/л, рН реакции – 3.5, температура 20 оС.
Отношение масса катализатора : объём раствора в колонне примем такое
же, как и в опытах M = 107 кг/м3 = г/л.
Расчёт диаметра колонны. Примем скорость движения жидкости по колонне
v = 0.02 м/с.
Тогда сечение колонны S = Q/v = 0.1157/0.02 = 5.8 м2, диаметр колонны D =
sqrt(4*S/3.14) = sqrt(7.37) = 2.71 м.
Расчёт константы К1 для данного случая. K1 = K3*CH2O2*M = 0.00015369
л2/мин/мг/г*15 мг/л*107 г/л = 0.247 1/мин.
Расчёт времени пребывания жидкости в колонне. Анализ показывает, что
пяти – шести секций достаточно для достижения режима, близкого к
поршневому течению. После этого, можно использовать найденные
кинетические закономерности. Тогда расчёт ведём по кинетическому
уравнению C = C0*exp(-K1*tp), tp = ln(C0/C)/K1 = ln(15/0.5)/ 0.247 = 13.77 мин
= 826.2 сек.
Расчёт объёма колонны. V = Q*tp = 0.1157 м3/сек*826.2 сек = 95.6 м3.
Расчёт высоты колонны H = V/S = 95.6 м3/5.8 м2 = 16.5 м.
Расчёт количества катализатора Mk = M * V = 107 кг/м3 * 95.6 м3 = 10230 кг =
10.23 т.
18
19. Выводы
1. Из литературных данных следует, что перспективным методом очистки сточных водот красителей является окисление на гетерогенно волокнистом катализаторе,
содержащим ионы переходных металлов.
2. В качестве волокнистого носителя удобно использовать объемный трикотажный
материал, состоящий из полипропиленовых мононитей придающих материалу форму
и упругость и комплексных полиакрилонитрильных нитей.
3. В качестве метода нанесения каталитически активного слоя была выбрана пропитка
материала водным раствором комплекса полиэтиленполиамин(ПЭПА)- переходный
металл.С дальнейшей сушкой на воздухе при 105 градусах цельсия.На второй стадии
волокно пропитывается ацетоновым раствором эпоксидной смолы ЭД-20 с
дальнейшей сушкой и прогревом на воздухе при 130 градусах.
4. Разработан способ измерения стационарного расхода исходного раствора красителя в
реакторе.
5. Установлены оптимальные расходные коэффициенты для модифицирующих
реагентов.
6. Изучено влияние природы переходного металла на каталитическую активность.
7. Изучено влияние концентрации красителя, пероксида водорода и кислотности среды
на скорость реакции. Получено математическое выражение для вычисления скорости.
8. Изучено окисление нескольких антрахиноновых красителей, получены коэффициенты
для расчёта скорости их окисления.
9. На основе полученных экспериментальных данных по кинетике рассчитан пример
19
каталитической колонны для очистки сточной воды от красителей.















 Промышленность
Промышленность








