Похожие презентации:
Относительная атомная и молекулярная массы
1. Самостоятельная работа №2
2. Относительная атомная и молекулярная масса
12.09.20173. Размеры различных объектов
Атом водородаПомидор
Лук репчатый
Картофель
Свекла
Перец Болгарский
4. Масса различных объектов
Атом водорода0,000000000000000000000001674 грамма
100 граммов
75 граммов
100 граммов
120 граммов
100 граммов
5. Масса различных атомов
С0,000000000000000000000026667
2,6667*10-23
н
0,000000000000000000000001674
1,674*10-24
0,000000000000000000000019930
1,993*10-23
О
С
н н
н н н
н н н
н н н н
Углерод в 12 раз тяжелее водорода
О
н
н
нн
н н
н н н
н н н
н н н н
Кислород в 16 раз тяжелее водорода
6. Относительная атомная масса
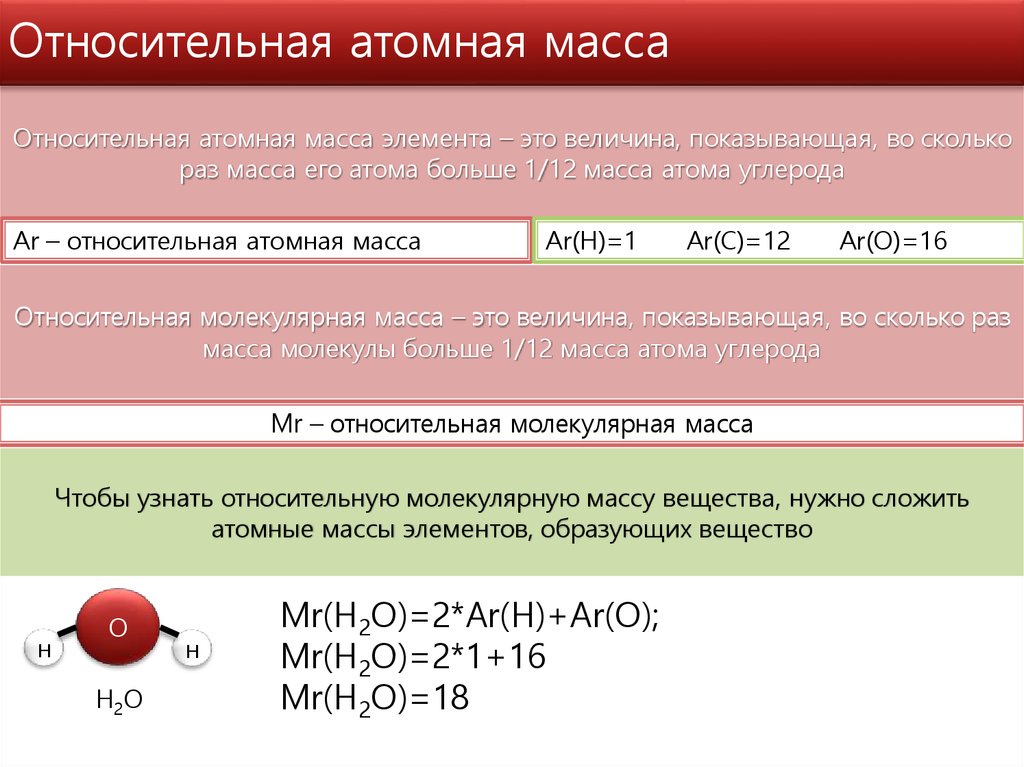
Относительная атомная масса элемента – это величина, показывающая, во сколькораз масса его атома больше 1/12 масса атома углерода
Ar – относительная атомная масса
Ar(H)=1
Ar(C)=12
Ar(O)=16
Относительная молекулярная масса – это величина, показывающая, во сколько раз
масса молекулы больше 1/12 масса атома углерода
Mr – относительная молекулярная масса
Чтобы узнать относительную молекулярную массу вещества, нужно сложить
атомные массы элементов, образующих вещество
н
О
H2O
н
Mr(H2O)=2*Ar(H)+Ar(O);
Mr(H2O)=2*1+16
Mr(H2O)=18
7. О чем говорит химическая формула
Массовая доляCO2
1. Конкретное вещество – углекислый
газ
2. Качественный состав – состоит из 2-х
элементов C и O
3. Тип вещества – сложное вещество
4. Количественный состав вещества 1
атом С и 2 атома О
5. Mr(CO2)=44
6. Соотношение масс элементов
m(C):m(O)=12:32=1:2,6
7. Массовые доли элементов






 Химия
Химия








