Похожие презентации:
Корреляция структуры ксенобиотика и его токсичности. Топологические индексы
1. Корреляция структуры ксенобиотика и его токсичности. Топологические индексы
ПОДГОТОВИЛА СТУДЕНТКА 5 КУРСАМАМЕДОВА МАЛИКА
2. Введение
Установление соответствия между строением ибиологическими свойства соединений положили
начало поиску активных групп или ядер,
ответственных за активность или токсичность.
Объяснения корреляции структуры ксенобиотика
получило свое объяснение к концу прошлого
века.
3. Практичность
При создании нового лекарства сначаласинтезируют ряд его аналогов.
В качестве кандидата выбирают вариант с
наиболее оптимальными физико-химическими
свойствами, характеристиками распределения,
био-трансформации и минимальной
токсичностью.
Для этого используют метод ККСА – метод
количественных корреляций структураактивность.
4. Дексрипторы
Выявление количественной корреляции свойствхимических соединений с их молекулярными
структурами возможно после математического
описания и цифрового представления структуры
молекулы.
В настоящее время предложено более различных
видов структурного описания(дескрипторов)
5. Корреляция структуры ксенобиотика и его токсичности.
6.
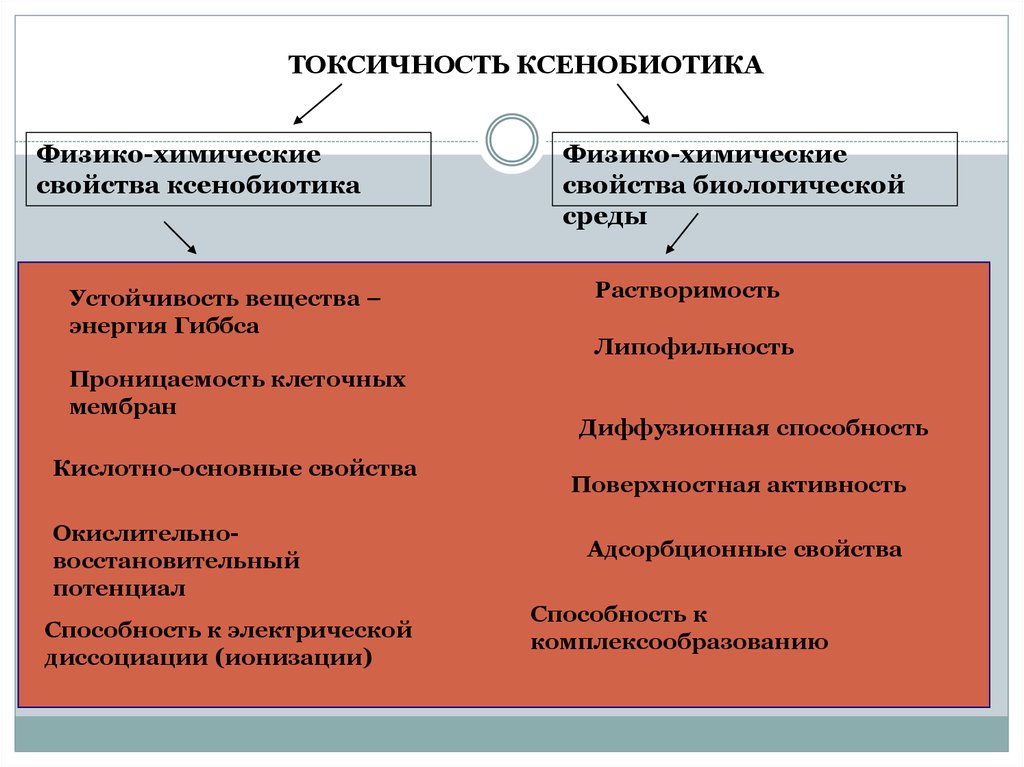
ТОКСИЧНОСТЬ КСЕНОБИОТИКАФизико-химические
свойства ксенобиотика
Устойчивость вещества –
энергия Гиббса
Проницаемость клеточных
мембран
Кислотно-основные свойства
Окислительновосстановительный
потенциал
Способность к электрической
диссоциации (ионизации)
Физико-химические
свойства биологической
среды
Растворимость
Липофильность
Диффузионная способность
Поверхностная активность
Адсорбционные свойства
Способность к
комплексообразованию
7.
а) Межфазные переходы тв↔ж, диаграммы рНрастворимость8.
в) Влияние кислотно-основной природы ксенобиотиков ирН биосред на межфазные равновесия ж1↔ж2
для кислот:
для оснований:
НА ↔ Н+ + А-.
ВН+↔ В + Н+
[неионизированнаяформ а]
pH pK a log
[ионизированнаяфориа ]
pH pK a log
[ионизированнаяформа ]
[неионизированнаяфори а]
[ A ]
pH pK a log
[ HA]
[ A ]
[ HA]
10
при рН= рКа
10
pH pKa
[A-] = [HA].
1
pKa pH
pH pK a log
рКа =14 - рKb
pH pKa
[ B]
10
[ BH ]
рН= рКа
1
[ B]
[ BH ]
[ВН+] = [В].
1
pH pK
a 1
10
моча ( рН 4,8-7,4), плазма крови (рН 7,35-7,45) желудочный сок (рН 1,5
9.
г) Влияние окислительно-восстановительного потенциала Е0 ирН среды на токсичность ксенобиотика. Диаграммы рНпотенциал для биосред и токсикантов.
10. Топологические индексы
Для количественного определения наибольшую популярностьимеют топологические индексы.
Первый такой индекс был предложен Х. Винером в 1947 г.
Молекулярную структуры также можно показать с помощью
графа. Ребра графа – ковалентные химические связи.
11.
12.
13. Индексы Винера, Балабана и индекс обхода
14. Пример использование индекса Винера
15. Список литературы
Плетенева Т.В., Саломатин Е.М.,Сыроешкин А.В. и др. Токсикологическая
химия. Учебник для ВУЗов / под ред.
Плетеневой Т.В. - Москва: Издательская
группа "ГЭОТАР-Медиа", 2005. - 512 с.















 Биология
Биология Химия
Химия








