Похожие презентации:
Обмен липидов
1. Цель: Дать представление о катаболических и анаболических путях превращение липидов и их биологической роли.
ОБМЕН ЛИПИДОВЦель: Дать представление о катаболических и анаболических путях
превращение липидов и их биологической роли.
• Основны вопросы:
• 1. Строение и биологические функции липидов. Резервные и структурные
липиды. Состав, строение и физиологическая роль транспортных
липопротеидов крови
• 2.Переваривание жиров, всасывание продуктов гидролиза, роль желчных
кислот. Нарушение переваривания и всасывания липидов.
• 3.Ресинтез триацилглицеринов в стенке кишечника.
• 4.Особенности биосинтеза жиров в печени и жировой ткани.
• 5.Резервирование и мобилизация жиров. Регуляция и физиологическая роль
резервирования и мобилизации жиров. Нарушение этих процессов при
ожирении.
• 6.Обмен жирных кислот. Бета-окисление как специфический путь
катаболизма жирных кислот. Карнитиновый челночный механизм.
• 7.Синтез, использование и физиологическое значение кетоновых тел
8.Биосинтез жирных кислот.
• 9.Эйкозаноиды и их роль в регуляции метаболизма и физиологических
функции.
2.
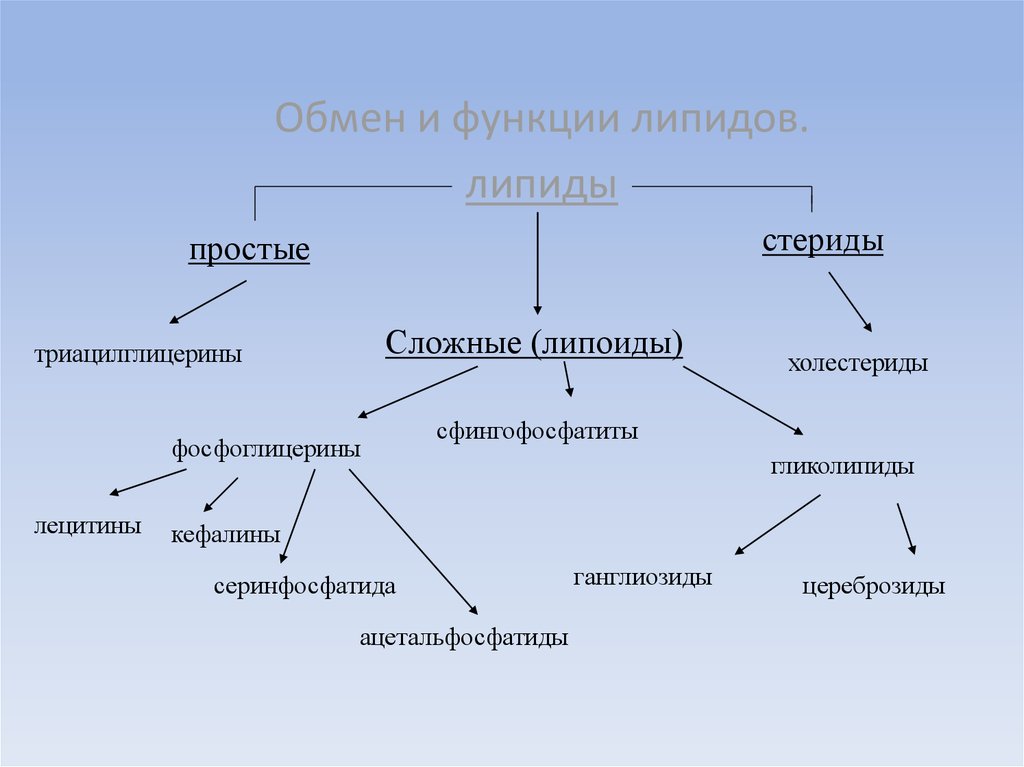
Обмен и функции липидов.липиды
стериды
простые
Сложные (липоиды)
триацилглицерины
фосфоглицерины
лецитины
холестериды
сфингофосфатиты
гликолипиды
кефалины
серинфосфатида
ацетальфосфатиды
ганглиозиды
цереброзиды
3. Биологические функции липидов
• Липиды являются энергетическим материалом, выполняютзащитные, пластические, транспортные и регуляторные
функции.
• По физиологическому назначению липиды организма делятся
на три группы: резервные липиды, протоплазматические или
структурные липиды и транспортные липиды
(липопротеины).
• Резервные липиды в основном представлены
триацилглицеринами. Они депонируются в больших
количествах в жировых депо и затем по мере необходимости
легко мобилизуются и расходуются как энергетический
материал.
• При полном окислении 1 грамма жира высвобождается 9,3 ккал
энергии (38,9 кДж).
• Протоплазматические липиды представлены фосфолипидами
глицеридами и не глицеридами (сфингофосфатиды),
гликолипидами и холестеридами. Это структурные компоненты
клеточных мембран и их содержание в организме постоянно.
4. Транспортные липиды
• Транспортные липиды - это липиды, находящиеся в комплексес белками и доставляемые экстрацелюлярными жидкостными
средами (кровь, лимфа) от одного органа к другому. Чаще их
называют транспортными липопротеинами (ЛП). Все
транспортные липопротеины построены по типу гидрофобной
мицелы и состоят из гидрофобного ядра, образованного
триацилглицеринами и холестеридами, и гидрофильного слоя,
образованного дифильными молекулами фосфолипидов,
гликолипидов и молекулами белка, формирующих гидратную
оболочку. Различают следующие типы транспортных
липопротеинов:
- хиломикроны (ХМ),
- липопротеины высокой плотности (ЛПВП),
- липопротеины очень низкой плотности (ЛПОНП),
- липопротеины низкой плотности (ЛПНП).
5. Хиломикроны (ХМ)
• Хиломикроны (ХМ) формируются в стенке кишечника иотличаются от других транспортных липопротеинов самым
высоким содержанием триацилглицеринов (85-90%),
низким содержанием холестерина, фосфолипидов и белка
(0,5-2,0%).
• Хиломикроны – это главная транспортная форма
экзогенных, ресинтезированных в стенке кишечника,
триацилглицеринов.
• Вследствие большого диаметра частиц (d=100-500нм), ХМ
не проникают через мембраны эндотелиальных клеток
кишечника в кровяные капилляры и хорошо диффундируют
в лимфу.
• Током лимфы оттекающей от кишечника, ХМ доставляются в
грудной лимфатический проток и затем только попадают в
кровоток.
• Концентрация ХМ в крови находится в пределах от 0 - 0,5 до
2,0г/л.
6. ЛПОНП или пре--липопротеины
ЛПОНП или пре- -липопротеины• ЛПОНП или пре- -липопротеины, формируются в печени и
частично в эпителиальных клетках тонкого кишечника.
• ЛПОНП отличаются, как и ХМ, высоким содержанием
триацилглицеринов (64-80%), но в отличие от ХМ содержат
много фосфолипидов (15-18%), холестеридов (8-15%) и белка
(10-13%).
• ЛПОНП являются главной транспортной формой ситезируемых
эндогенных триацилглицеринов.
• В эндотелии капилляров различных органов имеется фермент
липопротеинлипаза, связанная с гликозамингликанами
внутренней поверхности капилляров и непосредственно
контактирует с кровью.
• Этот фермент имеет центр связывания липопротеинов и
каталитический центр для гидролиза триацилглицеринов.
• Благодаря этому ферменту ЛПОНП и ХМ, постепенно
освобождаясь от триацилглицеринов, превращаются в ЛПНП, а
также, вероятно, и в ЛПВП.
• Концентрация ЛПОНП в крови находится в пределах 1,5-2,0 г/л.
7. ЛПНП или - липопротеины
ЛПНП или - липопротеины• ЛПНП или - липопротеины образуются в крови из
ЛПОНП и являются главной транспортной формой
холестерина из печени во все органы и ткани, на
поверхности клеток которых имеются рецепторы,
специфичные к ЛПНП, где холестерин используется
для построения клеточных мембран.
• Особенно легко проникают -липопротеиды к
клеткам стенки сосудов, доставляя в них
холестерин.
• Содержание холестерина в ЛПНП составляет 35-40
%, фосфолипидов 21-25% и белка 25%.
• Концентрация ЛПНП в крови здорового человека
составляет 3,0-4,5 г/л.
8. ЛПВП или -липопротеины
ЛПВП или -липопротеины• ЛПВП или -липопротеины, формируются в гепатоцитах и
характеризуются высоким содержанием фосфолипидов (25-27%),
холестеридов ( 17-20 %) и белка ( 45-49%) и являются главной системой
транспорта фосфолипидов из печени в ткани.
• Вследствие маленького диаметра частиц (d = 10-15нм) ЛПВП легко
проникают через мембраны клеток сосудов в сосудистую стенку и
удаляются оттуда лимфотоком.
• По этой причине ЛПВП осуществляют обратный транспорт холестерина
из тканей в печень и доставку фосфолипидов в ткани.
• В ЛПВП имеется белок-фермент лецитин-холестерин- ацилтрансфераза
(ЛХАТ), который катализирует синтез эфиров холестерина и освобождает
молекулы лизолецитина.
• Образующиеся холестериды легко перемещаются в ядерную часть
ЛПВП, еще больше уплотняя его и освобождая поверхностный слой
ЛПВП от холестерина.
• Все это облегчает транспорт холестерина от клеток разных тканей к
печени и к кишечнику.
• Концентрация альфа-липопротеинов в крови составляет у мужчин 1,254,25 г /л, у женщин 2,5-6,5 г/ л.
9. Липиды кожи человека
• Большое количество разветвленных жирныхкислот, как свободных, так и связанных
присутствует среди многочисленных липидов
кожи человека.
• Считается, что разветвленные жирные кислоты
играют определенную роль в поддержании
экологического баланса среды для
микроорганизмов, обитающих на коже.
• Кроме того, именно эти соединения придают
каждому индивидууму специфический запах,
своего рода химический "отпечаток пальцев".
10. Переваривание и всасывание продуктов переваривания липидов
• Содержание и разновидность липидов в пищезависит от употребляемых пищевых продуктов.
• Больше всего человек использует в пищу
триацилглицерины растительного и животного
происхождения, отличающиеся друг от друга
составом жирных кислот.
• В питательном отношении наибольшую ценность
представляют жидкие жиры (растительные масла), в
молекулах которых содержатся ненасыщенные
жирные кислоты.
• В организм человека с животными продуктами
(мясо, молоко, масло) поступают не только
триацилглицерины, но и липоиды и стериды.
• В яичном желтке, например, присутствуют в
большом количестве фосфолипиды (лецитины).
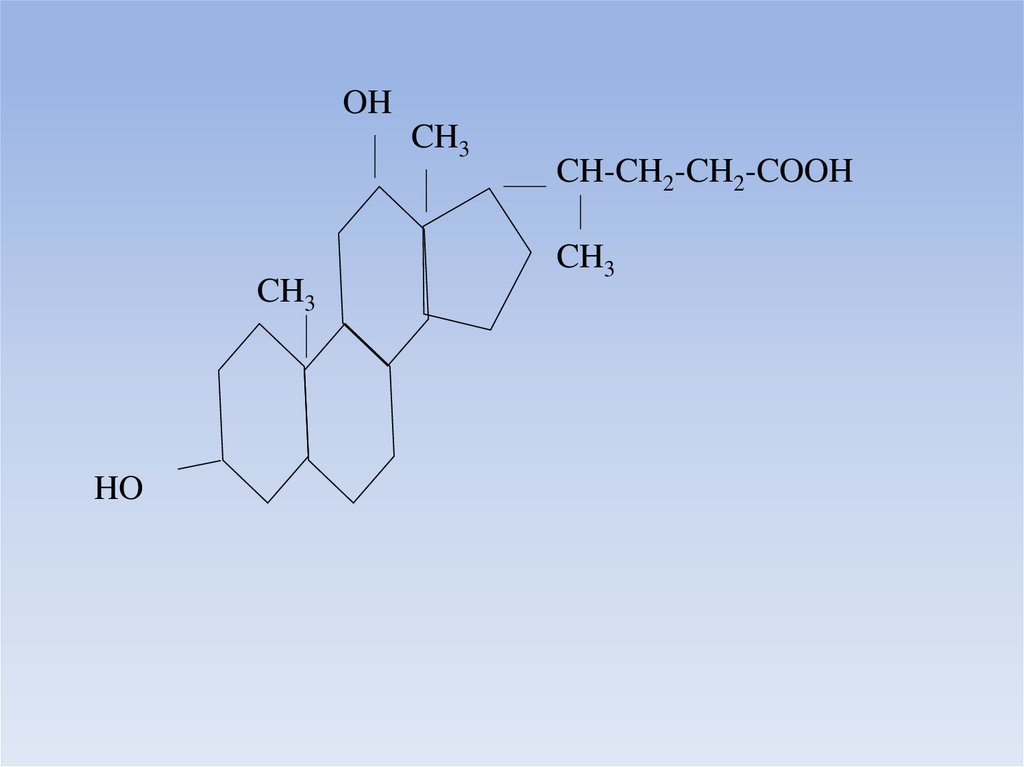
11. Желчные кислоты
• Обязательным условием для переваривания жиров являетсяперевод их эмульгированное состояние с помощью желчных
кислот.
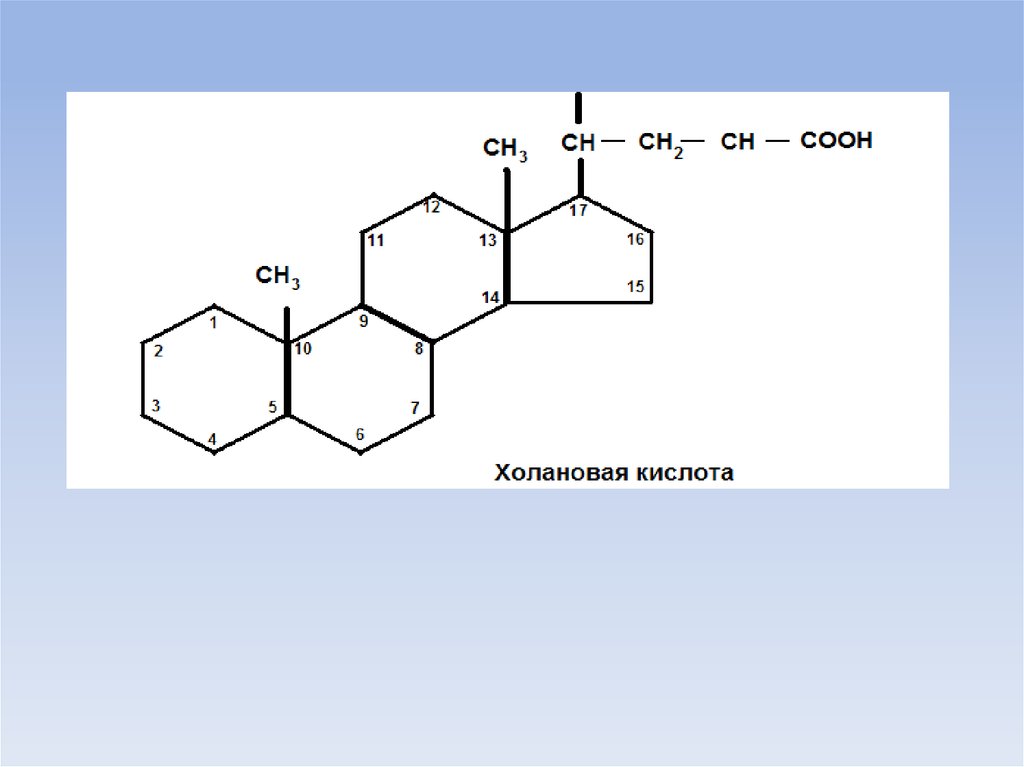
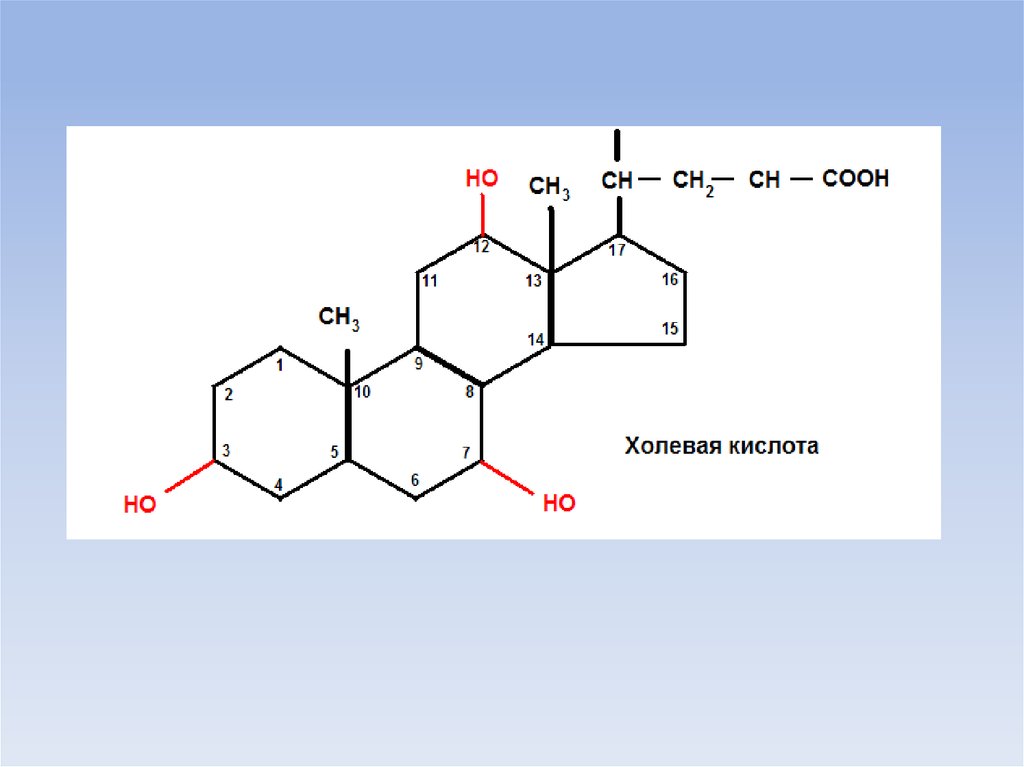
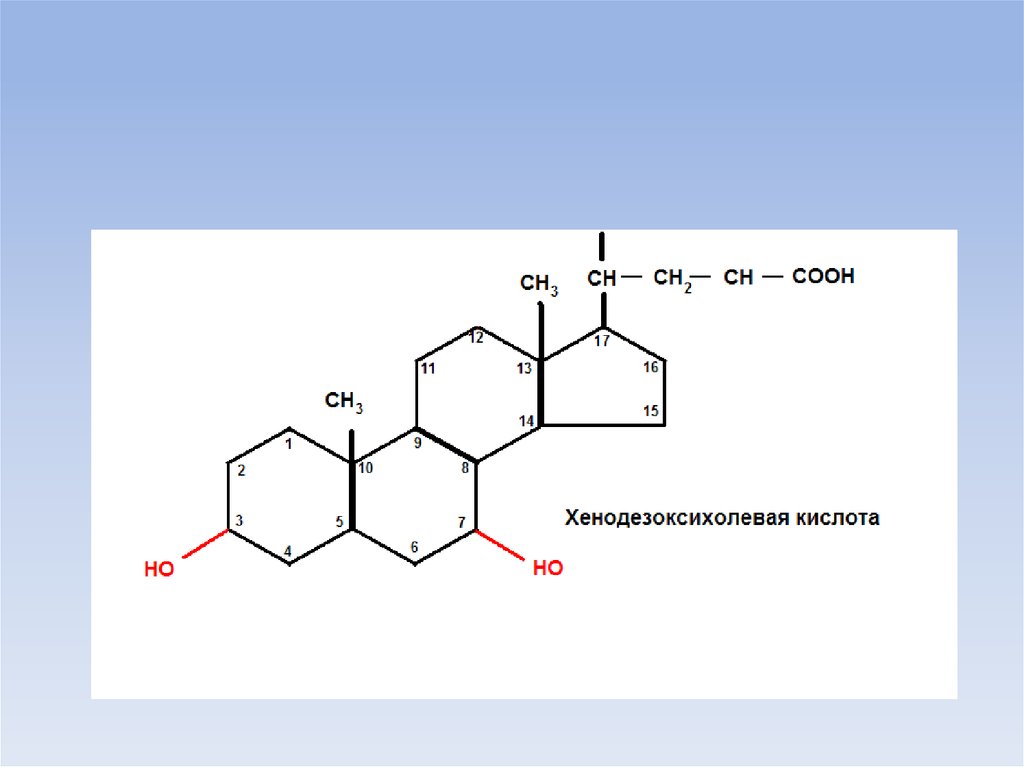
• Желчные кислоты (холевая, дезоксихолевая, литохолевая - 3оксихолановая кислота) являются производными холановой
кислоты.
• В составе желчи желчные кислоты коньюгированы либо с
таурином (Н2N-СН2-SО2-ОН), либо с гликоколом (Н2N-СН2СООН), образуя парные комплексы.
• Парные желчные кислоты (гликохолевая, таурохолевая,
гликодезоксихолевая, тауродезоксихолевая и др.) обладают
амфифильными свойствами, являются поверхностно
активными веществами и поэтому вызывают эмульгирование
жиров.
12.
13.
14.
15.
OHCH3
CH3
HO
CH-CH2-CH2-COOH
CH3
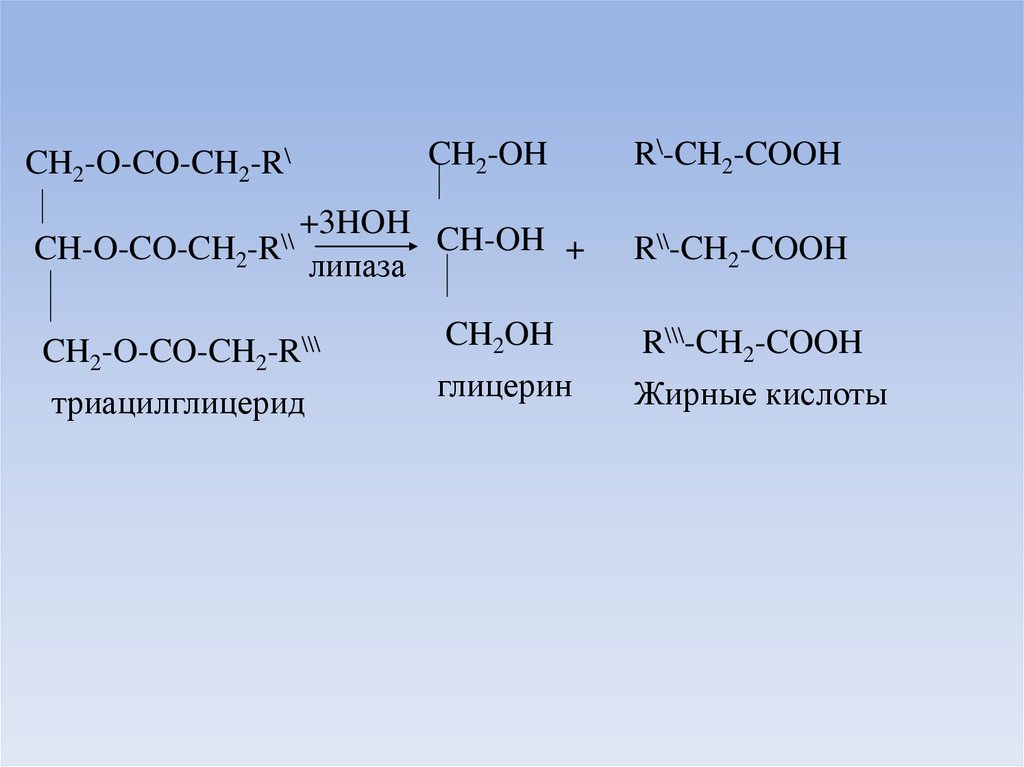
16. Переваривание триацилглицеридов
Триацилглицерины пищи разрушаются панкреатической липазой,которая поступает в кишечник в неактивном виде. Липаза активируется
желчными кислотами и кишечного происхождения - колипазой. Под
воздействием липазы эмульгированные триацилглицерины гидролитически
разрушаются до моноацилглицерина и жирных кислот. Моноацилглицерины
далее разрушаются карбоксиэстеразами кишечника и панкреатического сока
до глицерина и жирной кислоты.
СН2-О-СО-СН2-R`
|
+ 3 НОН
CН-О-СО-СН2-R``
|
липаза
СН2-О-СО-СН2-R```
триацилглицерид
СН2-ОН
|
CН-ОН +
|
СН2-ОН
глицерин
R`-СН2-COOH
R``-СН2-COOH
R```-СН2-COOH
жирные кислоты
17.
CH2-OHCH2-O-CO-CH2-R\
CH-O-CO-CH2
-R\\
+3HOH CH-OH
+
липаза
CH2-O-CO-CH2-R\\\
триацилглицерид
CH2OH
глицерин
R\-CH2-COOH
R\\-CH2-COOH
R\\\-CH2-COOH
Жирные кислоты
18. Переваривание фосфолипидов
Фoсфолипиды в кишечнике гидролизуются особой группой ферментовназываемых фосфолипазами. Существует несколько типов фосфолипаз,
обозначаемых как А, B (A2), C, D.
СН3
CH2OH
|+
|
СН3--N--СН2--СН2
CН-ОН
+ Н3РО4
|
|
|
фосфорная
СН 3
О
СН2-ОН
кислота
| (D)
глицерин
R-CН2-СН=СН-СН2 СН2---О--Р=О
|
|
\ОН
R-СН=CН-СН2-COOH
О=С---О--СН (С)
+ 4НОН
ненасыщенная жирная кислота
|
(А) СН2-О--С=О фосфолипаза R`-СН2-СН2-COOH
|
(А,В,С,D)
насыщенная жирная кислота
(B) СН2
CН3
|
|
R`-СН2-СН2
СН3--N-СН2-СН2-OH
лецитин
|
СН 3
холин
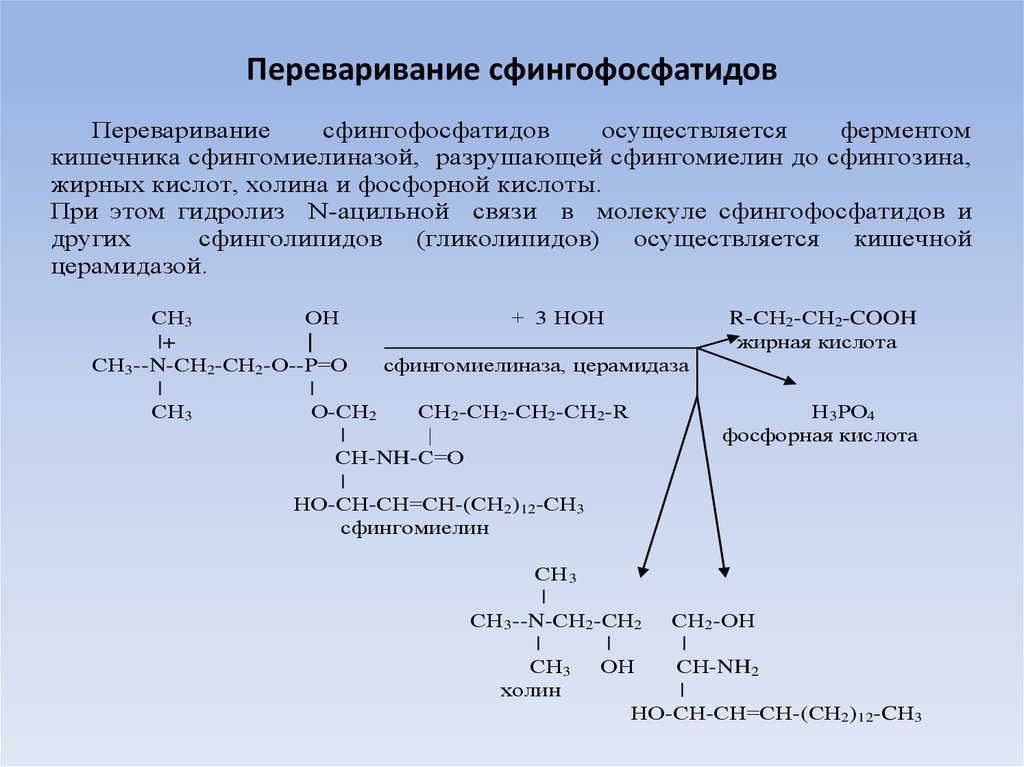
19. Переваривание сфингофосфатидов
Перевариваниесфингофосфатидов
осуществляется
ферментом
кишечника сфингомиелиназой, разрушающей сфингомиелин до сфингозина,
жирных кислот, холина и фосфорной кислоты.
При этом гидролиз N-ацильной связи в молекуле сфингофосфатидов и
других
сфинголипидов (гликолипидов) осуществляется кишечной
церамидазой.
CН3
ОН
+ 3 НОН
|+
|
СН3--N-СН2-СН2-О--Р=О
сфингомиелиназа, церамидаза
|
|
СН3
О-СН2
СН2-СН2-СН2-СН2-R
|
|
СН-NH-С=О
|
НО-СН-СН=СН-(СН2)12-СН3
сфингомиелин
R-СН2-СН2-COOH
жирная кислота
Н3РО4
фосфорная кислота
CН 3
|
СН 3--N-СН2-СН2 СН2-ОН
|
|
|
СН3 ОН
СН-NH2
холин
|
НО-СН-СН=СН-(СН2)12-CН3
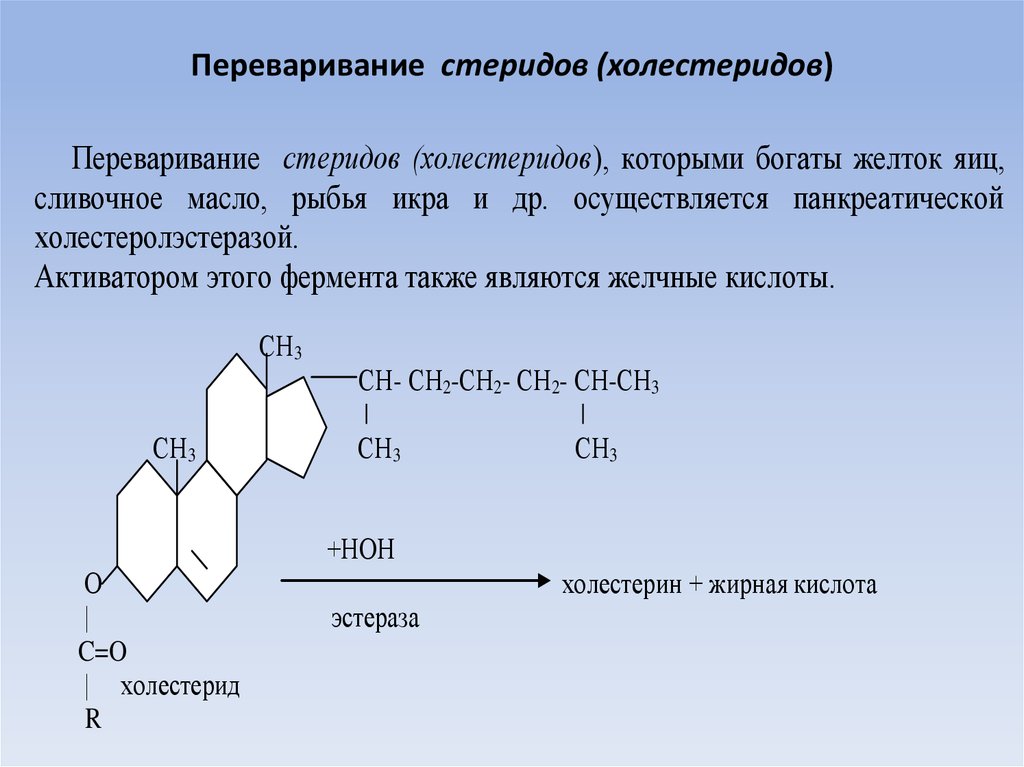
20. Переваривание стеридов (холестеридов)
Переваривание стеридов (холестеридов), которыми богаты желток яиц,сливочное масло, рыбья икра и др. осуществляется панкреатической
холестеролэстеразой.
Активатором этого фермента также являются желчные кислоты.
СН3
СН3
СН- СН2-СН2- СН2- СН-СН3
|
|
СН3
СН3
+НОН
О
|
C=O
| холестерид
R
холестерин + жирная кислота
эстераза
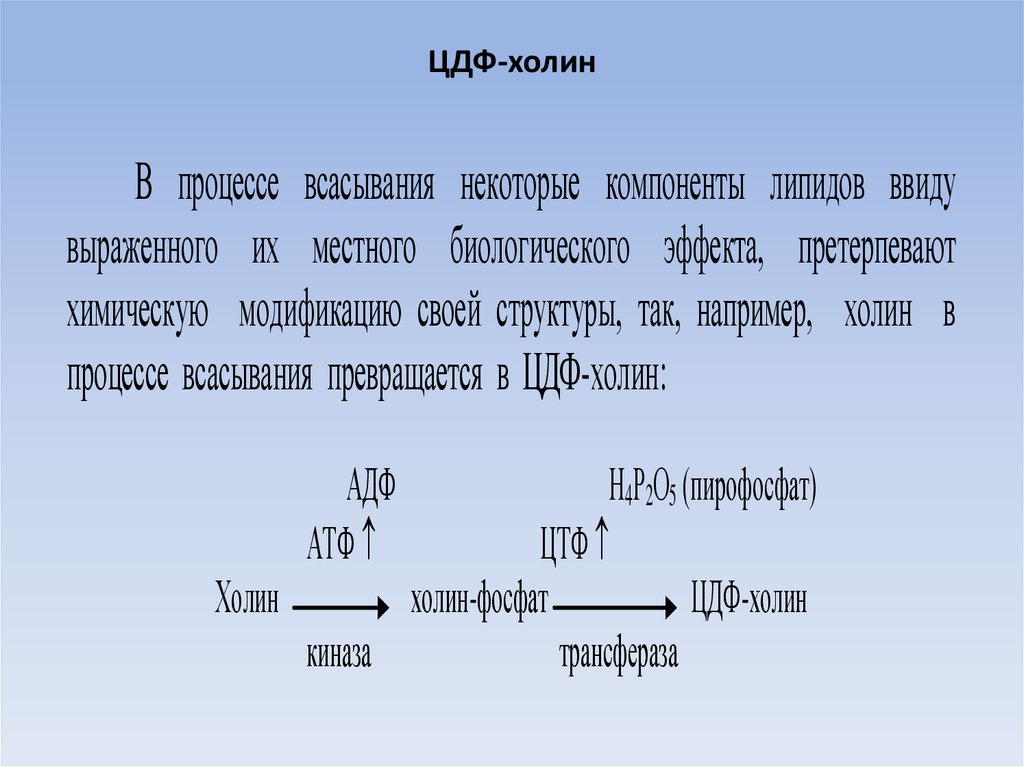
21. ЦДФ-холин
В процессе всасывания некоторые компоненты липидов ввидувыраженного их местного биологического эффекта, претерпевают
химическую модификацию своей структуры, так, например, холин в
процессе всасывания превращается в ЦДФ-холин:
Н4Р2О5 (пирофосфат)
ЦТФ
ЦДФ-холин
холин-фосфат
Холин
трансфераза
киназа
АДФ
АТФ
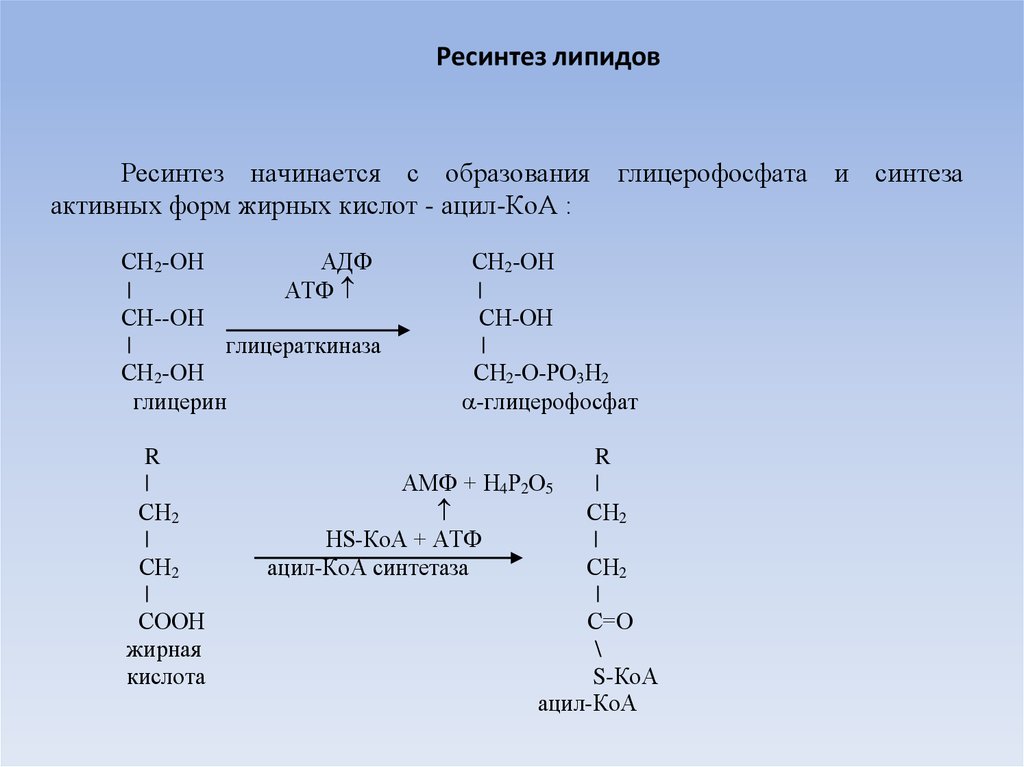
22. Ресинтез липидов
Ресинтез начинается с образования глицерофосфата и синтезаактивных форм жирных кислот - ацил-КоА :
СН2-ОН
АДФ
|
АТФ
CН--ОН
|
глицераткиназа
СН2-ОН
глицерин
R
|
СН2
|
СН2
|
СООН
жирная
кислота
СН2-ОН
|
CН-ОН
|
СН2-О-РО3Н2
-глицерофосфат
R
АМФ + Н4Р2О5
|
СН2
НS-КоА + АТФ
|
ацил-КоА синтетаза
СН2
|
С=О
\
S-КоА
ацил-КоА
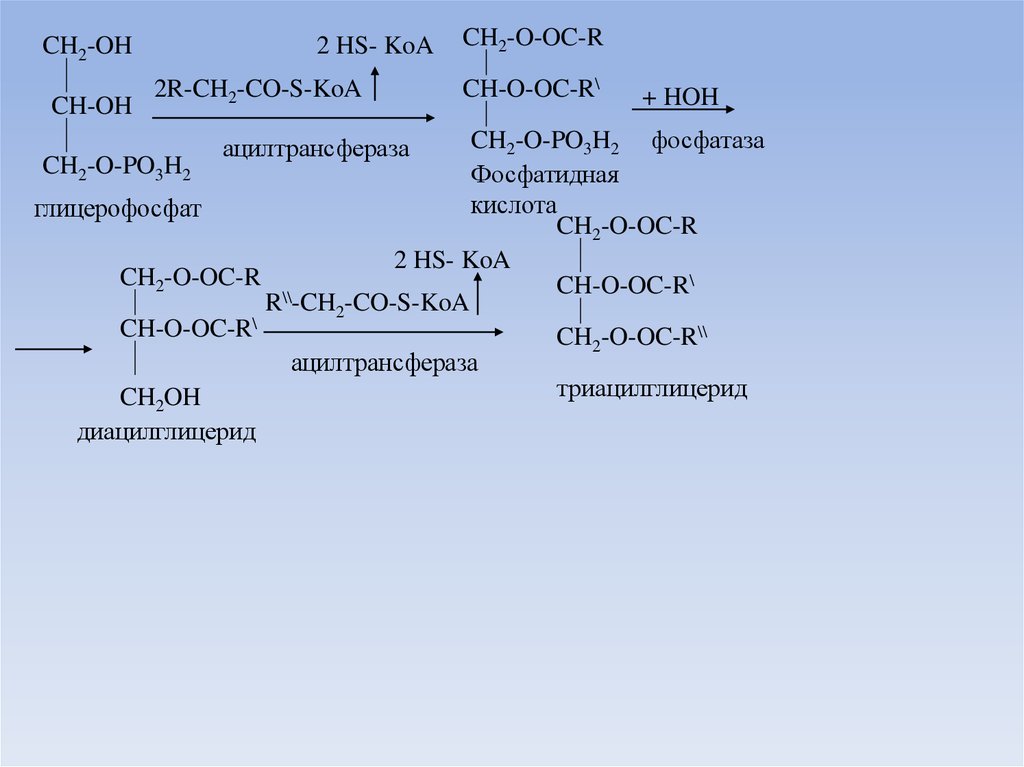
23.
CH2-OHCH-OH
2 HS- KoA
2R-CH2-CO-S-KoA
CH2-O-OC-R
CH-O-OC-R\
+ HOH
CH2-O-PO3H2 фосфатаза
CH2-O-PO3H2
Фосфатидная
кислота
глицерофосфат
CH2-O-OC-R
2 HS- KoA
CH2-O-OC-R
CH-O-OC-R\
\\
R -CH2-CO-S-KoA
\
CH-O-OC-R
CH2-O-OC-R\\
ацилтрансфераза
триацилглицерид
CH OH
ацилтрансфераза
2
диацилглицерид
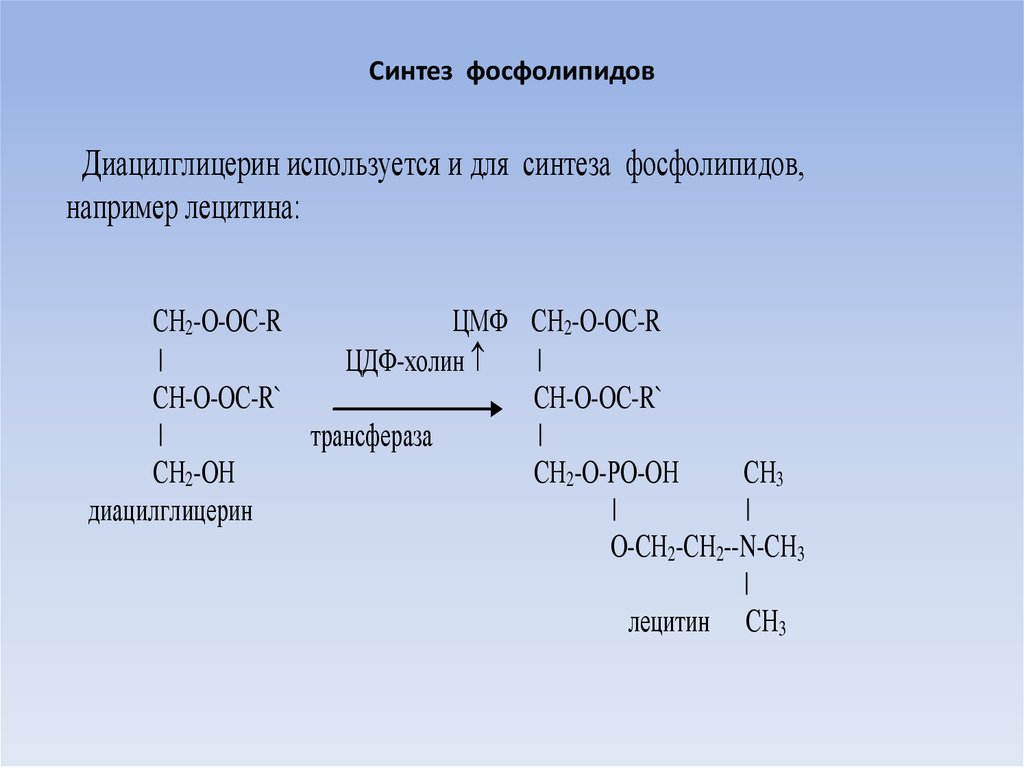
24. Синтез фосфолипидов
Диацилглицерин используется и для синтеза фосфолипидов,например лецитина:
СН2-О-ОС-R
ЦМФ
|
ЦДФ-холин
СН-О-ОС-R`
|
трансфераза
СН2-ОН
диацилглицерин
СН2-О-ОС-R
|
CН-О-ОС-R`
|
СН2-О-PО-ОН
СН3
|
|
О-СН2-СН2--N-CН3
|
лецитин СН3
25. Синтез липидов в жировой ткани (резервирование липидов)
Для синтеза триацилглицеридов в жировой ткани могут вовлекатьсяметаболиты углеводного обмена, где вместо глицерина используется
фосфодиоксиацетон, который в присутствии НАДН2 восстанавливается в
глицерофосфат:
СН2-ОН
НАД
СН2-ОН
|
НАДН2
|
C=О
CН-ОН
|
редуктаза |
СН2-О-РO3H2
СН2-О-РО3H2
фосфодиоксиацетон
-глицерофосфат
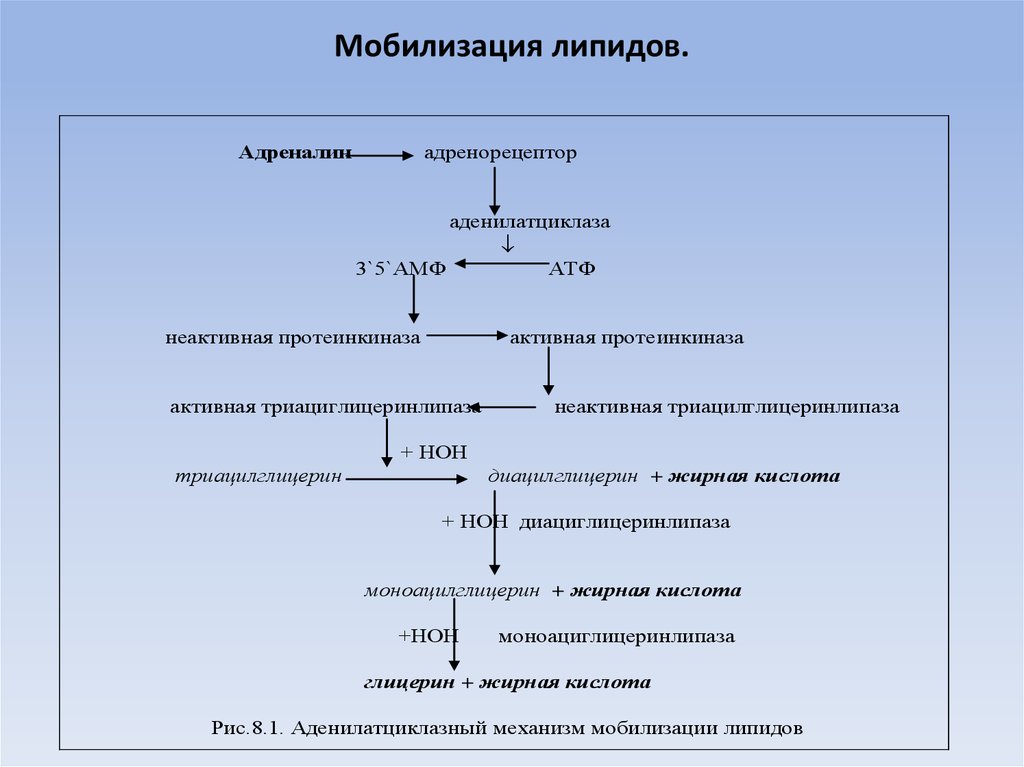
26. Мобилизация липидов.
Адреналинадренорецептор
аденилатциклаза
3`5`АМФ
АТФ
неактивная протеинкиназа
активная протеинкиназа
активная триациглицеринлипаза
неактивная триацилглицеринлипаза
+ НОН
триацилглицерин
диацилглицерин + жирная кислота
+ НОН диациглицеринлипаза
моноацилглицерин + жирная кислота
+НОН
моноациглицеринлипаза
глицерин + жирная кислота
Рис.8.1. Аденилатциклазный механизм мобилизации липидов
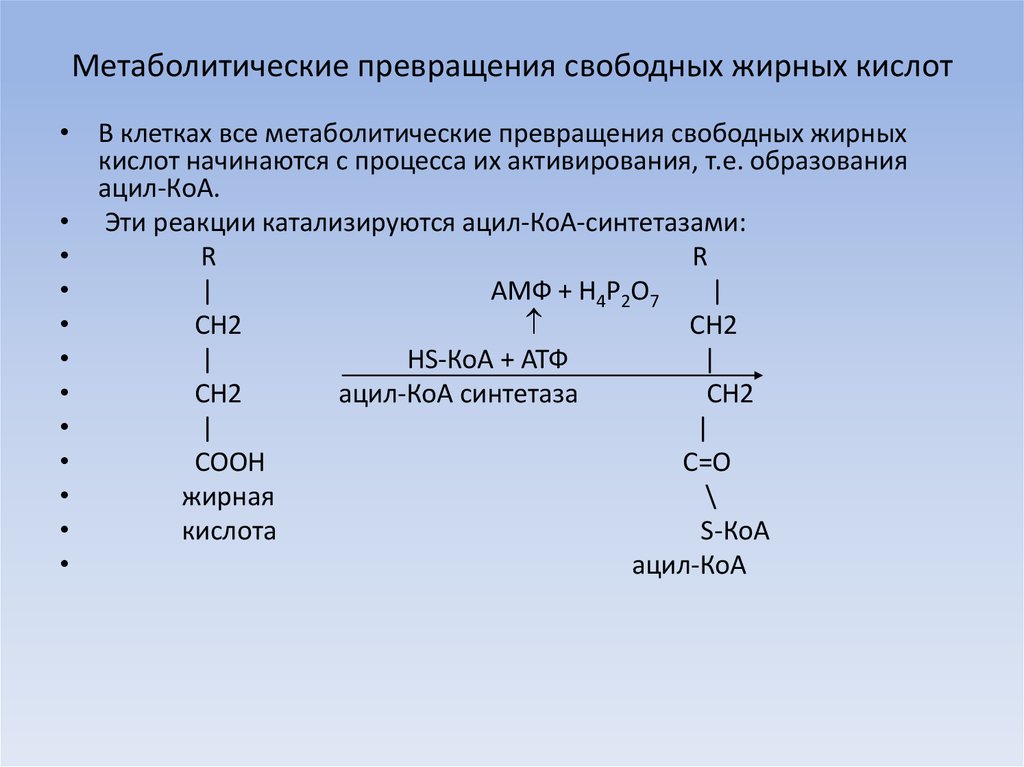
27. Метаболитические превращения свободных жирных кислот
• В клетках все метаболитические превращения свободных жирныхкислот начинаются с процесса их активирования, т.е. образования
ацил-КоА.
• Эти реакции катализируются ацил-КоА-синтетазами:
R
R
|
АМФ + Н4Р2О7
|
СН2
СН2
|
НS-КоА + АТФ
|
СН2
ацил-КоА синтетаза
СН2
|
|
СООН
С=О
жирная
\
кислота
S-КоА
ацил-КоА
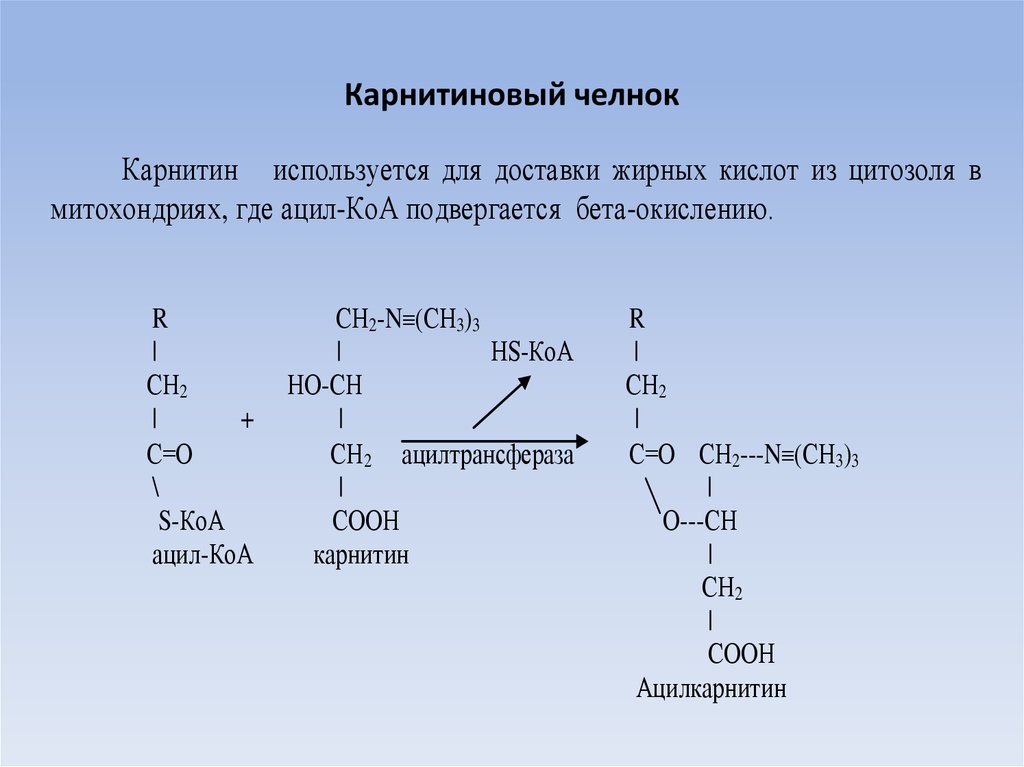
28. Карнитиновый челнок
Карнитин используется для доставки жирных кислот из цитозоля вмитохондриях, где ацил-КоА подвергается бета-окислению.
R
|
СН2
|
+
С=О
\
S-КоА
ацил-КоА
CН2-N (СН3)3
|
НS-КоА
НО-СН
|
СН2 ацилтрансфераза
|
СООН
карнитин
R
|
СН2
|
С=О CН2---N (СН3)3
|
О---СН
|
СН2
|
СООН
Ацилкарнитин
29. Бета-окисление жирных кислот
Β-окисление жирных кислот осуществляется при участии НS-КоА имультиэнзимного комплекса и завершается образованием ацетил-КоА:
НОН+2АТФ
ФАДН2---->1/2 О2
ФАД
НОН +3АТФ
R
R
R
|
|
|
НАДН2--->1/2О2
СН2
СН
+ НОН НО-С-Н
НАД
|
|
СН2
ацил-КоА дегидрогеназа
СН
гидратаза
СН2 дегидрогеназа
|
|
|
С=О
С=О
С=О
\
\
\
S-КоА
S-КоА
S-КоА
ацил-КоА (Сn)
еноил-КоА
бета-гидроксиацил-КоА
R
R
|
|
С=O
С=O
|
\
+
СН2
НS-КоА
S-КоА
|
тиолаза
ацил-КоА
С=О
(Сn-2)
\
S-КоА
бета-кетоацил-КоА (Сn)
СН3
|
С=О
\
S-КоА
ацетил-КоА
30. Далее окисляется укороченная на два углеродных атома молекула ацил-КоА
На последнем этапе образуется радикал кислоты, содержащий четыреуглеродных атома - бутирил-КоА, который окисляется с образованием двух
молекул ацетил-КоА и воды, высвобождаемая энергия аккумулируется в 5
молекулах АТФ:
НОН+2АТФ
СН3
СН3
|
ФАДН2---->1/2 О2 |
СН2 ФАД
СН
+ НОН
|
СН2
ацил-КоА
СН
гидротаза
|
дегидрогеназа
|
С=О
С=О
\
\
S-КоА
S-КоА
бутирил-КоА (С4)
СН3
|
С=O
|
СН2
|
С=О
\
S-КоА
НОН +3АТФ
НАДН2--->1/2О2
НАД
СН3
|
НО-С-Н
|
СН2
гидроксиацил-КоА
|
дегидрогеназа
С=О
\
S-КоА
кротонил-КоА
НS-КоА
тиолаза
ацетоацетил-КоА
СН3
|
С=O
\
S-КоА
+
бета-гидроксибутирил-КоА
СН3
|
С=О
\
S-КоА
ацетил-КоА
(С2)
ацетил-КоА
(С2)
31. Биоэнергетика процесса бета-окисления
• Биоэнергетика процесса бета-окисления жирных кислотскладывается из произведения числа циклов бета-окисления на
число молекул АТФ синтезируемых в каждом цикле (5АТФ):
(Сn/2 -1) 5 = Х (АТФ)
• Например, при бета-окислении стеариновой кислоты (Cn=18)
выход АТФ равен: (18/2-1)5= 40 АТФ.
• Выход энергии при полном окислении жирных кислот до
углекислого газа и воды складывается из суммы энергии
выделенной при бета-окислении (Cn/2-1)5 и энергии
высвобождаемой при окислении в цикле Кребса всех молекул
ацетил-КоА, образовавшихся при бета-окислении данной
жирной кислоты (Сn/2)12:
(Сn/2-1)5 + (Cn/2) 12 = Х АТФ
• Например, при полном окислении стеариновой кислоты (Cn=18)
выход АТФ равен:
(18/2-1) 5 + (18/2)12= 40+108 = 148 АТФ.
32. Оксиление ненасыщенных жирных кислот
• Природные ненасыщенные жирные кислоты имеютцис-конфигурацию, тогда как при окислении
насыщенных жирных кислот образующийся еноилКоА в находится в транс-конфигурации.
• В этой связи, ненасыщенные жирные кислоты до
места расположения двойной связи окисляются
как насыщенные.
• Затем под воздействием 4,3-цис-2,3-трансизомеразы двойная связь из положения 3-4
перемещается в положение 3-2 и приобретает трансформу, а далее процесс идет обычным путем.
33. Химизм окислениея ненасыщенных жирных кислот
RR
R
|
|
|
НОН +3АТФ
4 С-Н
СН2
СН2
|
|
НАДН2--->1/2О2
3 С-Н
С-Н НОН НО-С-Н НАД
|
изомераза
|
2 СН2
Н-С гидратаза
СН2 гидроксиацил-КоА
|
|
|
дегидрогеназа
1 С=О
С=О
С=О
\
\
\
S-КоА
S-КоА
S-КоА
3,4 цис-еноил-КоА 3,2 транс-еноил-КоА бета-гидроксиацил-КоА
…. и т.д.
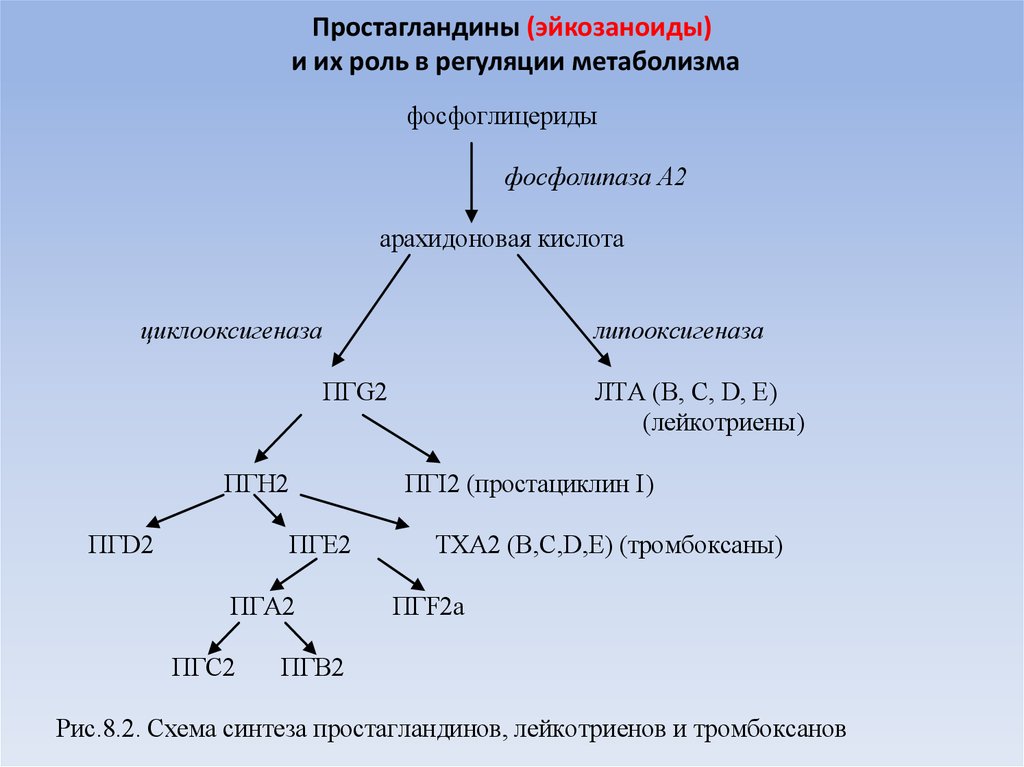
34. Простагландины (эйкозаноиды) и их роль в регуляции метаболизма
фосфоглицеридыфосфолипаза А2
арахидоновая кислота
циклооксигеназа
липооксигеназа
ПГG2
ПГН2
ПГD2
ПГI2 (простациклин I)
ПГЕ2
ПГА2
ПГС2
ЛТА (В, С, D, Е)
(лейкотриены)
ТХА2 (В,С,D,Е) (тромбоксаны)
ПГF2a
ПГВ2
Рис.8.2. Схема синтеза простагландинов, лейкотриенов и тромбоксанов
35. Синтез простагландинов
Синтез простагландинов
Арахидоновая кислота как источник простагландинов
подвергается действию фермента циклооксигеназы,
входящей в состав полиферментного комплекса простагландинсинтетазы.
Циклооксигеназа катализирует этот процесс только в
присутствии кислорода.
В результате образуются биологически активные
промежуточные продукты - эндопероксиды
простагландинов, называемые также простагландины
G2 и Н2 (ПГG2, ПГН2 ).
В стенке сосудов из эндопероксида типа ПГG2
синтезируется простациклин I (ПГI2) - сильнейший
природный ингибитор агрегации тромбоцитов.
36.
• В большинстве тканей из ПГН2 синтезируютсяпростагландины типа ПГЕ2, ПГF2a, ПГА2, ПГD2 и
тромбоксаны. При изомеризации двойной
связи в циклопентановом кольце ПГА2
образуются ПГС2 и ПГВ2.
• В лейкоцитах метаболизм арахидоновой
кислоты идет по иному пути.
• С участием фермента липооксигеназы она
превращается в нециклические ненасыщенные
производные, которые получили название
лейкотриенов (ЛТ) типа А,В,С,D,Е (ЛТА, ЛТВ,
ЛТС, ЛТD, ЛТЕ).
37. Биологическое действие простагландинов
• Повышая уровень цАМФ в эндокринных железах,простагландины стимулируют образование и
секрецию гормонов (стероидных горомонов,
иодтиронинов, инсулина, катехоламинов),
• в жировой ткани простагландины снижают уровень
цАМФ и тормозят липолиз подобно инсулину.
• ПГF2а регулируют сокращение гладкой мускулатуры
мышц матки, бронхов и кишечника, действуя через
цГМФ и ионы Са.
• ПГD2, ПГG2, ПГН2, ТХА2 и лейкотриены (ЛТ) вызывают
сокращение бронхов, ПГЕ - их расслабление.
• ПГF2a и тромбоксан А2 сужают кровеносные сосуды и
повышают артериальное давление,
38.
• Простациклины (ПГI2) и ПГЕ2 вызываютсосудорасширяющий эффект и падение давления,
увеличивают мочевыведение и выведение с мочей
натрия.
• Простагландины и особенно ПГF2a, усиливают
сокращение матки, маточных труб и вызывают
рассасывание желтого тела, тем самым, облегчая
прерывание беременности, оказывают
родостимулирующее действие.
• В этой связи простагландин ПГFa2 (динопрост,
энзопрост F) используют в акушерстве для прерывания
беременности и как родостимулирующее средство.
• ПГЕ тормозят секрецию желудочного сока, а ПГF2a - ее
усиливают.
39. Биологические эффекты простагландинов
• Аллергическая и анафилактическая реакции организмасвязаны с ускоренным образованием в легочной
ткани простагландинов (ПГG2, ПГН2) и тромбоксанов
(ТХА2) и смеси лейкотриенов (ЛТ).
• Аспирин, индометацин, диклофенак и др., ингибируя
циклооксигеназу, препятствуют синтезу
простагландинов.
• Глюкокортикоиды, блокируя фосфолипазу А2, снижают
образование простагландинов и оказывают
противовоспалительный эффект.
• Простагландин Е2 препятствует развитию язв желудка и
кишечника . Поэтому препараты (особенно
глюкокортикоиды, аспирин) подавляющие биосинтез
простагландинов, могут вызвать образование язв и
желудочно-кишечные кровотечения.
40.
• Простагландин Е2 (динопростон, простин Е2)применяют для купирования приступов спазма
бронхов, гипертонии и язвенной болезни.
• Простациклин (ПГI2), напротив, является сильнейшим
природным ингибитором агрегации тромобоцитов и
антитромообразующим веществом.
• Тромбоксан А2 способствует образованию тромбов в
сосудах, так как вызывает слипание и агрегацию
тромбоцитов.
• Антитромбический эффект аспирина и индометацина
объясняется тем, что они тормозят образование
тромбоксана и препятствуют агрегации тромбоцитов.
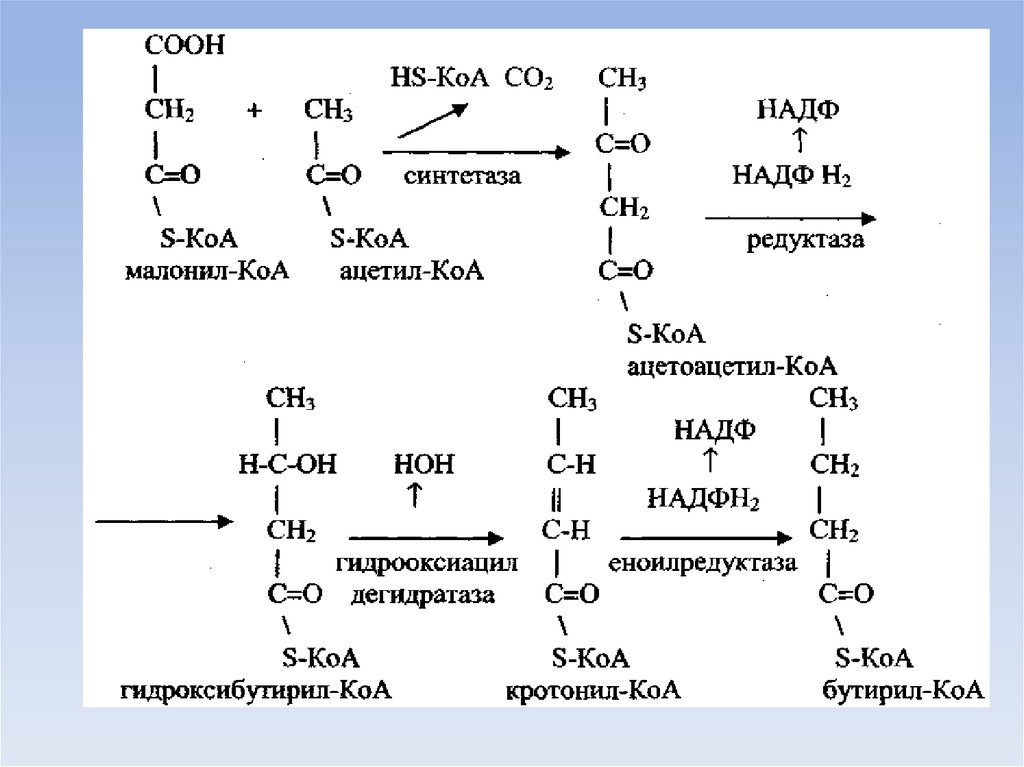
41. Биосинтез жирных кислот
• Источником для синтеза жирных кислот служитмалонил-КоА, образующийся из ацетил-КоА.
• Ацетил-КоА доставляется к месту синтеза жирных
кислот из митохондрий, где он образуется при бетаокислении жирных кислот.
• Доставка ацетил-КоА из митохондрий в цитозоль
осуществляется либо карнитиновым челночным
механизмом, либо с помощью цитрата.
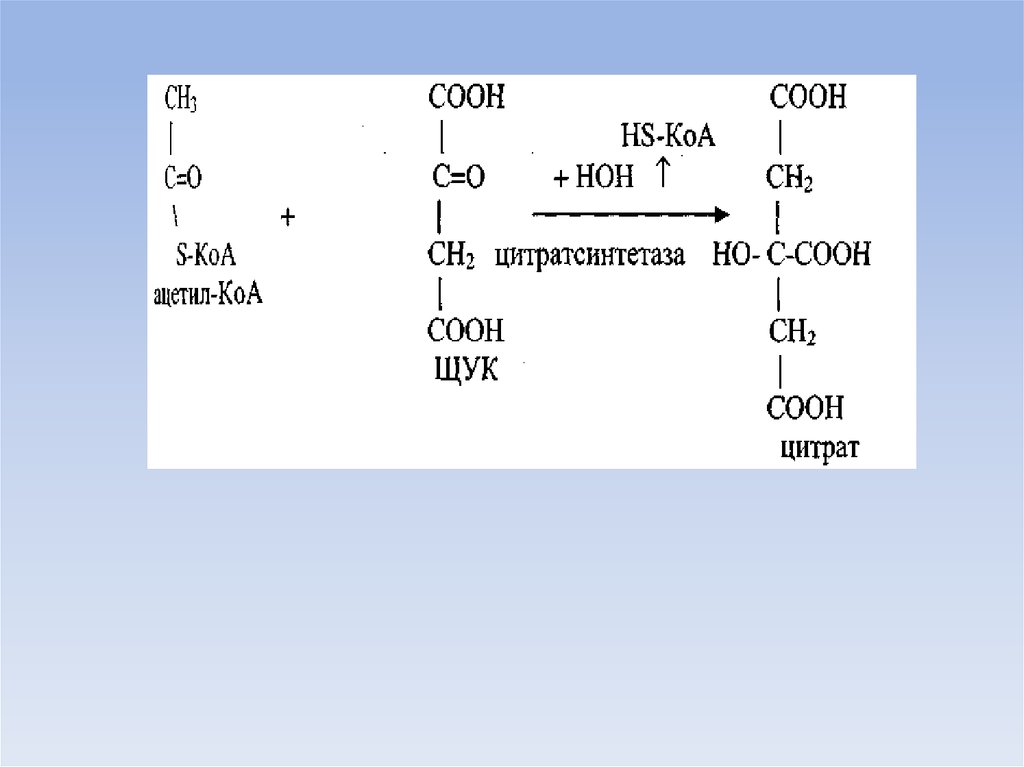
• В митохондриях из ацетил-КоА и щавелево-уксусной
кислоты (ЩУК) синтезируется цитрат, который при
участии специфической транслоказы
митохондриальной мембраны доставляется в цитозоль.
42.
43. Синтез малонил КоА
В цитозоле цитрат под воздействием цитозольной цитратлиазыразрушается и вновь образуется ацетил-КоА.
Далее, при участии биотин-содержащего фермента (ацетил-КоА карбоксилаза) в эндоплазматическом ретикулуме из ацетил-КоА и угольной
кислоты синтезируется малонил-КоА:
CООН
СН3
|
|
( Mg ++ )
СН2
С=О + Н2СО3 + АТФ
|
+ АДФ + Н3РО4
\
биотин-фермент С=О
S-КоА
|
ацетил-КоА
S-КоА
малонил-КоА
44.
45.
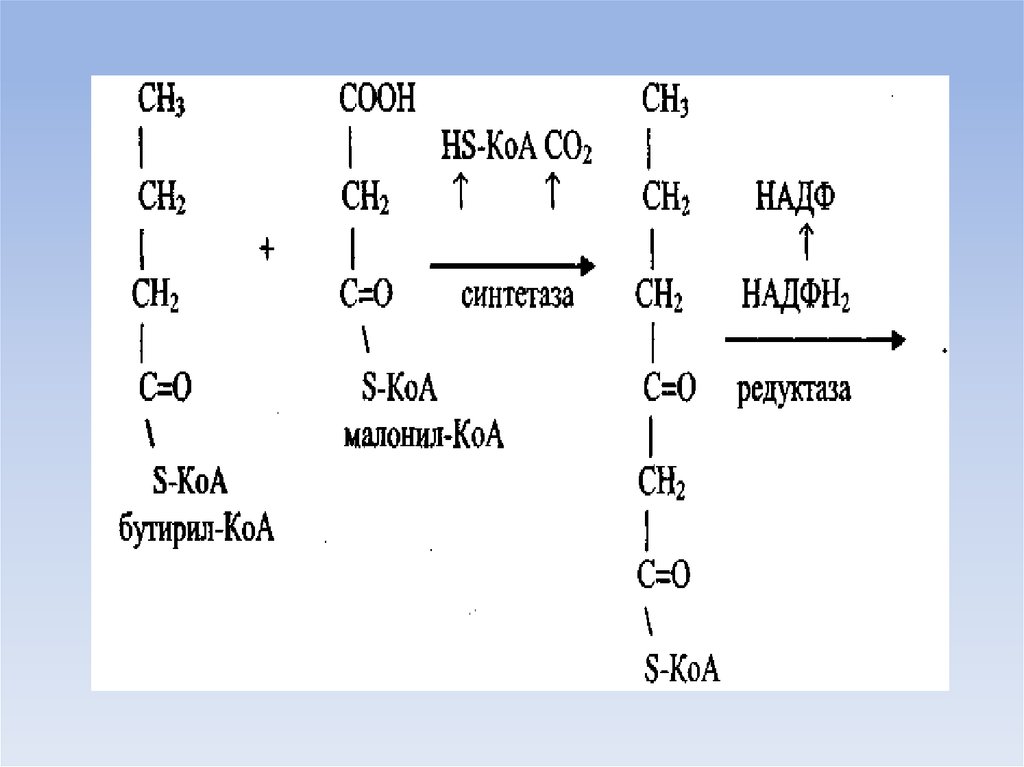
46. Синтез пальмитиновой кислоты
• Для синтеза пальмитиновой кислоты нужно семьтаких циклов, соответственно требуется семь
остатков малонила и один ацетил.
• Синтезированная пальмитиновая кислота
соединяется с КоА и образуется пальмитоил-КоА.
• Синтез жирных кислот с числом углеродных
атомов больше чем у пальмитиновой кислоты
может идти в митохондриях и в цитозоле.
• В митохондриях для этих целей к пальмитоил-КоА
присоединяется ацетил-КоА при участии
соответствующих ферментов, а в цитозоле
используется малонил-КоА.
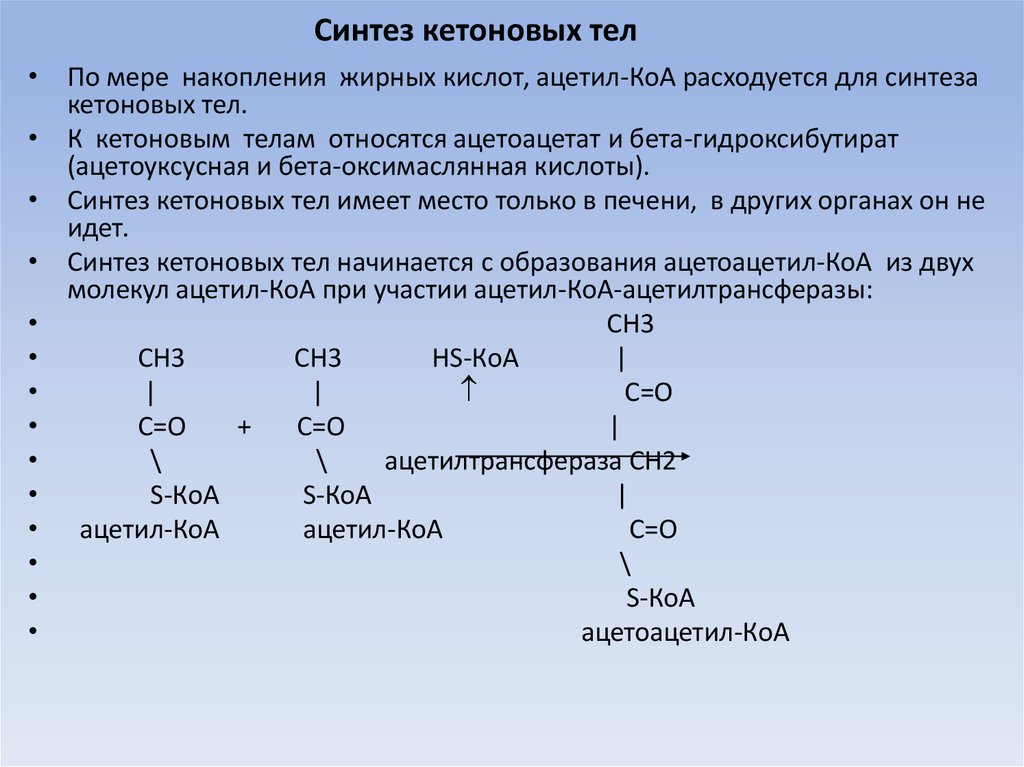
47. Синтез кетоновых тел
• По мере накопления жирных кислот, ацетил-КоА расходуется для синтезакетоновых тел.
• К кетоновым телам относятся ацетоацетат и бета-гидроксибутират
(ацетоуксусная и бета-оксимаслянная кислоты).
• Синтез кетоновых тел имеет место только в печени, в других органах он не
идет.
• Синтез кетоновых тел начинается с образования ацетоацетил-КоА из двух
молекул ацетил-КоА при участии ацетил-КоА-ацетилтрансферазы:
СН3
СН3
СН3
НS-КоА
|
|
|
С=О
С=О
+
С=О
|
\
\
ацетилтрансфераза СН2
S-КоА
S-КоА
|
• ацетил-КоА
ацетил-КоА
С=О
\
S-КоА
ацетоацетил-КоА
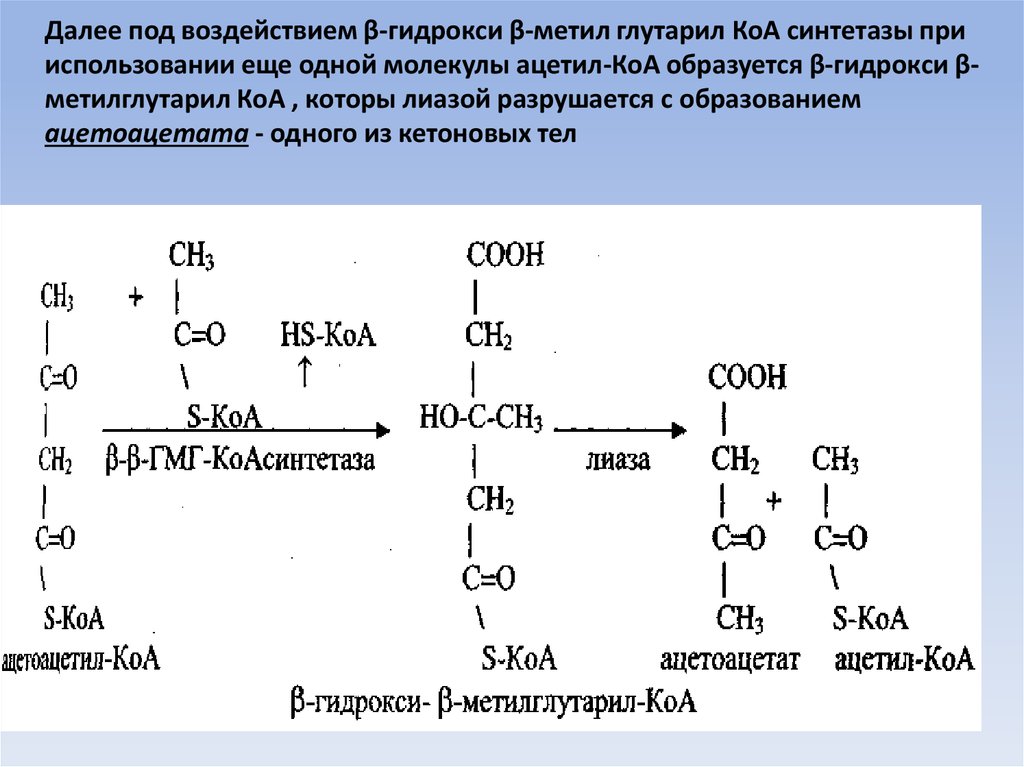
48. Далее под воздействием β-гидрокси β-метил глутарил КоА синтетазы при использовании еще одной молекулы ацетил-КоА образуется
β-гидрокси βметилглутарил КоА , которы лиазой разрушается с образованиемацетоацетата - одного из кетоновых тел
49. Восстановление ацетоацетата приводит к образованию второго кетоноого тела β-гидроксибутирата. В случае избытка ацетоацетата в
тканях возможно спонтанное декарбоксилирование ацетоацета иобразование ацетона
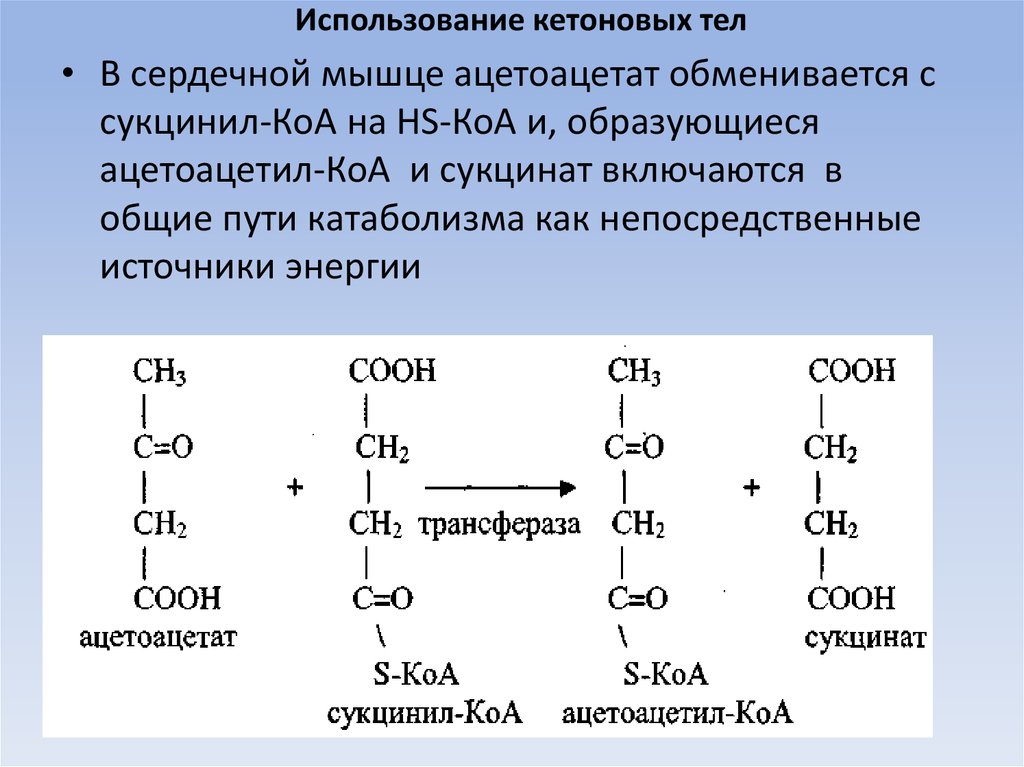
50. Использование кетоновых тел
• В сердечной мышце ацетоацетат обменивается ссукцинил-КоА на НS-КоА и, образующиеся
ацетоацетил-КоА и сукцинат включаются в
общие пути катаболизма как непосредственные
источники энергии
51. В норме в крови уровень кетоновых тел 0,1-0,6 ммоль/л.
• Повышение их уровня (гиперкетонемия)наблюдается при сахарном диабете и при
длительном голодании (2 и 3 фазы голода),
когда имеет место усиленный процесс
окисления жирных кислот.
• Появление кетоновых тел в моче называется
кетонурия. Глубокая кетонемия приводят к
метаболическому ацидозу.
52. Тема №7: Обмен липидов. Цель: Дать представление о катаболических и анаболических путях превращение липоидов и их биологической
роли• Основные вопросы лекции:
• 1.Обмен стероидов. Представление о биосинтезе холестерина,
регуляция этого процесса. Включение холестерина в ЛПОНП.
• 2.Синтез желчных кислот. Выведение холестерина и желчных
кислот из организма.
• 3.Гиперхолестеринемия, причины ее возникновения.
Внутрисосудистый липолиз.
• 4.Биохимия атеросклероза. Механизм развития желчнокаменной
болезни.
• 5.Представление о биосинтезе и катаболизме фосфолипидов и
гликолипидов.
• 6.Понятие о сфинголипидозах.
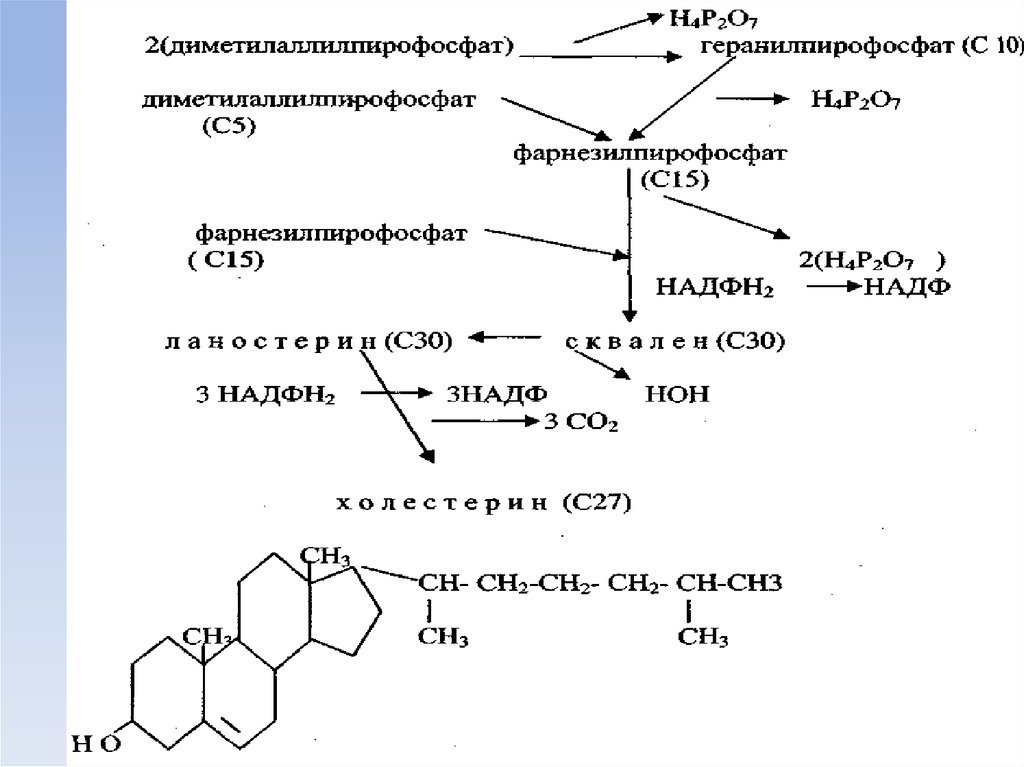
53. Биосинтез холестерина
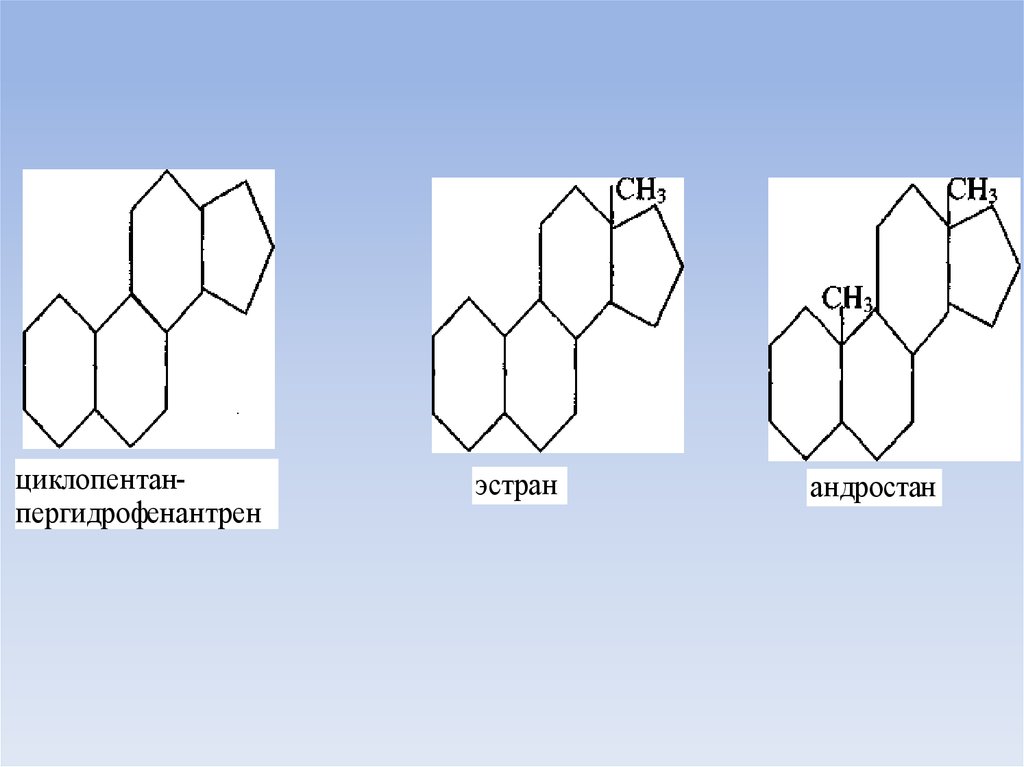
• К стероидам относятся углеводороды производные циклопентанпергидро-фенантрена, метилированные в положении 13 (эстран)или в положениях 10 и 13 (андростан)
• Многие стероиды имеют в положении 17 боковую цепь.
• По строению этой боковой цепи различают четыре группы
стероидов:
• - стерины (холестерин) - восьмиуглеродная боковая цепь,
• - желчные кислоты - пятиуглеродная боковая цепь,
• - кортикостероиды и прогестерон - двууглеродная цепь,
• - эстрогены и андрогены - в положении 17 цепи нет
54.
циклопентанпергидрофенантренэстран
андростан
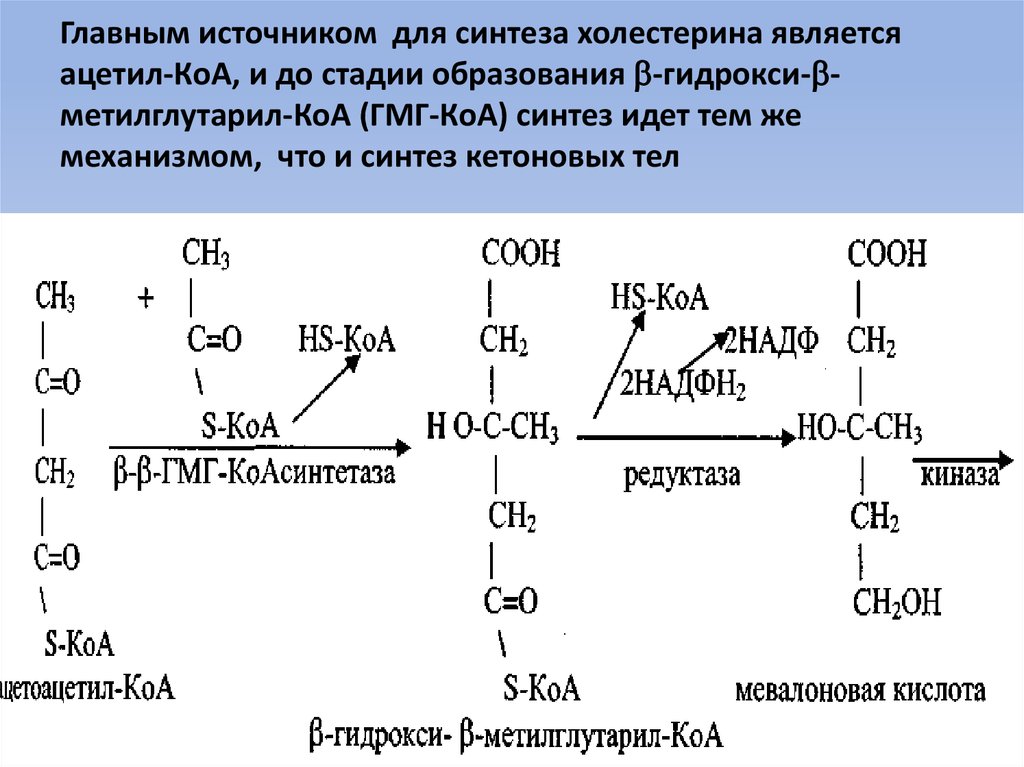
55. Главным источником для синтеза холестерина является ацетил-КоА, и до стадии образования -гидрокси--метилглутарил-КоА
Главным источником для синтеза холестерина являетсяацетил-КоА, и до стадии образования -гидрокси- метилглутарил-КоА (ГМГ-КоА) синтез идет тем же
механизмом, что и синтез кетоновых тел
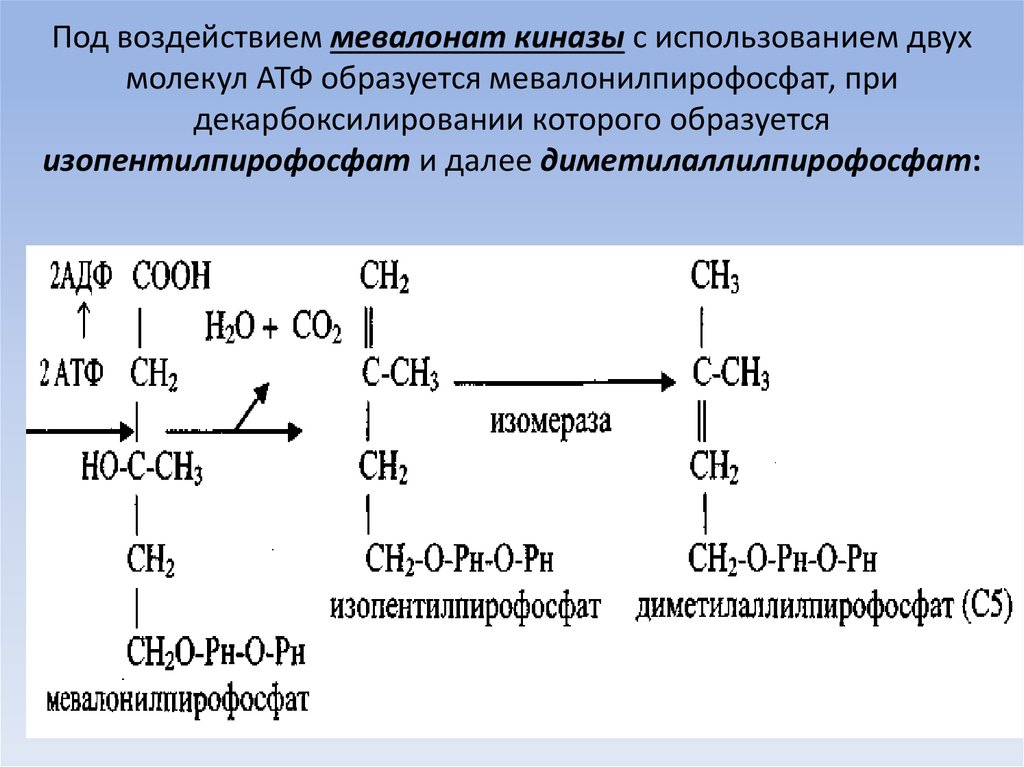
56. Под воздействием мевалонат киназы с использованием двух молекул АТФ образуется мевалонилпирофосфат, при декарбоксилировании
которого образуетсяизопентилпирофосфат и далее диметилаллилпирофосфат:
57.
58. Синтез фосфолипидов и гликолипидов
• Для синтеза фосфолипидов и гликолипидов- главных структурных компонентов
мембран клетки, кроме типичных
компонентов липидов (глицерофосфат и
жирные кислоты) необходимы сфингозин,
холин или коламин, сиаловые кислоты и
другие производные углеводы
Коламин и холин синтезируются из
аминокислоты серин.
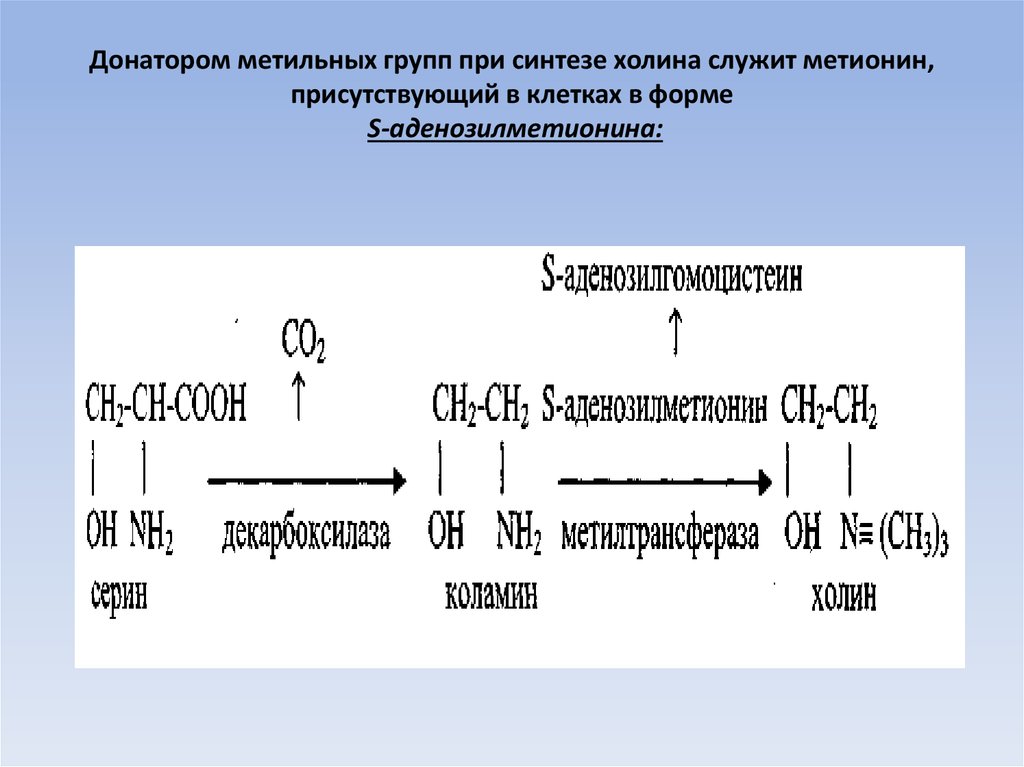
59. Донатором метильных групп при синтезе холина служит метионин, присутствующий в клетках в форме S-аденозилметионина:
60. Коламин под воздействием коламин фосфокиназы активируется образуя коламин фосфат
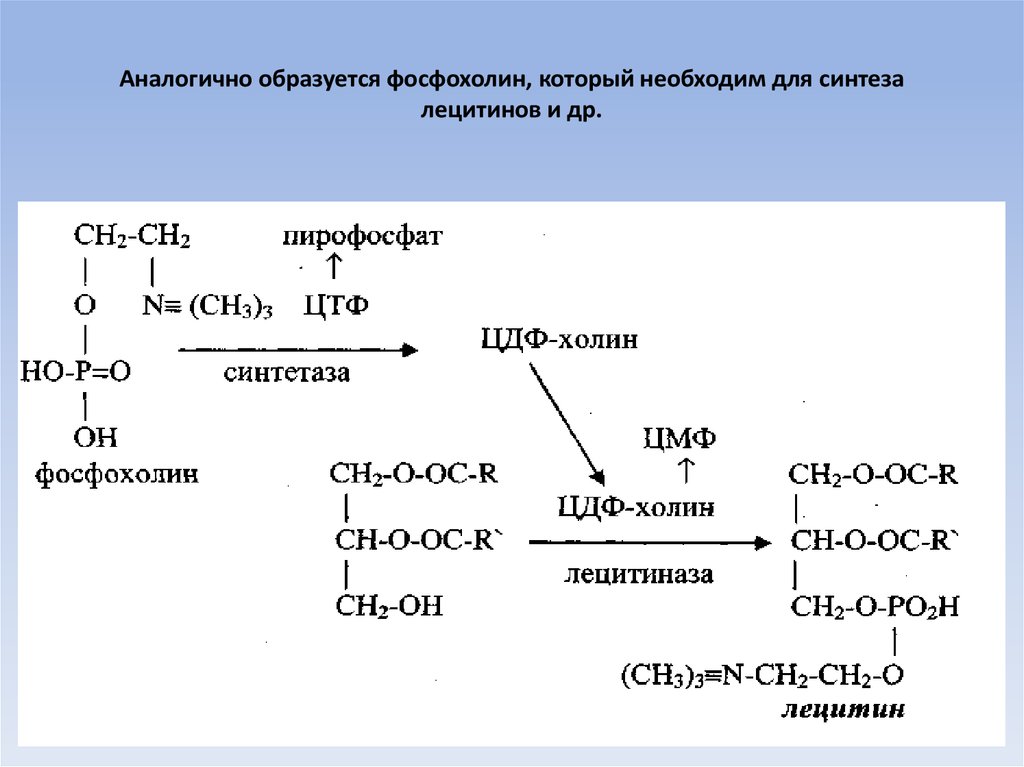
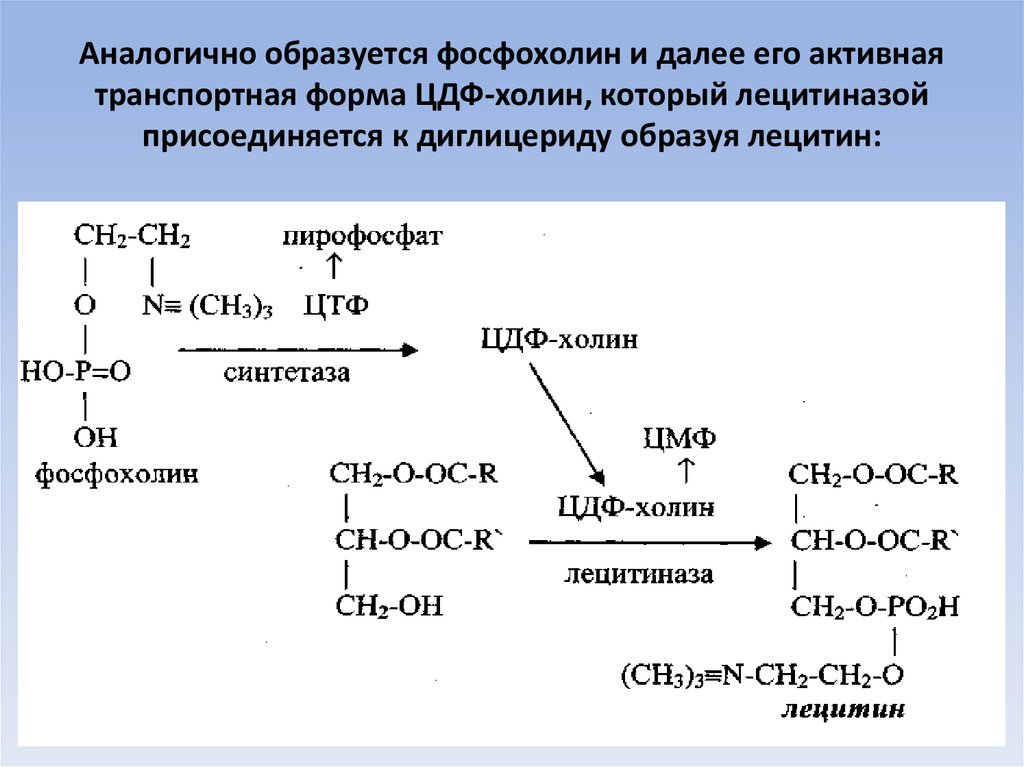
61. Аналогично образуется фосфохолин, который необходим для синтеза лецитинов и др.
62. Аналогично образуется фосфохолин и далее его активная транспортная форма ЦДФ-холин, который лецитиназой присоединяется к
диглицериду образуя лецитин:63. Синтез гликолипидов
• Синтез гликолипидов идет на мембранахэндоплазматического ретикулума,
• Образовавшиеся гликолипиды размещаются на
поверхности мембраны, выстилающей цистерны
эндоплазматического ретикулума.
• Отсюда они транспортируются в аппарат Гольджи и,
включаясь в состав наружной поверхности
плазматическиой мембраны, выходят из клетки.
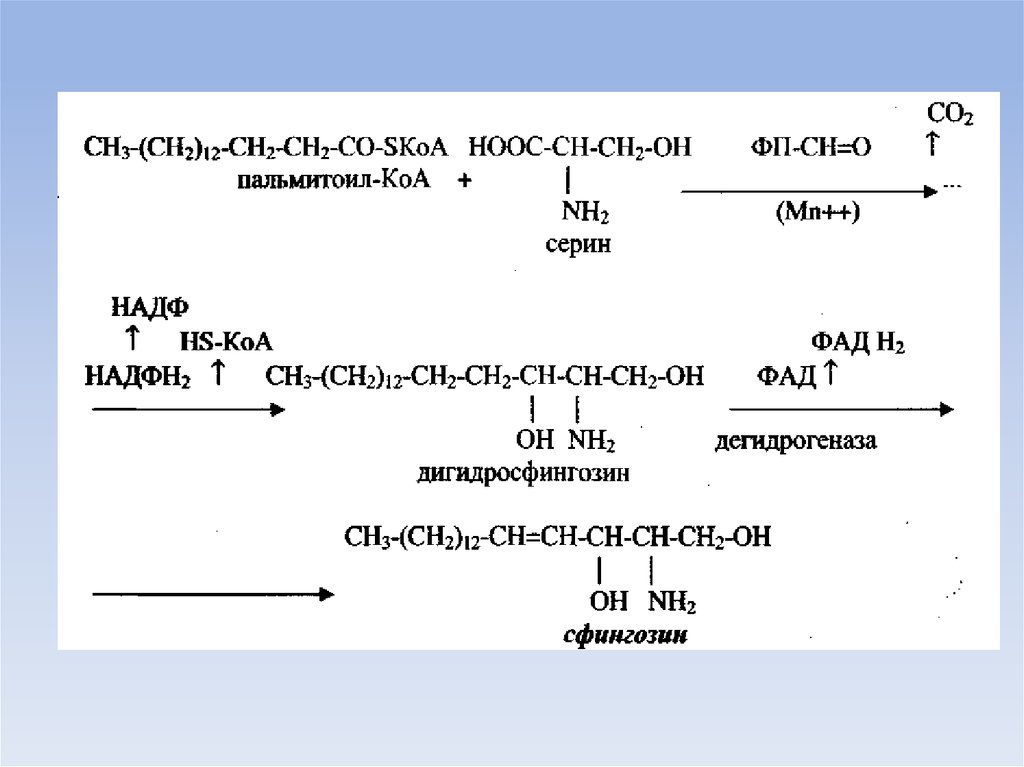
• Синтез сфингозина, главного структурного компонента
сфингофосфатидов и гликолипидов, также в основном
идет в печени.
• Источником служит аминокислота серин и пальмитоилКоА
64.
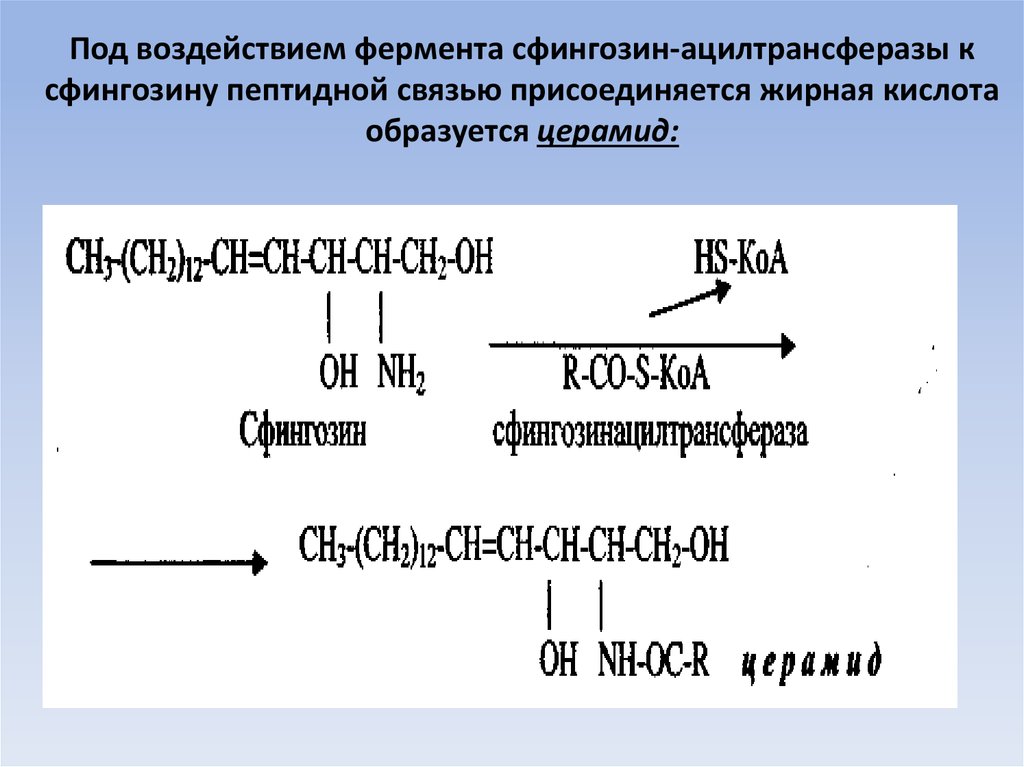
65. Под воздействием фермента сфингозин-ацилтрансферазы к сфингозину пептидной связью присоединяется жирная кислота образуется
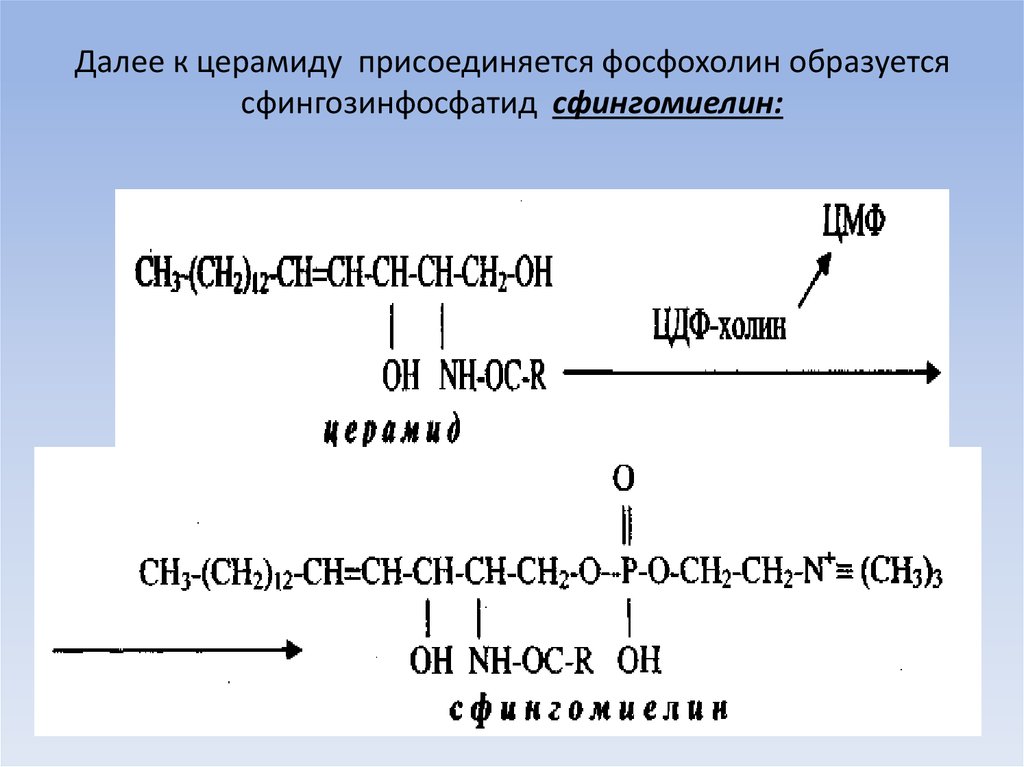
церамид:66. Далее к церамиду присоединяется фосфохолин образуется сфингозинфосфатид сфингомиелин:
67. Синтез гликолипидов
• Синтез гликолипидов также происходит сиспользованием церамидов.
• При синтезе цереброзидов к церамиду
присоединяются гликозидной связью
моносахариды (глюкоза или галактоза)
доставляемые в виде УДФ-глюкозы или УДФгалатозы:
• церамид + УДФ-глюкоза
цереброзид + УДФ
68. Цереброзиды могут синтезироваться по альтернативаному пути.
• Вначале образуется производное сфингозина игалактозы называемое психозин:
сфингозин + УДФ-галактоза
психозин + УДФ
• Затем психозин ацетилируется какой-либо
жирной кислотой и образуется цереброзид:
психозин + R-СО-S-КоА
цереброзид + НS-КоА
69. Синтез ганглиозидов
• Ганглиозиды - гликолипиды мембраннейронов синтезируются либо
• из церамидов, к которым последовательно
присоединяются остатки галактозы,
глюкозы и обязательно сиаловые кислоты,
• либо - из психозина.
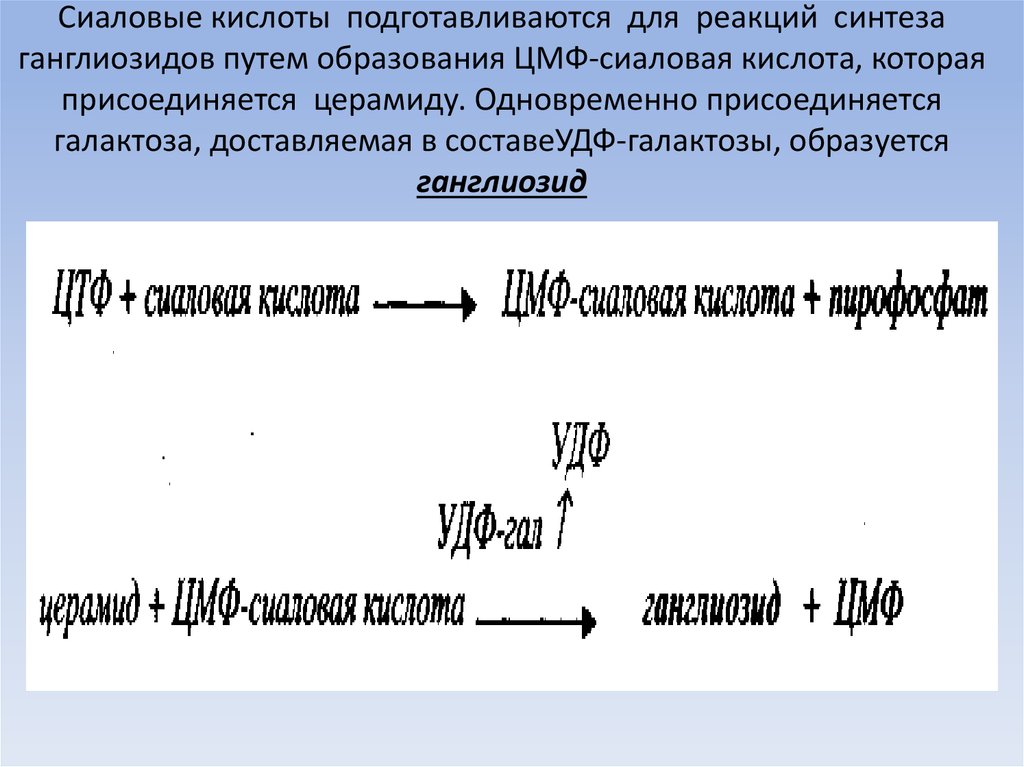
70. Сиаловые кислоты подготавливаются для реакций синтеза ганглиозидов путем образования ЦМФ-сиаловая кислота, которая
присоединяется церамиду. Одновременно присоединяетсягалактоза, доставляемая в составеУДФ-галактозы, образуется
ганглиозид
71. Катаболизм гликолипидов - сфинголипидозы
• Катаболизм гликолипидов обеспечивается группой специфическихферментов находящихся в лизосомах. Это сфингомиелиназа, бетаглюктозидаза, бета-галактозилгидролаза, альфа-галактозидаза,
гексозамидиназа А и В и другие.
• Существует около десятка специфических лизосомных болезней
накопления - сфинголипидозов (гликолипидозов).
• Одним из сфинголипидозов является болень Гоше (Gaucher),
наследуемая по аутосомно-рецессивному типу.
• При этом заболевании происходит накопление в клетках печени
селезенки, легких и др. глюкозилцерамида (цереброзида) вследствие
повреждения фермента бета-глюкозидазы, разрушающего этот
гликолипид на глюкозу и церамид.
• Это приводит к увеличению печени и селезенки в 4-5 раз по сравнении с
нормой. Развивается анемия, задерживается умственное развитие,
нередки явления геморрагического диатеза, остеопороз.
• В связи с инфильтрацией легких клетками Гоше появляются признаки
дыхательной недостаточности. Рентгенологические изменения в легких
напоминают милиарный туберкулез. Прогноз не благоприятен.
72. Гликолипидозы
• При болезни Фабри (Fabri) имеет место дефект сцепленного с Ххромосомой гена, транскрибирующего синтез фермента альфагалактозидазы. В результате в тканях накапливается тригликозилцерамид.Клиника болезни Фабри напоминает болезнь Гоше.
• Сфинголипидоз Тей-Сакса (амавротический идиотизм, болезнь Tay-Sachs).
Это заболевание сопровождается перерождением сетчатой субстанции
мозга, демиелинизацией нервных волокон, слепотой, слабоумием,
параличом. Заболевание связано с отсутствием фермента
гексозамидиназы А, обеспечивающий катаболизм ганглиозидов типа
GМ2, которые накапливаются в первую очередь в ганглиях и глиальных
клетках мозга.
• При болезни Нимана-Пика (Niemann-Hick) вследствие отсутствия
фермента сфингомиелиназы, разрушающего сфингомиелины, они
накапливаются в клетках ретикулоэндотелиальной системы, в клетках
нервной ткани, что ведет к резкому отставанию ребенка в нервнопсихическом развитии, появлении глухоты и слепоты
• Терапия сфинголипидозов введением недостающих лизосомальных
ферментов может быть благоприятной, если начать лечение с очень
раннего детского возраста.








































 Химия
Химия








