Похожие презентации:
Алкадиены: строение, номенклатура, гомологи, изомерия
1.
Алкадиены:строение, номенклатура,
гомологи, изомерия
2.
Алкадиены - ациклическиеуглеводороды, содержащие в
молекуле, две двойные связи
между атомами углерода
общая формула: CnH2n-2
3. Алкадиены с кумулированным расположением двойных связей (аллены)
Углеводороды содержащие дведвойные связи ,находящиеся
возле соседних атомов углерода.
1
2
3
4
СН2 =С=СН-СН3
бутадиен -1, 2
4.
Сопряженные алкадиеныУглеводороды содержащие две
двойные связи ,между которыми
находится одна одинарная связь.
1
2
3
4
5
6
СН3 -СН=СН-СН=СН-СН3
1
гексадиен-2, 4
2
3
4
СН2 =СН-СН=СН2
бутадиен -1, 3 (дивинил)
5. Алкадиены с изолированными двойными связями
Углеводороды содержащие дведвойные связи ,между которыми
находится несколько одинарных
связей.
8
7
6
5
4
3
2
1
СН3–СН2-СН=СН-СН2-СН2-СН=СН2
октадиен-1, 5
6. Номенклатура алкадиенов
Правила:1. Главная цепь должна содержать обе
двойные связи.
2. Нумерацию ведут с того конца где
ближе кратная связь.
3. Называют заместители и указывают
атомы углерода от которого они
отходят.
4. Указывают название алкадиена и
атомы углерода от которых образована
двойная связь.
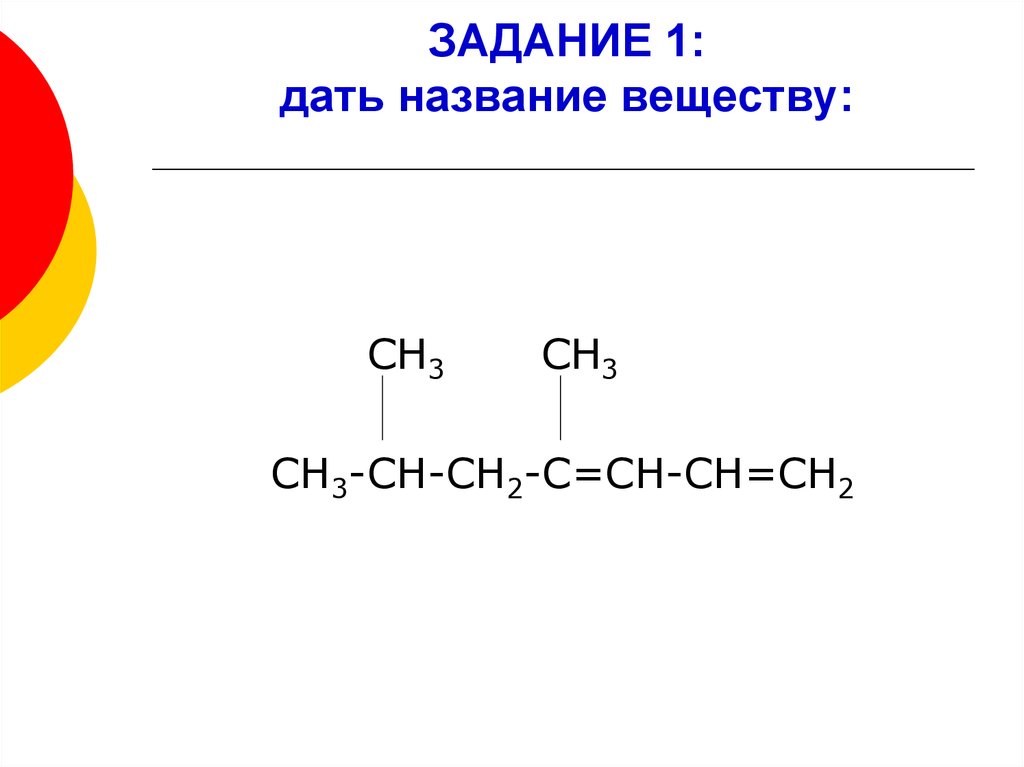
7. ЗАДАНИЕ 1: дать название веществу:
СН3СН3
СН3-СН-СН2-С=СН-СН=СН2
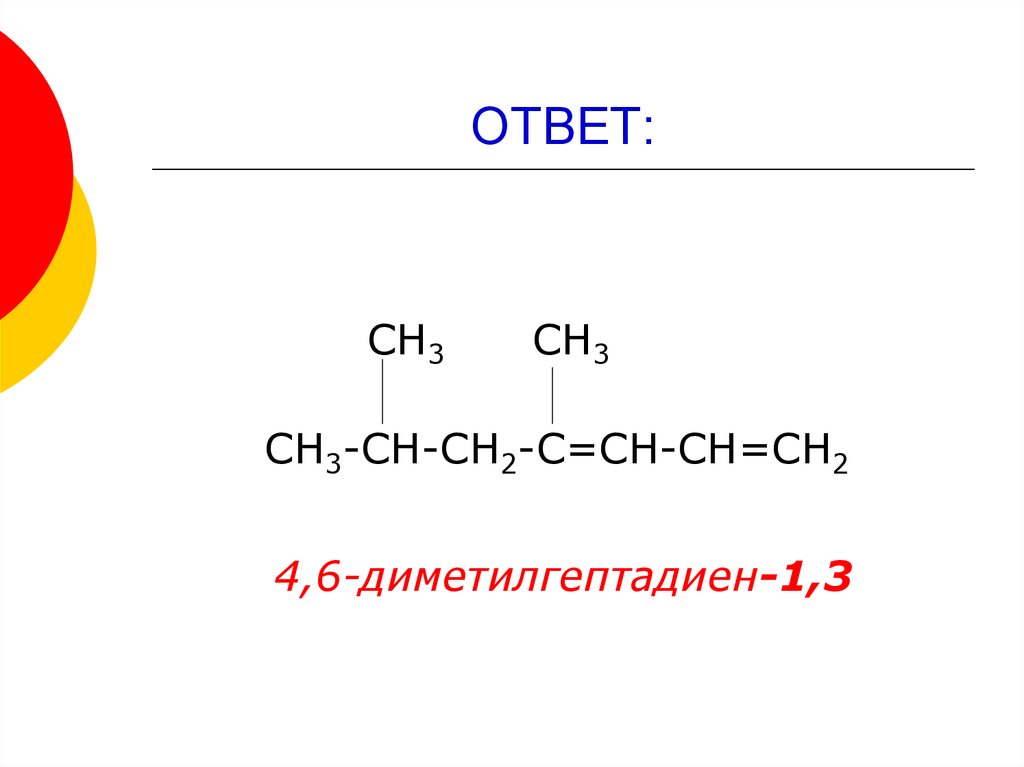
8. ОТВЕТ:
СН3СН3
СН3-СН-СН2-С=СН-СН=СН2
4,6-диметилгептадиен-1,3
9. ИЗОМЕРИЯ АЛКАДИЕНОВ
1. Структурная:а) изомерия углеродного скелета
б) изомерия положения двойных
связей.
2. Пространственная:
а)цис-транс изомерия
3. Межклассовая изомерия
(алкины)
10. ИЗОМЕРИЯ АЛКАДИЕНОВ
11. ПОЛУЧЕНИЕ АЛКАДИЕНОВ
Двухстадийное дегидрированиеалканов
СН3-СН2-СН2-СН3
бутан
СН2=СН-СН=СН2+2Н2
бутадиен -1, 3
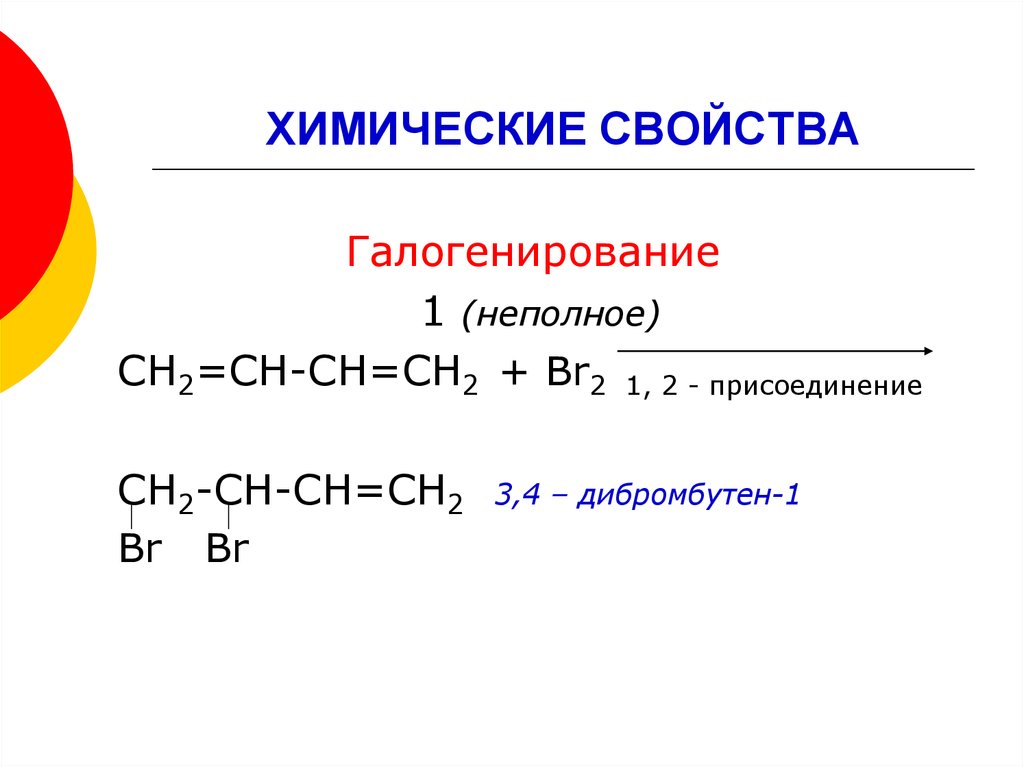
12. ХИМИЧЕСКИЕ СВОЙСТВА
Галогенирование1 (неполное)
СН2=СН-СН=СН2 + Br2 1, 2 - присоединение
СН2-СН-СН=СН2
Br Br
3,4 – дибромбутен-1
13. ХИМИЧЕСКИЕ СВОЙСТВА
Галогенирование2 (неполное)
СН2=СН-СН=СН2 + Br2 1, 4 -присоединение
СН2-СН=СН-СН2
Br
Br
1,4 – дибромбутен-2
14. ХИМИЧЕСКИЕ СВОЙСТВА
Галогенирование3 (полное)
СН2=СН-СН=СН2 + 2Br2 1,2,3,4 -присоединение
СН2-СН-СН-СН2
Br Br Br Br
1,2,3,4 – тетрабромбутан
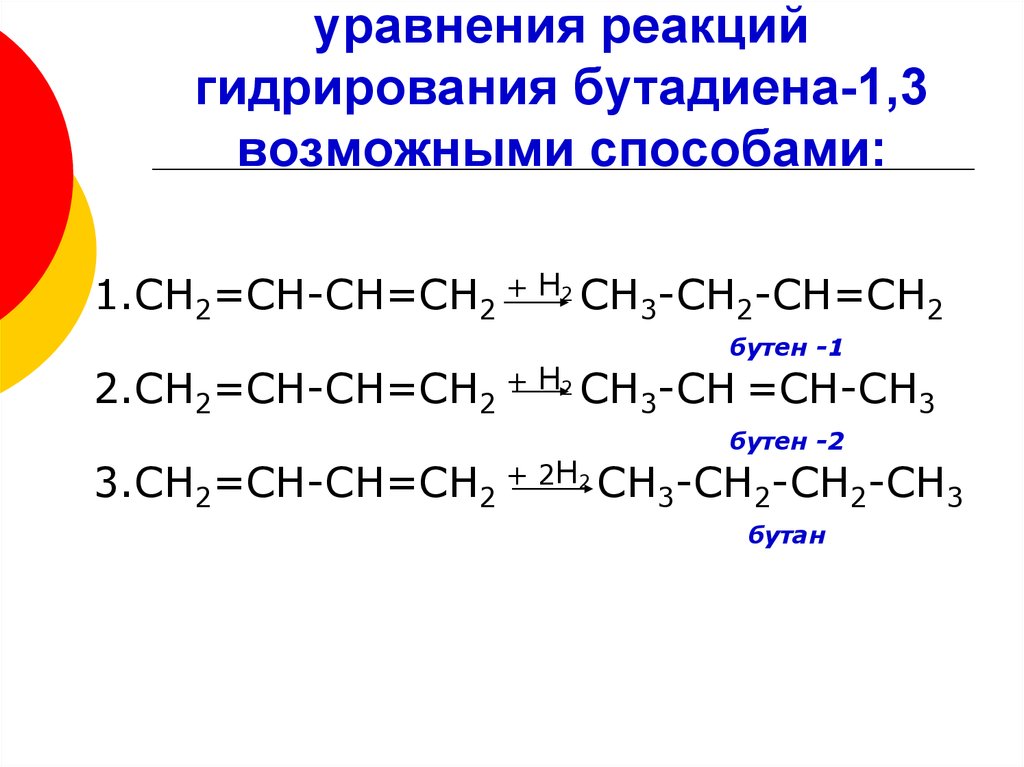
15. уравнения реакций гидрирования бутадиена-1,3 возможными способами:
1.СН2=СН-СН=СН2 + Н2 СН3-СН2-СН=СН2бутен -1
2.СН2=СН-СН=СН2 + Н2 СН3-СН =СН-СН3
бутен -2
3.СН2=СН-СН=СН2 + 2Н2 СН3-СН2-СН2-СН3
бутан
16. ХИМИЧЕСКИЕ СВОЙСТВА
Гидрогалогенирование(по правилу Марковникова)
1 стадия СН2=СН-СН=СН2 + НСI
СН3-СН-СН=СН2
СI
3-хлорбутен -1
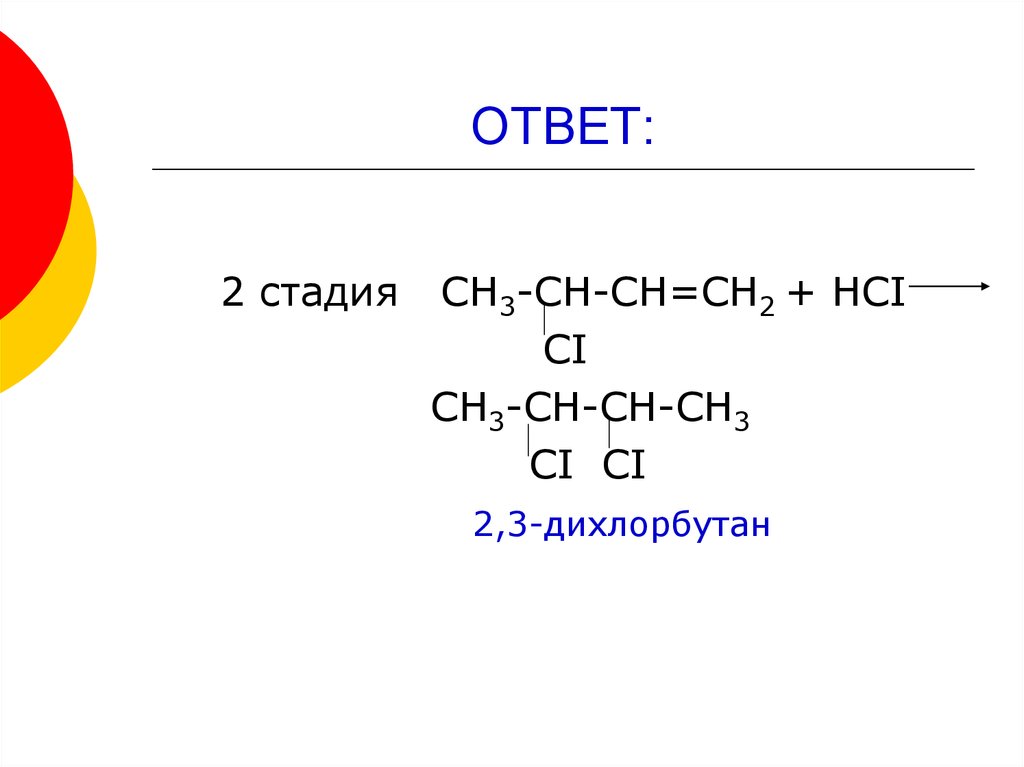
17. ОТВЕТ:
2 стадияСН3-СН-СН=СН2 + НСI
СI
СН3-СН-СН-СН3
СI СI
2,3-дихлорбутан
18. ХИМИЧЕСКИЕ СВОЙСТВА
ПолимеризацияПолимеризация диеновых УВ приводит
к образованию каучуков – полимеров,
обладающих высокой эластичностью.
бутадиен -1, 3
бутадиеновый каучук
19. История открытия каучука
Родина каучука –Центральная и Южная
Америка. Во влажных
жарких тропиках, по
берегам реки
Амазонки, растёт
необычное дерево,
которое называется
бразильская
гевея
20. История открытия каучука
Если на коре деревасделать надрез, то
из ранки вытекает
сок молочно-белого
цвета, называемый
латексом. На
воздухе сок
постепенно темнеет
и затвердевает,
превращаясь в
резиноподобную
смолу.
21. Синтетические каучуки
Основателем первого вмире
крупномасштабного
производства
синтетического
каучука по праву
считается русский
ученый
С.В.Лебедев.
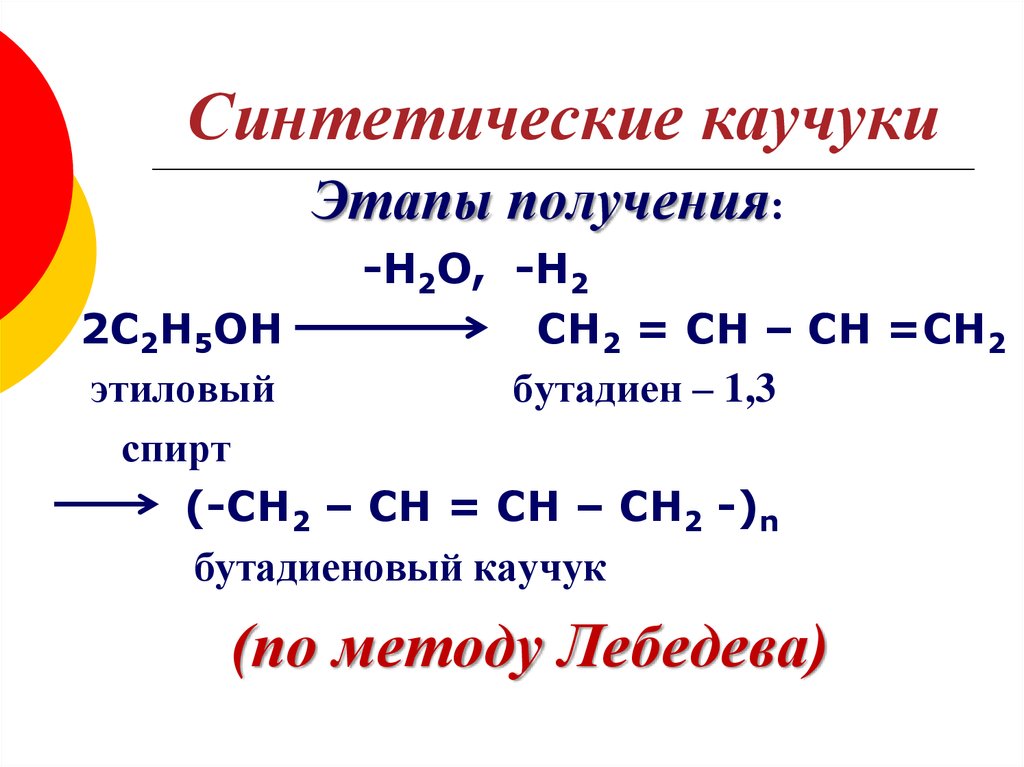
22. Синтетические каучуки
Этапы получения:-Н2О, -Н2
СН2 = СН – СН =СН2
бутадиен – 1,3
2С2Н5ОН
этиловый
спирт
(-СН2 – СН = СН – СН2 -)n
бутадиеновый каучук
(по методу Лебедева)
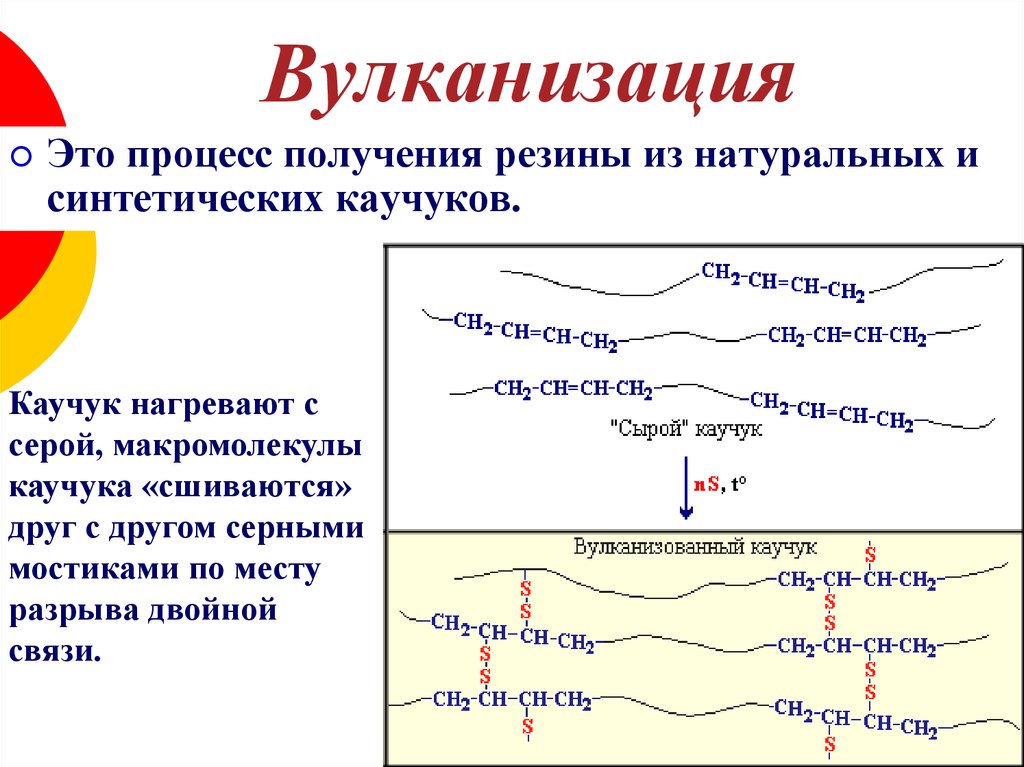
23. Вулканизация
Это процесс получения резины из натуральных исинтетических каучуков.
Каучук нагревают с
серой, макромолекулы
каучука «сшиваются»
друг с другом серными
мостиками по месту
разрыва двойной
связи.
24. Применение
25.
СПАСИБОЗА
Внимание!!!
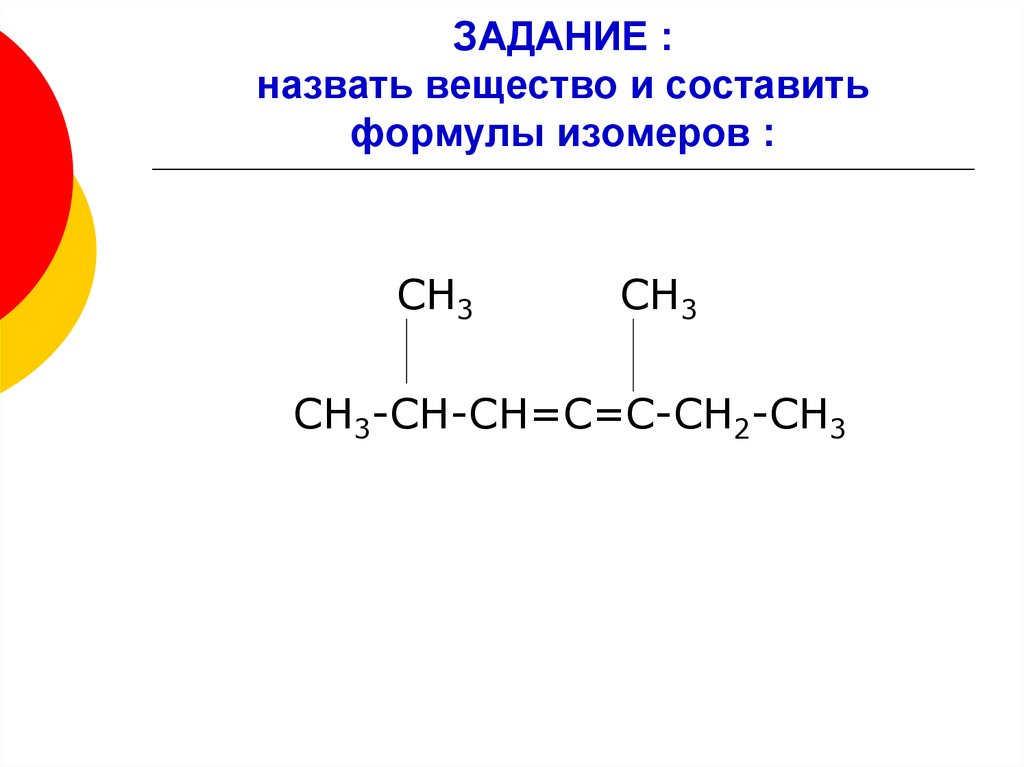
26. ЗАДАНИЕ : назвать вещество и составить формулы изомеров :
СН3СН3
СН3-СН-СН=С=С-СН2-СН3


















 Химия
Химия








