Похожие презентации:
Строение электронных оболочек атомов
1.
Разработал:Учитель химии, биологии
высшей квалификационной категории
Баженов Алексей Анатольевич
2.
Урок 14Проверка знаний
Устно
Письменно
1. Что такое электронная оболочка?
2. Как определить количество энергетических уровней у
элемента по периодической системе?
3. Какая формула расчета максимального количества
электронов на энергетическом уровне?
4. Как по периодической системе определить количество
электронов у электронейтрального атома химического
элемента?
5. Как определить количество электронов на последнем
уровне у элемента по периодической системе?
15.08.2018
ПС
3.
Урок 14Проверка знаний
Устно
Письменно
Нарисуйте
схемы
строения
электронных
0
0
0
7
24
40
оболочек
атомов:
Li
Mg
Ar
+3
+12
+18
2 1• Лития
2 8 2
2 8 8
• Магния
• Аргона
0
32
0
19
S
Фтора
F
+16
+9
2 8 6
• Серы
2 7
Проверка:
Далее:
15.08.2018
ПС
4.
Урок 14I. Строение электронной оболочки
-- Энергетический
Подуровень состоит
уровень
из орбиталей.
состоит из подуровней.
Первый уровень
1ss – подуровень
31
+15
2
Р
0
2ss – подуровень
2р
р – подуровень
8
Третий уровень
2 8 5
3ss – подуровень
3р
р – подуровень
5
15.08.2018
Второй уровень
3d
d – подуровень
ПС
5.
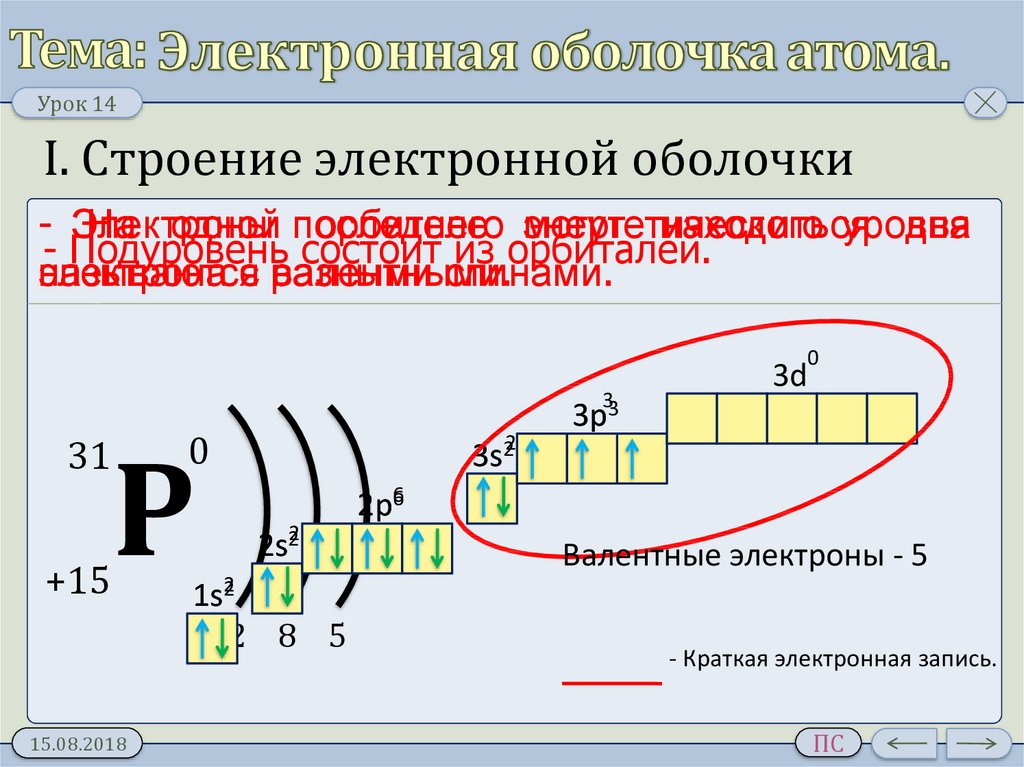
Урок 14I. Строение электронной оболочки
- Электроны
На одной последнего
орбителе энергетического
могут находиться
уровня
два
- Подуровень состоит из орбиталей.
электрона с разными
называются
валентными.
спинами.
0
3
31
+15
Р
15.08.2018
0
3s22
2s22
1s2
2 8 5
3d
3р3
3p
2р6
2p
Валентные электроны - 5
- Краткая электронная запись.
ПС
6.
Урок 14II. Составить строение электронной
оболочки элементов: В, Cl.
Проверка:
Сl
В
35
11
00
2p1
2s2
1s2
+17
+5
2 3
8 7
2s2
1s2
2p6
3p5
3s2
1s22s22p1
3d0
Вал. ē - 3
Вал. ē - 7
1s22s22p63s23p5
15.08.2018
ПС
7.
Урок 14Домашняя работа
& 8 Стр. 51 - 52
Составить строение электронной оболочки
элемента: Si
Дополнительный материал
Орбитально – планетарная модель строения
атома
Конструктор строения электронной оболочки
15.08.2018
ПС






 Химия
Химия








