Похожие презентации:
Углеводороды. Применение природных источников углеводородов и продуктов их переработки
1. 10 класс Углеводороды. Применение природных источников углеводородов и продуктов их переработки.
Презентация:Учителя химии
МОУ- лицея №4 имени
Героя России Горшкова Д. Е.
Н. И. Зайчиковой
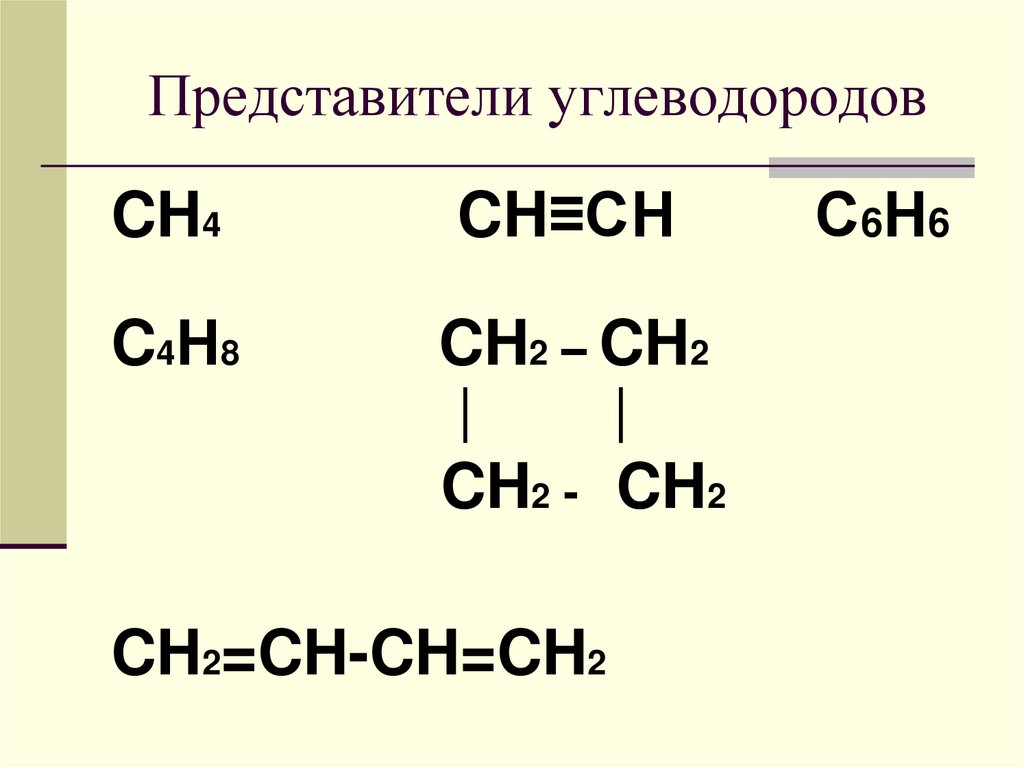
2. Представители углеводородов
CH4CH≡CH
C4Н8
CH2 – CH2
│
│
CH2 - CH2
CH2=CH-CH=CH2
С6 Н6
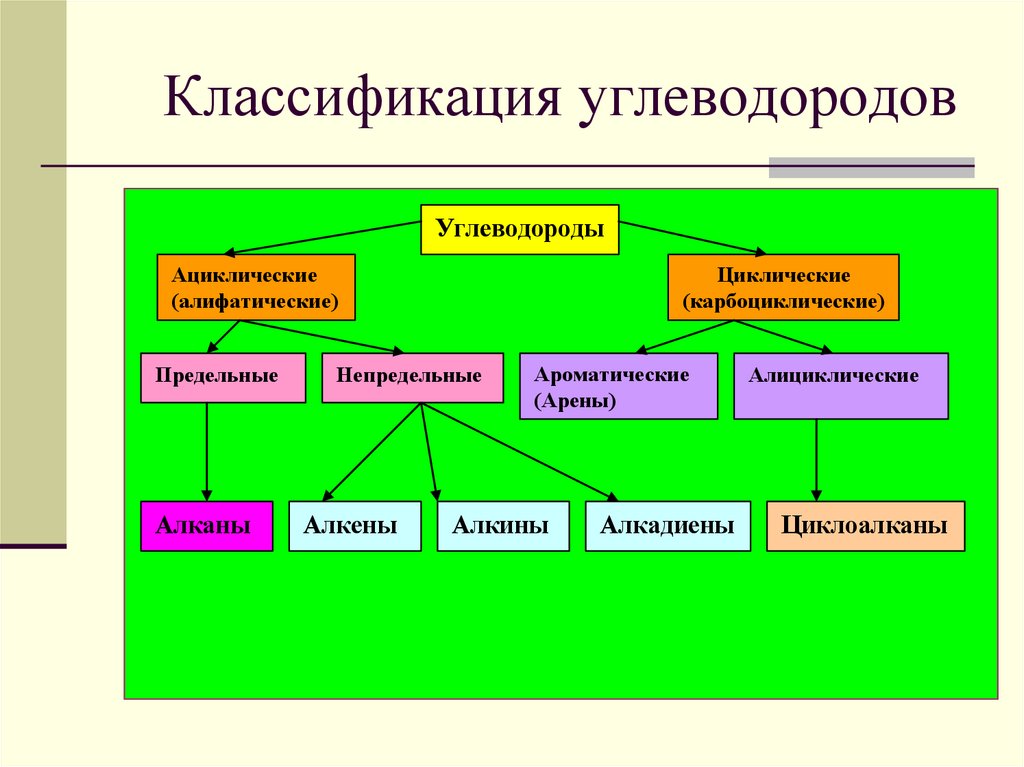
3. Классификация углеводородов
УглеводородыАциклические
(алифатические)
Предельные
Алканы
Циклические
(карбоциклические)
Непредельные
Алкены
Ароматические
(Арены)
Алкины
Алкадиены
Алициклические
Циклоалканы
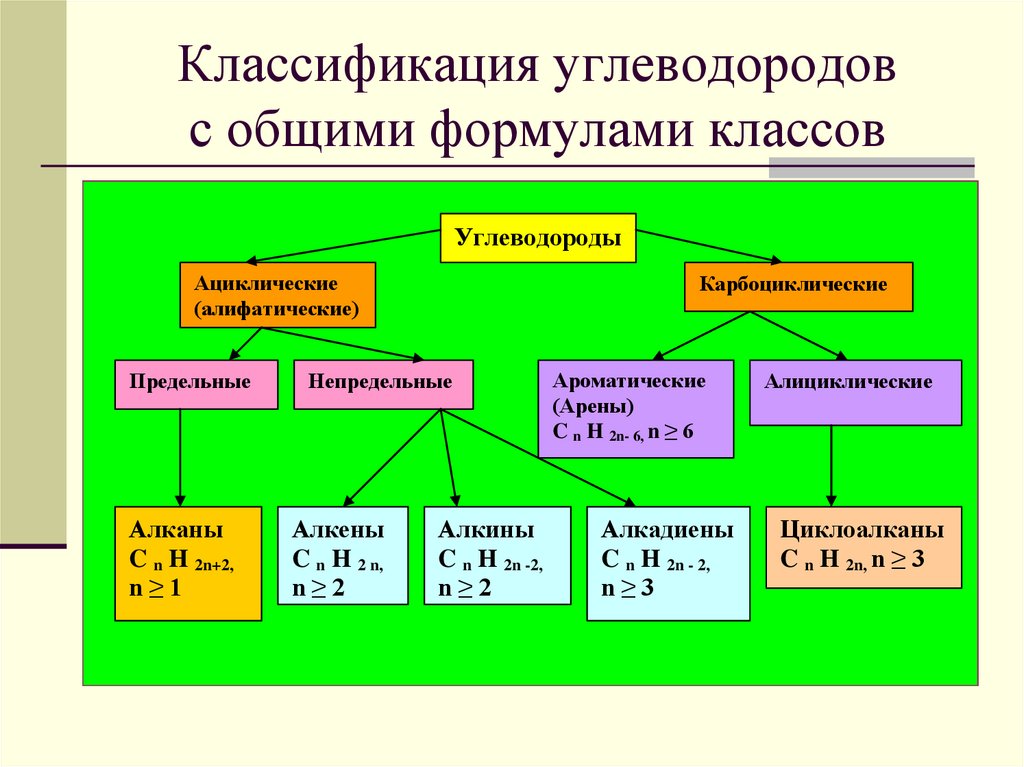
4. Классификация углеводородов с общими формулами классов
УглеводородыАциклические
(алифатические)
Предельные
Алканы
C n H 2n+2,
n≥1
Карбоциклические
Непредельные
Алкены
C n H 2 n,
n≥2
Алкины
C n H 2n -2,
n≥2
Ароматические
(Арены)
C n H 2n- 6, n ≥ 6
Алкадиены
C n H 2n - 2,
n≥3
Алициклические
Циклоалканы
C n H 2n, n ≥ 3
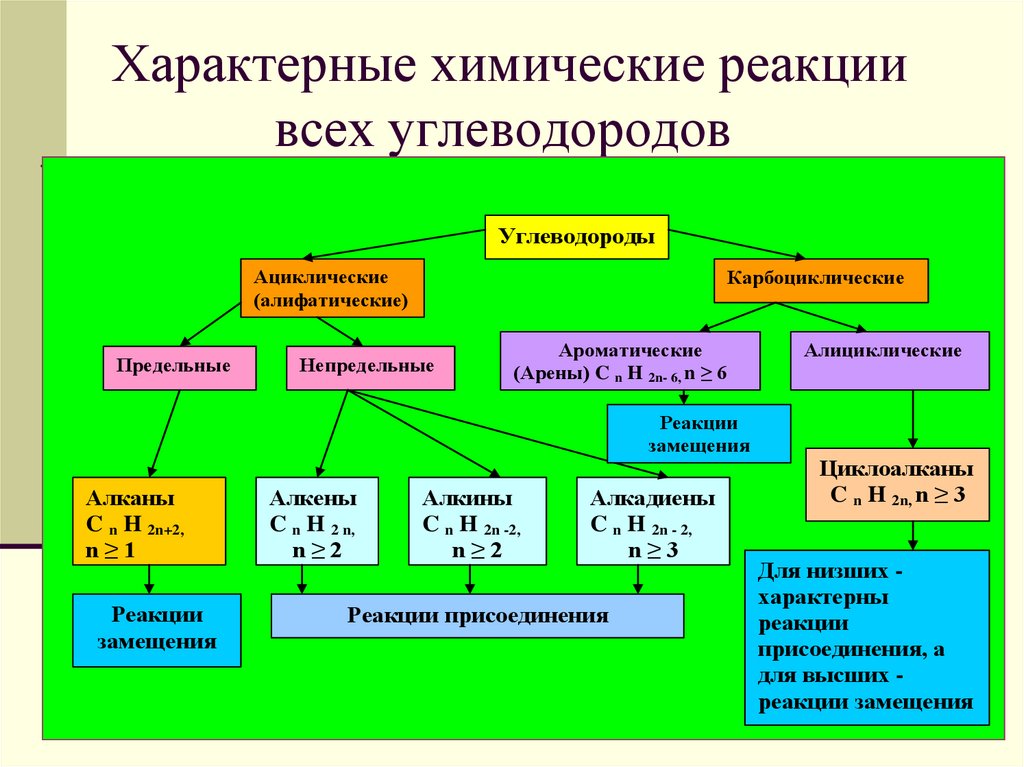
5. Характерные химические реакции всех углеводородов
УглеводородыАциклические
(алифатические)
Предельные
Карбоциклические
Непредельные
Ароматические
(Арены) C n H 2n- 6, n ≥ 6
Реакции
замещения
Алканы
C n H 2n+2,
n≥1
Реакции
замещения
Алкены
C n H 2 n,
n≥2
Алкины
C n H 2n -2,
n≥2
Алкадиены
C n H 2n - 2,
n≥3
Реакции присоединения
Алициклические
Циклоалканы
C n H 2n, n ≥ 3
Для низших характерны
реакции
присоединения, а
для высших реакции замещения
6. Реакции присоединения
Реакция гидрированияРеакция гидратации
СH2=CH-CH3 + H2 →
пропен
→ CH3-CH2-CH3
пропан
CH≡CH + H2 →
этин
→ CH2=CH2 + H2 →
этен
→ CH3-CH3 (этан)
CH2=CH2 + H2O →
этен
→ CH3-CH2-OH
этанол
CH≡CH + H2 O →
этин
→ CH3-COH (этаналь)
7. Реакции присоединения
Реакция галогенированияCH2=CH-CH=CH2 + Br2 →
бутадиен - 1, 3
1
2
3
4
→CH2-CH=CH-CH2
│
│
Br
Br
1,4 – дибромбутен-2
8. Великие ученые
В.В. Марковников -русскийМарковников Владимир Васильевич
(1837 – 1904 г г.)
химик – органик.
Сформулировал
(1869 г.) правила о
направлении реакций
замещения, присоединения
по двойной связи и
изомеризации в зависимости
от химического строения.
Исследовал (с 1880 г.) состав
нефти, заложил основы
нефтехимии как
самостоятельной науки.
Открыл новый класс
органических веществ –
циклопарафины (нафтены).
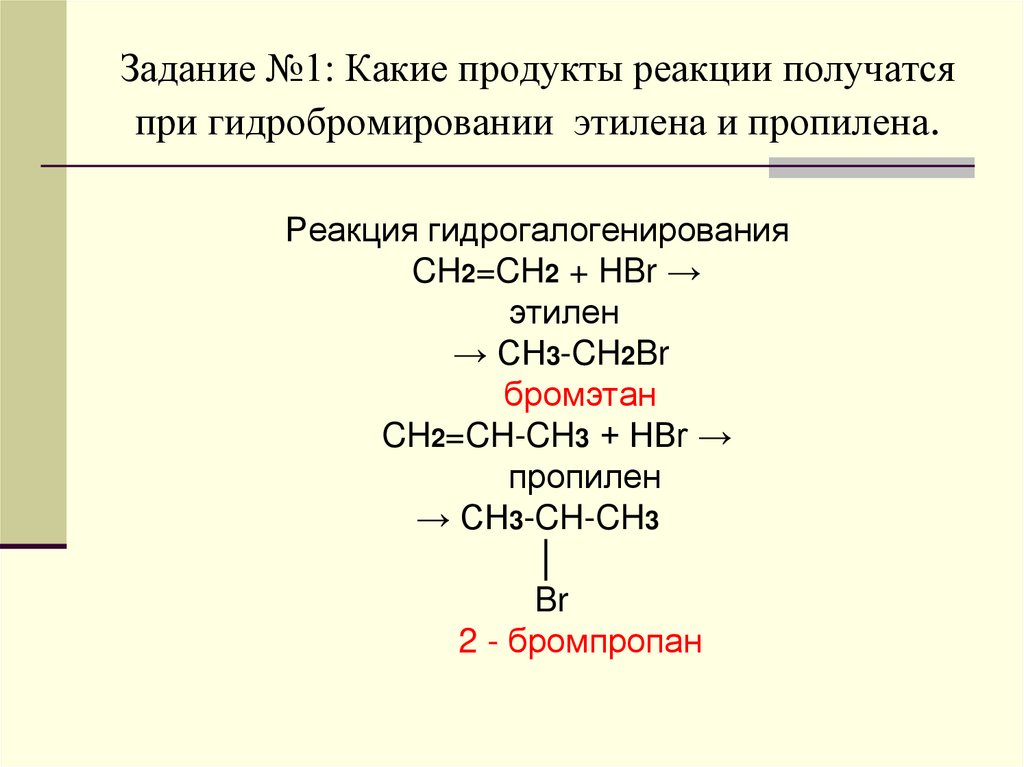
9. Задание №1: Какие продукты реакции получатся при гидробромировании этилена и пропилена.
Реакция гидрогалогенированияCH2=CH2 + HBr →
этилен
→ CH3-CH2Br
бромэтан
CH2=CH-CH3 + HBr →
пропилен
→ CH3-CH-CH3
│
Br
2 - бромпропан
10. Задание №2.
Знаякачественные
реакции на
углеводороды,
распознайте в
какой пробирке
находится этан,
а в какой – этен.
Пробирка №1
Пробирка №2
11.
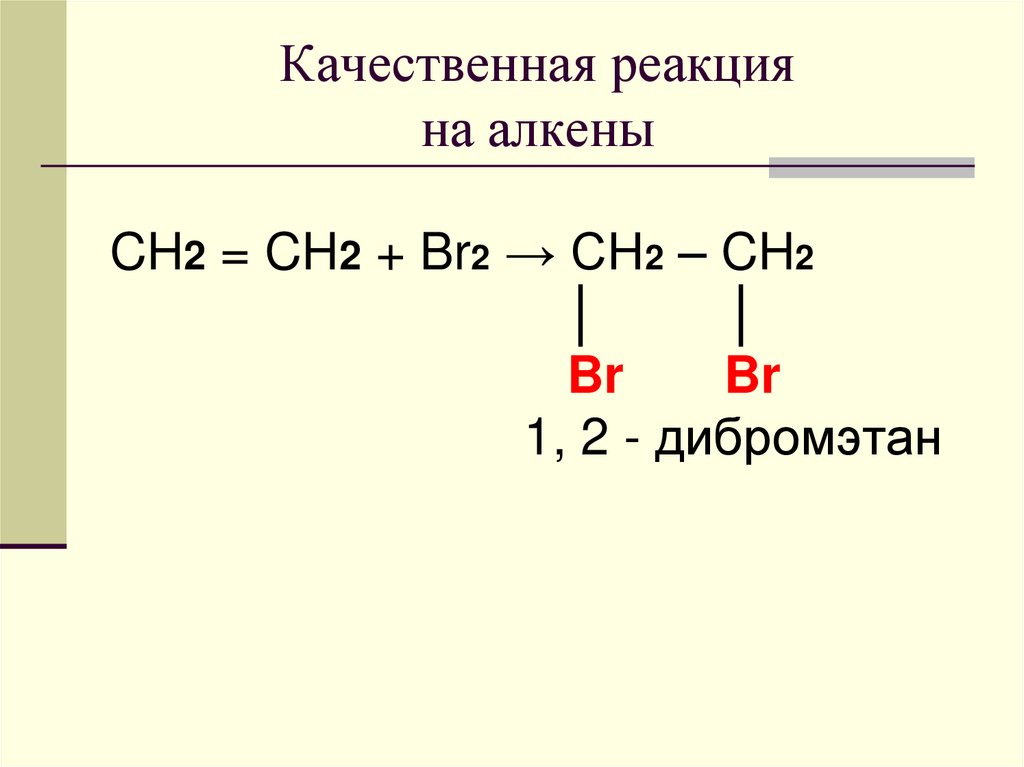
12. Качественная реакция на алкены
CH2 = CH2 + Br2 → CH2 – CH2│
│
Br
Br
1, 2 - дибромэтан
13.
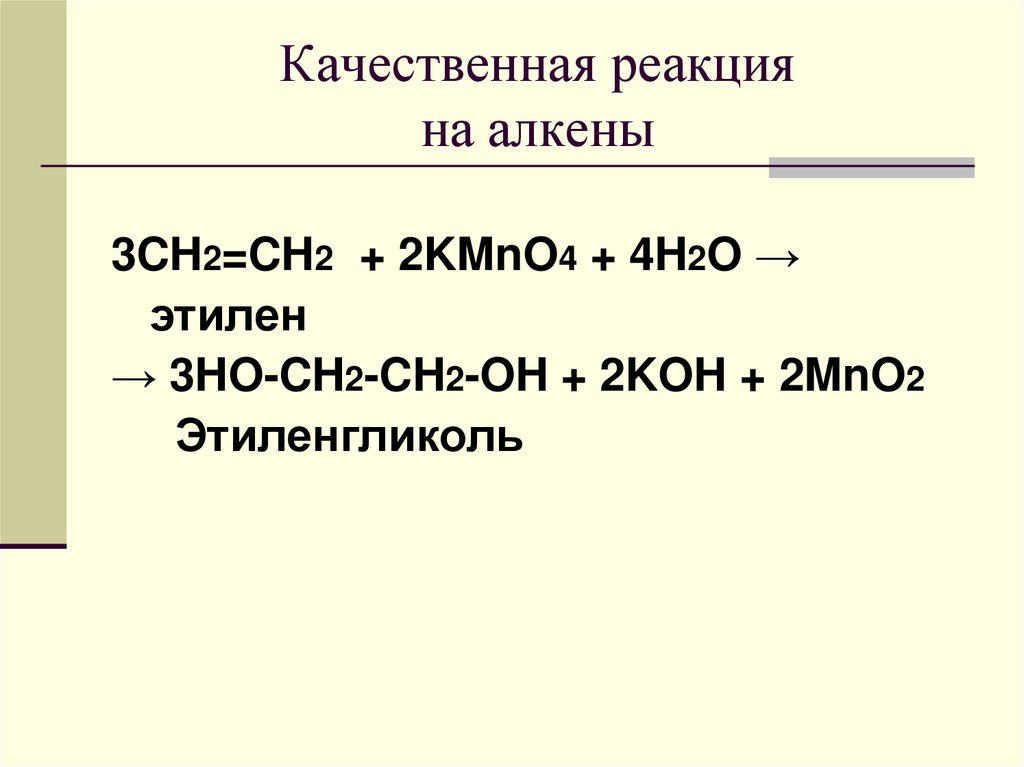
14. Качественная реакция на алкены
3CH2=CH2 + 2KMnO4 + 4H2O →этилен
→ 3HO-CH2-CH2-OH + 2KOH + 2MnO2
Этиленгликоль
15. Месторождения полезных ископаемых
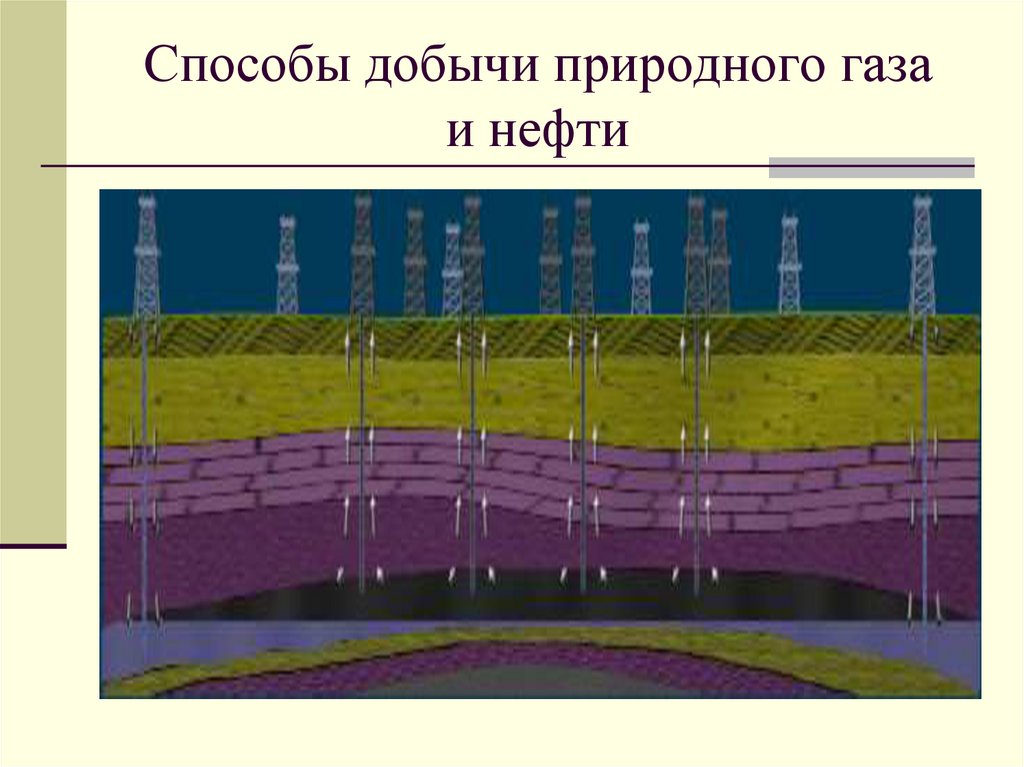
16. Способы добычи природного газа и нефти
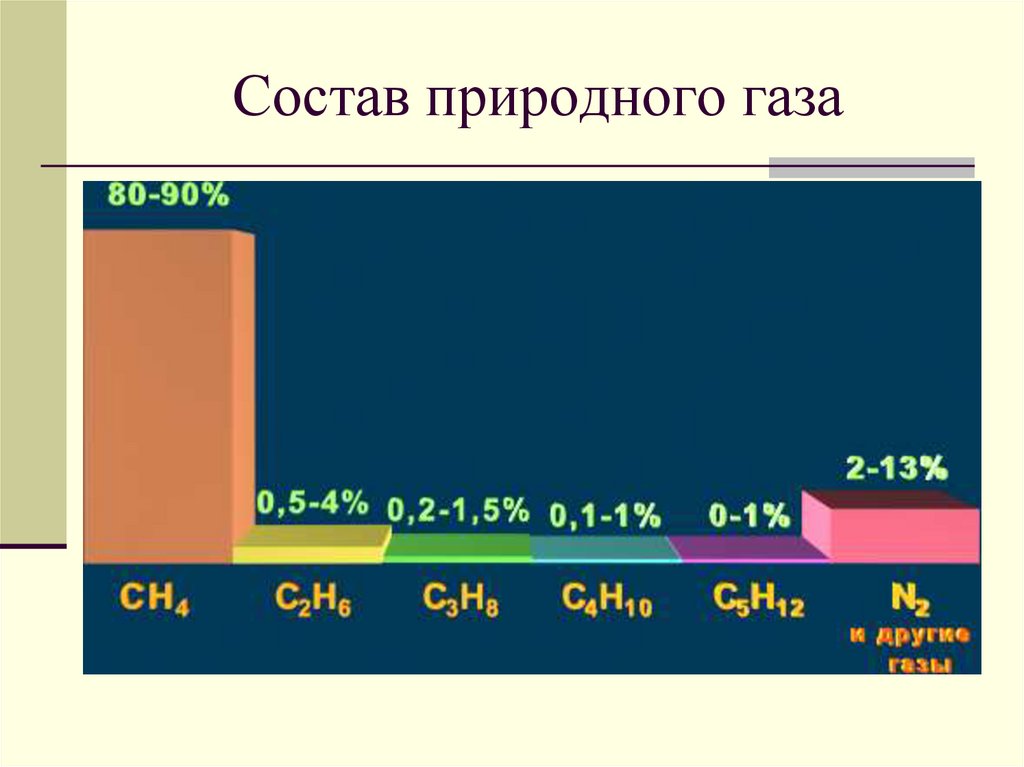
17. Состав природного газа
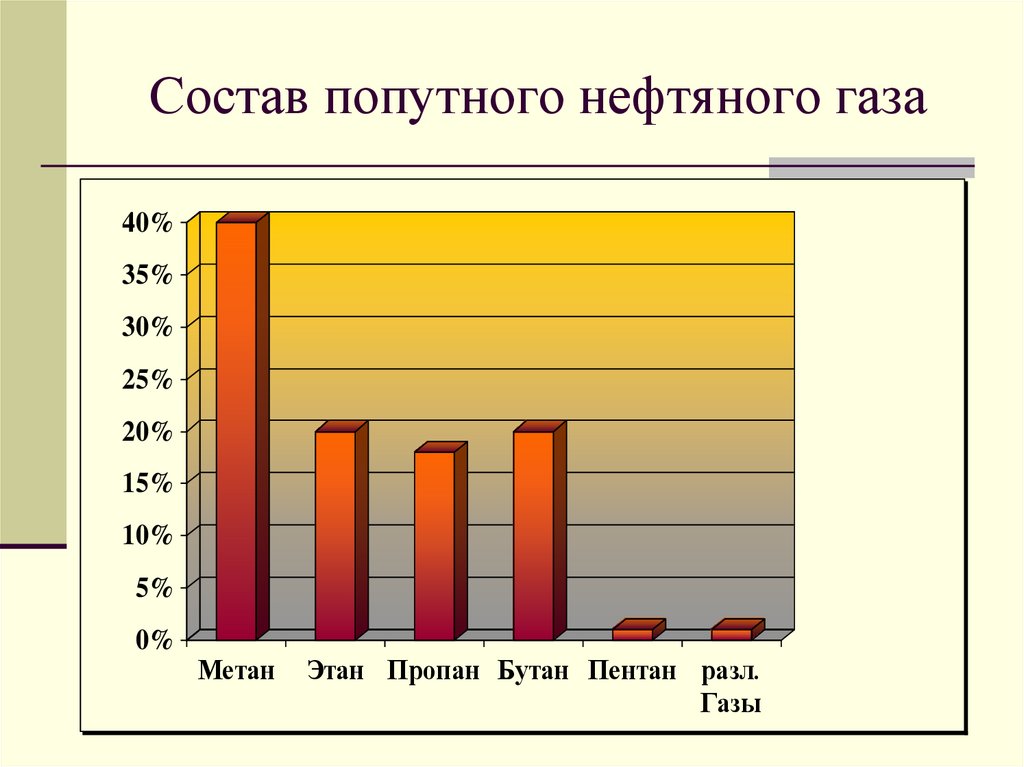
18. Состав попутного нефтяного газа
40%35%
30%
25%
20%
15%
10%
5%
0%
Метан
Этан Пропан Бутан Пентан разл.
Газы
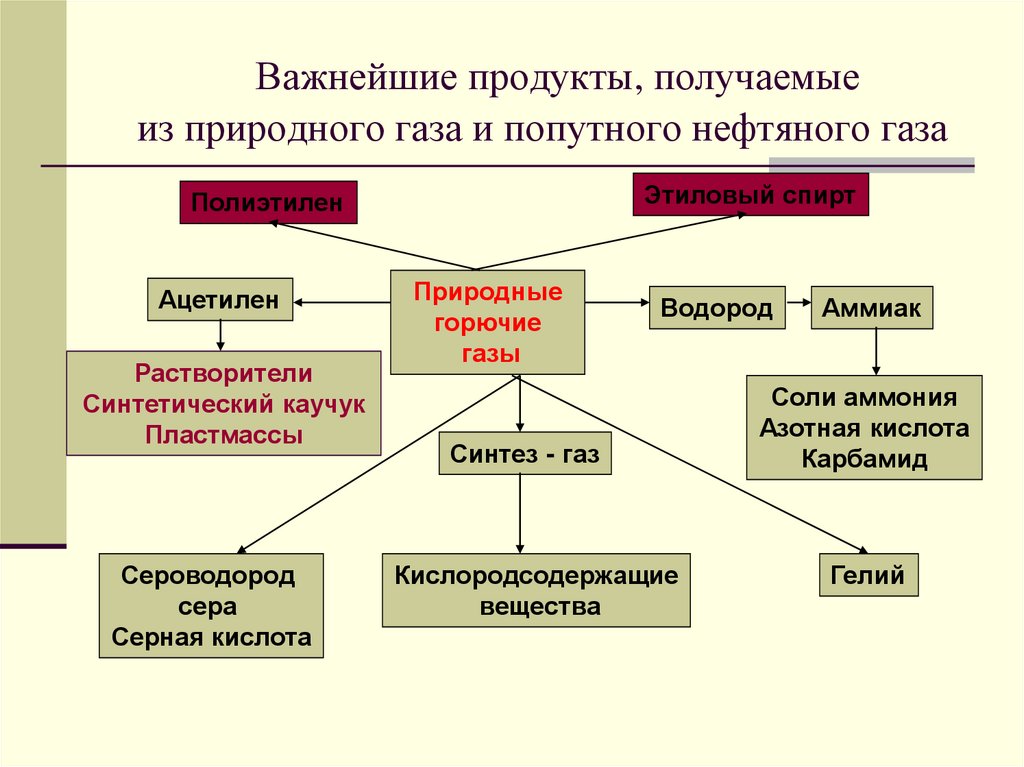
19. Важнейшие продукты, получаемые из природного газа и попутного нефтяного газа
Этиловый спиртПолиэтилен
Ацетилен
Растворители
Синтетический каучук
Пластмассы
Сероводород
сера
Серная кислота
Природные
горючие
газы
Водород
Синтез - газ
Кислородсодержащие
вещества
Аммиак
Соли аммония
Азотная кислота
Карбамид
Гелий
20. Горение нефти
21. Нефтеперерабатывающий завод
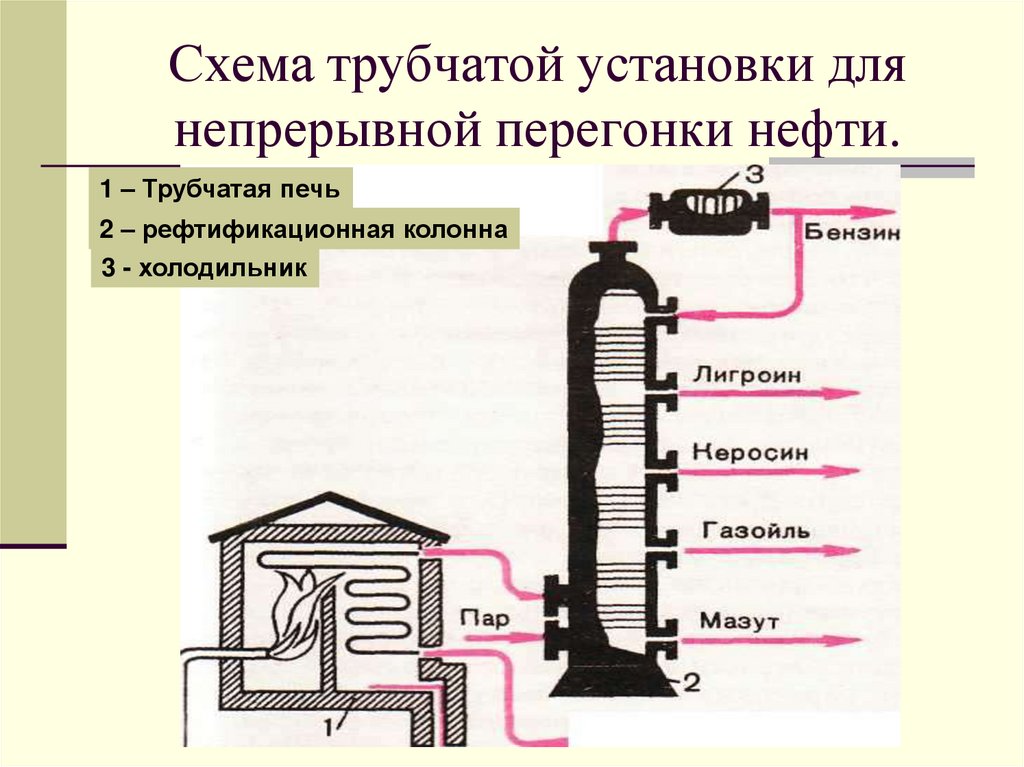
22. Схема трубчатой установки для непрерывной перегонки нефти.
1 – Трубчатая печь2 – рефтификационная колонна
3 - холодильник
23.
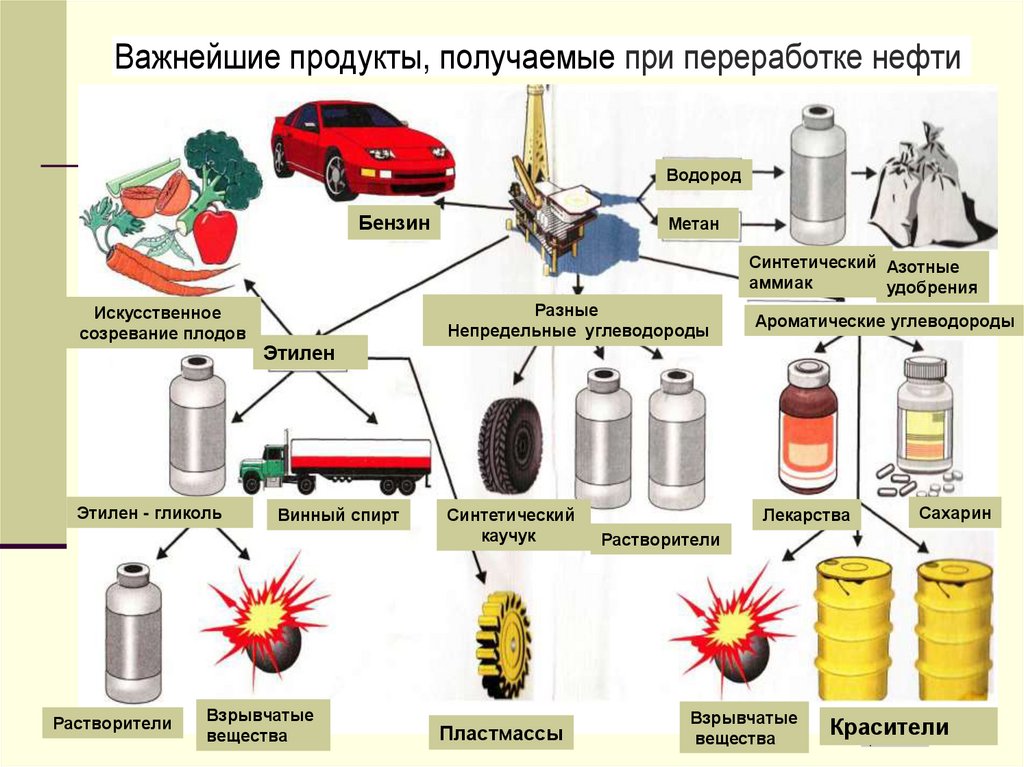
Важнейшие продукты, получаемые при переработке нефтиВодород
Бензин
Метан
Синтетический Азотные
Азотные
Синтетический
аммиак
удобрения
аммиак
удобрения
Искусственное
созревание
Искусственное
плодов
созревание плодов
Этилен - гликоль
Растворители
Растворители
РазныеРазные
непредельные
углеводороды
Непредельные углеводороды
Ароматические углеводороды
Ароматические
углеводороды
Этилен
Винный
спирт
Винный спирт
Взрывчатые
Взрывчатые
вещества
вещества
Синтетический
Синтетический
каучук
каучук
Растворители
Растворители
Пластмассы
Пластмассы
Лекарства
Взрывчатые
Взрывчатые
вещества
вещества
Сахарин
Сахарин
Красители
Красители
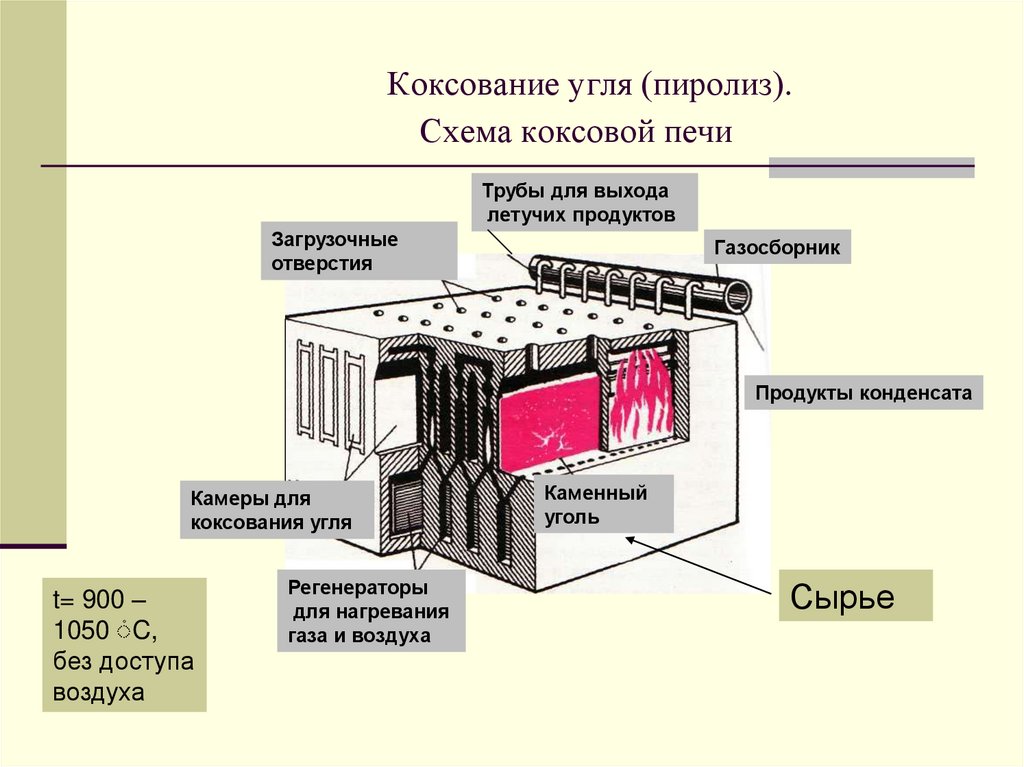
24. Коксование угля (пиролиз). Схема коксовой печи
Трубы для выходалетучих продуктов
Загрузочные
отверстия
Газосборник
Продукты конденсата
Камеры для
коксования угля
t= 900 –
1050 ۫C,
без доступа
воздуха
Регенераторы
для нагревания
газа и воздуха
Каменный
уголь
Сырье
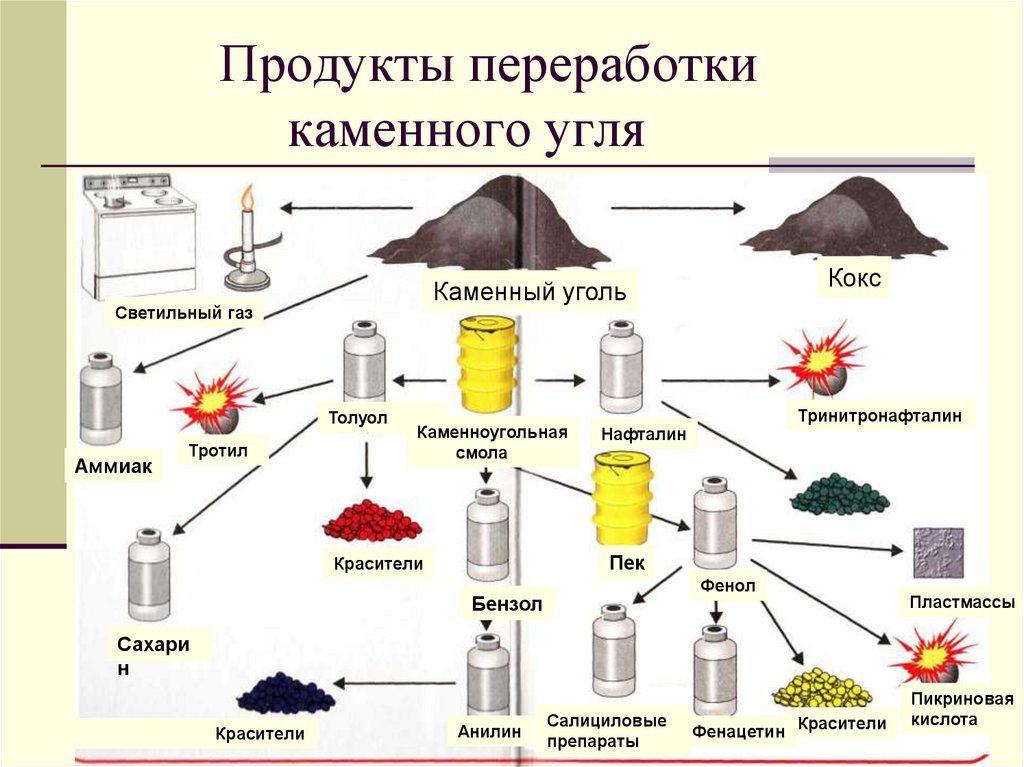
25. Продукты переработки каменного угля
Светильный газТолуол
Аммиак
Тротил
Кокс
Каменный уголь
Каменноугольная
смола
Тринитронафталин
Нафталин
Пек
Красители
Фенол
Бензол
Пластмассы
Сахари
н
Красители
Анилин
Салициловые
препараты
Фенацетин Красители
Пикриновая
кислота
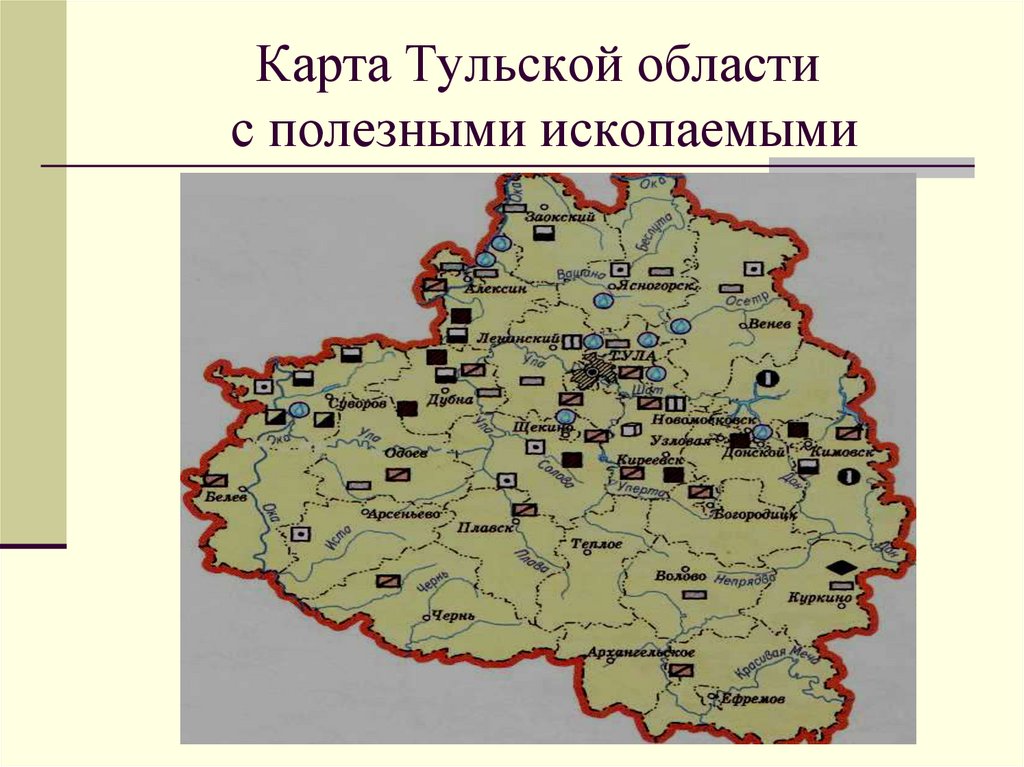
26. Карта Тульской области с полезными ископаемыми
27. Итог урока.
Углеводороды – это соединения, состоящие только изатомов углерода и водорода.
Наиболее важными источниками углеводородов
являются природный и попутный нефтяной газы,
нефть и уголь.
Природный газ, нефть и уголь – это не только
топливо, но и богатейший источник сырья для
химической промышленности.
Знание строения веществ и закономерностей их
превращений позволяет человеку искусственно
создавать вещества, которых нет в природе. Поэтому
вместе с другими науками органическая химия
становится все более могучей непосредственной
производительной силой.
28. Великие ученые.
Великий русский ученыйДмитрий Иванович Менделеев
(1834 – 1907 г г.)
- химик, Д. И. Менделеев,
один из
основоположников
современной химии
открывший
Периодический Закон
говорил, что топить
нефтью, значит топить
ассигнациями. Он
считал, что нефть
является ценным
сырьем для
производства многих
органических веществ.
Он автор
фундаментальной
работы «Основы химии».
29. Домашнее задание
§ 17, повт. §15,16, упр. №3, 4 (стр. 100),Природный газ содержит (по объему) 90% метана,
4% этана, 1% пропана, 1% бутана, 4% азота.
Рассчитайте, сколько л воздуха потребуется для
полного сгорания 1 л природного газа.
Предложите схему производства поливинилхлорида
из метана. Большое значение в народном хозяйстве
имеет полимер поливинилхлорид, его формула:
(- CH2 – CH -)n
│
Cl
Какие материалы, реагенты, аппараты потребуются
для этого?











 Химия
Химия








