Похожие презентации:
Белковый обмен. Обмен нуклеопротеинов
1. ОБМЕН НУКЛЕОПРОТЕИНОВ
2.
• Нуклеопротеины – сложные белки,простетической группой которых являются
нуклеиновые кислоты (ДНК и РНК).
• Их функция – хранение и передача генетической
информации, участие в синтезе белковой молекулы.
3.
Продукты, богатыенуклеопротеинами
мясо
печень
икра
яйца
горох
фасоль
крупы
кофе
шоколад
4. Переваривание нуклеопротеинов
• В желудке под влиянием НСl отщепляются белки(протамины и гистоны), которые денатурируют →
переваривание белков.
• В 12-перстной кишке ДНК-азы и РНК-азы
поджелудочной железы расщепляют нуклеиновые
кислоты на олигонуклеотиды.
• В тонком кишечнике: фосфодиэстеразы завершают
расщепление до мононуклеотидов,
• фосфатазы отщепляют фосфорную кислоту от
нуклеотидов,
• а нуклеозидазы расщепляют нуклеозиды на азотистое
основание и пентозу
• Всасываться могут нуклеозиды, азотистые основания,
пентозы, соли фосфорной кислоты.
5.
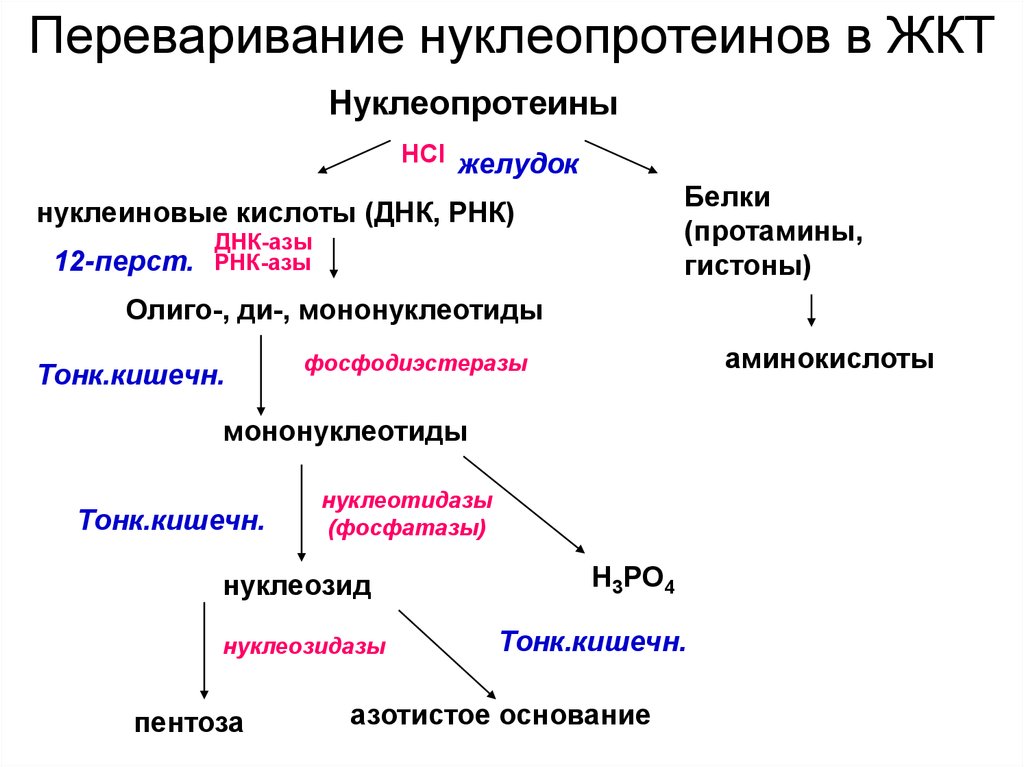
Переваривание нуклеопротеинов в ЖКТНуклеопротеины
НСl желудок
Белки
(протамины,
гистоны)
нуклеиновые кислоты (ДНК, РНК)
12-перст.
ДНК-азы
РНК-азы
Олиго-, ди-, мононуклеотиды
Тонк.кишечн.
аминокислоты
фосфодиэстеразы
мононуклеотиды
Тонк.кишечн.
нуклеотидазы
(фосфатазы)
нуклеозид
нуклеозидазы
пентоза
Н3РО4
Тонк.кишечн.
азотистое основание
6.
• Пищевые нуклеотиды почти полностьюраспадаются до конечных продуктов (вне
зависимости от поступившего количества).
• Часть нуклеозидов может быть использована в
биосинтезе НК.
• Гуанин не используется для синтетических целей,
другие азотистые основания могут быть
использованы.
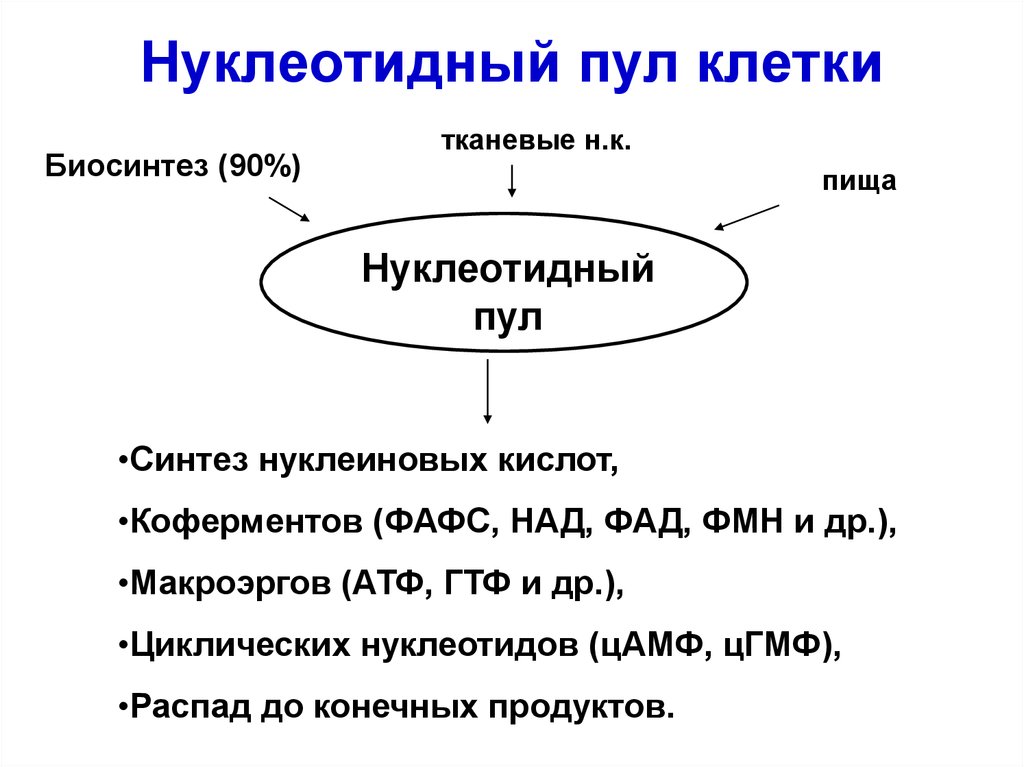
7. Нуклеотидный пул клетки
Биосинтез (90%)тканевые н.к.
пища
Нуклеотидный
пул
•Синтез нуклеиновых кислот,
•Коферментов (ФАФС, НАД, ФАД, ФМН и др.),
•Макроэргов (АТФ, ГТФ и др.),
•Циклических нуклеотидов (цАМФ, цГМФ),
•Распад до конечных продуктов.
8.
Синтез пуриновыхнуклеотидов
9.
2 пути синтеза:1. Синтез de novo
образованиe адениловой и гуаниловой кислот из
низкомолекулярных предшественников, продуктов
обмена углеводов и белков.
2. Реутилизация пуриновых оснований
Повторное использование свободных пуриновых
оснований для синтеза пуриновых нуклеотидов .
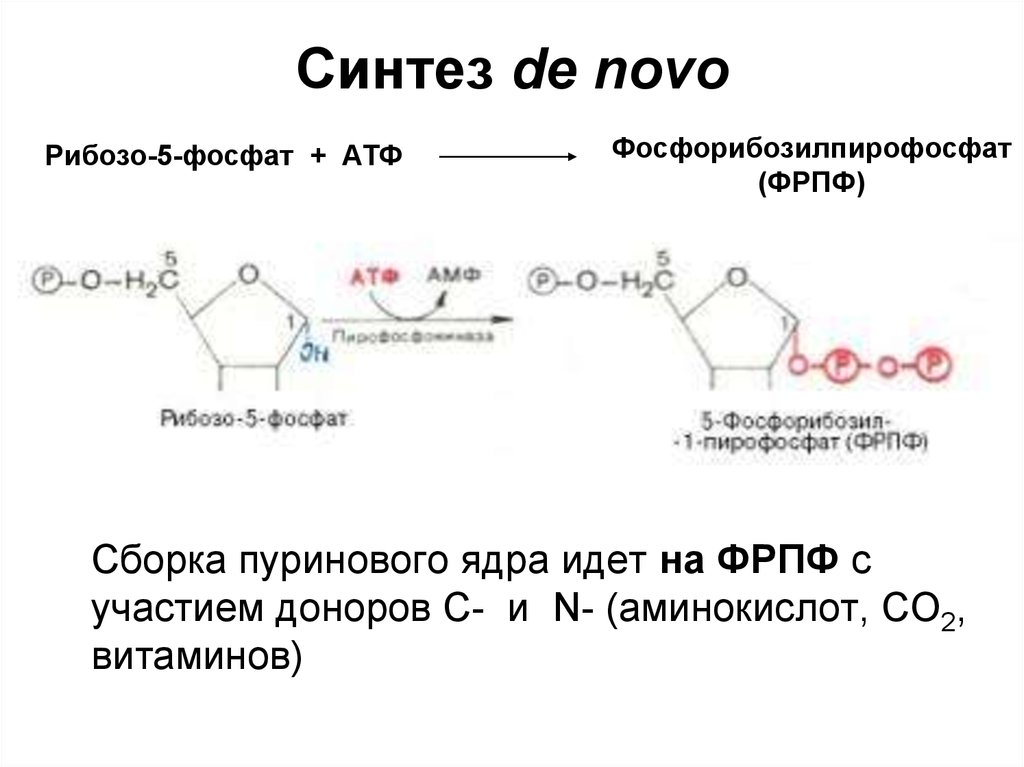
10. Синтез de novo
Рибозо-5-фосфат + АТФФосфорибозилпирофосфат
(ФРПФ)
Сборка пуринового ядра идет на ФРПФ с
участием доноров С- и N- (аминокислот, СО2,
витаминов)
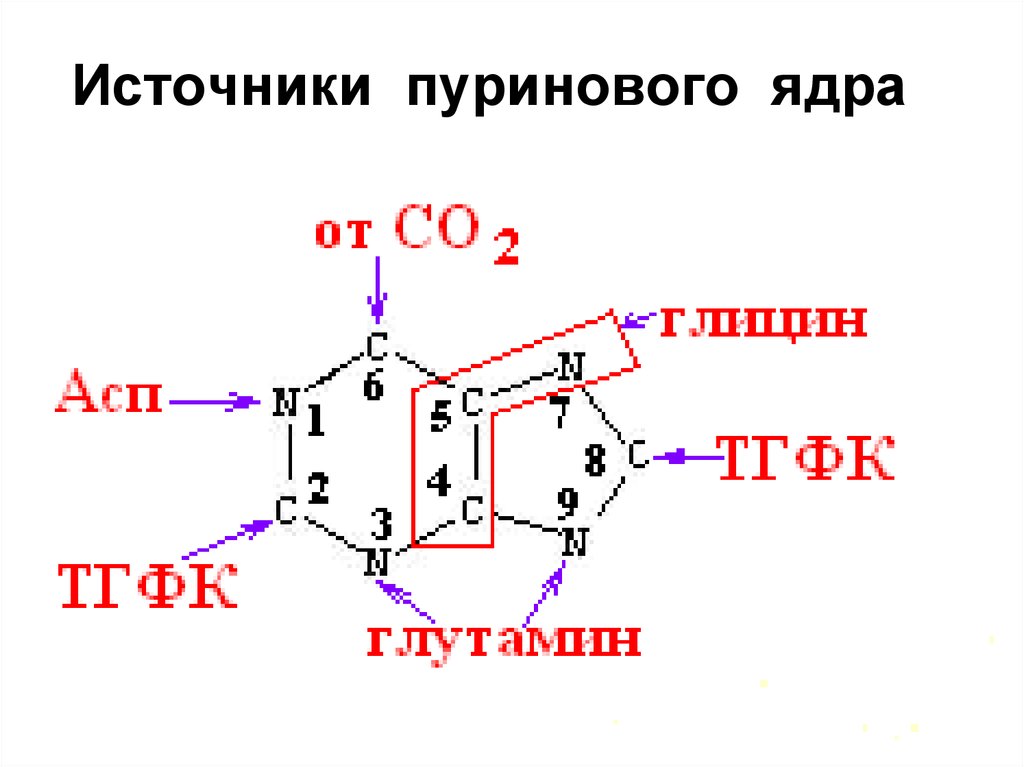
11. Источники пуринового ядра
12.
ФРПФ + ГлнРРн
амидотрансфераза
Фосфорибозиламин + Глу
• далее цепь реакций, формируется
пуриновое ядро и появляется нуклеотидпредшественник - инозиновая кислота.
• Регуляция синтеза пуриновых нуклеотидов
по принципу обратной связи. Накопление
нуклеотидов ингибирует первый фермент
синтеза пуринов – амидотрансферазу.
13.
• Процесс идет с затратой энергии• ИМФ - предшественник АМФ и ГМФ
Требуется:
на синтез ИМФ – 6 молекул АТФ,
на синтез АМФ – 7 молекул АТФ,
на синтез ГМФ – 8 молекул АТФ
14.
АМФАТФ
ИМФ
ГМФ
нуклеозидмонофосфат-
и
ГТФ
нуклеозиддифосфаткиназы
ГМФ + АТФ <=> ГДФ + АДФ; ГДФ + АТФ <=> ГТФ + АДФ
15. Путь реутилизации
• Это использование для синтеза пуриновыхнуклеотидов готовых азотистых
оснований, не подвергшихся дальнейшему распаду.
• Процесс простой и энергетически менее
затратный
16.
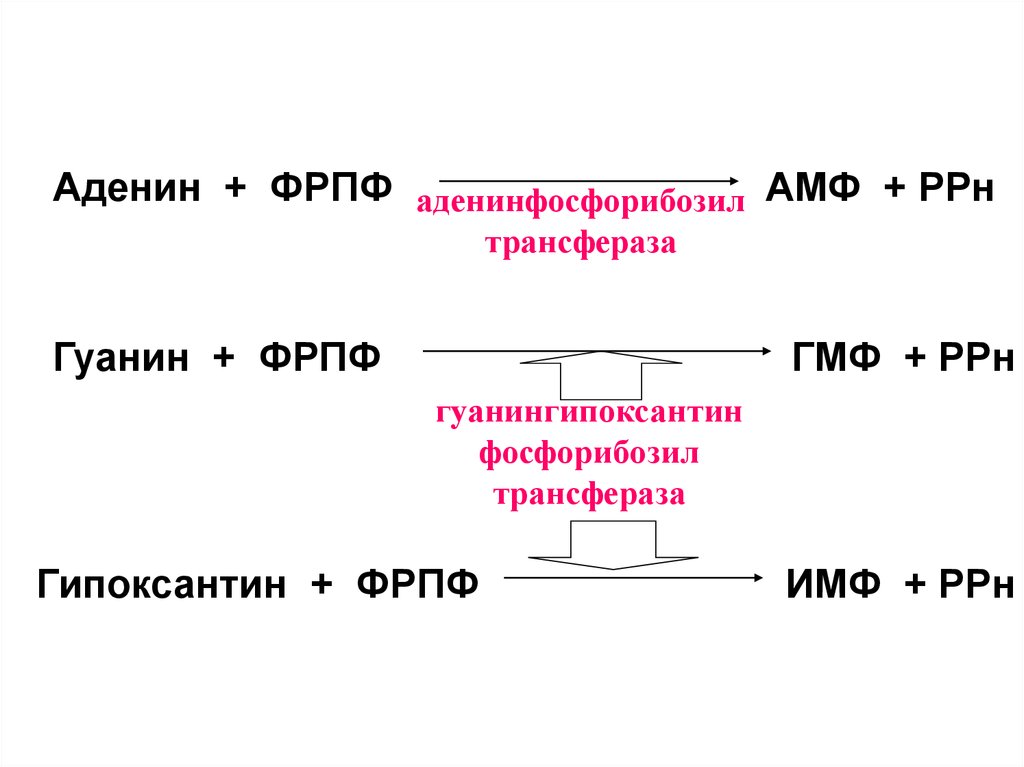
Аденин + ФРПФ аденинфосфорибозил АМФ + РРнтрансфераза
Гуанин + ФРПФ
ГМФ + РРн
гуанингипоксантин
фосфорибозил
трансфераза
Гипоксантин + ФРПФ
ИМФ + РРн
17.
Распад пуриновыхнуклеотидов
18.
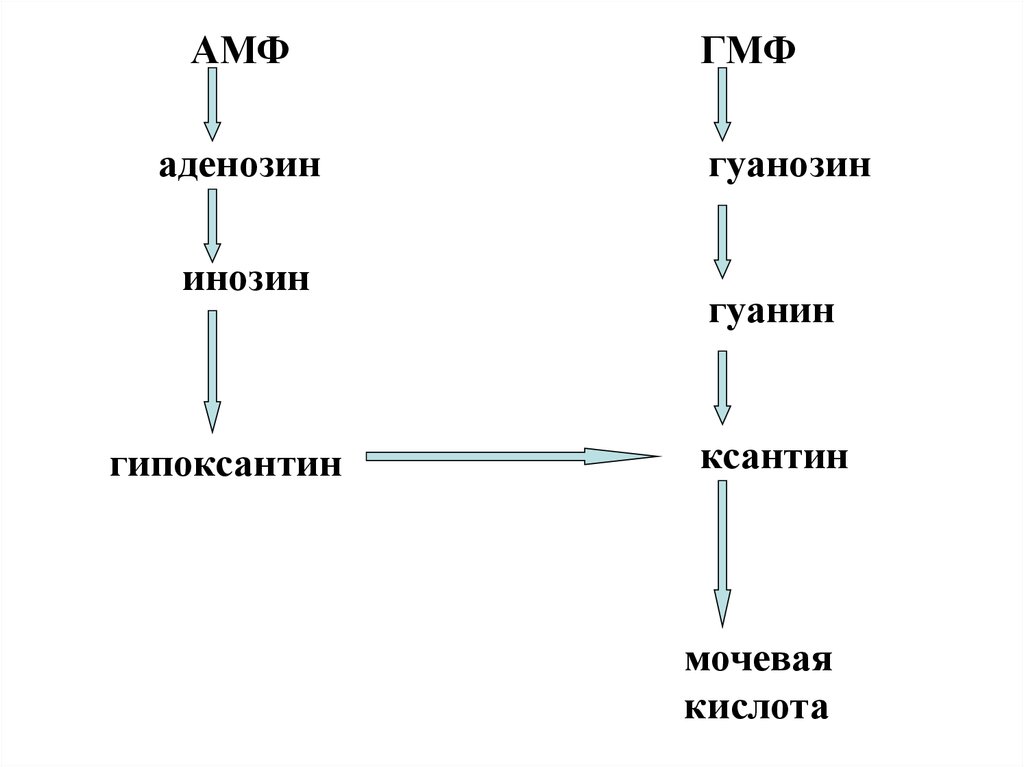
АМФаденозин
инозин
гипоксантин
ГМФ
гуанозин
гуанин
ксантин
мочевая
кислота
19.
NH2О
N
N
N
N
N
N
НО2НС
Н
ОН
NH3
аденозин
дезаминаза
О
Н
Н2О
Н
ОН
аденозин
Н
N
N
НОН2С
Н
рибозо-1Н3РО4 фосфат
нуклеозид
фосфорилаза
О
Н
Н
ОН
ОН
инозин
Н
20.
ОМо
N
2 Н2О
НN
О
2+
О2
2 Н2О2
N
НN
ксантиноксидаза
О
NН
N
NН
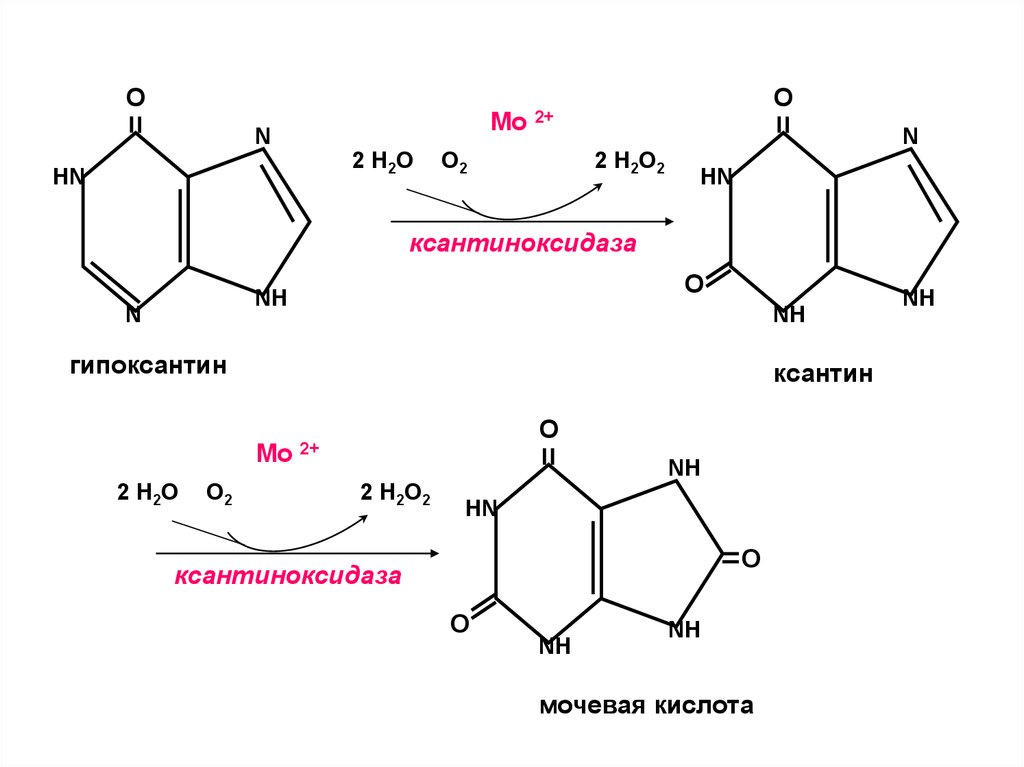
гипоксантин
ксантин
Мо
2 Н2О
О2
О
2+
2 Н2О2
NН
НN
О
ксантиноксидаза
О
NН
NН
мочевая кислота
NН
21.
ОО
N
N
Н3РО4
НN
нуклеозидфосфорилаза
Н2N
Н
Н2N
N
N
N
НОН2С
НN
рибозо-1фосфат
гуаниндезаминаза
Н
ОН
гуанин
Н2О
О
Н
NН
Н
NН3
ОН
О
N
НN
гуанозин
О
ксантиноксидаза
Мочевая кислота
NН
NН
ксантин
22.
• Мочевая кислота – труднорастворимое соединение(60 мг на 1 литр воды)
• Урат натрия в 17 раз более растворим.
• При рН менее 5,75 – мочевая кислота, более – урат
натрия.
• Из эндогенных нуклеозидов ≈ 500 мг/сут, из
поступающих с пищей ≈ 200 мг/сут.
• Мочевая кислота из тканей: 75% выделяется мочой,
остальное с калом.
• В сутки с мочой выделяется ≈ 0,7 г.
• Содержание мочевой кислоты в сыворотке крови 210
– 420 мкмоль/л (мужчины)
23. Гиперурикемия – увеличение содержания мочевой кислоты в сыворотке крови
Первичная при:• подагре
• синдроме Леша-Нихана
Вторичная при:
• почечной недостаточности
• сахарном диабете
• алкоголизме
• усиленном катаболизме нуклеиновых кислот
(метастазирование опухолей, голодание,
повреждение тканей, гемоглобинопатии и т.д.)
24. Синдром Леша-Нихана
• Отсутствует ферментгуанингипоксантинфосфорибозилтрансфераза, не
образуются ГМФ и ИМФ
• Гуанин и гипоксантин повторно не используются и
распадаются до мочевой кислоты
• Клиника: умственная отсталость, спастические
центральные парезы, приступы агрессии со
склонностью к членовредительству.
• Болеют мальчики (наследование с Х-хромосомой).
25. Подагра
Распространенное заболевание – до 1,7%
населения. Мужчины болеют в 20 раз чаще.
Этиология:
Нарушение синтеза ферментов утилизации
пуринов
Активация синтеза пуринов
Избыточное поступление пуринов с пищей
Усиленный распад НК в тканях (хронический
воспалительный процесс, пожилой возраст)
Недостаточность выделения уратов почками
26.
• Тофусы («узелки») - отложениякристаллов уратов в тканях,
суставах, сухожилиях, хрящах …
• Острый подагрический артрит
(боли в суставах)
• Деформация суставов
• Нефрит или мочекаменная
болезнь (у 15 – 20% больных)
• Встречается эндемическая
подагра (Армения), где почвы
богаты молибденом
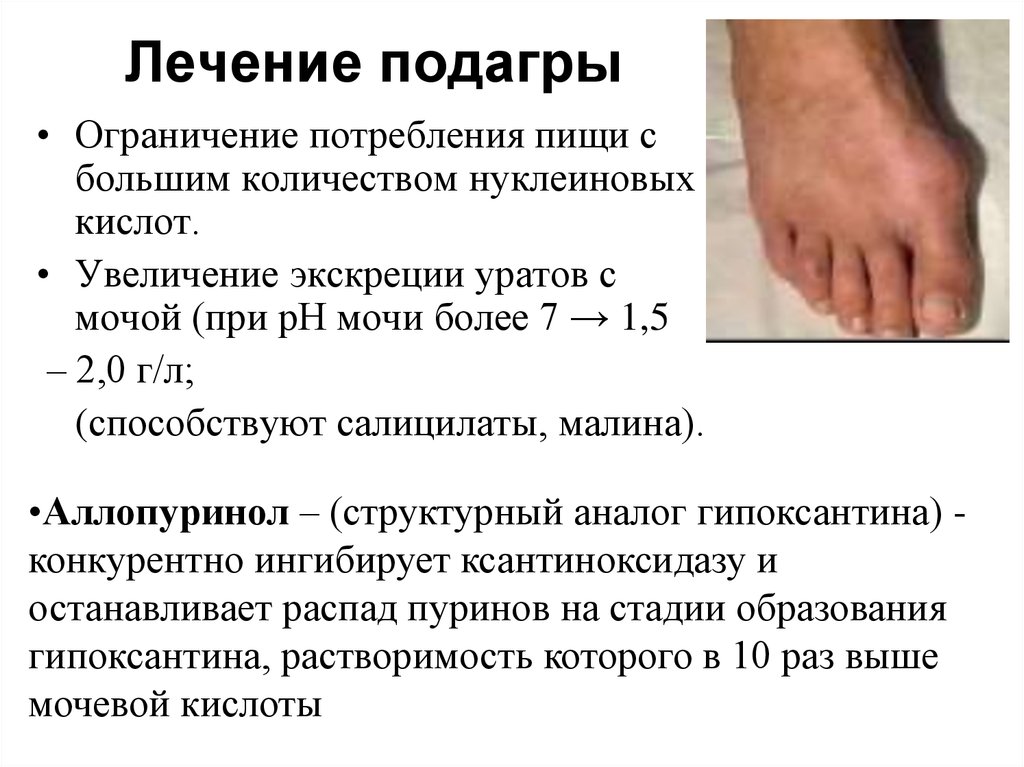
27. Лечение подагры
• Ограничение потребления пищи сбольшим количеством нуклеиновых
кислот.
• Увеличение экскреции уратов с
мочой (при рН мочи более 7 → 1,5
– 2,0 г/л;
(способствуют салицилаты, малина).
•Аллопуринол – (структурный аналог гипоксантина) конкурентно ингибирует ксантиноксидазу и
останавливает распад пуринов на стадии образования
гипоксантина, растворимость которого в 10 раз выше
мочевой кислоты
28.
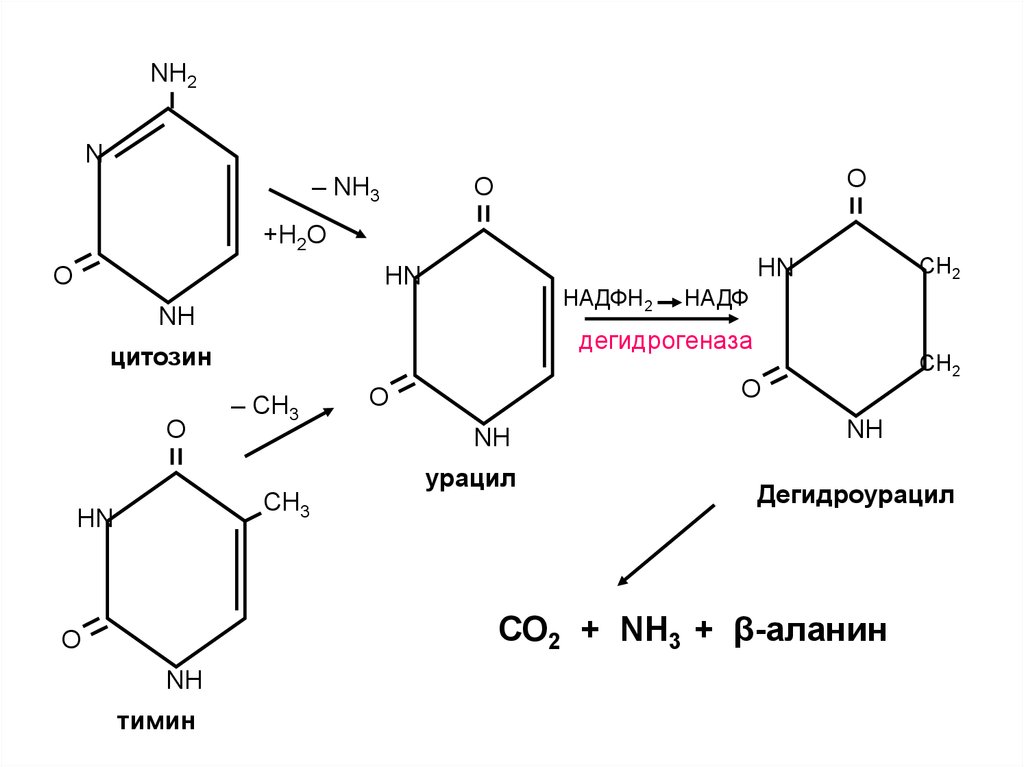
Распадпиримидиновых
нуклеотидов
29.
NH2N
– NH3
О
О
+H2О
НАДФН2
NH
– СН3
СН2
O
O
NH
СН3
НN
НАДФ
дегидрогеназа
цитозин
О
СН2
НN
НN
O
урацил
NH
Дегидроурацил
СО2 + NН3 + β-аланин
O
NH
тимин
30.
Синтезпиримидиновых
нуклеотидов
31.
• Биосинтез УМФ – общего предшественника всехпиримидиновых нуклеотидов включает 6 реакций.
• Первая реакция сходна с первой реакцией синтеза
мочевина, но отличается тем, что:
Реакцию катализирует карбамоилфосфатсинтетаза II
КФС II содержится в цитоплазме практически всех
клеток организма (КФС I только в митохондриях
печени → орнитиновый цикл)
С участием глутамина (а не аммиака)
32.
глутамин + CO2 + H2O + 2 ATФО
NH2 – C – O ~ P
карбамоилфосфат
Mg 2+
карбамоилфосфат
синтетаза II
+ АДФ + Рн + глутамат
33.
ОNH2 – C – O ~ P
СООН
Рн
+ СН2
карбамоилфосфат
СН – СООН
аспартаткарбамоил
трансфераза
NН2
аспартат
О
COOH
CH2
NH2
CH – COOH
CO – NH
карбамоиласпартат
Н2О
НN
дигидрооротаза
СООН
O
NH
дигидрооротат
34.
1О
НN
НАД
СН
СН – СООН
O
дегидрогеназа
РРн
НN
оротатфосфорибозил
трансфераза
НАДН2
дигидрооротат
ФРПФ
О
O
N
NH
оротовая
кислота
СООН
О
Р – ОН2С
ОН
ОН
Оротоидинмонофосфат
(ОМФ)
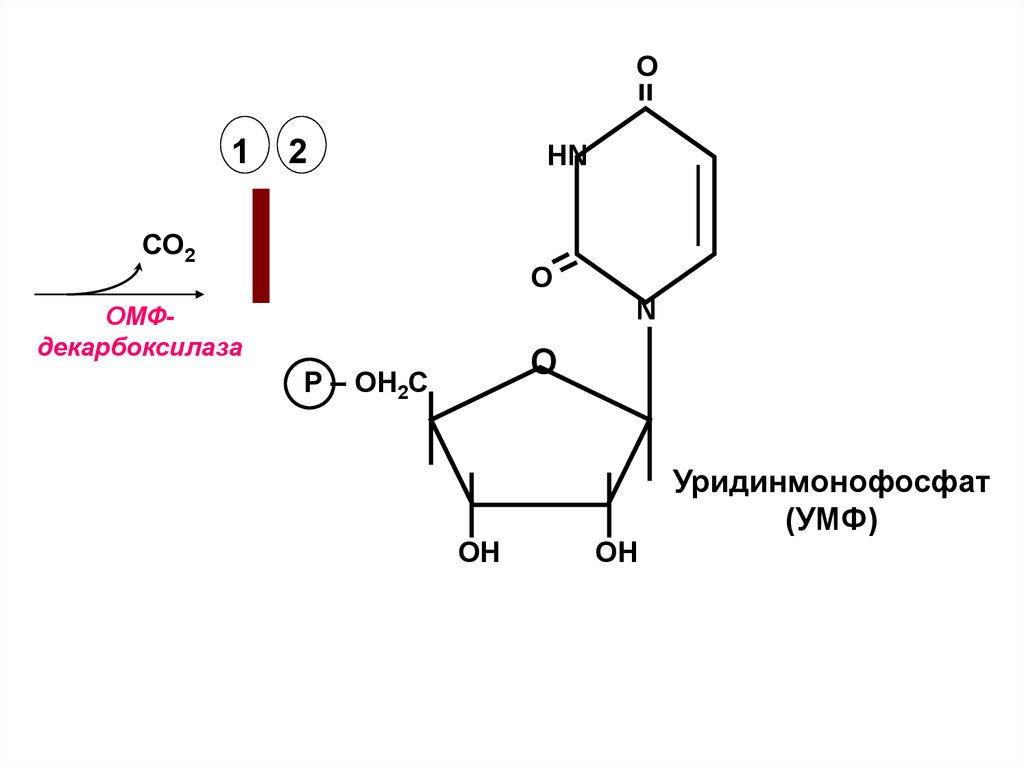
35.
О1
2
НN
СО2
O
N
ОМФдекарбоксилаза
О
Р – ОН2С
ОН
ОН
Уридинмонофосфат
(УМФ)
36.
нуклеозидмонофосфаткиназаУМФ + АТФ <=> УДФ + АДФ;
нуклеозиддифосфаткиназа
УДФ + АТФ <=> УТФ + АДФ
Mg 2+
УТФ + глутамин + АТФ
ЦТФ-синтетаза
ЦТФ + глутаминовая кислота + АДФ + Рн
37.
Оротовая ацидурия(«Оранжевая кристаллоурия»)
• Наследственная патология
недостаточной активности ферментов:
оротатфосфорибозилтрансферазы и ОМФдекарбоксилазы (оротовая ацидурия I типа).
Накапливается оротовая кислота
ОМФдекарбоксилазы (оротовая ацидурия II
типа). Накапливается ОМФ и меньше оротовой
кислоты
38.
• дети отстают в развитии• Мегалобластная анемия - нарушена скорость
деления клеток эритроцитарного ряда
• Мочекаменная болезнь (выделение оротовой
кислоты с мочой)
• нарушается работа ЖКТ, сердечно-сосудистой и
иммунной системы
• Лечение – пероральный прием уридина всю жизнь
39. Биосинтез дезоксирибонуклеотидов
• Происходит на уровне рибонуклеотиддифосфатов(РНДФ) с участием тиоредоксиновой системы.
• Образуются дезоксирибонуклетиддифосфаты (дРНДФ)
в процессе восстановления рибозы в дезоксирибозу.
рибонуклеозидредуктаза
дРНДФ
РНДФ
SH
TR
S
TR
SH
Тиоредоксин
восстановленный
S
тиоредоксинредуктаза
НАДФ
НАДФН2
Тиоредоксин
оксиленный
40. Биосинтез тимидиловых нуклеотидов
дЦДФдЦТФ
АТФ
дГДФ
дГТФ
нуклеозидкиназа
дАДФ
дАТФ
Биосинтез тимидиловых нуклеотидов
Метилентетрагидрофолат
дУДФ → дУМФ
дТМФ
АТФ
→
трансфераза
Дигидрофолат
Тимидилатсинтетаза
дТДФ
АТФ
→
трансфераза
дТМФ
дТТФ
41. Ингибиторы синтеза нуклеотидов
- синтетические аналоги азотистых оснований,нуклеозидов, нуклеотидов, фолиевой кислоты группа лекарственных препаратов в онкологии.
Цитотоксический эффект –
конкурентное ингибирование ферментов синтеза
нуклеиновых кислот
или искажение структуры ДНК при встраивании
аналога.
5-фторурацил, 5-фтордезоксиуридин (ингибирование
тимидилатсинтетазы)
Аминоптерин, метотрексат (ингибирование
дигидрофолатредуктазы)
42.
• 6-тиогуанин, 6–меркаптопурин (гидроксильныегруппы заменены на тиольные в 6 положении)
• Азатиоприн (in vivo в 6–меркаптопурин) – подавляет
реакцию иммунологического отторжения при
трансплантации органов.
• 6-азауридин, азацитидин, 8-азагуанин (содержат
дополнительный атом азота).
• Цитарабин (вместо рибозы – арабиноза) – при
лечении рака и вирусных инфекций.
• 5-йод-дезоксиуридин – эффективен при местном
лечении герпесного кератита.
43.
СПАСИБОЗА
ВНИМАНИЕ!

































 Биология
Биология








