Похожие презентации:
Периодические системы химических элементов
1. Периодические системы
ПЕРИОДИЧЕСКИЕСИСТЕМЫ
2.
3. История:
• Триады Дёберейнера (1817);• Спираль Шанкуртуа (1862);
• Октавы Ньюлендса (1864);
• Таблица Лотара Мейера (1864);
• Таблица Менделеева (1869).
4. Триады Дёберейнера
1817Гесс: 1849:
Иоганн-Вольфганг Дёберейнер
(1780—1849)
углерод − бор − кремний; азот −
фосфор − мышьяк; сера −
селен − теллур и хлор − бром −
иод.
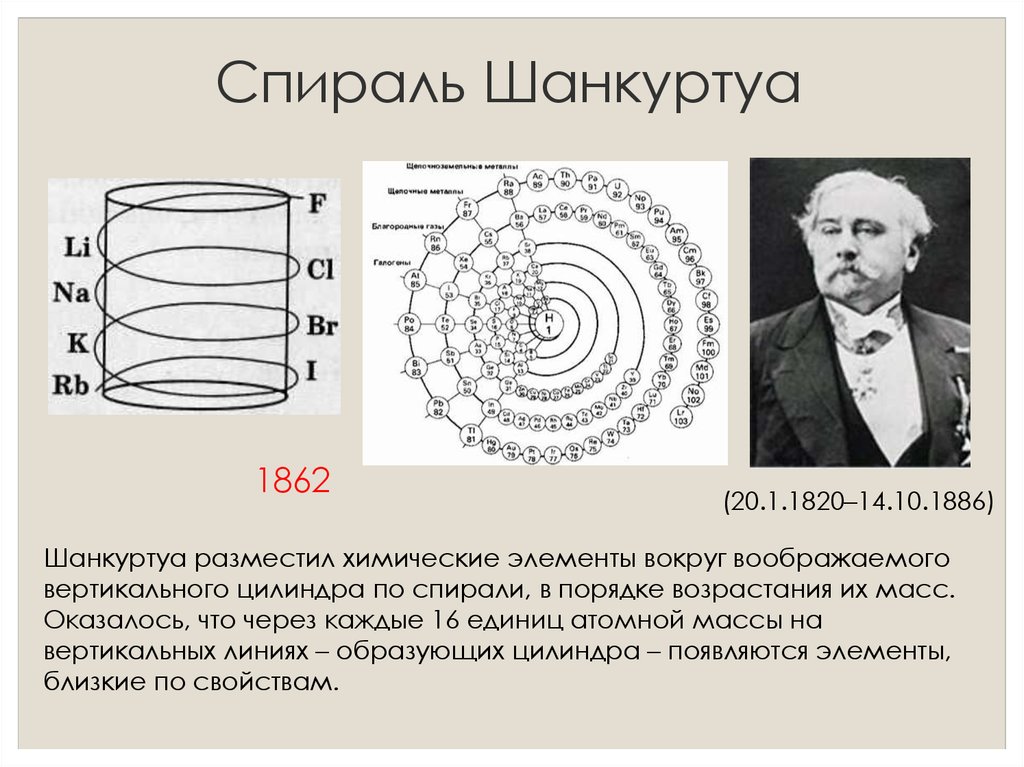
5. Спираль Шанкуртуа
1862(20.1.1820–14.10.1886)
Шанкуртуа разместил химические элементы вокруг воображаемого
вертикального цилиндра по спирали, в порядке возрастания их масс.
Оказалось, что через каждые 16 единиц атомной массы на
вертикальных линиях – образующих цилиндра – появляются элементы,
близкие по свойствам.
6.
7. Таблица Лотара Мейера
Лотар Юлиус Мейер(19.8.1830–22.6.1895)
1864
27 элементов
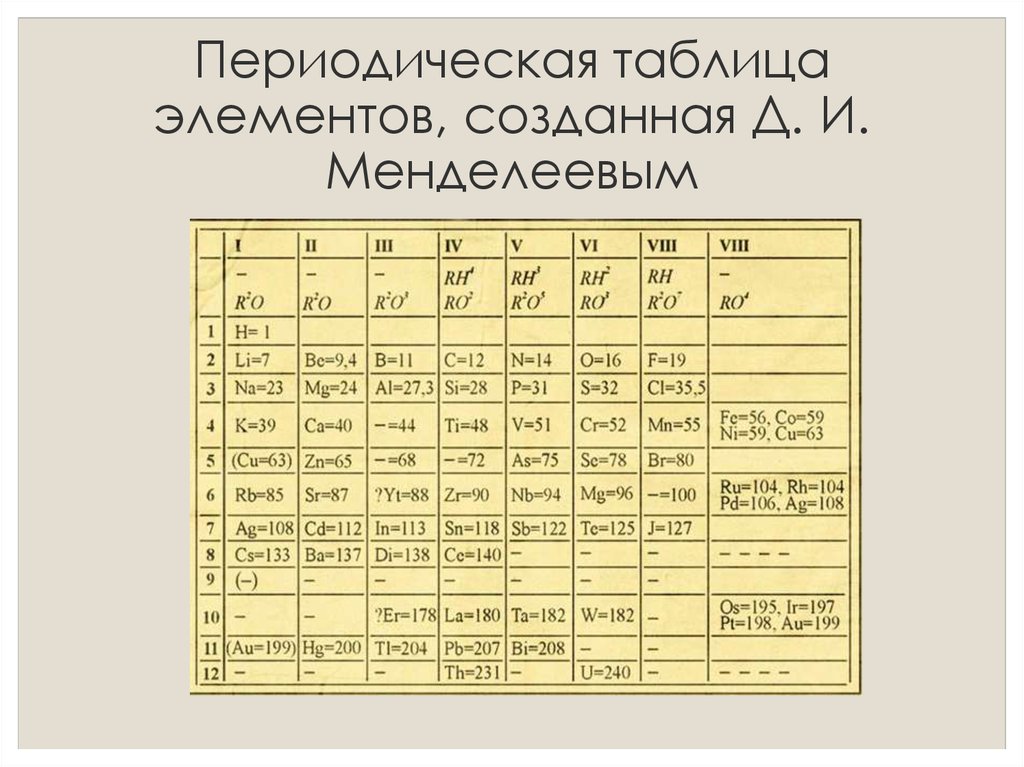
8. Периодическая таблица элементов, созданная Д. И. Менделеевым
9.
• Д.И. Менделеев исходил из убеждения, что в основу классификациидолжна быть положена фундаментальная количественная
характеристика элементов – атомная масса, от которой «должны
находиться в зависимости все остальные свойства». Но найти эту
зависимость было крайне трудно по двум причинам:
• 1) далеко не все химические элементы были известны к началу работы
Д.И. Менделеева;
• 2) атомные массы некоторых элементов были установлены неточно, и
их формальное сопоставление приводило к недоразумениям.
• В отличие от всех своих предшественников русский учёный сопоставил
между собой несходные элементы, расположив все известные
элементы в порядке возрастания атомных масс.
ослабление металлических свойств и усиление неметаллических
10. Закон периодичности
• Сходные в химическом отношении элементы встречаются вестественном ряду через правильные интервалы и, следовательно,
повторяются периодически.
• Свойства простых тел, а также форма и свойства соединений
элементов находятся в периодической зависимости от величины
атомных весов элементов.
«День рождения» системы Д.И.
Менделеева - 18 февраля 1869 г.
63 элемента
Предсказаны 45, 68, 70 и 180
11.
официальноотменена
ИЮПАК в
1989 году.
(ИЮПАК
(англ. и фр.
IUPAC) —
Международ
ный союз
теоретическ
ой (чистой)и
прикладной
химии
(International
Union of Pure
and Applied
Chemistry)
12.
13. Длиннопериодная таблица
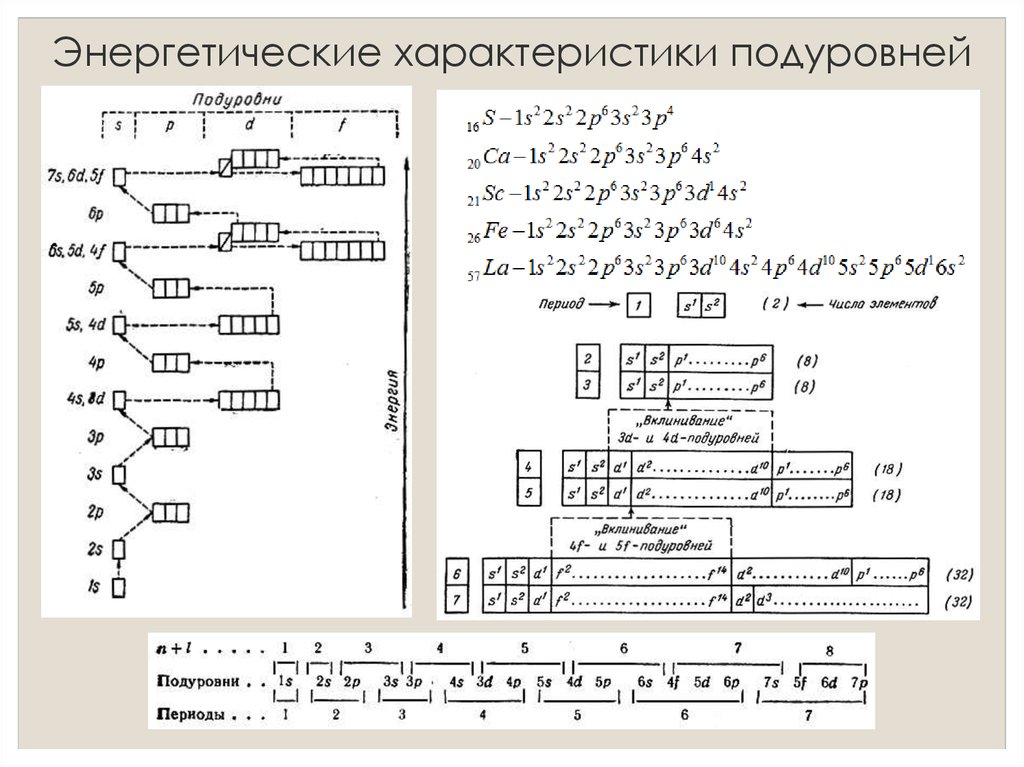
14. Энергетические характеристики подуровней
15.
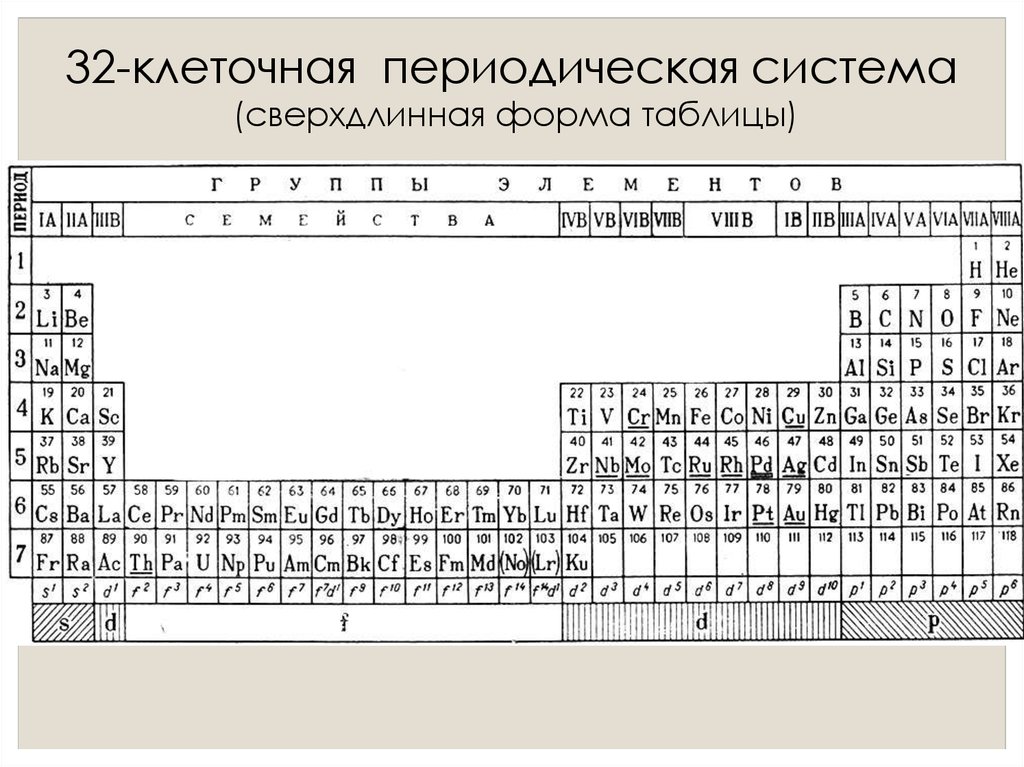
32-клеточная периодическая система(сверхдлинная форма таблицы)
16.
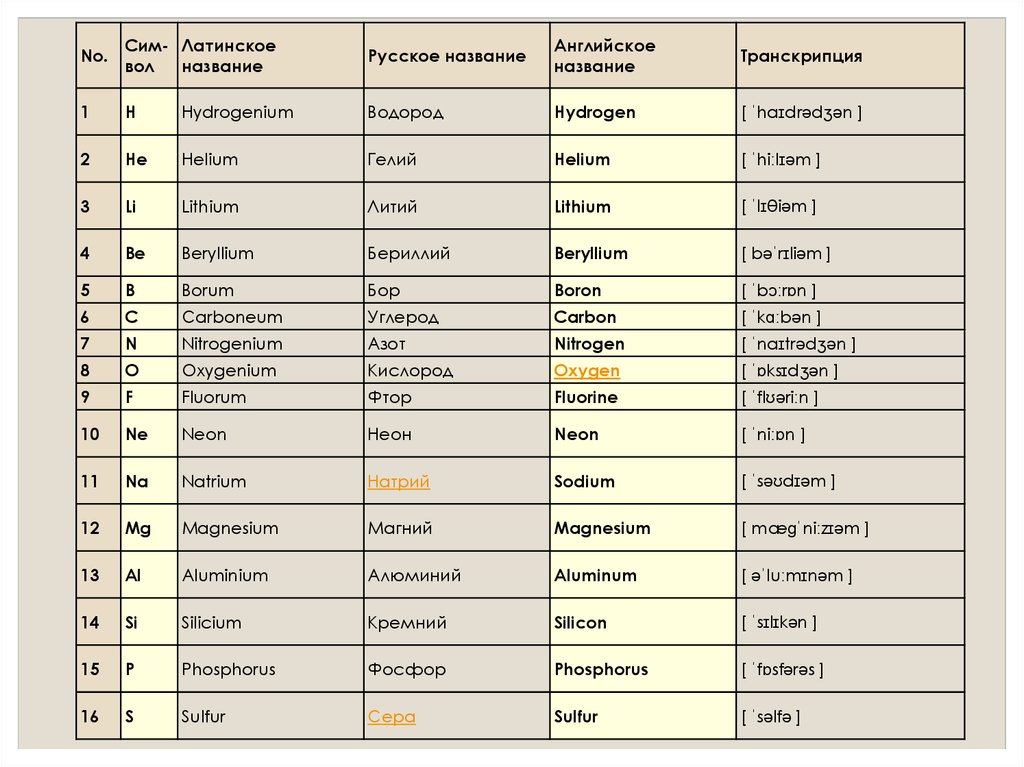
No.Сим- Латинское
вол
название
Русское название
Английское
название
Транскрипция
1
H
Hydrogenium
Водород
Hydrogen
[ ˈhaɪdrədʒən ]
2
He
Helium
Гелий
Helium
[ ˈhiːlɪəm ]
3
Li
Lithium
Литий
Lithium
[ ˈlɪθiəm ]
4
Be
Beryllium
Бериллий
Beryllium
[ bəˈrɪliəm ]
5
B
Borum
Бор
Boron
[ ˈbɔːrɒn ]
6
C
Carboneum
Углерод
Carbon
[ ˈkɑːbən ]
7
N
Nitrogenium
Азот
Nitrogen
[ ˈnaɪtrədʒən ]
8
O
Oxygenium
Кислород
Oxygen
[ ˈɒksɪdʒən ]
9
F
Fluorum
Фтор
Fluorine
[ ˈflʊəriːn ]
10
Ne
Neon
Неон
Neon
[ ˈniːɒn ]
11
Na
Natrium
Натрий
Sodium
[ ˈsəʊdɪəm ]
12
Mg
Magnesium
Магний
Magnesium
[ mæɡˈniːzɪəm ]
13
Al
Aluminium
Алюминий
Aluminum
[ əˈluːmɪnəm ]
14
Si
Silicium
Кремний
Silicon
[ ˈsɪlɪkən ]
15
P
Phosphorus
Фосфор
Phosphorus
[ ˈfɒsfərəs ]
16
S
Sulfur
Сера
Sulfur
[ ˈsəlfə ]











 Химия
Химия








